补体C1q 水平对急性心肌梗死后心衰的预测价值
于高修,伍 杨,李 攀,宋婧文,唐文栋,李 威,陈 峰*
1.海军军医大学长海医院心内科,上海 200433
2.烟台业达医院心内科,烟台 264000
动脉粥样硬化斑块破裂伴发血栓形成是急性心肌梗死(AMI)的主要原因之一[1]。对动脉粥样硬化的机制研究[2]已发现,免疫功能障碍和炎症在急性冠脉综合征(ACS)的发生、发展中起核心作用。发生AMI 后的免疫炎症反应是心梗面积的关键影响因素,持续促炎症反应可加重心梗后不良心室重构[3]。由此可见,炎症反应因子有望用于心梗预后及作为治疗靶点。
补体系统是先天免疫系统的一部分,补体激活是炎症的主要特征。补体级联激活可能导致负性心血管效应,如加重缺血-再灌注损伤[4]。补体C1 在触发激活经典免疫途径中扮演重要角色。其通过C-末端的球状结构域结合多种细胞和血浆蛋白来发挥生物活性。C1q 与多种具有相似球状结构域的非补体蛋白统称为C1q 家族蛋白[5]。补体系统的激活参与糖尿病患者缺血性心脏病发病,某些补体级联产物(如sC5b-9)可预测该患者群体的预后[6]。C1q 结合脂联素血清水平在男性ACS 患者中较健康组显著增高[7]。
然而,目前针对血清C1q 水平变化与AMI 预后的研究尚鲜见。因此,本研究拟通过观察AMI发生后早期血清C1q 水平变化和随访出院后是否发生心衰,探讨C1q 水平对心梗后心衰的预测价值,以期为临床预测心梗后心衰提供参考。
1 资料与方法
1.1 一般资料 选择 2020 年 3 月至 2021 年 3 月在海军军医大学长海医院心内科住院确诊为AMI并行冠状动脉造影(CAG)的患者162 例,其中男性120 例、女性42 例,平均年龄(66.1±13.5)岁。纳入标准:(1)符合2012 年全球心肌梗死统一定义标准[8],cTnI>0.09 µg/L,CAG 发现冠脉内血栓或相关血管闭塞;(2)出院时无心衰症状或体征;(3)配合术后1 年门诊随访;(4)年龄>18 岁。排除标准:(1)合并严重肝肾功能障碍、恶性肿瘤、结缔组织病、自身免疫疾病、血液系统疾病;(2)术前已有慢性心衰、长期卧床、扩张型心肌病、肥厚型心肌病、严重心脏瓣膜病等。本研究经本院伦理委员会审核批准(SK2020-044),研究对象均签署知情同意书。
1.2 观察指标及分组 收集患者的年龄、性别、体质量指数、心功能Killip 分级、高血压病史、糖尿病史、冠脉Gensini 评分。患者入院次日清晨,至少禁食 12 h 后,采取静脉血 3 mL,测定血清C1q、B 型利钠肽(BNP)、低密度脂蛋白(LDL)、胆固醇(TC)、估算肾小球滤过率(eGFR)等血清指标浓度。其中,TC 采用酶法测定,C1q 采用免疫透射比浊法试剂盒测定。通过心脏彩超测得左室射血分数(LVEF)。
据血清C1q 水平由高到低三分位分组,将患者分为高分位组(C1q>185 mg/L)、中分位组(158 mg/L<C1q≤185 mg/L)、低分位组(C1q≤158 mg/L),每组54 例。
1.3 CAG 评估 采用Judkins 法经桡动脉或股动脉穿刺行CAG 检查。由2 位中级以上职称心内科医生运用Gensini 评分系统对患者冠状动脉狭窄程度进行评价[9]:狭窄<25%计1 分,25%~50%计2 分,51%~75%计4 分,76%~90%计8 分,91%~99%计16 分,100%计32 分。不同冠状动脉病变节段分值乘以对应系数:左主干×5,前降支近段×2.5、中段×1.5、远段×1,对角支D1×1、D2×0.5,回旋支近段×2.5、中远段×1、钝缘支×1,右冠状动脉近、中、远段与后降支均×1,左室后支×0.5。最后相加所得总分即为Gensini 评分。
1.4 门诊及电话随访 嘱患者出院后第1、3、6、12 个月于心内科门诊随访,观察终点为随访期间发生急性或慢性心力衰竭(HF)。2021 年版欧洲急慢性心衰诊断和管理指南[10]将HF 定义为出现呼吸困难、下肢/踝关节水肿、活动耐力下降、易疲劳症状和(或)伴有颈静脉压升高、肝颈静脉反流征阳性、肺瘀血、第三心音为奔马律、心界扩大等体征,或心脏彩超见LVEF<50%。门诊随访时根据查体所见、患者纽约心功能分级(NYHA)、心脏彩超表现、6 min 步行试验(6MWT)结果等,判断患者是否发生心衰。
1.5 统计学处理 采用SPSS 22.0 统计软件进行数据分析,符合正态分布的计量资料以x±s 描述,组间比较采用独立样本t 检验或单因素方差分析;偏态分布的计量资料以M(P25,P75)描述,偏态分布的计量资料和等级资料的组间比较采用非参数检验分析;计数资料以n(%)表示,组间比较采用检验。用二元logistic 回归模型进行多个变量与心梗后心衰的相关性分析。用受试者工作特征曲线(ROC)分析C1q 水平预测心梗后心衰的价值。检验水准(α)为0.05。
2 结 果
2.1 一般基线资料与心功能比较 结果(表1)表明:3 组间患者年龄、BNP 水平、Gensini 评分、Killip 分级、LVEF、出院心梗后心衰比例差异均有统计学意义(P<0.05)。

表1 不同血清C1q 水平分组间患者一般资料和心功能比较
2.2 出院后是否发生心梗后心衰患者相关危险因素比较 162 例心梗患者出院后均获得随访,随访9~18 个月,中位随访12(11.5,15)个月,随访期间发生心衰36 例(22.22%)、死亡3 例(1.8%),发生心衰的中位时间为出院后4.5(3.5,7)个月。结果(表2)显示:中位出院后1 年内,与未发生心衰的患者相比,发生心衰患者的年龄偏大、血清C1q 水平偏低、使用螺内酯及ACEI/ARB 比例偏高(P<0.05)。
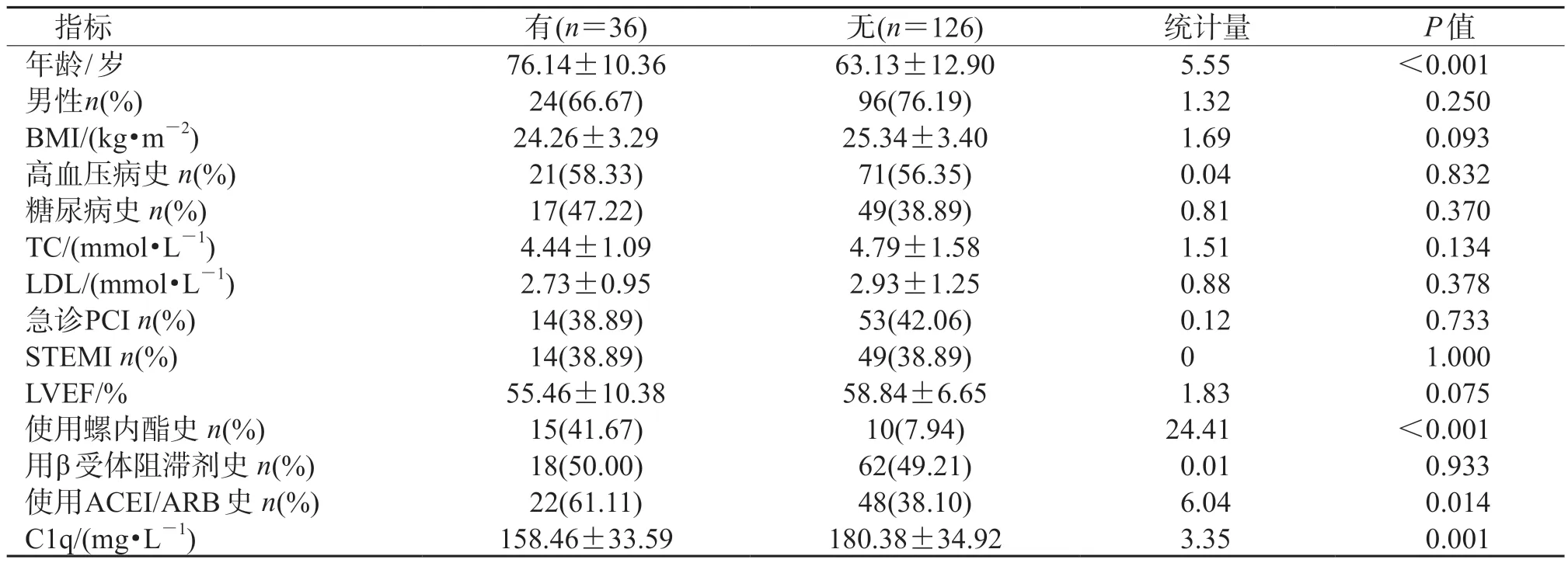
表2 中位出院后1 年内有无心梗后心衰患者相关指标比较
2.3 心梗后心衰多因素logistic 逐步回归分析 以心梗后心衰发生为因变量,以年龄、是否有高血压病史、糖尿病史,有无使用螺内酯、β 受体阻滞剂、ACEI/ARB 史,C1q 分组为自变量进行多因素logistic 逐步回归分析,结果(表3)显示:高龄、使用螺内酯、低分位C1q 水平是心梗后心衰发生的独立危险因素(P<0.05)。

表3 心梗后心衰多因素逐步logistic 分析
2.4 C1q 水平对患者出院后发生心衰的预测价值 ROC 曲线(图1)显示:心梗早期血清C1q水平预测患者中位出院后1 年发生心衰的AUC 为0.703(95%CI 0.627~0.772,P<0.001); 以 C1q血清浓度138.2 mg/L 为临界值,其预测灵敏度为41.67%、特异度为92.86%。

图1 C1q 预测心梗后心衰的ROC 曲线
3 讨 论
近年来发现C1q 识别启动的补体经典途径在动脉粥样硬化、心肌代谢过程中发挥重要作用[11-12]。在冠脉不同程度狭窄的患者中,尤其在急性冠脉综合征患者中,粥样硬化斑块的不稳定性与C1q 水平降低显著相关[13],说明补体C1q 的激活可能参与不稳定的冠脉粥样硬化斑块的炎症反应和血栓形成。
补体系统的经典途径通过识别凋亡细胞、免疫复合物、炎症因子(如C-反应蛋白)表面标记的脂蛋白等危险信号而启动。一方面,模式识别诱导补体清除上述危险产物不需全面激活,是有益的激活;另一方面,广泛的经典途径激活可以诱导促炎信号,这可能与心血管疾病发病进展有关。因此,补体经典激活途径对心血管疾病发病的作用是双向的[14-15]。
本研究中,Gensini 评分随患者C1q 水平降低而升高(P<0.001),即冠状动脉狭窄越严重、心肌梗死面积越大的患者,C1q 水平越低,与既往研究[16]结论相似。其机制可能在于C1q 是补体经典途径识别和激活的关键分子,发生AMI 后,心肌缺血坏死组织炎症反应剧烈,结合冠脉内急性血栓形成,导致补体系统过度激活,循环血中C1q 被大量消耗。AMI 患者受累的心肌越广泛,越易发生心室重构和心衰,远期预后越差。BNP 虽然是心梗后心衰的重要生物标志物,但能否用于远期预后预测尚未明确。本研究多因素logistic 回归分析发现,低分位C1q 水平患者出院后心梗后心衰发生风险约为高分位患者的4 倍。
冠脉血流再通时机的贻误、大量血栓形成,支架术后的慢血流状态等导致大面积心肌发生缺血性坏死,导致心室重构,进而发生远期心衰。而这些过程中涉及炎症反应,其中补体系统过度激活可能发挥重要作用,导致血C1q 大量消耗。为了进一步探讨心梗发病后早期C1q 水平对患者出院后发生心衰的预测价值,本研究对患者进行了中位为期1 年的随访,并绘制ROC 曲线,结果提示血清C1q 水 平 的 AUC 为 0.703,以 138.2 mg/L 为 临 界值,预测灵敏度为41.67%、特异度为92.86%。
综上所述,本研究中,不同C1q 水平组患者出院后心衰的发生率差异有统计学意义,发生心衰患者的C1q 水平低于未发生心衰的患者,低分位C1q水平为心梗后心衰发生的独立危险因素,对心梗后心衰有一定预测价值,但未发现中分位C1q 水平与心衰的关系,可能与入选病例较少、随访时间较短有关。本研究提示,对于C1q 水平降低的心梗患者,应警惕心肌重构,必要时服用药物,积极预防心衰的发生。此外,C1q 在炎症反应中如何被消耗以及如何进行干预,以减轻心梗后心肌炎症反应及持续炎症反应引起的心室重构,尚待深入的基础实验来发现。
利益冲突:所有作者声明不存在利益冲突。

