营养风险指数在可切除肝细胞癌患者术后并发症及预后预测中的作用
崔永康 于承平 许浩志 马新宇 麻勇 李林强
作者单位:哈尔滨医科大学附属第一医院肝脏微创外科(哈尔滨 150006)
原发性肝癌是消化系统常见的恶性肿瘤,发病率居我国恶性肿瘤第四位,死亡率居第二位,严重威胁我国人民的生命健康,其中肝细胞癌(Hepatocellular carcinoma,HCC)约占肝癌的75%~85%[1]。肝切除术作为HCC患者的首选治疗方案有助于改善临床结局,但研究显示,肝切除术术后并发症发生率为13.9%~43%,术后5年复发率高达70%,严重降低了患者的生活质量和总生存期(OS)[2-3]。HCC多由肝硬化发展而来,肝功能损害必然会导致不同程度的营养物质代谢紊乱,加上肿瘤消耗和营养摄入的减少,多数患者会出现营养不良[4]。有研究表明营养状态与患者的治疗、预后和临床结局密切相关,选择合适的营养风险筛查工具对患者的术前营养状态进行评估和管理,可以改善临床结局[5-8]。常用的营养评估方法包括营养风险筛查量表(Nutritional risk screening 2002,NRS 2002)、患者主观综合评估(Patient generated subjective global assessment tool,PG SGA)及营养不良通用筛查工具(Malnutrition universal screening tool,MUST)等在消化系统恶性肿瘤中已有相关报道,而营养风险指数(NRI)作为一种新兴的营养评估工具,综合考虑营养状态与炎症反应,评估更加全面。目前已有研究证实NRI在消化系统恶性肿瘤如口腔癌、食管癌和结直肠癌中的预后价值,且老年营养风险指数(GNRI)也被证实与老年肝癌术后并发症相关[9-11]。然而,有关NRI对于各年龄段HCC患者的术后疗效是否存在预测价值尚无定论。因此,本研究试图探索术前NRI值对HCC患者术后并发症情况及生存预后的预测价值,为HCC的临床诊治、预后和手术安全性提供参考依据。
1 资料与方法
1.1 研究对象
收集2016年1月—2017年12月哈尔滨医科大学附属第一医院收治入院期间行根治性肝切除的HCC患者的临床资料,根据纳入及排除标准,共计137例患者纳入到本次研究,男性109例(79.6%),女性28例(20.4%)。本研究经哈尔滨医科大学附属第一医院伦理审查委员会审查批准(审批号:2020011)。
1.2 纳入及排除标准
纳入标准:(1)病理诊断为HCC;(2)Child-pugh分级为A/B级,住院接受根治性肝切除手术治疗;(3)年龄在28~80岁之间;(4)术前一周进行血常规及肝功能检查;(5)临床资料完整。排除标准:(1)转移性肝癌、肝癌破裂出血或合并有其他恶性肿瘤;(2)术前接受介入、放化疗或其他治疗措施;(3)术前合并有严重基础疾病(如脑出血、脑梗死及严重心力衰竭等)、炎症性疾病或自身免疫性疾病;(4)术前一个月内输注白蛋白及血液制品;(5)临床资料不完整。
1.3 临床资料
收集研究对象的一般资料,如年龄、性别、体质指数(BMI)、高血压病史、糖尿病病史、手术方式、肿瘤大小及肿瘤CNLC分期;术前一周内的实验室检查结果如总蛋白(TP)、白蛋白(ALB)、前白蛋白(PALB)、白细胞(WBC)、中性粒细胞百分比(N%)、红细胞(RBC)、血红蛋白(Hb)、红细胞比容(Hct)和血小板(PLT);其他指标如手术时间和肿瘤分化程度。
1.4 随访
通过门诊病历和电话随访的方式,收集患者一个月内的术后并发症情况,根据Clavien-Dindo分级标准对并发症严重程度进行分类,将Ⅰ、Ⅱ级并发症定义为一般并发症,Ⅲ、Ⅳ、Ⅴ级并发症定义为严重并发症[12-13]。查阅病历及电话随访患者的术后5年生存情况,随访截止日期为2022年12月31日。无病生存期(DFS)为手术日期到肿瘤复发的时间,甲胎蛋白(AFP)升高伴影像学检查发现肝脏新发占位定义为复发;总生存期(OS)为手术日期到全因死亡或随访截止的时间。
1.5 NRI的计算公式
NRI的计算公式如下[14]:(1)NRI=1.519×血清白蛋白水平(g/L)+41.7×(当前体重/理想体重);(2)男性理想体重=身高-100-[(身高-150)/4],女性理想体重=身高-100-[(身高-150)/2.5];(3)血清白蛋白水平为术前1周之内空腹状态下测量所得,身高和体重为术前1日所测。在NRI的计算公式中,当前体重/理想体重>1时,其比值取1;当前体重/理想体重<1时,取实际比值。
1.6 分组方法
以NRI为检验变量,患者的生存结局为状态变量,绘制ROC曲线,计算得出AUC为0.720(95%CI:0.597~0.842),以敏感度为0.800和特异性为0.504计算出约登指数最大值为0.304,此时NRI为99被确定为最佳截断值,根据此结果将患者分为高NRI组(NRI≥99)和低NRI组(NRI<99)(图1)。
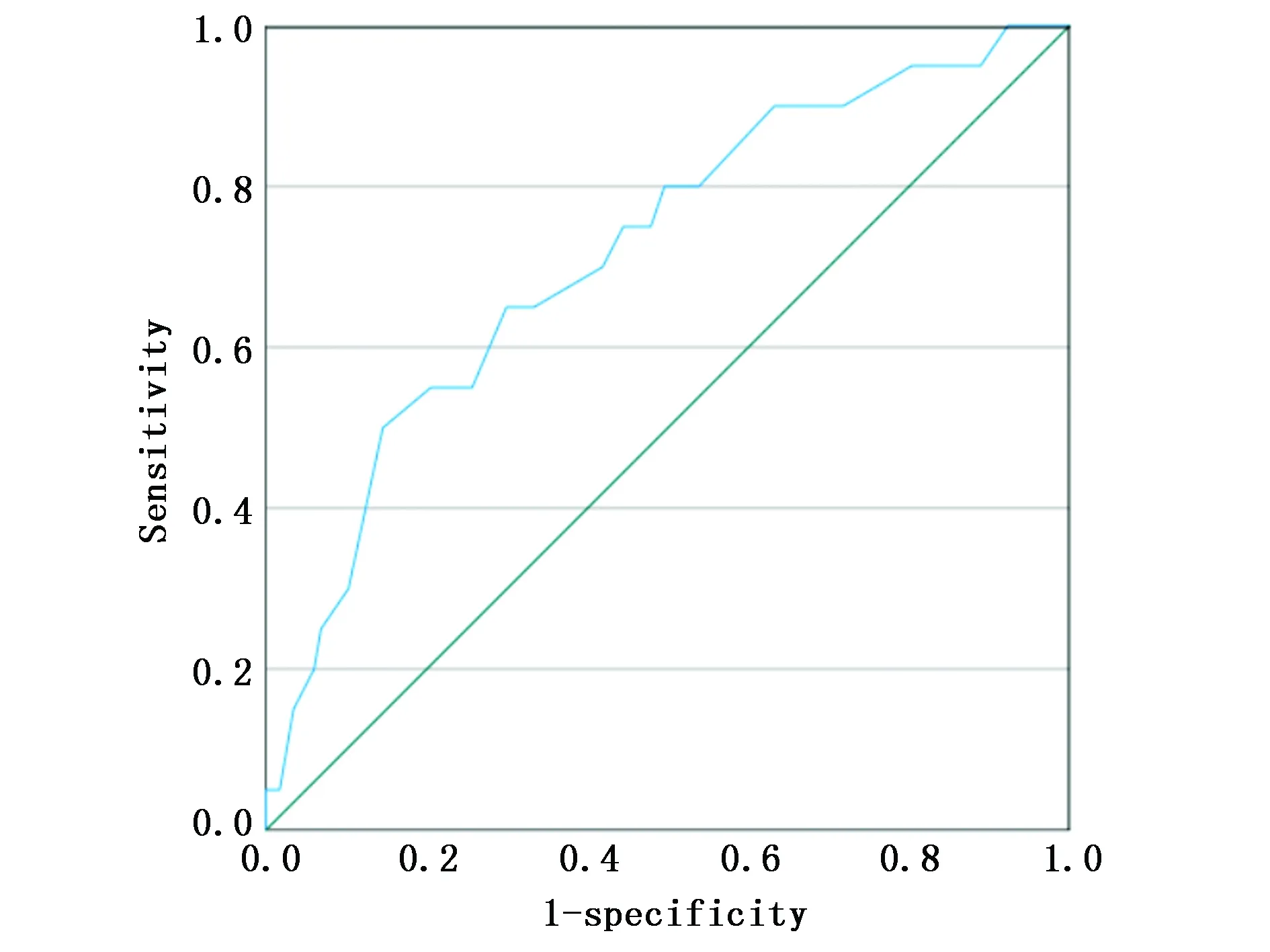
图1 NRI预测HCC患者生存结局的ROC曲线Figure 1 The ROC curve of NRI predicting survival outcomes in HCC patients
1.7 统计方法

2 结果
2.1 NRI与患者临床特征
高NRI组患者BMI高于低NRI组患者(P<0.001)。而两组患者的性别、年龄、身高、ASA分级、肿瘤大小、手术方式、手术切除位置、手术时间、肿瘤分化程度、CNLC分期、高血压及糖尿病病史的差异无统计学意义(P>0.05)(表1)。
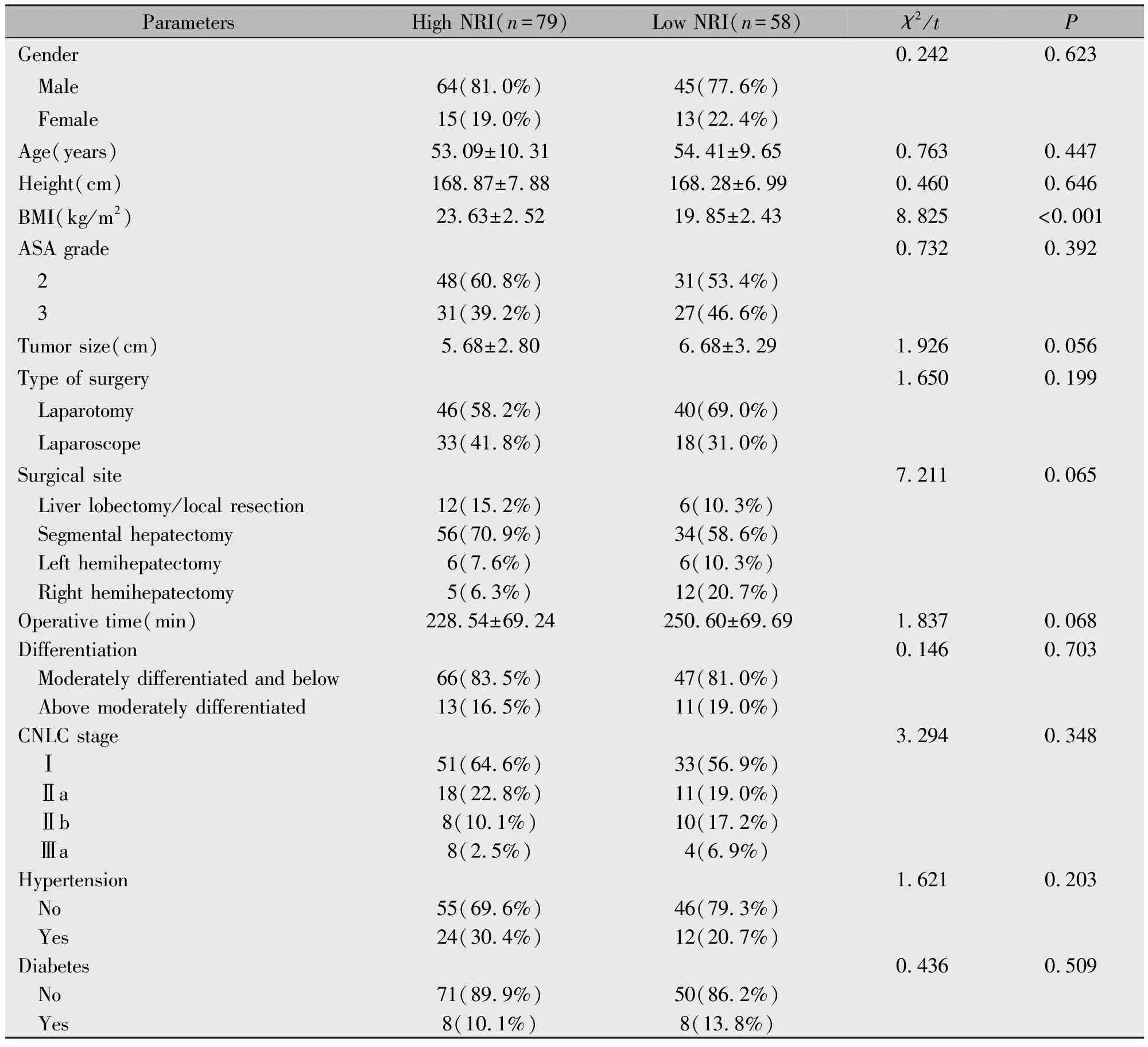
表1 患者的临床特征
2.2 术后并发症的危险因素分析
根据是否发生术后并发症将患者分为无并发症组(88例)和并发症组(49例),两组患者BMI、手术方式、手术切除位置、肿瘤大小、CNLC分期、NRI、手术时间、Hb及Hct存在统计学差异(P<0.05)(表2)。多因素logistic回归分析结果显示:CNLCⅡa期的患者相较于CNLCⅠ期的患者,发生术后并发症的风险高(OR=3.274,95%CI:1.031~10.394,P=0.044);手术时间越长,发生术后并发症风险越高(OR=1.011,95%CI:1.003~1.019,P=0.006);低NRI增加HCC术后并发症风险(OR=4.688,95%CI:1.485~14.797,P=0.008)(表3)。

表2 临床病理特征与术后并发症的关系

表4 NRI与术后并发症严重程度的关系
2.3 NRI对术后并发症严重程度的影响
根据Clavien-Dindo分级标准将发生术后并发症的患者分为一般并发症组27例和严重并发症组22例。高NRI组患者一般并发症14例(77.78%),严重并发症4例(22.2%);低NRI组患者一般并发症13例(41.9%),严重并发症18例(58.1%)。两组间严重并发症发生率的差异具有统计学意义(P=0.015)。
2.4 NRI对患者DFS和OS的影响
Kaplan-Meier生存曲线结果显示:高NRI组患者的中位DFS与OS分别为35个月和50个月,低NRI组患者的中位DFS与OS分别为26个月和38个月,低NRI组的DFS与OS均明显低于高NRI组(P<0.001)(图2a,2b)。

图2 HCC患者的DFS和OS的Kaplan-Meier生存曲线Figure 2 The Kaplan-Meier survival curves of DFS and OS in HCC patients
2.5 HCC患者DFS和OS的影响因素分析
DFS的单因素Cox回归分析结果显示:NRI、年龄、手术方式、手术切除位置、肿瘤大小、CNLC分期、白蛋白、前白蛋白以及中性粒细胞百分比与患者DFS的预后相关(P<0.05),将上述指标纳入多因素Cox回归模型,结果显示:NRI(HR=1.826,95%CI:1.138~2.928,P=0.013)、年龄(HR=1.028,95%CI:1.006~1.050,P=0.011)、肿瘤大小(HR=1.280,95%CI:1.173~1.396,P<0.001)以及CNLC分期(HR=1.794,95%CI:1.348~2.388,P<0.001)是DFS的影响因素(表5)。
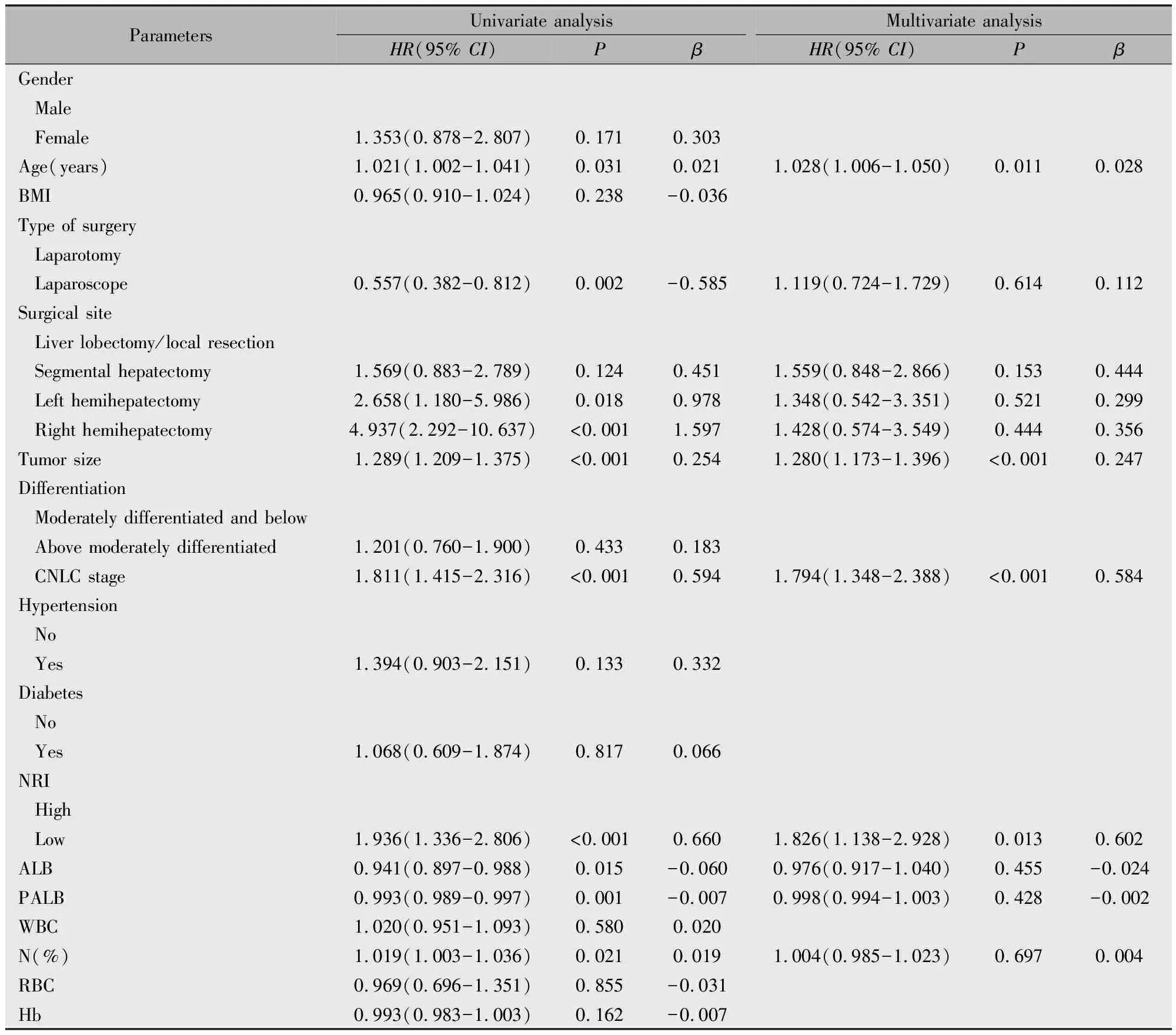
表5 HCC患者DFS的影响因素分析
OS的单因素Cox回归分析结果显示:NRI、手术方式、手术切除位置、肿瘤大小、CNLC分期、高血压病史、白蛋白、前白蛋白以及中性粒细胞百分比与患者OS的预后相关(P<0.05),将上述指标纳入多因素Cox回归模型,结果显示:NRI(HR=2.660,95%CI:1.536~4.607,P<0.001)、肿瘤大小(HR=1.418,95%CI:1.287~1.562,P<0.001)、CNLC分期(HR=2.471,95%CI:1.830~3.338,P<0.001)以及高血压病史(HR=2.490,95%CI:1.426~4.349,P<0.001)是OS的影响因素(表6)。

表6 HCC患者OS的影响因素分析
3 讨论
近年来,HCC的发病率和死亡率逐年上升,尽管肝切除术已经发展的十分成熟,但仍具有较高的手术风险,具有围手术期并发症及术后复发率高的特点,严重威胁着HCC患者的术后生存。研究表明[17],在恶性肿瘤患者中营养不良的发生率为30%~80%,而在HCC患者中,由于营养物质摄入不足及代谢紊乱等情况使得这一比例更高。营养不良的HCC患者行手术治疗会导致肝损伤加重、ALB合成减少、免疫功能和机体修复能力下降,增加术后并发症的发生率,影响生存预后[18]。术前积极的营养评估有助于早期发现营养不良状况,适时进行合理的营养支持可提高手术安全性,减少术后并发症的发生,延长生存期。因此,有必要开发一种准确的营养风险评估工具来预测手术治疗效果。
目前越来越多的研究探讨了NRI作为一种新型营养评估工具对消化系统恶性肿瘤术后疗效的预测价值,并证实NRI在生存分析和术后并发症的预测方面更为精确[19],如Clavier等[20]在一项以143例局限性食管癌患者为中心的回顾性研究中证实:NRI是患者OS的独立预后因素;Hirahara等[21]在对297例行手术治疗的老年胃癌患者进行回顾性分析时证实,老年营养风险指数(GNRI)与老年胃癌患者的OS显著相关且是OS的独立预测因子;另一项Meta分析结果表明[22],GNRI是胃肠道恶性肿瘤患者并发症和生存预后的独立预测因子。
本研究以NRI为术前营养评估指标对HCC患者进行临床回顾性分析,首次评估了NRI、术后并发症及生存预后之间关系。在两组患者的临床特征中,高NRI组患者的BMI高于低NRI组患者。本研究中两组患者出现这种差异可能与NRI的计算公式中也包含了体重有关,后续研究通过多因素分析控制了BMI的影响。术后并发症的影响因素分析结果显示:手术时间长和低NRI是HCC患者发生术后并发症的独立危险因素,CNLCⅡa期的患者相较于CNLCⅠ期的患者,发生术后并发症的风险高。既往研究表明[23-24],肿瘤大小、手术切除位置及术中出血量和输血量与肝切除术后发生并发症密切相关。结果的差异性考虑可能与研究样本量小且患者来源局限有关;此外,相较于低NRI组,高NRI组患者发生严重并发症的机会较小。
有研究认为[25],肿瘤大小、手术切除位置和肿瘤分期与HCC患者的术后生存密切相关。在本研究中,NRI、年龄、肿瘤大小和CNLC分期是DFS的独立预测因素;NRI、肿瘤大小、CNLC分期及高血压病史是OS的独立预测因素,这与国内外研究结果基本保持一致。而高血压病史对OS的预测价值考虑为高血压患者在经过外科手术和麻醉刺激后,因身体创伤易出现应激反应,增加了急性心脑血管疾病的风险,从而降低了术后OS。然而,本研究作为一项单中心的临床回顾性研究,仍具有一定的局限性。首先,无法完全排除混杂偏倚的影响,其次,样本量小且患者来源局限,最后,生存数据的随访部分取自患者及家属的回忆,可能出现信息偏倚。因此,本研究的结果还需纳入大量不同地区的人群进行多中心的前瞻性研究去进一步证实。
综上所述,NRI对HCC患者是一种可靠的营养风险筛查工具,可有效预测术后并发症情况和生存预后,为围手术期营养支持治疗和手术安全性评估提供理论依据。

