延迟Gd-DTPA增强MR软骨成像:全关节软骨成像的可行性分析
延迟钆喷替酸葡甲胺(Gd-DTPA)增强MR软骨成像(Delayed gado linium-enhanced MRI o f cartilage,dGEMRIC)是近年发展起来的一种功能MR成像技术,可反映关节软骨的早期退变[1~2]。其基本原理是在软骨早期退变时,软骨细胞外基质中的氨基葡聚糖含量将明显减少,此时若外环境中存在Gd-DTPA分子,Gd-DTPA则可替代性进入软骨内部,在退变区域分布更多,在非退变区域分布更少,退变区软骨t1值将显著低于非退变区[3],因此,准确测量软骨t1值是dGEMRIC技术的关键之一。单层快速反转恢复序列(inversion-recovery p repared fast spin echo,IR-TSE)是当前测量软骨t1值的通用方法[3~5],通过保持重复时间(time of repetition,TR)不变,多次变动反转时间(time of inversion,TI),通过曲线拟合获得软骨t1值。但是,利用单层IR-TSE测量软骨t1值具有两个显著缺点:①不能覆盖整个关节的软骨,因此不利于了解全关节软骨的t1值信息;②由于TR取值通常应>5倍的组织t1值,而TI值至少应变动5~7个,因此测量时间较长。为了解全关节软骨的t1值信息,多层IR-TSE测量[6]和三维梯度回波测量是可供参考的方法[7~8]。本研究在模型和离体动物软骨中,以单层IR-TSE为参照标准,评估多层IRTSE和可变翻转角的三维快速小角度激发(spoiled fast low-angle shot,FLASH)技术测量t1值的可行性。
1.材料和方法
1.1 模型制备 采用10m lGd-DTPA溶液和磷酸盐缓冲液配制不同浓度的钆溶液,浓度分别为0.062 5、0.125 0、0.175 0、0.250 0、0.500 0、1.000 0和2.000 0mmolGD/L,其t1值范围为100~1 600ms[9],各取15m l密封于圆柱形无菌玻璃管内(共7管)。MR扫描采用头线圈,层面垂直于玻管长轴。
1.2 离体标本制备 选择新鲜正常成年牛髌骨9例,用钢锯垂直于髌正中嵴锯出一道深沟,然后将一侧软骨浸泡于25m g/m l的胰蛋白酶液中4h,制作成早期软骨退变模型(退变侧);另一侧用0.9%的生理盐水平衡4h(对照侧)[10]。将牛髌骨浸泡于2 mmo l GD/L的稀释Gd-DTPA溶液中150min,捞出后用生理盐水冲洗数次,密封[11]。MR扫描时采用12cm的包裹式表面线圈,扫描层面垂直于髌后锯痕。
1.3 MR扫描方法 利用3.0 TMR扫描仪(MAGNETOM TRIO TIM,西门子)进行t1值测量,采用以下3个序列。①单层面 IR-TSE序列:TR/TE 5 000/12ms,TI取值为25、50、100、200、400、800和1 600m s,回波链长为13,平均次数4次,总测量时间为21min 49s;②多层面IR-TSE序列:参数同单层面IR-TSE序列,但扫描5层,层间距100%,其中第3层与单层IR-TSE扫描层面完全吻合;③可变翻转角的三维FLASH序列:采用M ap lt软件(西门子公司出品),TR/TE 15/2.42ms,配对翻转角选择为5°和26°,平均次数 14次,共扫描10层,总测量时间为9min 38s,其第5层与单层IR-TSE的扫描层面完全吻合。在上述3个序列中,FOV均为90mm×90mm,层厚均为3mm,层面内分辨率为0.35mm×0.35mm。
1.4 t1值计算方法 对于单层IR-TSE和多层IRTSE数据,利用两参数拟合公式STI=S0×[1-2× e(-TI/t1)+e(-TR/t1)],采用Origin 6.1软件进行非线性拟合获得t1值[12]。本研究使用的三维FLASH序列可自动计算出t1值分布图。选取3个序列中位置完全等同的层面,利用相同的感兴趣区(ROI)测量出各序列的t1值。在模型中,ROI尽可能大,但不超出玻管内壁轮廓;在软骨中,ROI包括软骨全层,其面积≥50 mm2。
1.5 统计学处理 在模型中,分别计算多层IR-TSE和三维FLASH测量值与单层IR-TSE测量值的Pearson相关系数(r)[13]。在牛软骨中,首先采用配对t检验评估退变侧和对照侧的t1值差异;之后评估多层IR-TSE和三维FLASH测量值与单层IR-TSE测量值的r值[14]。所有统计均采用SPSS 11.5软件包进行统计学处理。
2.结果
2.1 模型测量结果 多层IR-TSE与单层IR-TSE测量值的结果见图1,前者测量值略高,但与单层IRTSE的吻合性极好(r=1.000,P<0.001)。三维FLASH与单层IR-TSE测量值的结果见图2。虽然三维FLASH测量值比单层IR-TSE低15%~29%,但两者具有很高的相关性(r=0.997,P<0.001)。
2.2 牛髌软骨测量结果 对照侧和处理侧软骨t1值的比较见表1。可见,不管采用何种测量方法,处理侧软骨t1值均显著低于对照侧。图3和图4分别为多层IR-TSE和三维FLASH序列获得的t1值分布图。

表1 对照侧和处理侧软骨t1值的比较

图1 模型多层IR-TSE与单层IR-TSE测量值的相应关系。对7管不同浓度的稀释Gd-DTPA溶液,两种方法测量的t1值非常类似,相关系数为1.000
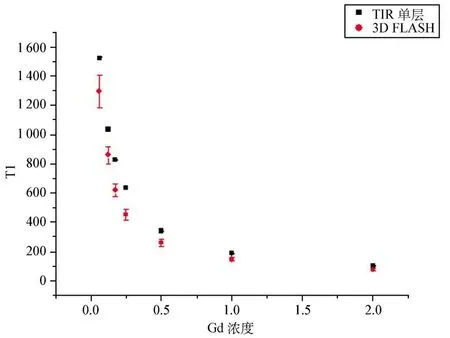
图2 模型三维FLASH与单层IR-TSE测量值的相应关系,前者测量的t1值相对低于后者,相关系数为0.997

图3 多层IR-TSE获得的t1分布图:上半为处理侧软骨,下半为对照侧软骨
多层IR-TSE与单层IR-TSE相比较,对照侧、处理侧和软骨总体(对照侧+处理侧)t1值的相关性分别为r=0.821(P=0.012)、r=0.968(P<0.001)和r =0.953(P<0.001)。三维FLASH与单层IR-TSE相比较,对照侧、处理侧和总体软骨t1值的相关性分别为r=0.199(P=0.637),r=0.757(P=0.030),和r=0.755(P=0.001)。
3.讨论

图4 三维FLASH获得的t1值分布图:软骨t1数据融合于FSSE T1W解剖图像上,上半为处理侧软骨,下半为对照侧软骨
本研究主要探讨了多层IR-TSE和可变翻转角三维FLASH序列测量软骨t1值的可行性,目的是为了进行覆盖全关节软骨的t1值测量。在dGEMRIC技术中,考虑到关节软骨病变的空间分布不均,以及对关节软骨病变纵向监测的必要性,而传统单层 IRTSE测量既不能覆盖全关节软骨,又不能在随访检查中准确重复定位,因此全关节软骨t1测量技术具有很强的临床适用性[13~15]。
由于层面交叉效应和磁化传递效应的影响,多层IR-TSE测量技术被认为不能可靠地进行软骨t1值测量[6]。然而,通过采用100%层间距,本研究发现多层IR-TSE是测量软骨t1值的可靠方法。与标准单层IR-TSE相比较,不管是在模型中,还是在对照侧或处理侧软骨标本中,从定量角度,两者测出t1值的相关性非常好(r为0.821~1.000)。从定性角度,在dGEMRIC技术中,多层IR-TSE同样可以区分正常软骨和早期退变软骨。
虽然本研究证实多层IR-TSE能够可靠地测量关节软骨t1值,但100%的层间距使其依然不能在一次测量中覆盖全部的关节软骨。再次进行一次100%层间距的多层IR-TSE测量是可行方案之一,但总测量时间也将增加1倍。由于IR-TSE测量t1值非常费时,因此2次100%层间距的多层IR-TSE测量方法在临床上依然存在应用限度。
因此,本研究探讨了另外一种更为快速的测量方法,即利用可变翻转角三维FLASH序列测量软骨t1值。利用此方法时,需要获得2个配对翻转角的三维FLASH数据,然后通过软件自动计算获得t1值三维分布图。理论上,在 FLASH序列中,当翻转角为Ernst角[Cos(Ernst角)=e-TR/t1]时,信号强度最高;而当选择的2个翻转角信号分别为最高信号两侧的71%时,测量t1值最为可靠[16]。本研究中,通过预实验我们发现,当固定三维FLASH序列的TR值为15m s时,变动可选的配对翻转角对模型结果的影响并不大,因此最后取固定配对值5°和26°(软件推荐值)。从定性角度,本研究发现三维FLASH序列可区分对照侧与处理组软骨的t1值差异,因而可用于关节软骨的快速三维dGEMRIC成像,这与文献报道结果相同[13~15]。不过,从定量测量 t1值的角度,三维FLASH序列与单层IR-TSE的吻合性要差于多层IR-TSE与单层IR-TSE间的吻合性。如在模型中,三维FLASH序列的实测值比单层IR-TSE低15%~29%;在软骨标本中,三维FLASH序列与单层IRTSE的相关系数也相对更小;而且,在对照侧软骨中,三维FLASH序列与单层IR-TSE并不存在统计学意义的相关(R=0.199,P=0.637)。
本研究尚存在以下不足:①没有在活体中进一步比较3种测量方法,而活体温度对软骨t1值具有肯定的影响,活体的运动相关伪影也可能影响t1值测量结果;②三维FLASH序列选用了2个固定的翻转角,没有根据被测组织t1值的变动进行翻转角的精确选择。
总的说来,在dGEMRIC技术中,多层IR-TSE序列和三维FLASH序列均可实现全关节软骨的t1值测量。层间距100%的多层IR-TSE方法不但可以进行定性诊断,其定量测量值与标准单层IR-TSE序列也具有非常好的相关性,但需要测量2次才能覆盖全关节软骨,因此总测量时间较长。变动翻转角的三维FLASH序列可以在较短的时间内达到全关节软骨定性诊断的目的,但定量测量值与标准单层IR-TSE间的相关性相对更低。
[1] Bisw alS,Resnick D L,Ho ffman JM,etal.Molecular imaging:Integration ofmolecular imaging into themusculoskeletal imaging p ractice.Radiology,2007,244:651
[2] Kneeland J B,Reddy R.Frontiers in musculoskeletal M RI:A rticu lar cartilage.JM agn Reson Imaging,2007, 25:339
[3] Tiderius C J,O lsson L E,Leander P,etal.Delayed gadolinium-enhanced M RI of cartilage(dGEMRIC)in ear ly knee osteoarthritis.Magn Reson Med,2003,49:488
[4] W illiams A,Gillis A,M cKenzie C,et al.G lycosam inog lycan distribution in cartilageas determined by delayed gadolinium-enhanced MRIof cartilage(dGEMRIC):potential clinical app lications.Am JRoentgenol,2004,182:167
[5] Laurent D,Wasvary J,OBy rne E,et al.In vivo qualitative assessments of articular cartilage in the rabbit knee with high resolution MRIat 3T.Magn Reson Med,2003,50: 541
[6] Gray M L,Burstein D,Lesperance LM,et al.Magnetization transfer in cartilage and its constituentmac romo lecules.Magn Reson M ed,1995,34:319
[7] M cKenzie CA,W illiams A,Prasad PV,et al.Three-dimensional delayed gadolinium-enhanced M RI of cartilage (dGEMRIC)at1.5T and 3.0T.JMagn Reson Imaging, 2006,24:928
[8] LiW,Scheidegger R,Wu Y,et al.Accuracy of T1MeasurementWith 3D Look-Locker Technique for dGEMRIC. JMagn Reson Imaging,2008,27:678
[9] 尚瑶,郑卓肇,李选.利用快速自旋回波序列测量骨骼肌肉系统的T2时间.中华放射学杂志,2007,41:1349
[10]Gillis A,Gray M,Burstein D.Relaxivity and diffusion of gadolinium agents in cartilage.M agn Reson Med,2002, 48:1068
[11]W ayne JS,K raft KA,Shields KJ,et al.M R imaging of normal and matrix-dep leted cartilage:correlation with biomechanical func tion and biochem ical composition.Radio logy,2003,228:493
[12]Samosky JT,Burstein D,Eric G rimson W,et al.Spatially-localized correlation of dGEM RIC-measured GAG distribution and mechanical stiffness in the human tibial plateau.JO rthop Res,2005,23:93
[13]W ang L,Schw eitzer M E,Padua A,et al.Rapid 3D-T1 M apping of CartilageWith Variable Flip Ang le and Parallel Imaging at 3.0T.JMagn Reson Imaging,2008,27: 154
[14]Regatte R R,Akella SVS,Borthakur A,et al.In V ivo Proton M R Three dimensional T1-Mapping of H uman A rticular Cartilage:Initial Experience.Radiology,2003, 229:269
[15]T rattnig S,Marlovits S,Gebetsroither S,et al.Three-Dimensional Delayed Gadolinium-Enhanced MRI of Cartilage(dGEM RIC)for In V ivo Evaluation o f Reparative Cartilage after Matrix-Associated Auto logous Chond rocyte Transp lantation at 3.0T:Prelim inary Results.J M agn Reson Imaging,2007,26:974
[16]Deoni Sean CL,Rutt B K,Peters T M.Rapid combined T1 and T2mapping using gradient recalled acquisition in the steady state.Magn Reson Med,2003,49:515

