酒类主要风味物质对乙醇-水体系中氢键的影响
郑飞云,姜 甜,董建军,单连菊,李 崎,*,顾国贤
(1. 江南大学 教育部工业生物技术重点实验室,江苏 无锡 214122;2.青岛啤酒股份有限公司科研中心,山东 青岛 266101)
酒类主要风味物质对乙醇-水体系中氢键的影响
郑飞云1,姜 甜1,董建军2,单连菊2,李 崎1,*,顾国贤1
(1. 江南大学 教育部工业生物技术重点实验室,江苏 无锡 214122;2.青岛啤酒股份有限公司科研中心,山东 青岛 266101)
研究酒类主要风味物质对乙醇-水体系中的氢键缔合影响。Plackett-Burman试验可知,异丁醇、β-苯乙醇、乙酸乙酯、KCl、NaCl、MgSO4、苹果酸、乳酸、丙酮酸对乙醇-水体系中氢键缔合影响最大。根据相关性分析,酒精度与啤酒中氢键缔合强度的相关系数为0.629,是主要影响因素;原麦汁浓度、异丁醇、氯离子、钾离子、丙酮酸、乳酸与氢键缔合均有一定的正相关性。
氢键;乙醇-水;啤酒;核磁共振(NMR)
氢键是广泛存在的分子级弱作用力,在水及其溶液、醇、羧基溶剂、无机酸、酸碱式盐、碳水化合物、氨和氨合物、酰胺、氨基酸、蛋白质等物质中扮演着重要角色[1]。含醇体系存在非常复杂的缔合作用,包括醇自缔合、与水缔合及与其他化合物交叉缔合。醇水溶液中,1H-NMR化学位移能反映水水、水醇、醇醇之间氢键结构的一般特性和氢键所处环境[2]。氢键X—H…Y形成时,由于质子接受体(Y)存在,形成的静电场将H拉向Y,而将X—H键的电子推向X,使H周围电子云密度降低,去屏蔽效应增加,因此质子化学位移向低场移动[3]。
乙醇和水都是缔合液体,分别具有不同的缔合结构群,混合后形成新的缔合结构[4-6],随乙醇-水物质的量浓度及温度等不同而变化,其缔合程度可用1H-NMR谱中质子化学位移来量度,质子化学位移越大,缔合度越大[7]。Coccia等[5]认为在水中加入少量醇会强化氢键缔合,并形成新的醇水氢键。当乙醇物质的量分数(f)增加到0.25<f<0.75甚至更高(>0.8)时,会破坏水结构。25℃乙醇水溶液中,乙醇体积分数为20%时的物质的量分数为0.077,此时水分子缔合度最高。乙醇体积分数为20%水溶液中,几乎所有盐类(除了MgCl2和KF)都会减弱氢键缔合,使化学位移向高场移动[2]。通过1H-NMR化学位移发现:酸能解离出质子并加强醇水氢键缔合[2],而共轭基团阴离子(质子受体)可以结合解离出的质子[2]。酚类物质能促进醇水之间质子交换,苯酚和焦酚能使羟基质子峰向低场微弱移动,而多酚和苯羧基酸能使羟基质子峰向低场强烈移动[2],均能不同程度加强醇水溶液中氢键缔合。
酒精饮料是一种具有特殊风味和口感的醇水溶液。根据国内外对白酒[8]、米酒[9]、蒸馏酒[10]、日本清酒[11]、威士忌[12]等酒的研究,醇、水结构变化对酒类口感有较大影响[11],酒入口刺激感降低,变得柔和绵软,与醇水结构变化有关,而醇水含量和结构又与氢键缔合有关[13]。啤酒中乙醇和水约占95%,其混合体系主要以氢键形式发生缔合[13]。当然,由于啤酒中醇、酯、酚、酸等物质含有大量强极性氢原子和电负性大的氧原子,也能形成大量的氢键[14]。目前人们只是初步确定醇、酯、有机酸、离子等对醇水氢键缔合有一定影响,但并未确定对氢键缔合影响的主次和差异。本实验主要研究各风味物质对乙醇-水和啤酒体系氢键缔合影响的大小,旨在为酒精饮料中氢键缔合的研究提供参考。
1 材料与方法
1.1 材料与试剂
市售35种不同品牌啤酒。
草酸、α-酮戊二酸、柠檬酸、琥珀酸、酒石酸、丙酮酸、苹果酸、乳酸、乙酸、乙酸乙酯、正丙醇、异丁醇、β-苯乙醇、乙酸异戊酯、异戊醇、甲醇、DSS[(CH3)3Si-(CH3)3-SO3Na]、3-庚酮均为色谱级;无水乙醇(纯度99.7%)、30%硫酸锌溶液、15%亚铁氰化钾溶液、硝酸银、盐酸、氯化钡、氯化钠、浓硝酸、超纯水、KCl、MgSO4、MgCl2、Na2SO4、K2SO4、CaCl2、NaOH、D2O均为化学纯。
1.2 仪器与设备
Avance AV-500型核磁共振波谱仪 瑞士Bruker公司; Shimadzu GC-2010气相色谱仪 日本岛津公司;高效液相色谱和Sep-Pak C18Cartridge样品处理柱 美国Waters公司; SpectraAA220原子吸收分光光度计 美国Varian公司;K、Na、Mg、Zn、Ca空心阴极灯 北京威格拉斯有限公司;PHS-3C型精密pH计;UV-2000分光光度计。
1.3 方法
1.3.1 乙醇-水体系的制备
用超纯水将99.7%的无水乙醇调配成质量分数为3.5%的乙醇溶液,依Plackett-Burman试验要求,分别在3.5%乙醇溶液中添加不同量的有机酸、高级醇和酯、盐类物质,制备不同风味物质含量的乙醇-水体系。
1.3.2 啤酒体系的NMR测定
35种啤酒样品(表1)经过滤脱气处理,将样品和D2O加到12cm一端封口熔点毛细管内,置于Avance AV-500型核磁共振波谱仪核磁检测测定。测定条件:氢核共振频率500.130MHz;5mm QNP(四核探头13C-1H-31P-19F)探头;D2O锁场;内标物质DSS[(CH3)3Si-(CH2)3-SO3Na];检测温度18℃。

表1 35种市售啤酒的特性Table 1 Characteristics of 35 kinds of beer samples
1.3.3 高级醇和酯的测定
静态顶空自动进样气相色谱检测,在顶空瓶中加入1.8g NaCl和4mL啤酒样品,并加入1mL 30mg/L内标3-庚酮,在水浴锅中微热使NaCl充分溶解。
色谱分析条件:色谱柱CP-WAX 52 CB(30m× 0.32mm,0.52μm);载气N2;色谱柱室温40℃保持2min,以10℃/min升到180℃保持4min;气化室温度200℃;检测室温度250℃;进样时间0.04min;顶空瓶平衡时间30min;顶空瓶平衡温度70℃;传输线温度130℃。
1.3.4 无机离子的测定
参照文献[15]的方法测定。
1.3.5 有机酸的测定
采用高效液相色谱法[16]。
1.3.6 酒精度、原麦汁浓度、真实麦芽汁浓度、总酸的测定
参照文献[17]的方法测定。
2 结果与分析
2.1 风味物质对乙醇-水体系氢键的影响
Plackett-Burman试验设计是一种二水平的部分因子设计方法,基于非完全平衡块原理,能用最少试验次数估计出因素的主效应,从众多的考察因素中快速有效地筛选出最为重要的几个因素。以Nose等[2]报道的成分为单因素,结合啤酒中的含量范围进行Plackett-Burman试验。

表2 有机酸的Plackett-Burman试验设计及响应值表Table 2 Experimental design and response values of Plackett-Burman for organic acids
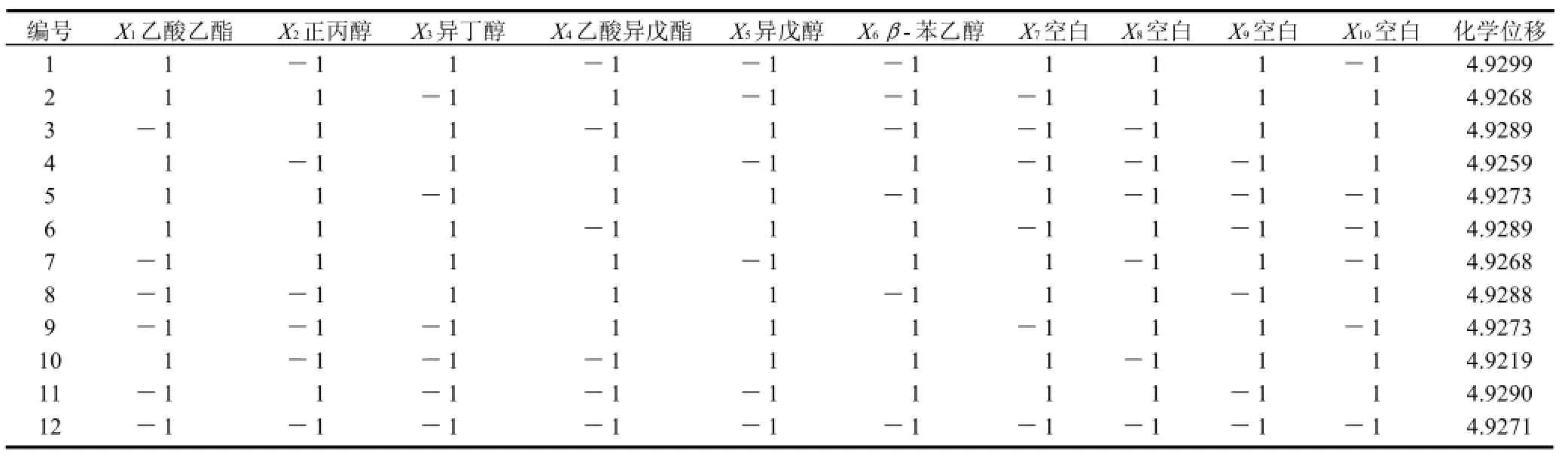
表4 醇和酯的Plackett-Burman试验设计及响应值表Table 4 Experimental design and response values of Plackett-Burman for alcohol and ester
2.1.1 有机酸对乙醇-水氢键的影响
大多数有机酸均能不同程度地促进乙醇-水体系中氢键的缔合,但在混合体系中并不知道究竟是哪些有机酸对氢键的缔合起主要作用,为此,设计n=12的Plackett-Burman试验筛选主要影响因素。试验设计及响应值如表2所示,结果如表3所示。

表3 有机酸试验因素水平及其主效应分析Table 3 Factors, levels and major response-effect analysis of Plackett-Burman experiments for organic acids
由表3可知,有机酸相关性大小排序为:苹果酸、乳酸、丙酮酸、乙酸、酒石酸、柠檬酸、琥珀酸,决定系数R2为95.93%,前3个因素的可信度都在80%左右,即有机酸中苹果酸对乙醇-水缔合氢键影响最大,乳酸、丙酮酸次之。
2.1.2 高级醇和酯对乙醇-水体系中氢键的影响

表5 醇和酯试验因素水平及其主效应分析Table 5 Factors, levels and major response-effect analysis of Plackett-Burman experiments for alcohol and ester
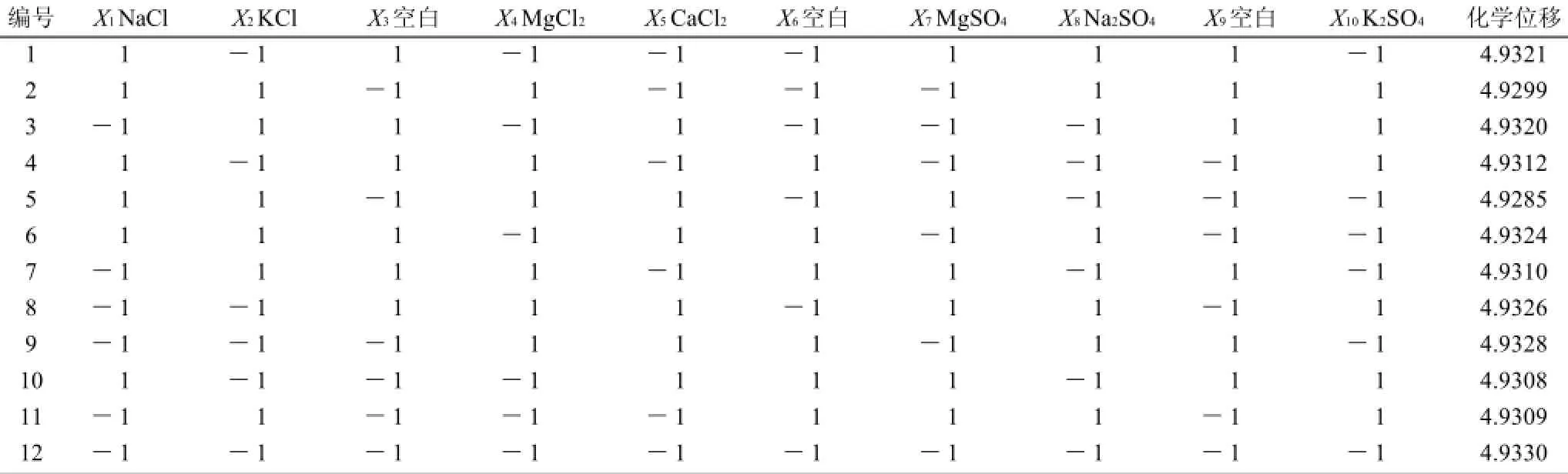
表6 盐类的Plackett-Burman试验设计及响应值表Table 6 Experimental design and response values of Plackett-Burman experiments for salts
醇和酯分子中含有电负性大的氧原子,易于形成氢键,并且能对乙醇和水之间的羟基氢键产生影响。设计n=12的Plackett-Burman试验筛选主要影响因素。试验设计及响应值如表4所示,结果如表5所示。
由表5可知,醇和酯相关性大小排序为:异丁醇、β-苯乙醇、乙酸乙酯、正丙醇、乙酸异戊酯、异戊醇,决定系数R2为89.09%,前3个因素的可信度在80%左右,即异丁醇对乙醇-水体系中氢键的影响最大,β-苯乙醇、乙酸乙酯次之。
2.1.3 盐类对乙醇-水体系中氢键的影响
大部分的盐类除了(MgCl2和KF)都会减弱氢键结构的缔合,使化学位移向高场处移动。盐类对乙醇-水体系中氢键结构的影响与结晶离子半径和离子电荷有关。设计n=12的Plackett-Burman试验筛选主要影响因素。试验设计及响应值如表6所示,结果如表7所示。
由表7可知,盐类相关性大小排序为:K C l、NaCl、MgSO4、MgCl2、Na2SO4、K2SO4、CaCl2,决定系数R2为97.91%,前3个因素的可信度在85%左右,即盐类物质中KCl对乙醇-水体系中缔合氢键的影响最大,NaCl、MgSO4的影响次之。

表7 盐类试验因素水平及其主效应分析Table 7 Factors, levels and major response-effect analysis of Plackett-Burman experiments for salts
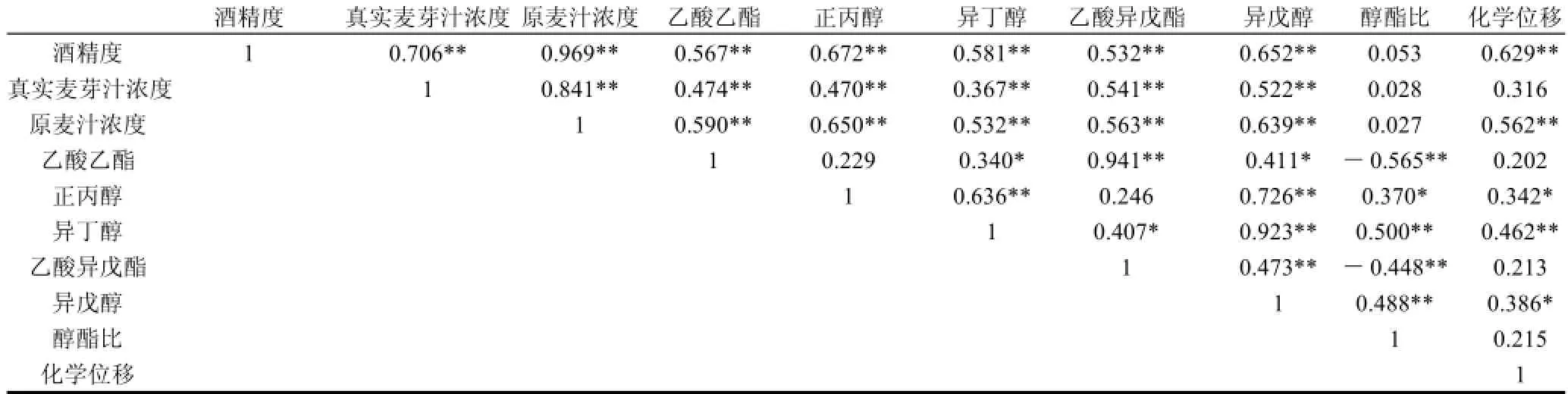
表8 醇和酯含量与质子化学位移的Pearson相关矩阵(相关系数)Table 8 Pearson correlation matrix of alcohol and ester contents to proton chemical shift
2.2 风味物质对啤酒体系缔合氢键的影响
2.2.1 醇和酯与啤酒体系氢键缔合的相关性
以1.3.3节和1.3.6节的实验方法测定35种啤酒中的乙酸乙酯、正丙醇、异丁醇、乙酸异戊酯、异戊醇、酒精度、真实麦芽汁浓度、原麦汁浓度,并以其为自变量。用1.3.2节的方法测定35种啤酒中质子化学位移,并以其为因变量。用SPSS软件做Pearson相关分析,结
果见表8。啤酒中质子化学位移与酒精度的相关性系数为0.629,且在0.01水平上显著,说明酒精度是影响质子化学位移的主要因素,因为乙醇是啤酒中除水外含量最多的成分,且乙醇分子较小,空间结构简单,含有强极性的羟基质子和电负性大的氧原子。原麦汁浓度、异丁醇、异戊醇、正丙醇与质子化学位移有较大的正相关性,酯类物质与质子化学位移的相关性较小,推测可能是与它们特有的羟基和羰基结构有关。
为了更加直观的反映各单因素对啤酒羟基质子缔合的影响,考察醇和酯各主要因素与羟基质子化学位移的相关性拟合曲线及方程,结果见图1~3。酒精度、原麦汁浓度、异丁醇质量浓度均与质子化学位移呈正相多项式相关,拟合度分别为0.7487、0.6672、0.6362,说明该方程能较好的拟合自变量与因变量之间的关系。

图1 酒精度与质子化学位移相关性拟合曲线Fig.1 Fitting curve between alcohol concentration and proton chemical shift
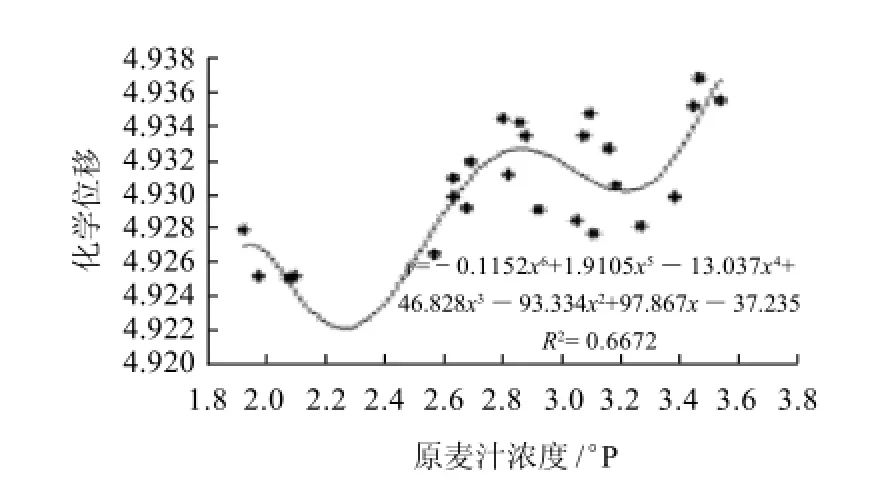
图2 原麦汁浓度与质子化学位移相关性拟合曲线Fig.2 Fitting curve between original wort concentration and proton chemical shift
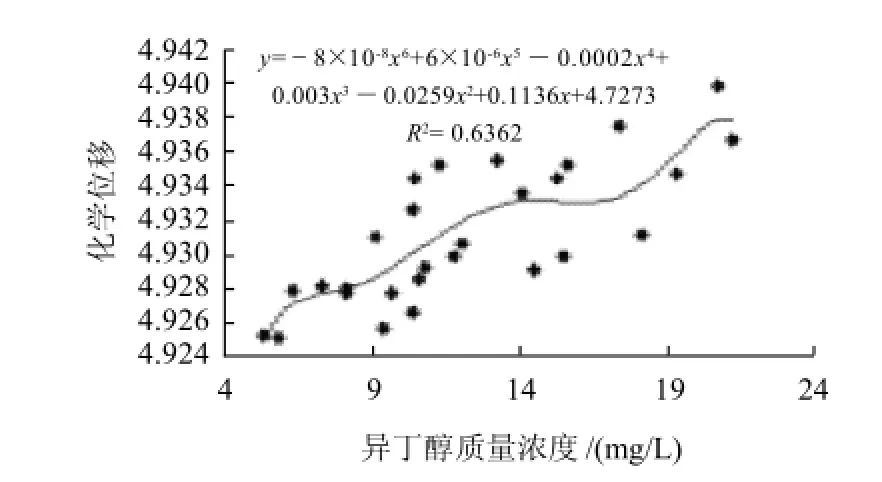
图3 异丁醇质量浓度与质子化学位移相关性拟合曲线Fig.3 Fitting curve between isobutanol and proton chemical shift
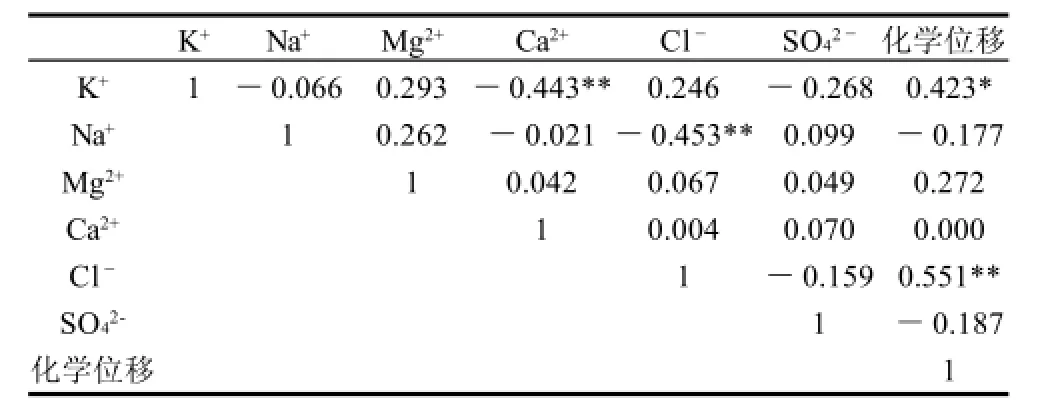
表9 无机离子质量浓度与质子化学位移的Pearson相关矩阵(相关系数)Table 9 Pearson correlation matrix of inorganic ion contents to proton chemical shift
2.2.2 无机离子与啤酒体系氢键缔合的相关性
以1.3.4节的方法测定35种啤酒的K+、Na+、Mg2+、Ca2+、Cl-、SO42-无机离子,以其为自变量。用1.3.2节的方法测定35种啤酒中质子化学位移,以其为因变量,用SPSS软件做Pearson相关分析,结果见表9。质子化学位移与Cl-、K+有较大的正相关性,而SO42-、Na+成负相关性,与Mg2+、Ca2+的相关性较小,推测无机离子对啤酒中氢键结构的影响与结晶离子半径和离子电荷有关。
为了更加直观的反映各单因素对啤酒羟基质子缔合的影响,考察无机离子各主要单因素与羟基质子化学位移的相关性拟合曲线及方程,结果见图4、5。C l-、K+均与质子化学位移成正相多项式相关,拟合度分别为0.562、0.5364,说明该方程能较好的拟合自变量与因变量之间的关系。
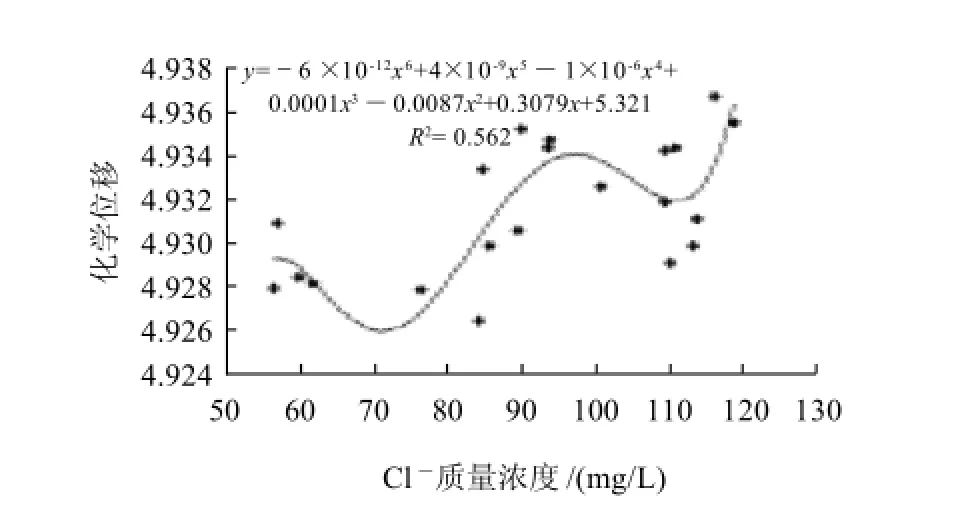
图4 Cl-质量浓度与质子化学位移相关性拟合曲线Fig.4 Fitting curve between Cl-and proton chemical shift
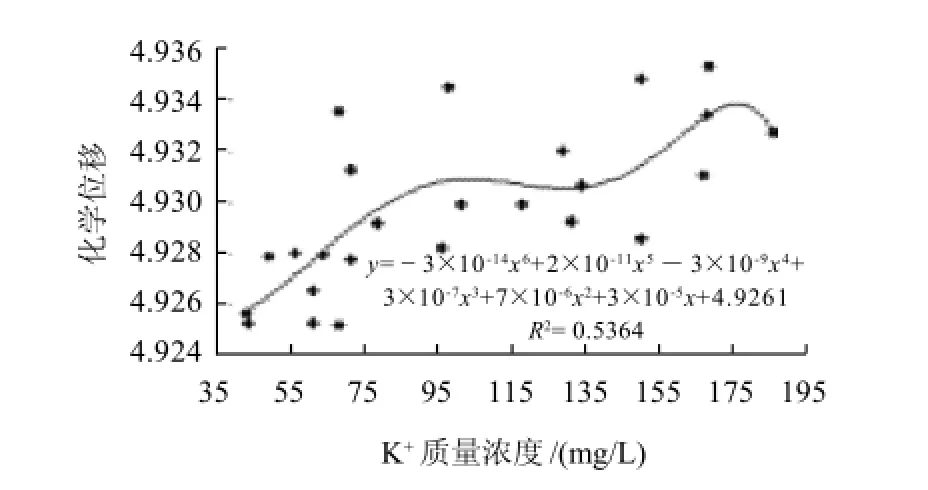
图5 K+质量浓度与质子化学位移相关性拟合曲线Fig.5 Fitting curve between K+and proton chemical shift
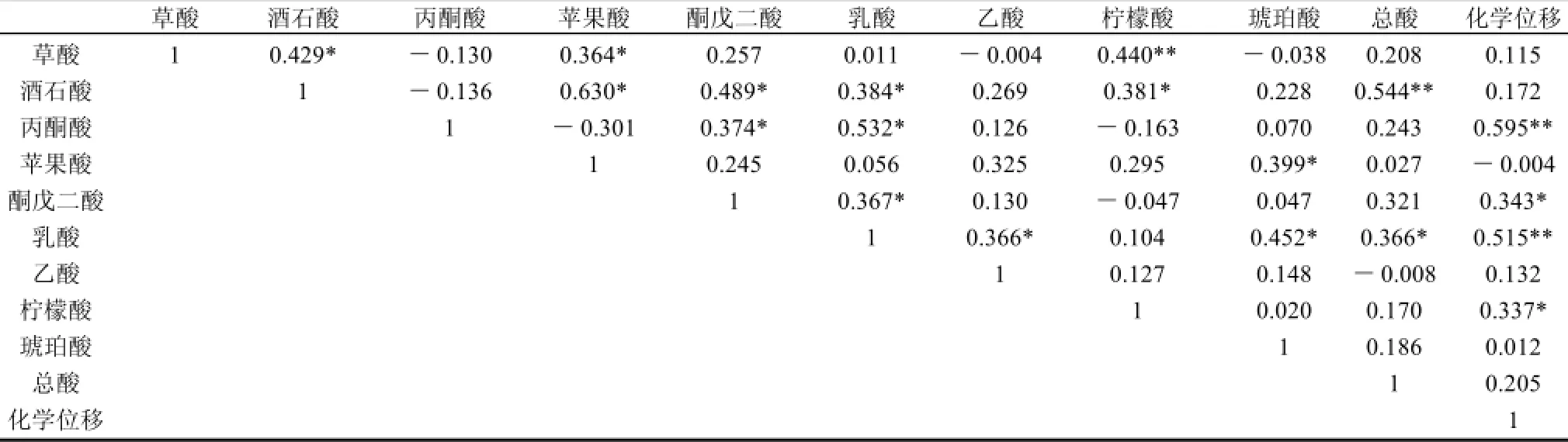
表10 有机酸含量与质子化学位移的Pearson相关矩阵(相关系数)Table 10 Pearson correlation matrix of organic acid contents to proton chemical shift
2.2.3 有机酸与啤酒体系氢键缔合的相关性
以1.3.5、1.3.6节的方法测定35种啤酒中9种有机酸和总酸含量,以其为自变量。用1.3.2节的方法测定35种啤酒的质子化学位移,以其为因变量,用SPSS软件做Pearson相关分析,结果见表10。
由表10可知,啤酒中质子化学位移与丙酮酸的相关系数为0.595,在0.01水平上极显著,说明丙酮酸也是影响啤酒氢键缔合的重要因素,因为丙酮酸分子结构简单,具有弱酸性的羧基和极性较大的羰基,并且其羧羟基质子容易解离,易于形成较稳定的强氢键;与乳酸的相关性系数为0.515,在0.01水平上显著,对啤酒氢键缔合也有较大的影响,乳酸分子中含有弱酸性易解离的羧基和醇羟基,也易于氢键的形成;与柠檬酸和酮戊二酸有较小的正相关性,与其他酸的相关性并不大。推测酸类物质影响羟基质子化学位移的变化可以归结为未解离的酸分子(HA)和解离的H+。同时,酸类物质对质子化学位移的作用在一定程度上取决于酸度,酸通过解离出质子(质子供体)使乙醇-水体系中氢键缔合加强,而共轭基团阴离子(质子受体)可以结合解离出的质子。
为了更加直观的反映各单因素对啤酒羟基质子缔合的影响,考察有机酸的各主要因素与羟基质子化学位移的相关性拟合曲线及方程,结果见图6、7。

图6 丙酮酸质量浓度与质子化学位移相关性拟合曲线Fig.6 Fitting curve between pyruvic acid and proton chemical shift
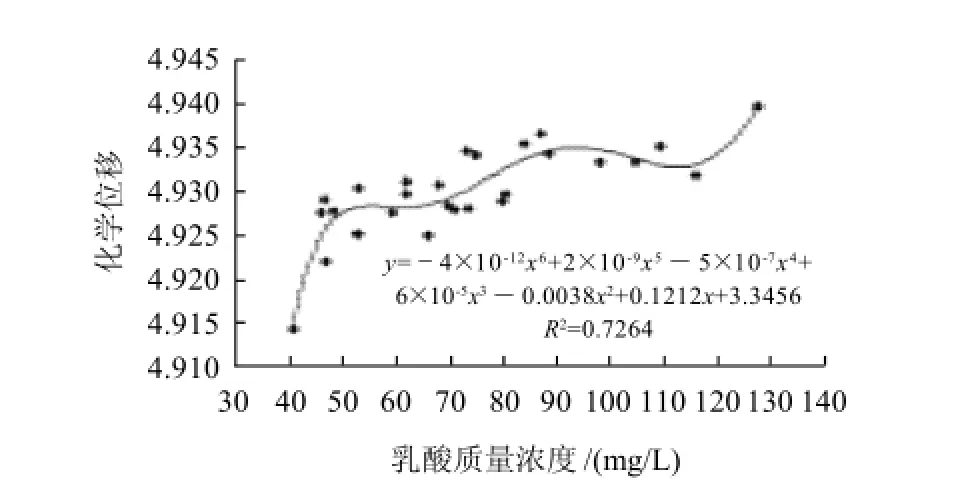
图7 乳酸质量浓度与质子化学位移相关性拟合曲线Fig.7 Fitting curve between lactic acid and proton chemical shift
丙酮酸、乳酸均与质子化学位移成正相多项式相关, 拟合度分别为0.7237、0.7264,说明该方程能较好的拟合自变量与因变量之间的关系。
3 结 论
3.1 由Plackett-Burman试验可知,高级醇和酯对乙醇-水体系氢键缔合影响大小排序为:异丁醇、β-苯乙醇、乙酸乙酯、正丙醇、乙酸异戊酯、异戊醇,决定系数R2为89.09%,前3个因素可信度在80%左右。有机酸对乙醇-水体系氢键缔合影响大小排序为:苹果酸、乳酸、丙酮酸、乙酸、酒石酸、柠檬酸、琥珀酸,决定系数R2为95.93%,前3个因素可信度在80%左右。盐类对乙醇-水体系氢键缔合影响大小排序为:KCl、NaCl、MgSO4、MgCl2、Na2SO4、K2SO4、CaCl2,决定系数R2为97.91%,前3个因素可信度在85%左右。
3.2 啤酒中质子化学位移与酒精度相关性系数为0.629,在0.01水平上显著,说明酒精度是影响质子化学位移的主要因素。原麦汁浓度、异丁醇、异戊醇、正丙醇与质子化学位移有较大的正相关性,酯类物质与质子化学位移的相关性较小。啤酒中质子化学位移与Cl-、K+有较大正相关性,而与SO42-、Na+成负相关性,与Mg2+、Ca2+相关性较小。啤酒中质子化学位移与丙酮酸和乳酸
的相关系数分别为0.595和0.515,在0.01水平上显著,说明它们是影响啤酒氢键缔合的重要因素;与柠檬酸和酮戊二酸正相关性较小,与其他酸相关性不大。
3.3 各风味物质对乙醇-水体系和啤酒体系羟基质子氢键缔合的影响大小并不完全相同,高级醇和酯中异丁醇对两种体系均有较大影响;离子中Cl-、K+对两种体系均有较大影响;有机酸中丙酮酸、乳酸对两种体系均有较主要影响,而其他物质对两种体系的影响各不相同。推测啤酒体系是由大量物质组成的胶体,氢键缔合强度受各种物质的相互影响,是相互作用的结果,与乙醇-水体系有所不同。
[1]张广宏, 马文霞, 万会军. 氢键的类型和本质[J]. 化学教学, 2007(7)∶72-75.
[2]NOSE A, HOJO M. Hydrogen bonding of water-ethanol in alcoholic beverages[J]. Journal of Bioscience and Bioengineer, 2006, 102(4)∶ 269-280.
[3]HINDMAN J C. Proton resonance shift of water in the gas and liquid states[J]. J Chem Phys, 1966, 44(6)∶ 4582-4592.
[4]WEIRBERG L, ZIMMORMANN J R. Concentration dependence of chemical exchange and NMR multiple structure in water-ethanol mixtures [J]. J Chem Phys, 1995, 23(3)∶ 748-761.
[5]COCCIA A, INDOVINA P L, PODO F, et al. NMR studies on the stuctures of water-ethyl alcohol mixtures[J]. J Chem Phys, 1975, 7(5)∶30-40.
[6]POPLE J A, SCHEIDER W G, BEMSTEIN H J. High resolution nuclear magneti resonance[M]. Now York∶ McGraw-Hill Press, 1959, 13 (5)∶ 130-145.
[7]李才广. 略论白酒陈酿与其质量的关系[J]. 食品与发酵工业, 1989 (4)∶ 75-78.
[8]王夺元, 何慧珠, 张麟华, 等. 白酒中氢键缔合作用的模型研究[J].化学通报, 1985(4)∶ 21-25.
[9]曾新安, 扶雄, 李国基, 等. 电场催陈米酒核磁共振分析[J]. 光谱学与光谱分析, 2004, 24(6)∶ 748-751.
[10]NOSE A. Hydrogen bonding in alcoholic beverages(distilled spirits)and water-ethanol mixtures[J]. J Agric Food Chem, 2005, 53(2)∶ 7074-7081.
[11]NOSE A. Proton nuclear magnetic resonance and raman spectroscopic studies of Japanese Sake, an alcoholic beverage[J]. Journal of Bioscience and Bioengineer, 2005, 99(5)∶ 493-501.
[12]NOSE A. Solute Effects on the interaction between water and ethanol in aged whiskey[J]. J Agric Food Chem, 2004, 52(6)∶ 59-65.
[13]郝荣华. 高稀释率啤酒风味柔和性与协调性研究[D]. 无锡∶ 江南大学, 2007.
[14]姜甜, 李崎, 顾国贤, 等. 啤酒高浓酿造后稀释工艺对体系氢键的影响[J]. 食品工业科技, 2009, 30(3)∶ 143-146.
[15]李鹏飞. 高稀释率啤酒风味柔和性与协调性研究∶ 无机离子对啤酒风味的影响[D]. 无锡∶ 江南大学, 2008.
[16]杨毅, 李崎, 陈蕴, 等. 反相高效液相色谱法(RP-HPLC)测定啤酒中有机酸[J]. 食品与发酵工业, 2003, 29(8)∶ 6-12.
[17]管敦仪. 啤酒工业手则[M]. 北京∶ 中国轻工业出版社, 1985.
Effect of Flavor Substances on Hydrogen Bonds of Water-ethanol System
ZHENG Fei-yun1,JIANG Tian1,DONG Jian-jun2,SHAN Lian-ju2,LI Qi1,*,GU Guo-xian1
(1. Key Laboratory of Industrial Biotechnology, Ministry of Education, Jiangnan University, Wuxi 214122, China;2. Center of Research and Development, Tsingtao Brewery Co. Ltd., Qingdao 266101, China)
The effect of major flavor compounds in wine on hydrogen bonds of water-ethanol system was studied. Plackett-Burman experiments confirmed that hydrogen bonds of water-ethanol system were greatly affected by isobutanol, β-phenylethyl alcohol, ethyl acetate, KCl, NaCl, MgSO4, malic acid, lactic acid and pyruvic acid. Correlation analysis indicated that coefficient between alcohol concentration and hydrogen bond intensity was 0.629. Therefore, alcohol concentration was the primary factor to hydrogen bond intensity although original wort concentration, isobutanol, Cl-, K+, pyruvic acid and lactic acid also exhibited an influence on hydrogen bond intensity to some extent.
hydrogen bond;water-ethanol system;beer;NMR
TS201.2
A
1002-6630(2010)09-0106-07
2009-05-22
郑飞云(1974—),男,讲师,本科,主要从事啤酒风味研究。E-mail:feiyunzh@jiangnan.edu.cn
*通信作者:李崎(1971—),女,教授,博士,主要从事啤酒酿造和风味研究。E-mail:liqi@jiangnan.edu.cn

