半胱胺修饰金电极分离多巴胺和抗坏血酸
汤波,许光日,许明录,张裕平
(河南科技学院,河南新乡 453003)
多巴胺(DA)是脑内独立存在的神经递质,其在纹状体内的含量占全脑的70%以上,脑内多巴胺神经功能失调是精神分裂症和帕金森氏症的最主要原因.此外,多巴胺为拟肾上腺素药,具有兴奋心脏、增加肾血流量的功能,用于心源性先血性及感染性休克治疗.因此对其测定方法的研究,无论是在生理功能研究方面还是在临床应用方面都具有重要的实际意义[1].抗坏血酸(AA)是维护机体正常生理功能的重要维生素之一,广泛存在于蔬菜和水果中,人体不能自身合成.抗坏血酸参与机体氧化、还原等复杂代谢过程,能促进生长和抗体的形成增强免疫活性,所以对抗坏血酸的检测也相当重要.抗坏血酸和多巴胺共同存在于人体内,进行电化学测定时,会相互干扰[2].在裸电极上扫描测定的结果显示,DA和AA的峰电位几乎重合,这就对分别测定AA和DA的工作造成了麻烦,要实现对DA和AA的分离,才能对DA或AA进行精确的电化学研究.
自组装膜修饰电极的研究是当前电化学和电分析化学领域的热门课题之一.自组装膜是分子通过化学键相互作用自发在固/液或气/固界面形成的一种热力学稳定和能量最低的有序膜,具有明晰的微结构且稳定性好.按其形成分子层的层数分类可分为:自组装单层膜、自组装双层膜和自组装多层膜.自组装单层膜具有离子(或分子)识别和呈现选择性的功能[3-6].这种单分子层膜在其它离子共存下能选择性的识别某一指定的离子,因而呈现特定的电极响应.半胱胺分子中含有巯基,能与Au、Ag等配位形成稳定的半胱胺自组装单分子膜修饰电极,对抗坏血酸 (AA)及多巴胺(DA)都有明显的催化作用.本文将半胱胺自组装于金电极表面形成稳定的单分子修饰层,发现该自组装单分子膜修饰金电极对多巴胺和抗坏血酸有明显的分离作用,二者共同存在于同一缓冲溶液中时,用示差脉冲法的扫描结果显示,二者峰电位差达220mV,已达到完全分离.实验发现用这种方法对多巴胺和抗坏血酸进行测定简单、准确、快速,而且灵敏度高.
1 实验
1.1 仪器与试剂
CHI430A电化学分析仪器(上海辰华仪器公司);超声波清洗器;三电极系统:半胱胺自组装膜修饰金工作电极,铂丝对电极,Ag/AgCl参比电极;多巴胺(MERCK-schuchardt);抗坏血酸(ACROSORGANICS New Jersey);无水乙醇;不同pH的缓冲溶液.
1.2 实验方法
1 mmol/L多巴胺标准溶液:准确称取0.0096 g多巴胺,用缓冲溶液溶解定容于50 mL容量瓶中;同法配制1mmol/L抗坏血酸溶液和多巴胺的混合溶液.金电极依次用0.05μmα-Al2O3抛光粉抛光,依次用蒸馏水、乙醇溶液和二次水超声清洗 5min,用二次水冲洗.在1.0mol/L的H2SO4溶液中极化,扫描电压0~1.5 V.置于空气中晾干后立即浸泡20mmol/L的半胱胺水溶液中12 h.每次自组装前均用上述方法处理以更新电极,即得到半胱胺自组装膜修饰金电极[5].电位扫描范围为:-0.2~0.8 V,从-0.2 V开始扫描,扫描速度为100mV/s,记录CV曲线.示差脉冲条件,脉冲电位50mV,脉冲持续50ms,脉冲周期0.2 s.
2 结果与分析
2.1 DA在半胱胺修饰电极和裸电极上的电化学行为
DA峰电位如图1,ΔEp=104mV,修饰电极上峰电流比裸电极上峰电流明显增大,在pH 2.0缓冲溶液中,半胱胺修饰金电极对多巴胺具有电催化作用.
2.2 AA在半胱胺修饰电极上的电化学行为
AA峰在半胱胺修饰金电极上的电位比裸电极负移,ΔEp=280mV.峰电流比在裸金电极上峰电流明显增加,表明在pH=2.0缓冲溶液中,半胱胺修饰金电极对AA的电化学氧化具有明显电催化作用(见图 2).
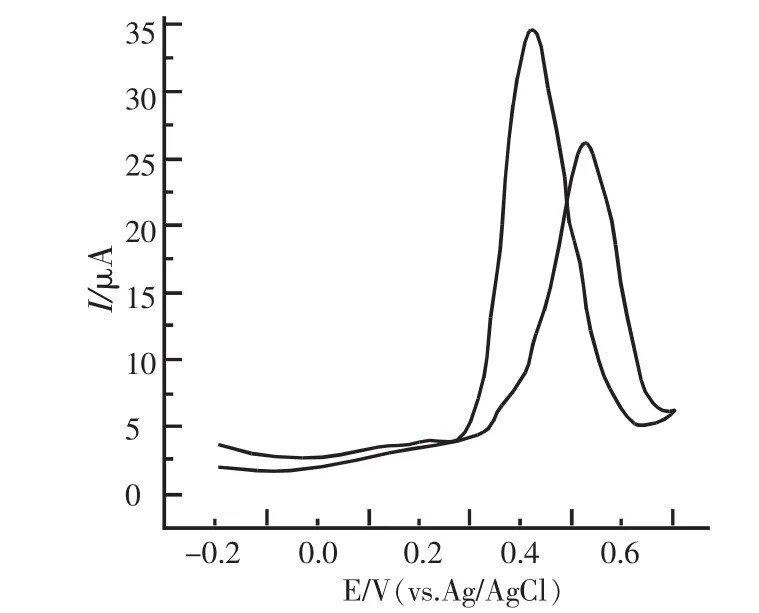
图1 1.0mmol/LDA缓冲液(pH 2.0)在裸金电极(a)和半胱胺修饰电极(b)上示差脉冲

图2 1.0mmol/LAA在半胱胺修饰金电极(a)和裸金电极(b)上的示差脉冲(pH 2.0)
导致峰电位负移的催化作用可从微观角度阐述:AA的离子参加电化学反应,修饰电极上携带许多表面具有正电荷的功能基团(如-NH2等),这些亲水的富氧基团增强了对AA的静电排斥力,导致AA的峰电位负移.同样,这种催化作用也降低了出现峰电位的电压门槛,而且大大加强了峰电流,使测量工作变得更加容易.
2.3 pH对半胱胺修饰电极分离DA和AA的影响
配制1×10-4mol/LDA和1×10-3mol/LAA混合的不同pH值缓冲溶液.pH=4.0时,DA、AA在半胱胺修饰电极上的循环伏安图如图3所示.DA和AA的氧化峰电位重叠,DA的阳极峰电位为0.47 V,AA的阳极峰电位为0.30 V,但AA的阳极峰电流受到抑制.在电化学反应中,峰电位与pH是密切相关的.随着PH的增加,DA和AA的峰电位都逐渐负移.这与氧化过程去质子的步骤有关,高的pH有利于反应的进行,但是DA和AA的峰电位差随着pH的升高而降低[7].在pH=7.0时DA的峰电位为0.20 V而AA的峰电位为0.18 V,二者峰电位差很微小,几乎重叠在一起,不能达到分离效果.在pH=4.0的情况下,虽然DA和AA的阳极电位差达到了170mV,由于AA的电流受到抑制,并不能得到完全分离的图形如图3.图4为pH=2.0时DA和AA在裸电极(图4曲线b)半胱胺修饰电极上(图4曲线a)的示差脉冲图.DA峰电位为0.46 V,AA峰电位为0.24 V,二者峰电位差:ΔEp=220mV,已经达到了完全分离.

图3 1.0mmol/LDA,AA在半胱胺修饰电极上的CV图,扫速:100 m V/s

图4 1.0 mmol/L DA和1.0mmol/LAA在半胱胺修饰电极PBS(pH 2.0)中的示差脉冲
半胱胺修饰金电极对DA和AA进行分离的微观原理如下:

式(1)中 R-Ph—(—OH)2为 DA,R—Ph-(=O)2为多巴胺醌,式(2)中 AH2为 AA.由上面两式可知,式(2)为不可逆反应,AA在电位为0.24 V时发生了氧化反应,在电位达到0.46 V时DA发生氧化反应.AA和DA就这样先后发生反应,而且互不影响,宏观上就得到了完全分离的峰.
综合以上实验得知,pH=2.0的0.1mol/L缓冲溶液是半胱胺修饰金电极分离DA和AA的最佳pH条件.峰位差能达到220mV,已经实现完全分离.因此,测定DA和AA的最佳pH值是2.0.
3 结论
半胱胺修饰金电极对pH=2.0的AA与DA磷酸盐缓冲液反复进行测定20次,测定结果的相对标准偏差分别为3.4%和2.8%,电极重现性好,对DA和AA有明显的催化作用.修饰电极放置在空气中两星期后,自组装膜被空气中氧气氧化,对AA的催化作用降低,但对AA及DA仍能分离.综上所述,半胱胺修饰金电极能很好的分离DA和AA,且有很好的稳定性和重现性.
[1]Ju Chou,Terri J.Ilgen,ScottGordon etal.Investigation of the enhanced signals from cations and dopamine in electrochemical sensors coated with Nafion[J].Journal of Electroanalytical Chemistry,2009,632(1-2):97-101.
[2]Nien PC,Chen PY,Ho K C.On the amperometric detection and electrocatalytic analysis of ascorbic acid and dopamine using a poly(acriflavine)-modified electrode[J].Sensors and ActuatorsB:Chemical,2009,140(1):58-64.
[3]李海英,张浩力,张锦,等.新型偶氮苯硫醇衍生物自组装膜的制备与结构表征[J].物理化学学报,2004,15(3):197-198.
[4]王俊,曾百肇,周性尧.自组装膜技术在电分析化学中的应用[J].分析科学学报, 2003,16(3):253-258.
[5]王升富,杜丹,蔡火操,等.L-半胱氨酸自组装膜电极对米吐尔的电催化及其分析应用[J].分析化学,2001,29(11):1288-1291.
[6]董献堆,陆君涛,查全性.逐层自组装修饰金电极[J].电化学,1995,1(1):25-29.
[7]汪海燕,柳鹏,王晔,等.纳米金双巯基修饰金电极差分脉冲伏安法测定多巴胺和抗坏血酸[J].电化学,2007,13(2):127-131.

