45例血塞通药品不良反应回顾性分析
邹 薇,徐月萍,吴海雯
(1.浙江省慈溪市人民医院,浙江 宁波 315300; 2.浙江省宁波市药品不良反应监测中心,浙江 宁波 315040)
血塞通的主要成分为三七总皂苷,药理作用主要有扩张血管,增强冠脉血流量,降低心肌耗氧量,抑制血小板聚集、降低血黏度,临床主要用于治疗中风偏瘫、瘀血阻络证,动脉粥样硬化性血栓性脑梗死、脑栓塞、视网膜中央静脉阻塞见瘀血阻络证。笔者就血塞通引起的药品不良反应(ADR)进行了分析,旨在探讨其ADR的发生特点,为临床合理安全用药提供参考。
1 资料与方法
从全国药品不良反应监测网络下载2007年1月至2008年8月由宁波市16家医疗机构上报且经省中心评价的血塞通ADR报告45例,根据患者性别、年龄、ADR累及器官及临床表现等进行回顾性分析。
2 结果
2.1 患者一般情况
45例 ADR患者中,男 23例(51.11%),女22例(48.89%),男女比例接近1∶0.96。患者年龄、性别分布见表1。发生ADR的患者年龄主要在50岁以上(占53.33%),说明血塞通ADR在中、老年人群发生率相对较高。患者原患疾病为骨折25例(55.56%),供血不足5例(11.11%),冠状动脉硬化性心脏病、偏头痛及眩晕各3例(6.67%),高血压及高血脂、腰椎间盘脱出、外伤各 2例(4.44%),脑动脉硬化、脑梗死、不详各1例(2.22%)。
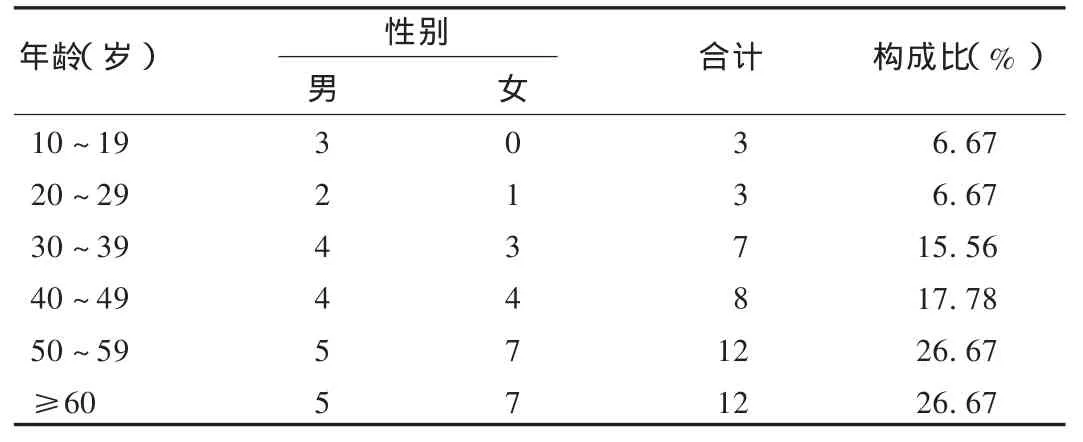
表1 患者年龄性别分布[例(%)]
2.2 ADR情况
ADR程度分级及转归:45例ADR报告中,新的严重ADR 4例(8.89%),严重的 ADR 5例(11.11%),新的一般的 ADR 11例(24.44%),三者占总数的44.44%;一般的ADR 25例(55.56%)。45例 ADR 中,治愈 21例(46.67%),好转 24例(53.33%);22例(48.89%)是停药后未经治疗好转或治愈,23例(51.11%)是停药后经对症及时治疗后好转或治愈的;对原患疾病影响不明显44例(97.78%),病程延长1例(2.22%)。
ADR发生时间分布:45例ADR中,在使用过程中或使用当天发生的 23例(51.11% ),在用药第 2天发生的13例(28.89% ),≥3 d出现的 6例(13.33% ),≥7 d出现的 3例(6.67% );出现ADR时间最短为首次使用后5 min即出现,最迟为连续用药至16 d后才发生。过敏性休克等严重的ADR多在使用过程中或使用当天发生。
累及系统-器官及主要临床表现:见表2。

表2 ADR累及系统-器官分类统计
2.3 药品情况
45例ADR中,药品剂型为注射剂43例(95.56%),胶囊剂、片剂各1例(2.22%);涉及生产厂家7家,涉及生产批号25个,其中有2个批号产品引起的ADR例数分别为5例(11.11%)和6例(13.33%),类似群体性ADR。具体见表3。

表3 ADR涉及的生产厂家统计
2.4 用药情况
用药剂量:43例静脉滴注引起的ADR中,用量为800 mg/次21 例(48.84%),用量为 500 mg/次 1 例(2.33%),用量为 400 mg/次20 例(46.51%),用量为 200 mg/次 1 例(2.33%)。
合并用药:45例ADR中,单一用药32例(71.11%),合用1种6例 (13.33% ),合用 2种 4例 (8.89% ),合用 3种以上 3例(6.67%),其中最多1例是7种药物并用。
给药途径:静脉滴注43例(95.56%),口服2例(4.44%)。
稀释用输液:45例ADR中,18例(40%)是5%葡萄糖注射液,5例(11.11%)是果糖注射液,4例(8.89%)是0.9%氯化钠注射液,16 例(35.56%)不详。
3 ADR原因分析
3.1 药物方面
ADR发生率与剂型有一定的关系,血塞通的多种剂型及给药途径均可引起过敏反应,以注射剂多见。中药注射剂物理性质变化主要是由酸碱度的改变所致[1]。当变化后的pH不在有效成分稳定的pH范围内时,有效成分则会变质或溶解度降低而沉淀。pH对微粒的影响也较大。2005年版《中国药典(一部)》规定的血塞通注射液pH范围为5.0~7.0,5%葡萄糖注射液的pH范围为3.2~5.5,果糖注射液pH范围为3.5~5.8,0.9%氯化钠注射液pH值范围为4.5~7.0。在实际应用中,由于输液生产厂家或批号不同,pH会有所不同,上述3种输液配伍都可能引起ADR。因此配置输液时,应注意药物配伍时的不溶性微粒情况。
3.2 临床使用
剂量过大是引起ADR的原因之一,45例ADR中有24例(53.33%)是超说明书剂量使用(说明书规定静脉注射一次200~400 mg)。联合用药在临床上普遍存在,且中药和西药的配伍应用相当普遍,有的能提高疗效,有的则降低疗效甚至产生毒性、导致药源性疾病[2]。45例ADR中有13例 (28.89%)是合并用药引起的,并用的药物既有中药又有西药,以西药为多,与抗生素并用者有4例。在2例过敏性休克中,有1例为血塞通注射液和盐酸消旋山莨菪碱合用引起。因此,提醒临床应尽可能单独使用血塞通注射液。
3.3 患者方面
血塞通的ADR在高年龄组发生率较高,且再次或反复数次用药后发生率高(48.89%)。这与用药原因及老年人体质下降、对药物的敏感性增加而易发生ADR有关,临床应重点观察老年人群用该药时的反应。另外,含三七总皂苷类注射剂所致ADR具有速发性,这主要包括过敏性休克等严重ADR,但对迟发性的ADR也要关注,以免漏报。提示临床医护人员对首次用药过程应认真观察,以便及早发现、及时处理,防止严重ADR的发生。
3.4 说明书
查阅血塞通的说明书时发现:一是不写或漏写ADR,如对于最常见的ADR(发热、寒战、过敏性休克、恶心),很多文献[3-6]都有记载,但说明书中却没有任何描述;二是描述不全,如ADR项描述为“偶见有皮疹,个别病人出现咽干、头昏和心慌症状,停药后均能恢复正常”。很多ADR是停药后经对症及时治疗后好转或治愈的。药品说明书是药物信息最基本、最重要的来源,是指导临床用药的主要依据,并具有法律效应,简单而内容不完全的说明书往往会误导患者,影响医生用药和ADR治疗。
4 建议
随着血塞通的ADR报告增多,首先医护患三者均应提高警惕性,临床使用的应掌握用药指征,注意用法用量,对用药过程密切观察,如出现ADR立即停药并对症处理;其次,生产厂家应不断改进工艺,尽可能除去多余的杂质和微粒,提高药物纯度;再次,监管部门应加强规范管理,提高并统一药品质量标准;督促企业及时修订、补充和完善药品说明书,切实保障公众用药安全。
[1]赵新先.中药注射剂学[M].广州:广东科学技术出版社,2000:610,238,611.
[2]徐冬英.中西药配伍疗效的研究[J].医药论坛杂志,2004,25(2):10.
[3]陈套红,吕复清.血塞通静脉滴注致过敏性休克1例[J].中国药物与临床,2003,3(3):213.
[4]陆 妙,黎 涛.我院16例血塞通注射液致不良反应回顾性分析[J].中国药房,2007,18(14):1 103.
[5]曾聪彦,梅全喜.81例含三七总皂苷类注射剂致不良反应的文献分析[J].中国药房,2007,18(33):2 616-2 618.
[6]徐冬英,黄海滨.三七及其制剂的不良反应分析[J].中国中药杂志,2005,30(18):1 465.

