二氧化碳和甲醇直接合成碳酸二甲酯的研究进展*
孟跃中,陈惠玲,肖 敏,王拴紧,韩冬梅
(中山大学低碳化学与过程节能广东省重点实验室, 广东 广州 510275)
碳酸二甲酯(DMC)分子中含有甲基、甲氧基、羰基和羰基甲氧基等基团,化学性质活泼,氧含量高达53.3%。DMC可以作为一种清洁的有机化学试剂使用,一方面可替代光气、硫酸二甲酯、氯甲烷及氯甲酸甲酯等剧毒或致癌物进行羰基化、甲氧基化、甲酯化及酯交换等反应生成多种重要化工产品;另一方面,以DMC为原料可以开发、制备多种高附加值的精细专用化学品,在医药、农药、合成材料、燃料、润滑油添加剂、食品增香剂、电子化学品等领域都有广泛的应用[1];更为重要的是,由于氧含量高、相容性好,可用作低毒溶剂和燃油添加剂[2-3]。DMC是近年来受到国内外广泛关注的环保型绿色化工产品,已被欧盟等国际组织列为无毒溶剂,被我国列入国家“九五”重点开发的50个精细化工品种之一。因此,DMC具有重要的应用价值和广阔的市场前景。
二氧化碳(CO2)是主要的工业排放物,是引起全球温室效应的主要物质,但又是一种潜在的碳资源。对环境和能源枯竭问题日益重视的今天,CO2的有效固定和利用引起越来越多研究者的关注,其中之一就是以CO2为原料合成DMC的研究。目前,CO2和甲醇直接合成DMC还未达到工业化应用的程度,其主要原因是:①CO2的活化困难;②反应生成的水易使催化剂失活;③反应的热力学限制。
CO2和甲醇直接合成DMC反应中依甲醇相态变化分以下两种:
(1)
(2)
据文献[4-5]热力学数据,反应式(1)合成反应热效应和吉布斯自由能为:
ΔrHθ=-613.78-285.83-2(-239.10)+393.51=-27.90 kJ/mol
ΔrGθ=-457.78-237.14+394.38-2(-166.60)=32.66 kJ/mol
反应式(2)合成反应热效应和吉布斯自由能为:
ΔrHθ=-569.69-241.83-2(-201.25)+393.51=-15.51 kJ/mol
ΔrGθ=-464.23-228.59+394.38-2(-161.92)=25.40 kJ/mol
由以上热力学函数变化值可知无论甲醇以液相或气相参与合成反应,该反应都是放热反应,且吉布斯自由能均为正值,因此,从热力学观点考虑高温下不利于DMC的合成,而提高压力则有利于反应的自发进行。
1 催化剂体系
1.1 均相催化体系
1.1.1 烷氧基金属有机化合物 烷氧基金属有机化合物主要集中在有机锡、钛烷氧基化合物及甲氧基金属化合物,其中以有机锡、钛烷氧基化合物[Bu2Sn(OEt)2,Sn(OMe)4,Sn(OBu)4,Ti(OMe)4,Ti(OBu)4]等的研究较早[6],而甲氧基金属化合物一般为甲氧基铌[7-8]、甲氧基钾[9]、甲氧基镁和甲氧基钙等[10]。
Kizlink等[11-12]探讨了一系列有机锡化合物Bu2SnX1X2[X1=OMe, OEt, OBu, Cl, Br, OPh, OOCMe, OOC(CH2)10Me, SSNET2; X2= O, (OH, Cl)]对CO2和甲醇合成DMC反应的影响,得出Bu2Sn(OR)2(R = Me, Et, Bu)为最有效的催化剂,反应在130~190 ℃间进行,DMC产率为有机锡化合物的60%~220%(摩尔比),提出的反应机理如下:
Bu2Sn(OMe)2+(MeO)2CO+H2O
机理认为CO2通过插入烷氧基金属有机化合物中的金属-氧键之间得以活化,这种活性中间体则进一步与甲醇作用,在生成DMC的同时,催化剂得到循环利用。此外,还探讨了金属烷氧基化合物和金属醋酸盐存在下,CO2与甲醇直接合成DMC的反应,其中Ti(Ⅳ)和Sn(Ⅳ)烷氧基化合物催化反应效果较好,在吸水剂存在下DMC收率可达金属烷氧基化合物的330%(摩尔比)。
Kazufumi等[13]以有机锡金属化合物(Bu2SnO)n为催化剂,研究了2,2-二甲氧基丙烷对CO2与甲醇合成DMC的影响。研究认为在CO2压力下,2,2-二甲氧基丙烷的存在可加速(Bu2SnO)n与甲醇反应生成二甲氧基四丁基二锡氧二聚物,而二甲氧基四丁基二锡氧二聚物与二甲氧基二丁基二锡同样具有高催化活性。此外,研究还发现,当以有机锡和有机钛催化CO2与甲醇合成DMC时,在脱水剂2,2-二甲氧基丙烷作用下,加入少量呈酸性的三氟甲基磺酸盐,以与脱水剂摩尔比计算可使得DMC产率由17%提高到40%,而传统的酸如硫酸、盐酸、磷酸等都不能起到类似的作用[14]。
1.1.2 乙酸盐、碳酸盐催化体系 赵天生等[15]研究了镍、铜、锰、锌、汞、钴等金属乙酸盐对CO2和甲醇直接合成DMC反应的催化活性,结果得出体系反应压力和甲醇含量对合成反应结果影响较大,镍、锰、汞、钴乙酸盐具有较好的活性。在非超临界条件下,乙酸镍催化时副产物乙酸甲酯最低,DMC产率最高,是催化剂的0.66倍(摩尔比)。以乙酸镍为催化剂,在超临界条件下,DMC为唯一有机产物,收率是非超临界条件下的12倍。通过对超临界条件下DMC合成机理的研究,他们认为反应机理是体系中的镍离子活化甲醇生成甲氧基镍,CO2插入甲氧基和金属之间生成活性中间物种,进一步在助催化剂、甲醇作用下生成DMC。
Fujita等[16]研究了碘甲烷存在下不同碱催化剂催化甲醇和CO2合成DMC。通过对K2CO3、KHCO3、Na2CO3、(NH4)2CO3等催化性能和催化过程的比较,得出K2CO3的催化效率最高,DMC收率为催化剂的3.97倍(摩尔比),这可归因于金属离子半径不同导致的碱性差别,碱性越大催化效率越高,反应过程都伴有二甲醚和单质碘的生成。研究认为碘甲烷作为反应物之一,生成二甲醚和生成DMC是两个平行反应,催化机理如图1所示。

图1 不同碱催化剂的催化机理
均相催化体系多以甲醇为溶剂条件下存在的烷氧基金属类的碱性催化体系,催化剂制备较简单,目前对这类碱性催化剂的催化机理已有较清楚的认识。但由于这类催化剂易水解,其寿命与活性明显受产物水的影响,导致催化效率较低,此外催化剂的分离、再生问题也是这类催化剂致命的弱点,而且使用甲基化试剂势必会造成生产成本的大幅增加。
1.2 非均相催化体系
非均相催化体系具有催化剂种类多、产物易分离、催化剂不易失活而易于回收等优点,但反应中催化剂活性不高,且反应生成的水多数情况下仍不能及时的排出反应体系而造成逆反应存在,限制了DMC产率。此外,由于反应的影响因素较多(特别是较复杂的催化剂体系),对反应机理的认识还存在很多不足。
1.2.1 负载型催化剂 负载型催化剂解决了催化剂的分离和再生问题,是目前研究最广的催化体系。活性组分多见为金属、固体碱或烷氧金属,载体一般为具有高的比表面积或者特定的物理结构。
钟顺和等[17-20]采用等体积浸渍法分别制备了Cu-Ni/ZrO2-SiO2, Cu-Ni/V2O5-SiO2、Cu-Ni/MoO3-SiO2和Cu-Ni/MgSiO-KF等负载型催化剂,用于CO2和甲醇直接合成DMC,并对催化活化机理做了探讨,如图2所示。
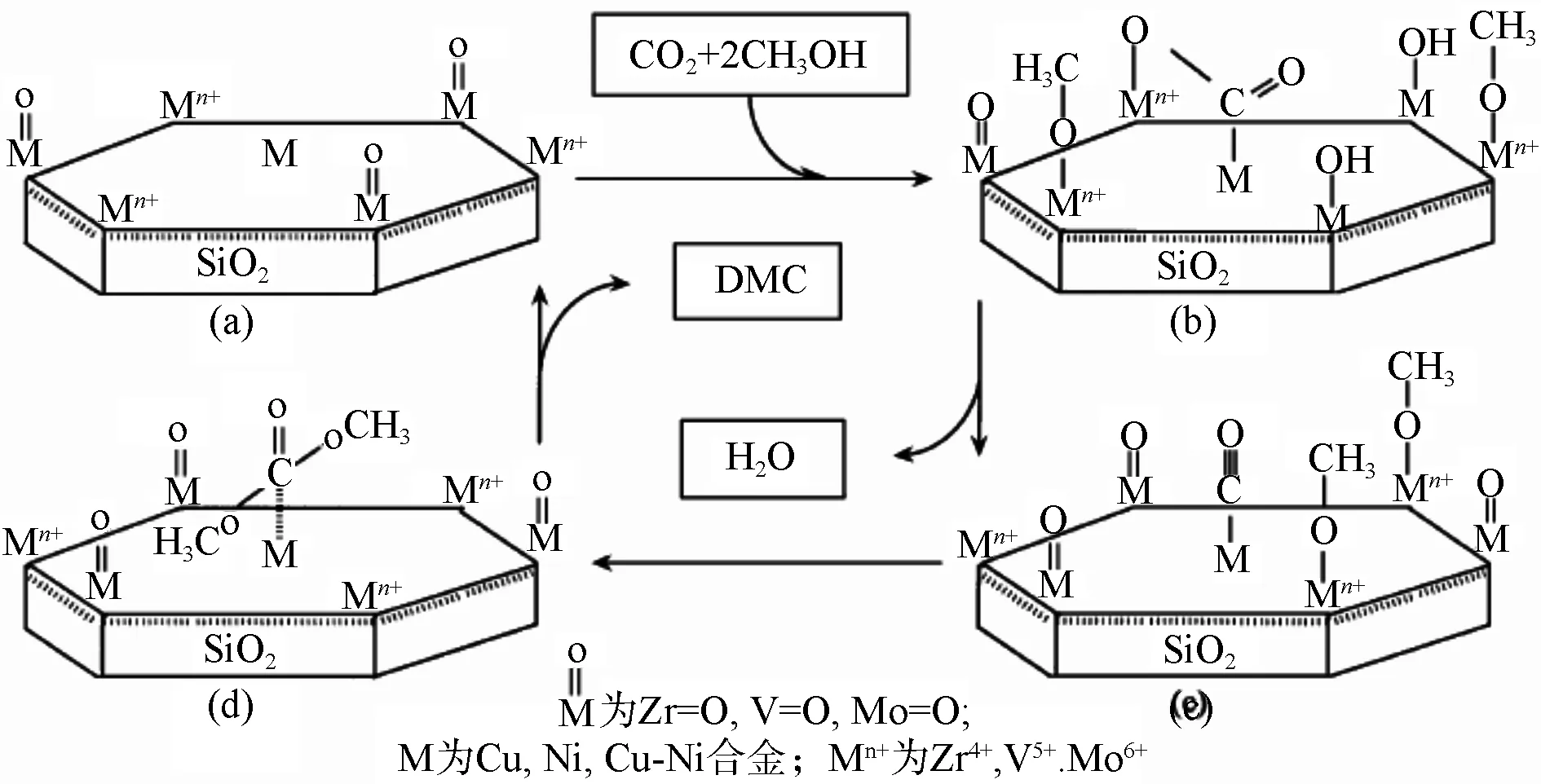
图2 不同载体负载双金属型催化剂的催化机理
研究认为上述催化剂上存在着金属位Cu-Ni合金、Lewis酸位(Zr4+、V5+或Mo6+)和Lewis碱位(Zr=O、V=O或Mo=O)三类活性中心,CO2在金属位和Lewis酸位协同作用下生成的CO2卧式吸附态(整个反应得以进行的关键活性体),甲醇在Lewis酸位和Lewis碱位协同作用下形成解离吸附态(CH3O-+H+),CO2和甲醇在金属位催化剂表面上的反应产物主要为DMC、CH2O、CO和H2O。随后在上述体系中加入K2O或KF作助剂[21-22],结果认为K是良好的电子转移促进剂,K的引入可增加金属位周围的电荷密度、降低其功函数,使得CO2和甲醇在催化剂表面吸附和解离性能增加,在140 ℃、0.6 MPa下,甲醇转化率由7.94%提高到12%,DMC选择性不变,均在87.8%左右。
近年来,孟跃中课题组对金属负载型催化剂在CO2和甲醇直接合成DMC中的应用条件、表征技术、催化机理等进行了探索。Wu等[23-24]将Cu-Ni双金属负载于磷酸改性的V2O5-SiO2上作为反应催化剂,探讨了催化剂还原条件以及反应温度压力条件对反应转化率和选择性的影响,并对反应过程作了在线拉曼测试以研究其催化合成机理。Bian等[25-31]充分利用了价格低廉的碳系列载体的高比表面积和特定的物理结构,制备了一系列碳载金属催化剂,分别是将Cu-Ni双金属负载于膨胀石墨、碳纳米管、活性碳及氧化石墨上,研究了载体表面预处理、催化剂煅烧还原条件和添加助剂对催化性能的影响,并且在连续式固定床气相反应装置上考察了金属负载量、反应温度、反应压力和反应时间对甲醇转化率和DMC选择性的影响。综合研究结果得出金属氧化物质量分数为20%时,氧化石墨负载Cu-Ni双金属的催化活性最好,在最佳反应条件(105 ℃ ,1.2 MPa)下,甲醇最高转化率达到10.13%,DMC选择性接近90%。此外,采用连续式固定床气相反应装置能够实现及时带走生成的水,促使平衡反应右移,利于产物的生成。
此外,负载型烷氧金属催化剂也有报道。钟顺和等[32-34]报道了二氧化硅负载的烷基金属类催化剂,如Ti2(OMe)4/SiO2、Sn2(OMe)4/SiO2、Ni2(OCH3)2/SiO2等,其中Sn2(OMe)4/SiO2的催化性能最好,在0.5 MPa、140 ℃下,总碳转化率为6.05%,DMC选择性接近100%。
1.2.2 ZrO2类催化剂 ZrO2具有亚稳的四方晶型和单斜晶型,并具有Lewis酸位和Lewis碱位,是催化领域研究较多的催化剂和载体,用于合成DMC中ZrO2类催化剂主要有ZrO2、ZrO2-H3PO4和ZrO2-CeO2等。这类催化剂存在的Lewis酸碱对是催化反应的活性中心,对催化有促进作用,但由于影响因素较复杂,对催化机理的认识还存在不足。
Tomishige等[35-36]用由不同条件下煅烧ZrO2·xH2O得到的ZrO2作催化剂,结果表明,673 K煅烧得到的ZrO2催化效果最好(160 ℃,ZrO2用量0.5 g时,甲醇转化率1%左右),煅烧得到的ZrO2结构以亚稳的四方晶型为主,表面以单斜晶型为主;催化剂表面相邻的Lewis酸碱位数量影响催化剂活性,甲氧碳酸酯基为反应中间体,但是平衡反应的存在使得反应的转化率很低。在随后的工作中[37-38],引入H3PO4修饰ZrO2,使得同等反应条件下甲醇转化率提高到4.5%左右,且反应能够在更低的温度(110~170 ℃)下进行,这归因于引入H3PO4产生的桥式OH以及由Zr与P原子间相互作用而在ZrO2表面产生的弱Brønsted酸位对甲醇的活化作用。还需指出的是,弱酸位是维持高选择性的关键,因为副产物二甲醚极易在强酸位点上生成[39]。
Bell等[40-41]通过在线原位拉曼和原位红外分析了CO2和甲醇在ZrO2催化剂作用下合成DMC的反应机理,其过程如图3所示。催化剂表面的两性Zr—OH和不饱和的Zr4+O2-形成Lewis酸碱对成为活性中心,甲醇在不饱和的Zr4+上吸附、解离,形成CH3O—Zr,然后甲基迁移到甲基碳酸酯基的终端氧原子上,从而形成DMC。研究指出ZrO2的晶型对催化过程的动力学有明显影响,与四方晶型ZrO2催化作用下得到的DMC产率相比较,在单斜晶型ZrO2催化作用下得到DMC产率明显较高的主要原因是单斜晶型ZrO2表面存在更多的弱Brønsted酸位,能够对甲醇产生了更高的有效活化效率,而且在单斜晶型ZrO2表面的Zr4+O2-Lewis酸碱对更多。
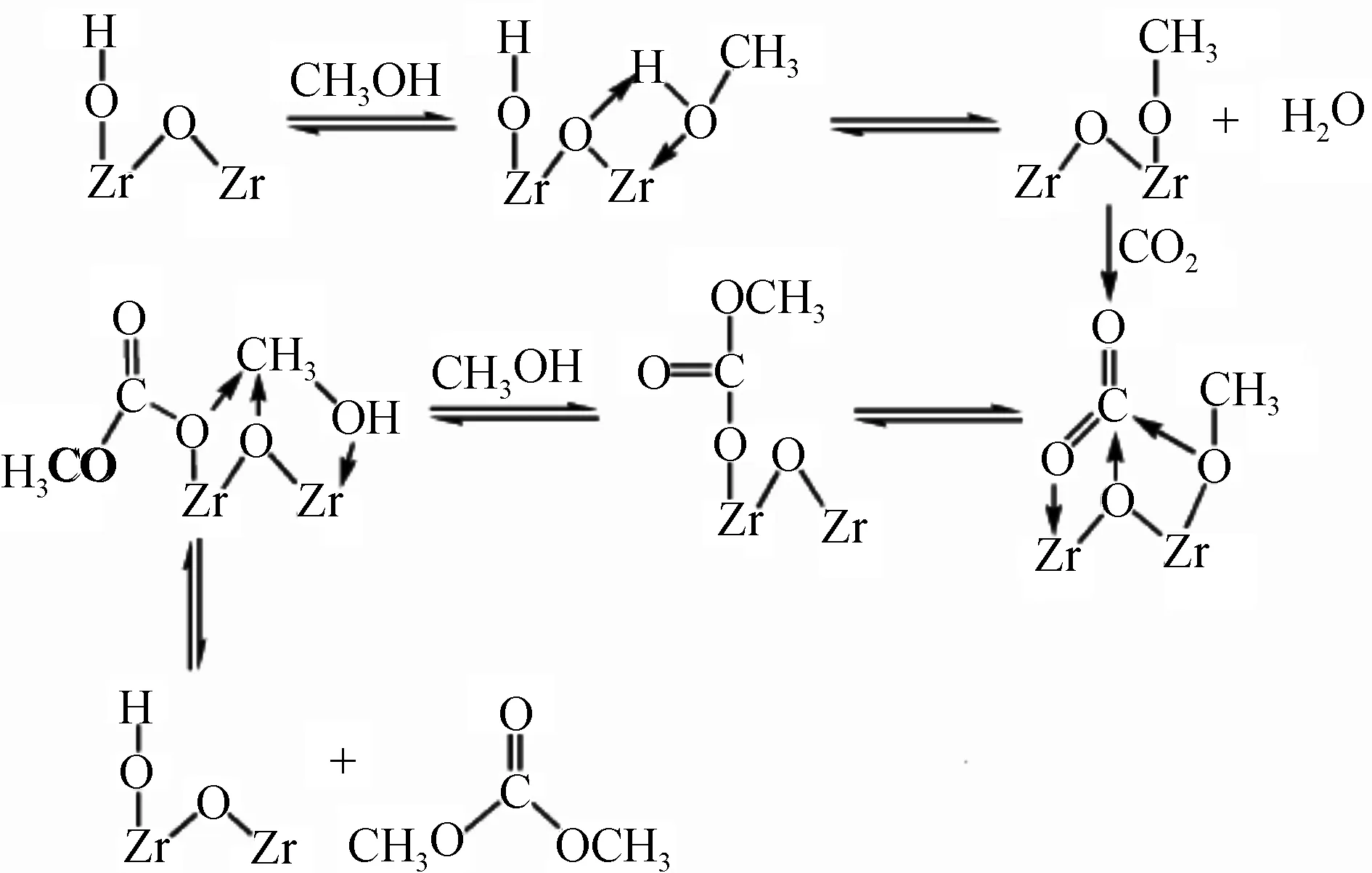
图3 ZrO2催化剂的催化机理
Han等[42]采用柠檬酸络合技术制备了Ce1-xZrxO2催化剂,研究指出DMC的生成速率与催化剂中Zr的含量相关。Tomishige等[43]基于ZrO2的弱两性,研究了一系列含不同Ce/Zr比值的Ce1-xZrxO2催化剂的催化性能,得出Ce0.2Zr0.8O2的催化效率最高,甲醇转化率为7%左右(110 ℃,0.5 g催化剂用量)。
1.2.3 杂多酸催化剂 杂多酸是一类含氧桥的多酸配合物,具有酸强度远高于通常无机酸的Brønsted酸位、氧化还原性、“准液相”行为及多功能(酸、氧化、光电催化)等优点,在催化研究领域中受到广泛重视,但是杂多酸的比表面较小(<10 m2/g),在催化应用中受到一定限制,因此目前的研究中也有将杂多酸负载于适合的载体上以提高其比表面积,增强催化活性。
Allaoui等[44]通过比较H3PMo12O40和Cu1.5PMo12O40的催化性能,研究了Brønsted酸位及反应温度对催化性能的影响。当铜离子取代H3PMo12O40中的质子后,酸性降低,催化剂的活性也降低,DMC产率由1.6%下降到1.2%(反应条件均为50 ℃,0.25 g催化剂用量)。研究指出Brønsted酸位有利于提高催化剂的活性,更有助于DMC生成,较低的反应温度也有利于DMC的生成。
基于非均相催化CO2和甲醇直接合成DMC催化剂表面需同时具有酸、碱双活性中心的认识,Jiang等[45]比较了H3PW12O40/ZrO2和ZrO2的催化性能,发现前者具有更好催化性能,甲醇转化率是后者的8倍;通过溶胶-凝胶法制备的催化剂催化性能比浸渍法制备的催化剂的效果好,且23.2%H3PW12O40/ZrO2催化剂显示出最佳催化性能,在4 MPa、100 ℃下,甲醇转化率4.2%左右。受此启发,Kyung等[46-48]研究了由溶胶-凝胶法制备的H3PW12O40/CexTi1-xO2直接催化CO2和甲醇合成DMC的催化活性。实验表明,CexTi1-xO2的催化活性远远高于CeO2和TiO2,当CexTi1-xO2被H3PW12O40改性后,其催化活性显著增加,Ce含量与催化剂活性呈火山型曲线,如图4所示。H3PW12O40/CexTi1-xO2为酸碱双功能催化剂,其中酸性位由H3PW12O40提供,碱性位由CexTi1-xO2产生,随着催化剂表面酸碱位的增加,H3PW12O40/CexTi1-xO2的活性也逐步提高。当催化剂各组分比值为H3PW12O40/Ce0.1Ti0.9O2时,具有最高的酸碱性,此时催化剂的催化活性也最大。

图4 不同催化剂的催化性能
1.2.4 离子液体催化体系 离子液体是一类具有独特物理和化学性质的“软”功能材料或介质,作为催化剂、溶剂,可以为反应提供优良的反应环境。近年来离子液体在CO2和甲醇直接合成DMC反应中有较广的应用。
Cai等[49]采用K2CO3主催化剂、CH3I促进剂,考察了离子液体1-乙基-3-甲基咪唑溴化物在CO2和甲醇直接合成DMC反应中的促进作用,通过加入离子液体,DMC的收率从4.11%提高到5.58%。蔡振钦等[50-52]利用高压间歇反应釜,研究了离子液体对K2CO3/CH3I催化CO2与甲醇直接合成DMC的反应规律,指出离子液体不会改变反应的最佳条件和整体规律性,对反应几乎没有催化活性,但有明显的促进作用,DMC收率可由5.52%提高到6.46%,此外离子液体对CH3OH、DMC和CO2良好的溶解性,也是促进作用的主要原因。
2 催化工艺技术
如前所述,在CO2和甲醇合成DMC的反应中,平衡常数和CO2的平衡转化率都很小,在热力学上是难以进行的,设计催化工艺技术也就是为了打破反应的化学平衡限制,使反应顺利进行,从而提高DMC收率。
2.1 超临界体系
CO2和甲醇合成DMC反应中,近临界或超临界CO2压力使得CO2既做溶剂,又直接参与反应。由于超临界流体具有很强的溶解性、较强的可极化性和较大的扩散系数,使一些有机物溶于CO2中,提高传质效率,改善了反应条件。此外,超临界流体对反应产物具有抽提作用,使得在催化剂表面上进行的可逆反应转化为不可逆反应,引起反应平衡的移动,从而突破热力学平衡的限制。超临界CO2流体的引人,对提高反应的转化率、目的产物的选择性和催化剂的寿命都具有促进作用[53]。
Guo等[54]以四相体系甲醇-CO2-DMC-H2O为反应模拟体系,研究了由甲醇和超临界CO2合成DMC反应体系的临界温度和临界压力,指出反应体系的临界参数与反应体系的初始组成及反应程度密切相关。Raúl等[55]采用PT方程、PRSV方程以及IPVDW混合规则,模拟了四组分体系CO2-甲醇-水-DMC的临界参数和相行为,为优化操作和分离参数提供了可靠的依据。
Hong等[56]采用固体碱(主催化剂)、CH3I(助催化剂)和2,2-二甲氧基丙烷(脱水剂)在甲醇和超临界CO2流体中合成DMC,通过控制操作参数,研究了不同固体碱、反应温度及压力对反应催化性能的影响,得出K2CO3作主催化剂时,在130~140 ℃、20 MPa的条件下DMC的收率最高为12 mol%。此外,也有研究表明相态的不同对甲醇的平衡转化率影响很大,超临界流体对DMC直接合成反应具有一定的促进作用[57-58]。
2.2 电化学合成体系
电化学合成方法主要是在电化学反应器内进行以电子转移为主的合成反应。该氧化还原反应不用化学试剂做氧化剂和还原剂,而用清洁无污染的电子来引发,在电化学反应器中可一步进行且反应条件温和,缺点是选择性较低,副产物较多。
罗仪文等[59]在含0.1mol/L四乙基铵四氟硼酸盐的乙腈和N,N-二甲基酰胺溶液中,研究了CO2在铜电极上电化学活化及其与甲醇合成DMC的反应。结果表明,CO2在电位E=-2.3 V(以镁为牺牲阳极,铜为工作电极,Ag/AgI电极为参比电极)发生不可逆还原,在这电位下体系添加烷基化试剂CH3I,常温常压条件下得到DMC收率达14.92%。Yuan等[60]以铂为电极,在离子液体-CH3OK-甲醇体系中常温常压下由CO2和甲醇电催化合成DMC,并研究了其电催化机理。
2.3 光辅助催化反应体系
最近几十年,半导体催化剂因其具有能够引发氧化还原反应的光催化反应活性而引发了研究者的广泛关注。CO2经由SrTiO3、TiO2、SiC、CdS、ZnO、WO3和BaTiO3等半导体催化剂光催化还原来制备甲醛、甲酸、甲醇、甲烷和草酸等产品的结果已有报道[61-62],而紫外和可见光也被证明是打破热力学限制或促进热力学不宜进行的反应的有效手段[63-64]。
Wang等[65]采用SiO2或SiC负载铜掺杂的(Ni、V、O)半导体复合氧化物为光催化剂,在连续的固定床气相反应器上紫外光催化CO2和甲醇合成DMC。采用的连续固定床气相反应装置能够及时带走生成的水,形成无水反应体系,避免了催化剂的失活,有利于DMC的生成。研究结果显示,半导体NiO与V2O5复合后部分形成V-O-Ni键联,增强了对光的吸收强度,Cu和NiO的引人提高了V2O5在SiO2表面的分散度,并扩展了催化剂的光响应范围。在1个大气压条件下,同单纯热表面催化反应相比,紫外光照射下使得DMC产率由2.3%提高到了4.0%。
2.4 脱水剂和膜反应器
在CO2和甲醇合成DMC的平衡反应中,反应副产物水的存在,一方面会使DMC水解,反应平衡左移,反应平衡常数和CO2平衡转化率都很低;另一方面,水还会引起均相催化剂的水解、失活。因此,反应副产物水的去除在整个合成反应中是十分重要的。常加入的物理或化学脱水剂有分子筛[66]、2,2-二甲氧基丙烷[56]、醋酸原三酯[67]、双环己基碳二亚胺(DDC)等[15,68],实验结果均表明,这些脱水剂对反应起到了明显的促进作用。
Li等[69]把膜反应器技术应用到直接合成DMC反应中。采用膜反应器,在不改变反应机理的情况下能及时、不断的把反应生成的水从反应体系中分离、脱除,使化学平衡向DMC生成方向移动。在PSMCR膜反应器上,甲醇转化率为9.2%,DMC选择性为96.0%,相对于普通间歇式反应器分别增加了2.65%和6%。
3 环氧烷烃存在下的甲醇和CO2一步法合成DMC
以甲醇、CO2、环氧烷烃为原料的直接法是将酯交换的两步反应合并为一步反应,环氧烷烃在催化剂作用下开环生成中间产物,再由CO2插入反应生成环状碳酸酯,然后在催化剂作用下与甲醇酯交换生成DMC,反应历程如下[70-71]:
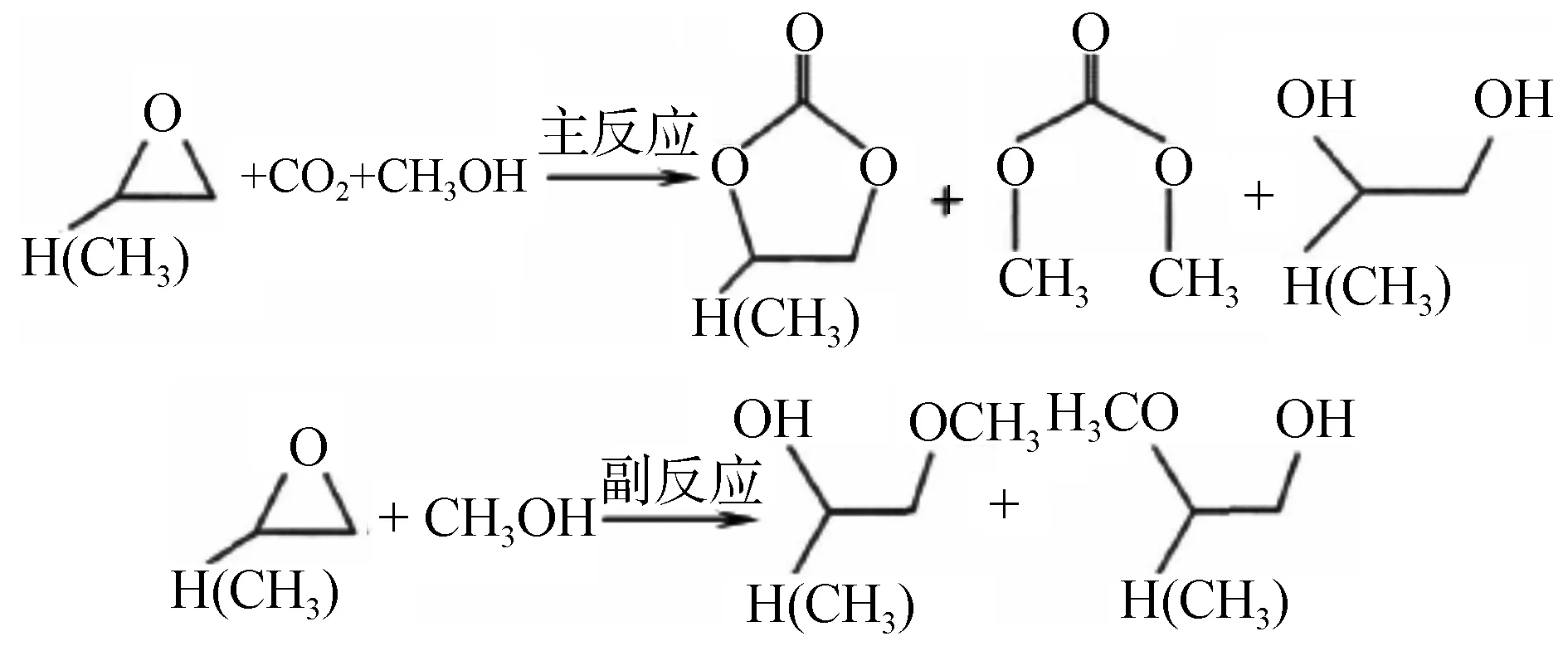
一步法合成DMC过程中,CO2和环氧烷烃合成环状碳酸酯(EC/PC)反应在较温和的条件下就可得到将近100%的转化率和选择性,所以这种方法的关键是第二步的环状碳酸酯与醇发生酯交换反应[72]。综合目前的研究数据来看[73-77],如表1所示,采用一步法合成的DMC选择性都偏低,而且副产物过多,不利于后续产物的分离提纯,因此有效的催化剂应对一步法合成反应中的两步反应均起到催化作用,又能够对副反应起到抑制作用,才能够大幅降低生产成本,同时联产环状碳酸酯和乙(丙)二醇(EG/PG)。
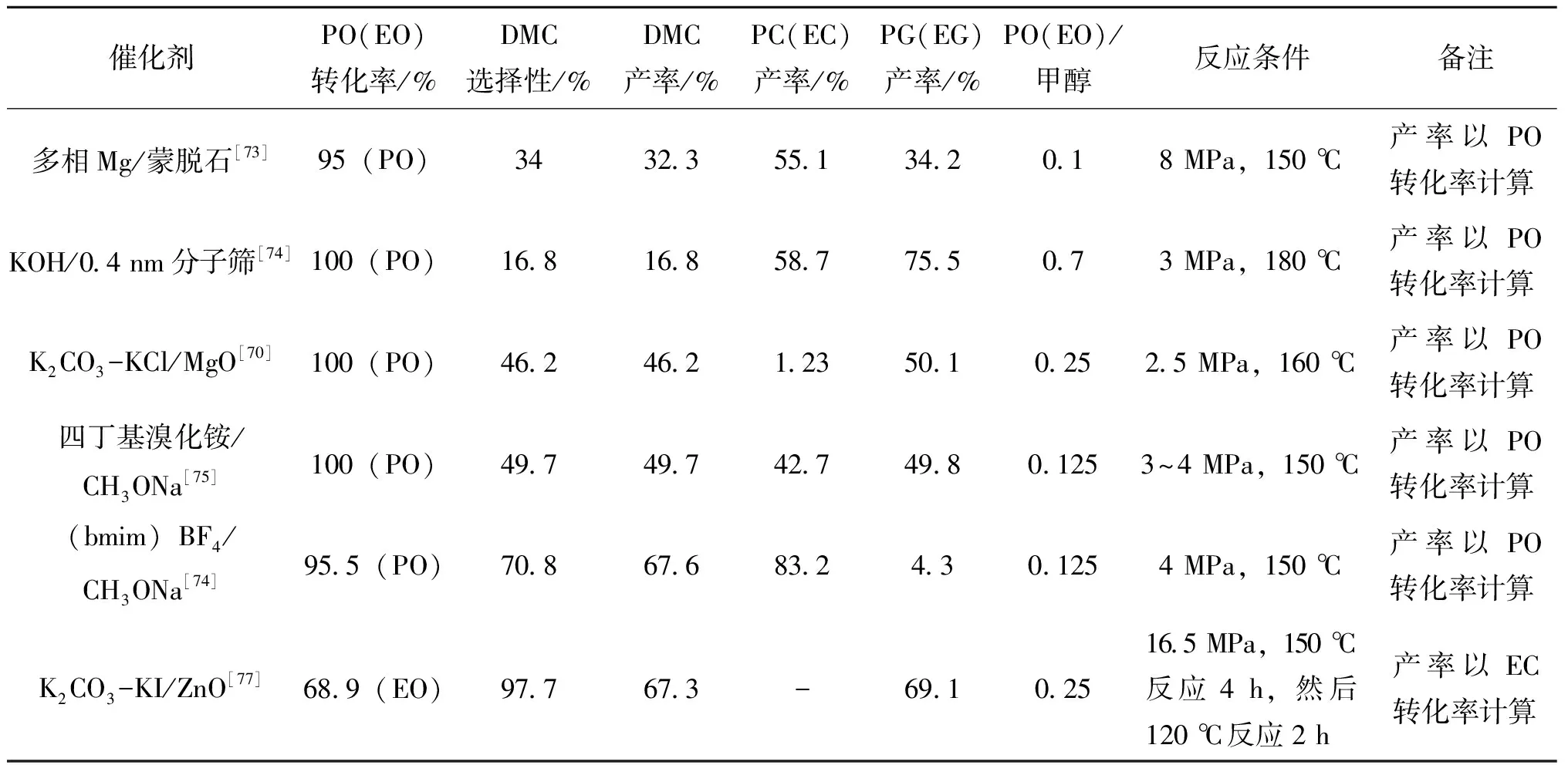
表1 不同催化剂一步法合成DMC的催化性能
4 展 望
CO2和甲醇直接合成DMC是一种绿色合成方法,不仅能够使温室气体CO2资源化利用,而且合成的DMC也具有特殊化学结构,是潜在的燃油添加剂,因此这一课题是两头环保的重要的研究领域。由CO2和甲醇直接合成DMC反应在热力学上是难以进行的,尽管采用了许多方法试图通过降低反应自由能、打破化学平衡的限制等推动反应的进行,但到目前为止,这一合成工艺仍处于实验室研发阶段,还未有能促使真正实现工业化的有效催化体系和化工工艺。因此,不断提高DMC产率和选择性,实现CO2、甲醇的有效活化以及反应机理的研究,解决反应化学平衡限制和反应产物的分离等问题仍将是研究的重点。
参考文献:
[1] 田恒水,张广遇,黄振华.开创明日化学的新的低污染泛用基础化学原料-碳酸二甲酯[J].化工进展,1995,11(6):7-14.
[2] MICHAEL A P, CHRISTOLPHER L M. Review of dimethyl carbonate(DMC) manufacture and its characteristics as a fuel additive[J]. Energy Fuel, 1997(11):2-29.
[3] ONO Y. Dimethyl carbonate for environmentally benign reactions[J]. Pure Appl Chem, 1996, 68(2):367-375.
[4] 刘定华,刘晓勤,钟秦.甲醇液相氧化羰基合成碳酸二甲酯过程热力学分析[J].天然气化工,2009,34(3):44-47.
[5] 赵天生,韩怡卓,孙予罕.甲醇和CO2合成碳酸二甲酯体系的热力学分析[J].天然气化工,1998,23(5):52-55.
[6] YAMAZAKI N, NAKAHAMA S, HIGASHI F. Chemical reactions of carbon dioxide[J]. Kenkyu Hokoku-Asahi Garasu Kogyo Gijutsu Shoreikai, 1978, 33:31-45.
[7] ARESTA M, DIBENEDETTO A, PASTORE C, et al. Reaction mechanism of the direct carboxylation of methanol to dimethylcarbonate: experimental and theoretical studies[J]. Topics in Catalysis, 2006, 40(1/2/3/4):71-81.
[8] ARESTA M, DIBENEDETTO A, PASTORE C, et al. Synthesis and characterization of Nb(OR)4[OC(O)OR](R=Me,Et,Allyl) and their reaction with the parent alcohol to afford organic carbonates[J]. Inorg Chem, 2003, 42(10):3256-3261.
[9] CAI Q H, JIN C, LU B, et al. Synthesis of dimethyl carbonate from methanol and carbon dioxide using potassium methoxide as catalyst under mild conditions[J]. Catalysis Letters, 2005, 103(3/4):225-228.
[10] 桂新胜,曹发海,房鼎业.间接搅拌釜中甲醇与CO2合成碳酸二甲酯[J].华东理工大学学报,1998,24(1):7-10.
[11] KIZLINK J, PASTUCHA I. Preparation of DMC from methanol and carbon dioxide in the presence of organotin compounds[J]. Collect Czech Chem Commun, 1993, 58(9):1399-1401.
[12] KIZLINK J, PASTUCHA I. Preparation of DMC from methanol and carbon dioxide in the presence of Sn(Ⅳ) and Ti(Ⅳ) alkoxides[J]. Collect Czech Chem Commun, 1995, 60(4):687-692.
[13] KAZUFUMI K, JUN-CHUL C, YOSHIHIRO O, et al. Reaction of dibutyltin oxide with methanol under CO2pressure relevant to catalytic dimethyl carbonate synthesis[J]. Journal of Organometallic Chemistry, 2008, 693(7):1389-1392.
[14] JUN-CHUL C, KAZUFUMI K, YOSHIHIRO, et al. Tin-or titanium catalyzed dimethyl carbonate synthesis from carbon dioxide and methanol: large promotion by a small amount of triflate salts[J]. Catalysis Communications, 2008, 9(7):1630-1633.
[15] ZHAO T S, HAN Y Z, SUN Y H. Novel reaction route for dimethyl carbonate synthesis from CO2and methanol[J]. Fuel Proc Tech, 2000, 62(2/3):187-194.
[16] FUJITA S, BHANAGE B M, IKUSHIMA Y et al. Synthesis of dimethyl carbonate from carbon dioxide and methanol in the presence of methyl iodide and base catalysts under mild conditions-effect of reaction conditions and reaction mechanism[J]. Green Chem, 2001, 3(2):87-91.
[17] 钟顺和,黎汉生,王建伟,等.CO2和CH3OH直接合成碳酸二甲酯用Cu-Ni/ZrO2-SiO2催化剂[J].催化学报,2000,21(2):117-120.
[18] 钟顺和,黎汉生,王建伟,等.CO2和CH3OH直接合成碳酸二甲酯用Cu-Ni/V2O5-SiO2催化剂[J].物理化学学报,2000,16(3):226-231.
[19] 钟顺和,黎汉生,王建伟,等.用二氧化碳和甲醇直接合成碳酸二甲酯的研究[J].石油炼制与化工,2000,31(6):51-55.
[20] LI C F, ZHONG S H. Study on application of membrane reactor in direct synthesis DMC from CO2and CH3OH over Cu-KF/MgSiO catalyst[J]. Catalysis Today, 2003, 82(1/2/3/4):83-90.
[21] 黎汉生,钟顺和,王建伟,等.K2O助剂对合成碳酸二甲酯用Cu-Ni/ZrO2-SiO2催化剂的吸附和催化性能的影响[J].催化学报,2001,22(4):353-357.
[22] 钟顺和,孔令丽,雷泽,等.KF在CO2和CH3OH直接合成DMC负载型金属催化剂中作用的研究[J].分子催化,2002,16(6):401-407.
[23] WU X L, CAO M, MENG Y Z, et al. Direct synthesis of dimethyl carbonate on H3PO4modified V2O5[J]. Journal Molecular Catalysis A: Chemieal, 2005, 238(1/2):158-162.
[24] WU X L, MENG Y Z, XIAO M, et al. Direct synthesis of dimethyl carbonate(DMC) using Cu-Ni/VSO as catalyst[J]. Journal of Molecular Catalysis A: Chemical, 2006, 249(1/2):93-97.
[25] BIAN J, XIAO M, MENG Y Z, et al. Direct synthesis of DMC from CH3OH and CO2over V-doped Cu-Ni/AC catalysts[J]. Catal Commun, 2009, 10(8):1142-1145.
[26] BIAN J, XIAO M, MENG Y Z, et al. Graphite oxide as a novel host material of catalytically active Cu-Ni bimetallic nanoparticles[J]. Catal Commun, 2009, 10(11):1529-1533.
[27] BIAN J, XIAO M, MENG Y Z, et al. Novel application of thermally expanded graphite as the support of catalysts for direct synthesis of DMC from CH3OH and CO2[J]. J Colloid Interf Sci, 2009, 334(1):50-57.
[28] BIAN J, XIAO M, MENG Y Z, et al. Highly effective synthesis of dimethyl carbonate from methanol and carbon dioxide using a novel copper-nickel/graphite bimetallic nanocomposite catalyst[J]. Chem Eng J, 2009, 147(2/3):287-296.
[29] BIAN J, XIAO M, MENG Y Z, et al. Carbon nanotubes supported Cu-Ni bimetallic catalysts and their properties for the direct synthesis of dimethyl carbonate from methanol and carbon dioxide[J]. Appl Surf Sci, 2009, 255(16):7188-7196.
[30] BIAN J, XIAO M, MENG Y Z, et al. Highly effective direct synthesis of DMC from CH3OH and CO2using novel Cu-Ni/C bimetallic composite catalysts[J]. Chin Chem Lett, 2009, 20(3):352-355.
[31] BIAN J, XIAO M, MENG Y Z, et al. Activated carbon supported Cu-Ni bimetallic catalyst for direct synthesis of DMC from CH3OH and CO2: effect of pretreatment of activated carbon supports[J]. Res J Chem Environ, 2009, 13(1):66-80.
[32] 钟顺和,孔令丽,黎汉生,等.Ti2(OMe)4/SiO2催化剂的制备及其合成碳酸二甲酯的反应性能[J].燃料化学学报,2002,30(5):454-458.
[33] 钟顺和,程庆彦,黎汉生,等.负载型Sn2(OMe)4/SiO2催化剂的制备及其催化CO2与CH3OH直接合成碳酸二甲酯的性能[J].催化学报,2002,23(6):543-548.
[34] 钟顺和,王爱菊,黎汉生,等.Ni2(OCH3)2/SiO2催化剂的制备及其合成碳酸二甲酯的反应性能[J].分子催化,2002,16(5):321-326.
[35] TOMISHIGE K, SAKAIHORI T, IKEDA Y, et al. A novel method of direct synthesis of dimethyl carbonate from methanol and carbon dioxide catalyzed by zirconia[J]. Catalysis Letters, 1999, 58(4):225-229.
[36] TOMISHIGE K, IKEDA Y, SAKAIHORI T, et al. Catalytic properties and structure of zirconia catalysts for direct synthesis of dimethyl carbonate from methanol and carbon dioxide[J]. Journal of Catalysis, 2000, 192(2):355-362.
[37] IKEDA Y, SAKAIHORI T, TOMISHIGE K, et al. Promoting effect of phosphoric acid on zirconia catalysts in selective synthesis of dimethyl carbonate from methanol and carbon dioxide[J]. Catalysis Letters, 2000, 66(1/2):59-62.
[38] IKEDA Y, ASADULLAH M, FUJIMOTO K, et al. Structure of the active sites on H3PO4/ZrO2catalysts for dimethyl carbonate synthesis from methanol and carbon Dioxide[J]. Journal of Physical Chemistry B, 2001, 105(43):10653-10658.
[39] TOMISHIGE K, FURUSAWA Y, IKEDA Y, et al. CeO2-ZrO2solid solution catalyst for selective synthesis of dimethyl carbonate from methanol and carbon dioxide[J]. Catalysis Letters, 2001, 76(1/2):71-74.
[40] XIE S B, BELL A T. Aninsituraman study of dimethyl carbonate synthesis from carbon dioxide and methanol over zirconia[J]. Catalyst Letters, 2000, 70(3/4):137-143.
[41] JUNG K T, BELL A T. Effects of catalyst phase structure on the elementary processes involved in the synthesis of dimethyl carbonate from methanol and carbon dioxide over zirconia[J]. Topics in Catalysis, 2002, 20(1/2/3/4):97-105.
[42] HAN G B, PARK N K, JIN J H, et al. Synthesis of dimethyl carbonate from CH3OH and CO2with Ce1-xZrxO2catalysts[J]. Studies in Surface Science and Catalysis, 2004, 153:181-184.
[43] TOMISHIGE K, KUNMORI K. Catalytic and direct synthesis of dimethyl carbonate starting from carbon dioxide using CeO2-ZrO2solid solution heterogeneous catalyst: effect of H2O removal from the reaction system[J]. Applied Catalysis A: General, 2002, 237(1/2):103-109.
[44] ALLAOI L A, JI C J, HEESOO K, et al. Effect of Brønsted acidity on the behavior of CO2methanol reaction[J]. Journal of Molecular Catalysis A: Chemical, 2006, 259(1/2):281-285.
[45] JIANG C J, GUO Y H, WANG C G, et al. Synthesis of dimethyl carbonate from methanol and carbon dioxide in the presence of polyoxometalates under mild conditions[J]. Applied Catalysis A: General, 2003, 256(1/2):203-212.
[46] KYUNG W L, JI C J, HEESOO K, et al. Effect of acid-base properties of H3PW12O40/CexTi1-xO2catalysts on the direct synthesis of dimethyl carbonate from rnethanol and carbon dioxide: a TPD study of H3PW12O40/CexTi1-xO2catalysts[J]. Journal of Molecular Catalysis A: Chemical, 2007, 269(1/2):41-45.
[47] KYUNG W L, MIN H Y, JIN S C, et al. Synthesis of dimethyl carbonate from methanol and carbon dioxide by heteropoly-acid/metal oxide catalysts[J]. Diffusion and Defect Data Pt B: Solid State Phenomena, 2007, 119:287-290.
[48] KYUNG W L. Direct synthesis of dimethyl carbonate from CH3OH and CO2by H3PW12O40/CexTi1-xO2catalyst[J]. Reaction Kinetics and Catalysis Letters, 2006, 89(2):303-309.
[49] CAI Q H, ZHANG L, SHAN Y K, et al. Promotion of ionic liquid to dimethyl carbonate synthesis from methanol and carbon dioxide[J]. Chinese Journal of Chemistry, 2004, 22(5):422-424.
[50] 蔡振钦,赵锁奇,徐春明.离子液体中K2CO3/CH3I直接催化合成碳酸二甲酯[J].石油化工,2006,35(5):425-428.
[51] 蔡振钦,赵锁奇,徐春明,等.离子液体对直接合成碳酸二甲酯反应的促进作用及机理分析[J].化工进展,2006,25(5):546-550.
[52] 蔡振钦,徐春明,赵锁奇.离子液体对K2CO3/CH3I催化二氧化碳和甲醇直接合成碳酸二甲酯反应性能的影响[J].天然气化工,2007,32(1):23-26.
[53] BEKTESEVIC S, KLEMAN A M, MARTEEL-PARRISH A E, et al. Hydroformylation in supercritical carbon dioxide: catalysis and benign solvents[J]. J Supercrit Fluid, 2006, 38(2):232-241.
[54] GUO X C, QIN Z F, WANG G F, et al. Critical temperatures and pressures of reacting mixture in synthesis of dimethyl carbonate with methanol and carbon dioxide[J]. Chinese Chemical Letters, 2008, 19(2):249-252.
[55] RAúL P, JUAN G, MAIA S, et al. Modelling of the phase behavior for the direct synthesis of dimethyl carbonate from CO2and methanol at supercritical or near critical conditions[J]. The Journal of Chemical Thermodynamics, 2007, 39(4):536-549.
[56] HONG S T, PARK H S, LIM J S, et al. Synthesis of dimethyl carbonate from methanol and supercritical carbon dioxide[J]. Res Chem Intermed, 2006, 32(8):737-747.
[57] DABUEKKE B T, STéPHANE C, RIITTA K, et al. Direct synthesis of dimethyl carbonate with supercritical carbon dioxide: characterization of a key organotin oxide intermediate[J]. Caralysis Today, 2006, 115(1/2/3/4):80-87.
[58] BALLIVET T D, LIGABUE R A, PLASSERAUD L. Synthesis of dimethyl carbonate in supercritical carbon dioxide[J]. Brazillan Journal of Chemical Engineering, 2006, 23(1):111-116.
[59] 罗仪文,张丽,钮东方,等.温和条件下电活化CO2合成碳酸二甲酯[J].应用化学,2007,24(9):1071-1073.
[60] YUAN D D, YAN G H, LU B, et al. Electrochemical activation of carbon dioxide for synthesis of dimethyl carbonate in an ionic liquid[J]. Electrochimica Acta, 2009, 54:2912-2915.
[61] LINSEBIGLER A L, LU G Q, YATES J T. Photocatalysis on TiO2surfaces: principles, mechanisms and selected results[J]. Chemical Reviews, 1995, 95(3):735-758.
[62] EMELINE A V, OTROSHCHENKO V A, RYABCHUK V K, et al. Abiogenesis and photostimulated heterogeneous reactions in the interstellar medium and on primitive earth relevance to the genesis of life[J]. Journal of Photochemistry and Photobiology C: Photochemistry Reviews, 2003, 3(3):203-224.
[63] MILLS A, LE H S. An overview of semiconductor photocatalysis[J]. Journal of Photochemistry and Photobiology A: Chemistry, 1997, 108(1):1-35.
[64] MAEDA K, TERAMURA K, LU A L. et al. Photocatalyst releasing hydrogen from water[J].Nature, 2006, 440(7082):295.
[65] WANG X J, XIAO M, MENG Y Z, et al. Direct synthesis of dimethyl carbonate from carbon dioxide and methanol using supported copper(Ni,V,O) catalyst with photao-assistance[J]. Journal of Molecular Catalysis A: Chemical, 2007, 278:92-96.
[66] SAKAKURA T, SAITO Y, OKANO M, et al. Selective conversion of carbon dioxide to dimethyl carbonate by molecular catalysis[J]. J Org Chem, 1998, 63(20):7095-7096.
[67] CHU G H. Synthesis of dimethyl carbonate from carbon dioxide over polymer-supported iodide catalysts[J]. Inorganic chemical Acta, 2000, 307(1/2):131-133.
[68] 蔡振钦,徐春明,赵锁奇.碳酸二甲酯直接合成反应重新技术的运用[J].石油化工腐蚀与防护,2005,22(4):51-54.
[69] LI C F, ZHONG S H. Study on application of membrane reactor in direct synthesis DMC from CO2and CH3OH over Cu-KF/MgSiO catalysts[J]. Catal Today, 2003, 82(1/2/3/4):83-90.
[70] JIANG Q, YANG Y. The double component catalyst for the direct synthesis of dimethyl carbonate from carbon dioxide, propylene oxide and methanol[J]. Catalysis Letters, 2004, 95(3/4):127-133.
[71] CHANG Y H, TAO J, HAN B X, et al. One-pot synthesis of dimethyl carbonate and glycols from supercritical CO2, ethylene oxide or propylene oxide, and methanol[J]. Appl Catal A, 2004, 263(2):179-186.
[72] WEI W, TONG W, SUN Y H. A new route for carbon dioxide cycloaddition to propylene carbonate[J]. Division of Fuel Chemistry, 2002, 47(1):289-290.
[73] BHANAGE B M, FUJITA S, IKUSHIMA Y, et al. Synthesis of dimethyl carbonate and glycols from carbon dioxide, epoxies and methanol using heterogeneous Mg containing snectite catalysts: effect of reaction variables on activity and selectivity performance[J]. Green Chem, 2003, 5(1):71-75.
[74] LI Y, ZHAO X Q, WANG Y J. Synthesis of dimethyl carbonate from methanol, propylene oxide and carbon dioxide over KOH/4A molecular sieve catalyst[J]. Appl Catal A, 2005, 279(1/2):205-208.
[75] CHEN X Z, HU C W, GAO Z M. One-pot synthesis of dimethyl carbonate in the presence of a two-component catalyst[J]. Chem Res Chin Univ, 2005, 21(6):714-717.
[76] CHEN X Z, HU C W, SU J H, et al, One-pot synthesis of dimethyl carbonate catalyzed by [bmim]BF4/CH3ONa[J].Chinese Journal of Catalysis, 2006, 27(6):485-488.
[77] CHANG Y H, JIANG T, HAN B X, et al. One-pot synthesis of dimethyl carbonate and glycols from supercritical CO2, ethylene oxide or propylene oxide, and methanol[J].Appl Catal A, 2004, 263(1):179-186.

