粤北大宝山酸性矿山废水氧化亚铁硫杆菌及其相关性能研究*
王智美,陈炳辉, 江春苗,万茉莉
(1.广东药学院公共卫生学院,广东 广州 510224;2.中山大学地球科学系,广东 广州 510275)
粤北大宝山大型铁铜多金属矿的酸性矿山废水(AMD)已使下游生态环境产生严重的Pb、Zn、Cu、Cd等重金属污染,引起了政府和有关媒体的广泛重视。有关专家也对受大宝山矿区污染的水体和土壤中的重金属含量、形态和危害性及生态环境退化等现象进行了深入的研究工作,并探讨了有关治理途径[1-6]。事实上,大宝山矿业有限公司已经投入大量的经费对尾矿库进行了处理,对民采产生的铁龙尾矿坝也进行了加高,但铁龙尾矿水(pH低至2.5)还在继续向下游排放(2008年11月18日现场考察),进入横石河,最终流入翁江,不断产生新的污染。
已有研究认为,AMD的形成主要是由于矿山采冶过程中,黄铁矿(FeS2)和其它硫化物矿物暴露后氧化作用形成的,而且在微生物如化能自养菌如Acidithiobacillusferrooxidans(以前称Thiobacillusferrooxidans)(即氧化亚铁硫杆菌)等的作用下,其氧化速度大大加快,特别是在pH<4的情况下,以生物化学氧化过程为主[7]。虽然国内已有一些学者开始研究酸性矿山废水中的微生物与硫化物矿物的相互作用及其环境效应问题[8-10],但对大宝山酸性矿山废水中的微生物对硫化物矿物的氧化作用及其环境效应等还未见有研究报道。
本文从粤北大宝山酸性矿山废水(铁龙尾砂库选矿废水和槽对坑尾砂库选矿废水)采集水样,进行pH值、部分阳离子和阴离子测定,并对其中的氧化亚铁硫杆菌进行分离培养,初步研究了其生长特性以及不同pH培养基溶液对AMD中重金属含量的影响,为进一步研究该矿区AMD中微生物对硫化物矿物的氧化作用及其环境效应提供基础。
1 实验材料和设备
1.1 采样点及样品采集
韶关曲江大宝山槽对坑尾砂库和铁龙尾砂库共设采样点5个,分别为铁龙尾砂库选矿废水入水口(编号01,下同),铁龙尾砂坝出水口(02),槽对坑尾砂库选矿废水入口(03),槽对坑尾砂库中央(04),槽对坑尾砂坝出水口(05),每个采样点均取水样,并现场用精密pH试纸测试其pH值。
1.2 实验试剂
(NH4)2SO4、KCl、K2HPO4、MgSO4·7H2O 、Ca(NO3)2、H2SO4、FeSO4·7H2O 、结晶紫、乙醇、草酸铵、碘、碘化钾、沙黄,以上均为分析纯(AR);硝酸、高氯酸,均为优级纯(GR),水为双蒸水。
1.3 实验设备
SHA-C水浴恒温振荡器(江苏金坛市宏华仪器厂);PHS-25型精密pH计(上海雷磁仪器厂); 电子天平(常熟双杰测试仪器厂);DSX-280B型不锈钢手提式压力蒸汽灭菌锅(上海中安医疗器械厂);洁净工作台,洁净等级100级(上海博讯实业有限公司医疗设备厂);IRIS(HR)等离子体原子发射光谱仪(ICP-AES);DX-600离子色谱仪。
2 实验方法
2.1 9K培养基(选择性培养基)配制
(NH4)2SO43.00 g,KCl 0.10 g,K2HPO40.10 g ,MgSO4·7H2O 0.50 g,Ca(NO3)20.01 g ,双蒸水600.0 mL,用1∶1H2SO4调PH为2.00,在121 ℃灭菌15 min;取FeSO4·7H2O 44.30 g溶于400.0 mL双蒸水,用同样的方法将pH调为2.00,用孔径为0.22 μm过滤器过滤除菌,然后将两者混合。
2.2 实验步骤
1)菌株分离。将5份水样静置,各吸取10.00 mL上层清液接入100.0 mL 9K液体培养基中,进行30 ℃、150 r/min振荡培养,第2天溶液颜色由浅绿色变成浅黄色;第4-6天浅黄色变成土黄色,锥形瓶内壁和瓶底逐渐生成一层黄色沉淀物;第7-9天颜色变成棕红色并产生大量沉淀。培养期间,溶液颜色转变成土黄色、并有沉淀生成时,进行一次加富培养(FeSO4·7H2O为能源),培养直至锥形瓶中的溶液变成棕红色不再改变并生成沉淀,停止培养。静置培养液,吸取上层清液进行革兰氏染色,镜检观察菌体形态。
2)菌株纯化。通过镜检结果挑选生长较好的培养液利用梯度稀释方法进行纯化。取上述培养较好的培养液上层澄清液10.00 mL接入装有100.0 mL 9K培养基的锥形瓶(1号瓶)中,两者充分混合。然后从1号瓶中取出10.00 mL溶液放入到2号瓶中,依次类推到9号瓶(9号瓶取出的10.0 mL溶液舍弃),进行30 ℃、150 r/min摇床培养,直至培养基颜色发生明显变化,即浅绿色→浅黄色→土黄色→棕红色,并出现沉淀,整个变化过程持续一周左右。最迟出现棕红色的培养基培养出的菌体为最纯菌体。上述纯化过程反复进行,最终得到生命力较强的实验菌株M培养液。
3)实验菌体的生长规律。吸取实验菌株M培养液10.00 mL接入100.0 mL的9K培养基中进行30 ℃,150 r/min培养,在培养液刚转变为棕红色并刚出现浑浊时即停止培养,用滤纸过滤。滤液用30 ℃、5 000 r/min离心10 min,收集菌体,用1∶1H2SO4调至pH为2.00的无菌水洗涤菌体,再次离心收集,重复3次,以除去可溶性的各种金属离子,最后用pH 2.00无菌水悬浮菌体。用血球计数板计数,菌悬液浓度为3.5×105个/mL。
分别吸取上述菌悬液10.00 mL接种到6个分别装有100.0 mL 9K培养基的250 mL锥形瓶中,进行30 ℃、150 r/min摇床培养,每隔12h计数细菌数量、测量pH值,培养7 d后将沉淀物收集,用X射线衍射分析。
2.3 水样中阳离子和阴离子含量测定
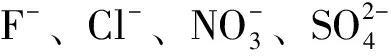
2.4 不同pH培养基溶液对AMD重金属含量的影响实验
陆建军等[10]认为,矿山环境中生物参与形成的铁硫酸盐矿物具有很高的比表面积和表面能,可作为理想的吸附剂;当pH=3时,酸矿水存在相对较多的氧化亚铁硫杆菌,污染元素降到最低[8]。
为了研究氧化亚铁硫杆菌的作用下,AMD的pH值对溶液重金属含量的影响,选取pH值为1.9、2.0、2.5和3.0分别配制9K培养基50.0 mL。各吸取铁龙尾砂坝出水口水样(02样品)5.00 mL,分别接入不同pH值的9K培养基中,并且同步配制试剂空白,用30 ℃,150 r/min摇床培养10 d,用滤纸过滤除去沉淀物。滤液用ICP-AES进行Cd2+,Cu2+,Zn2+,Pb2+的含量测定。
3 结果与讨论
3.1 水样的pH值和离子含量
对编号01-05 的5个水样进行pH测定,结果分别为2.5、2.5、3.0、3.5和3.5,02和05号水样的阳离子和阴离子的含量分别如表1所示。

表1 水样的离子浓度
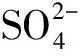
3.2 菌体的生物特性和生长规律
1) 形态特征。菌体为短杆状,革兰氏染色阴性(图1)。
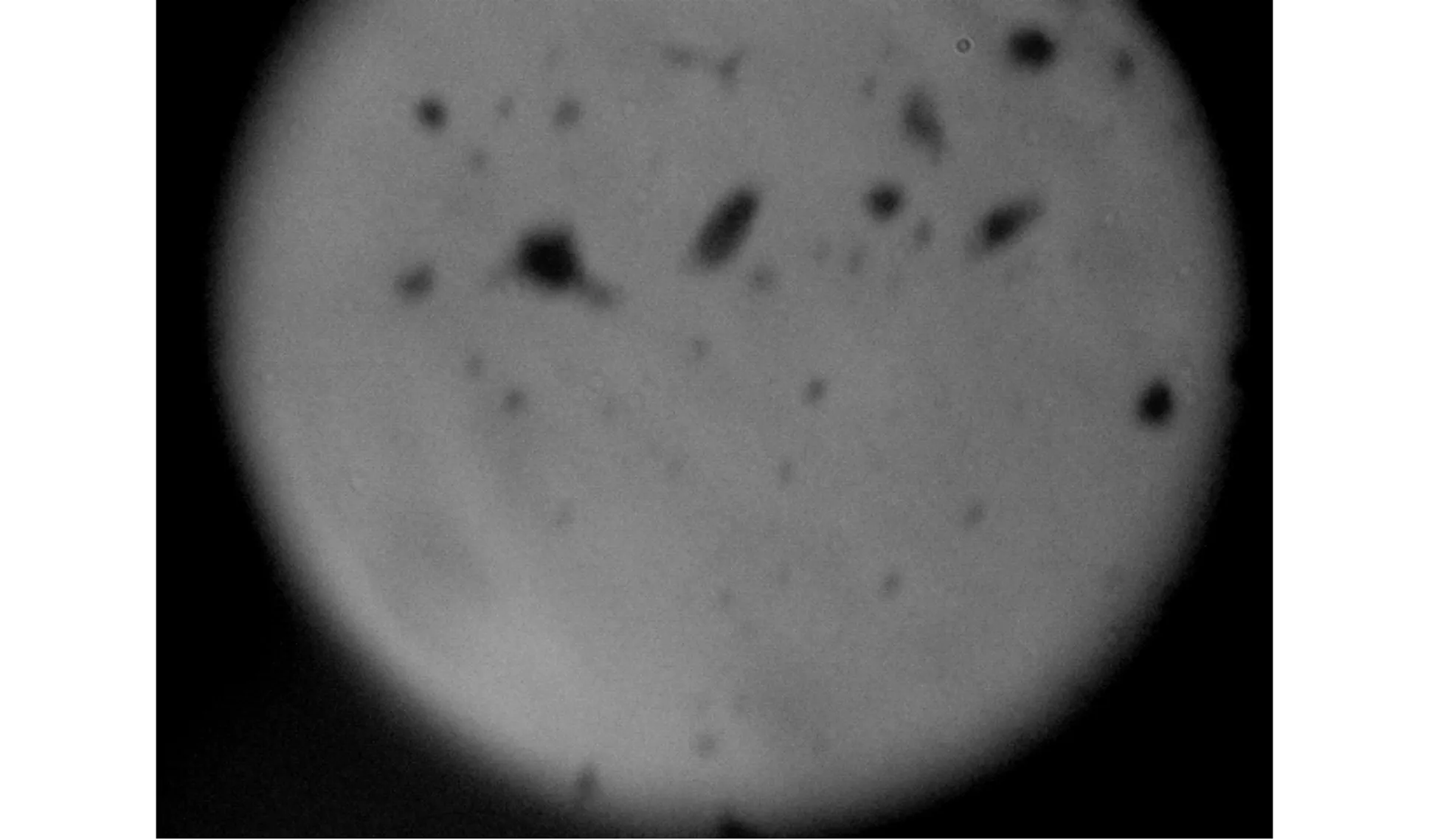
图1 革兰氏染色氧化亚硫铁杆菌的形态
2) 生长规律。菌体生长规律实验研究结果如图2所示。细菌菌数和pH值均呈先升后降趋势。0~12 h细菌菌数无明显变化;24~36 h细菌菌数快速增长;36~48 h菌数逐渐下降。0~36 h pH值逐渐升高;36~48 h pH值逐渐降低。沉淀物X衍射分析结果(图3)表明,黄色沉淀物主要成分为黄钾铁矾(KFe3(SO4)2(0H)6)。
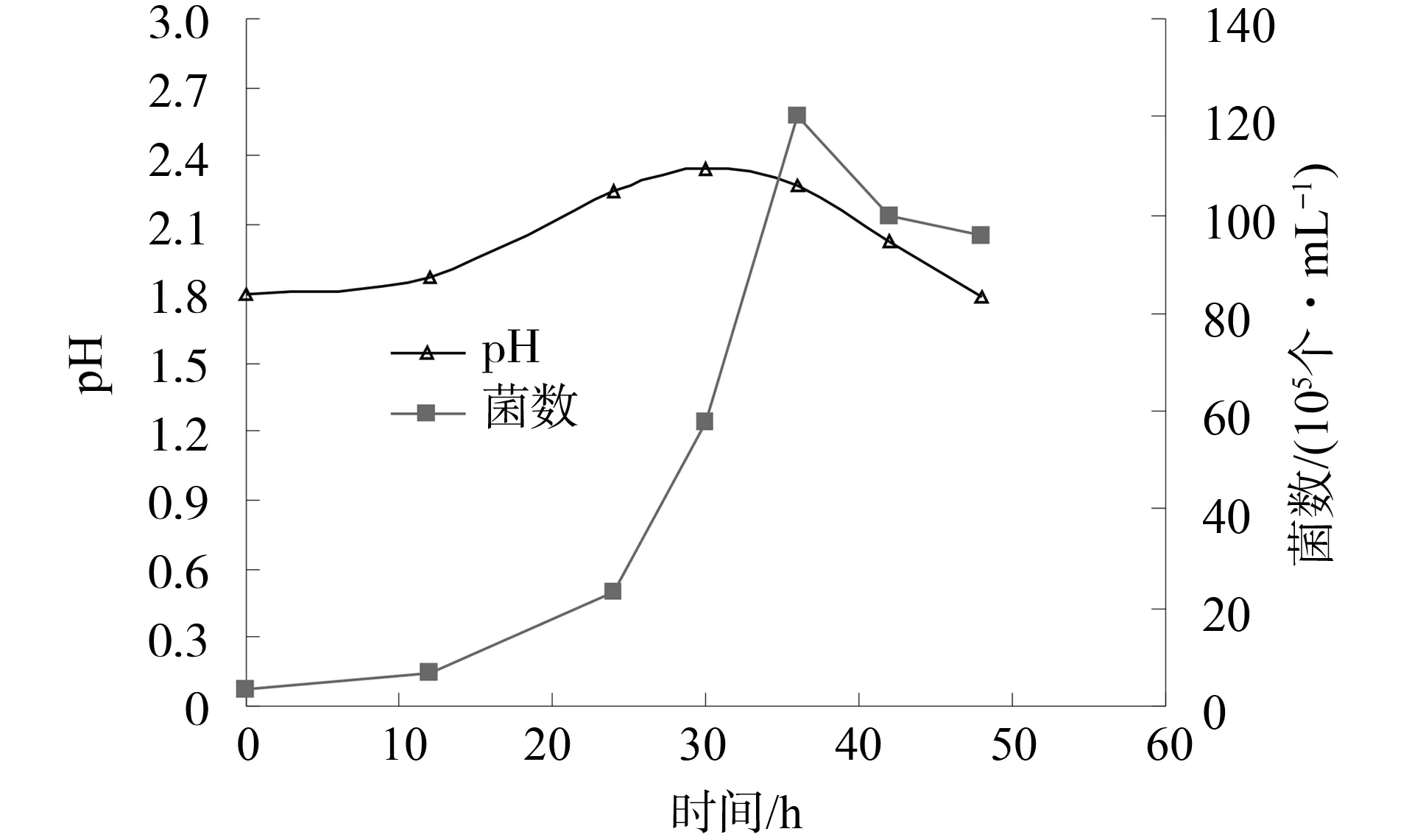
图2 溶液中细菌(A.f.) 数量和pH值随时间的变化
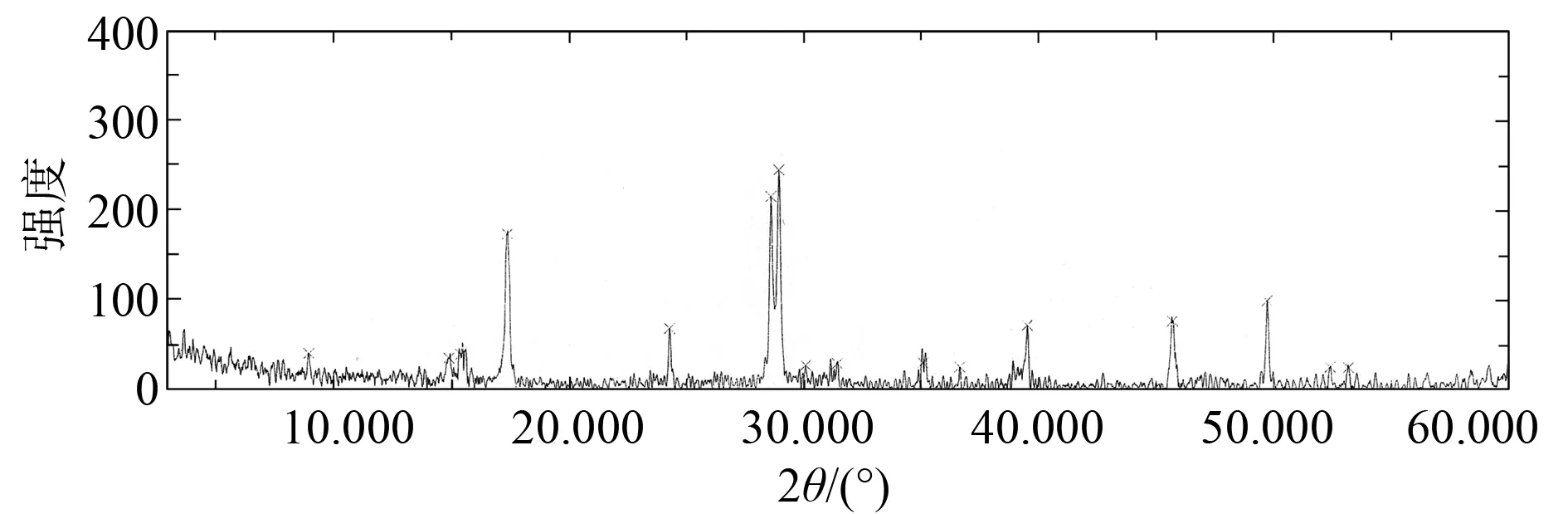
图3 黄色沉淀物(黄钾铁矾)的X射线衍射谱
由于0~12 h氧化亚铁硫杆菌处于诱导期,受到外环境改变的影响,数量增加缓慢,因此菌液值变化不明显;24~36 h氧化亚铁硫杆菌进入对数期,杆菌繁殖增快,值亦随之升高,生长周期内细菌个数最高达到120×105个/mL,pH值最高为2.35;36~48 h,杆菌进入稳定生长期及衰退期,菌液pH值亦随之降低[12]。沉淀物黄钾铁矾的形成过程可由下列方程式表示[9,13]:
KFe3(SO4)2(OH)6+8H+
上述研究表明,黄钾铁矾的生成是溶液pH值下降的主要原因。
3)溶液的pH对重金属含量的影响。表2表示氧化亚铁硫杆菌在不同pH值的培养基下,培养10 d后,溶液中几种重金属离子的含量。由此可见,在pH值为2.0~2.5时,溶液中的重金属离子含量相对较高;而pH值为3.0时,被测定的金属离子含量降低。表明在pH为2.0~2.5时,即氧化亚铁硫杆菌相对数量较多时,溶液的重金属含量反而比较高,结果与前人的研究结论不同[8],有待进一步研究。
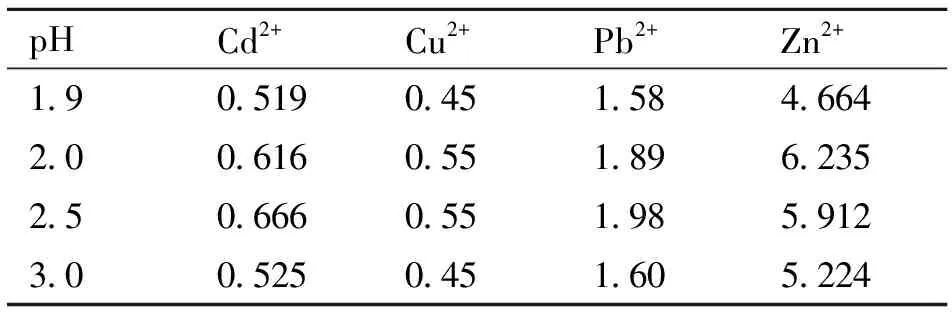
表2 不同pH培养基中AMD溶液的重金属离子含量
分析单位:中山大学测试中心
4 结 论
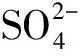
2)利用9K培养基从大宝山酸性矿山废水中培养出了氧化亚铁硫杆菌,菌体为短杆状,革兰氏染色阴性。培养过程中细菌菌数和溶液pH值均呈先升后降趋势。0~12 h细菌菌数无明显变化;24~36 h细菌菌数快速增长;36~48 h菌数逐渐下降;即细菌生长经历诱导期、对数期和稳定生长期及衰退期。0~36 h pH值逐渐升高;36~48 h值pH逐渐降低。
3)培养过程中出现黄色沉淀物,其主要成分为黄钾铁矾。黄钾铁矾的生成是溶液pH值下降的主要原因。
4)利用pH为2.0~2.5的9K培养基培养10 d后,AMD溶液中的Cd2+、Cu2+、Pb2+、Zn2+等重金属离子的含量较高,pH为3.0时降低。
5)大宝山铁龙尾矿水不仅应加入石灰等进行中和处理[4],更重要的是由于尾矿水中存在的氧化亚铁硫杆菌会加速硫化物矿物的氧化作用,应充分考虑利用微生物治理技术进行有效治理。
参考文献:
[1] 吴永贵,林初夏,童晓立,等.大宝山矿水外排的环境影响:Ⅰ.下游水生生态系统[J]. 生态环境,2005(2):165-168.
[2] 林初夏,卢文洲,吴永贵,等.大宝山矿水外排的环境影响:Ⅱ.农业生态系统[J]. 生态环境,2005(2):169-172.
[3] 周建民,党志,蔡美芳,等.大宝山矿区污染水体中重金属的形态分布及迁移转化[J]. 环境科学研究,2005(3):5-10.
[4] 陈炳辉,韦慧晓,周永章.粤北大宝山多金属矿山的生态环境污染原因及治理途径[J].中国矿业,2006,15(6):40-42.
[5] 付善明,周永章,赵宇鴳,等.广东大宝山铁多金属矿废水对河流沿岸土壤的重金属污染[J]. 环境科学, 2007(4):805-812.
[6] 周永章,付善明,张澄博,等.华南地区含硫化物金属矿山生态环境中的重金属元素地球化学迁移模型—重点对粤北大宝山铁铜多金属矿山的观察[J].地学前缘,2008,15(5):248-255.
[7] JOHNSON D B, HALLBERG K B. Acid mine drainage remediation options:a review [J]. Sci Total Environment,2005,338:3-14.
[8] 陆建军, 陆现彩,朱长见,等.氧化亚铁硫杆菌对矿山酸矿水中金属污染元素分布的影响[J].南京大学学报:自然科学,2005,41(2):113-119.
[9] 蒋磊,周怀阳,彭晓彤.广东云浮硫铁矿山氧化亚铁硫杆菌的分离及生长规律研究[J].高校地质学报,2006,12(1):93-97.
[10] 陆建军,陆现彩,王睿勇,等.金属矿山环境中矿物的微生物分解及环境效应研究进展[J].高校地质学报,2007,13(4):621-629.
[11] 国家环境保护总局,国家质量监督检验检疫总局.GB3838-2002地表水环境质量标准[S].2002.
[12] 周顺桂,周立详,黄焕忠.黄钾铁矾的生物合成与鉴定[J].光谱学与光谱分析,2004,24(9):1140-1143.
[13] 王艳锦,郑正,彭晓成,等. 氧化亚铁硫杆菌的分离及生长特性研究[J]. 环境保护科学,2007(4):30-33.

