TiO2纳米管/UV/O3对腐殖酸的降解及应用基础
潘留明,季 民,王秀朵,赵乐军,陆 彬
TiO2纳米管/UV/O3对腐殖酸的降解及应用基础
潘留明1,2,季 民1,王秀朵2,赵乐军2,陆 彬1
(1. 天津大学环境科学与工程学院,天津 300072;2. 天津市市政工程设计研究院,天津 300051)
用自制的二氧化钛纳米管(TNTs)作为催化剂,对腐殖酸进行TNTs/UV/O3工艺降解研究,优化了工艺参数,对相应的应用基础进行了研究.结果表明,在最佳工艺条件下,本工艺对总有机碳(TOC)去除率高达80.12%,显示了很好的降解能力.投加叔丁醇的实验得出TNTs/UV/O3对腐殖酸的降解遵循羟基自由基理论.从无机碳(IC)的角度分析得出,高pH值易于CO2溶解,从而使原水IC值增大,有助于反应过程中IC值的积累,无机碳多以CO32-及HCO3-存在,对·OH有很强的抑制作用.随着反应时间的推移,催化剂污染越来越严重,一定阶段后污染率达到最大值,随后污染情况得到改善.TNTs对TiO2/UV/O3工艺具有很好的催化性能.
TiO2纳米管;腐殖酸;光催化;臭氧化;污染率
长期大量存在的腐殖酸是导致渗滤液处理难度大、出水不易达标的一个重要原因,因为其基本分布于胶体态组分上,而可生物降解的有机物绝大多数存在于溶解态组分中[1].一般渗滤液生化出水的化学需氧量(chemical oxygen demand,COD)在500~2,000 ,mg/L范围内,其中大分子有机物主要由腐殖酸组成[2].因此,腐殖酸的降解研究对垃圾渗滤液的深度处理具有较强的指导意义.作为主要的深度处理技术,高级氧化技术(advanced oxidation process,AOPs)因其可产生强氧化性、无选择性的自由基得到广泛研究[3].相比其他的AOPs,光催化和臭氧化工艺由于其无毒、反应速率快、易于操作和无二次污染等优势成为研究热点.姜安玺等[4]应用光催化氧化体系对腐殖酸的降解进行了深入研究,最终生成小分子乃至二氧化碳、水和无机酸等.臭氧与腐殖酸反应时,往往与碳-碳双键反应,首先产生过氧化物中间产物,然后生成H2O2和羰基产物.近年来,由于2种或多种AOPs协同使用可增强羟基自由基的产生能力,提高反应速率,同时可克服各自存在的劣势,光催化和臭氧化联合工艺日益受到关注.Sánchez等[5]研究了光催化和臭氧化联合使用处理水中苯胺的效果,得出光催化与臭氧化具有明显的协同效应,现已用来处理无机阴离子和简单有机物,如甲氧萘丙酸[6]、草酸盐[7]、胺甲萘[8]和磺胺甲唑[9]等.随着TiO2催化剂的不断开发,光催化臭氧化(TiO2/UV/O3)逐渐作为一种单独的AOP来研究[10].目前,作为光催化臭氧化的TiO2催化剂多集中于纳米粉体、薄膜和掺杂的纳米粉体等方面,国内外对高比表面积的TiO2纳米管(titanium dioxide nanotubes,TNTs)作为光催化臭氧化催化剂的研究报道尚少.
本次实验用水热法制备了无毒、高比表面积、沉降性能较好的TiO2纳米管,前期实验表明,与P25相比TNTs在光催化臭氧化处理垃圾渗滤液过程中吸附性能和催化性能两方面均有较大提高[11].本次实验选择与垃圾渗滤液中相同浓度的腐殖酸为处理对象,以高比表面积的TiO2纳米管为催化剂,考察了光催化和臭氧化工艺的协同效应、催化剂煅烧温度、反应温度、初始pH值、TNTs投加量和O3投加量及光强I对总有机碳(total organic carbon,TOC)降解效果的影响,结合处理成本考虑,得出TNTs/UV/O3处理腐殖酸的最佳工艺,探讨了反应机理.
1 材料和方法
1.1 TiO2纳米管的制备
称取1.0,g,P25(德国Degussa),加入到16.0,mL浓度10,mol/L的NaOH溶液中,磁力搅拌0.5,h,移入聚四氟乙烯内衬的反应釜在105,℃下反应24,h,冷却至室温,蒸馏水洗涤至中性,用0.1,mol/L盐酸浸泡0.5,h后再次洗涤至中性,60,℃干燥,马弗炉中一定温度下煅烧2,h,研磨即得[12-13].
1.2 腐殖酸溶液的配置
称取1.0,g腐殖酸(分析纯)溶于100,mL浓度0.1,mol/L的NaOH溶液中,在30,℃水浴中加热10,min至腐殖酸溶解,用普通滤纸过滤,移入容量瓶中定容至1,L,作为腐殖酸储备液,测定其TOC值.实验中,取一定体积的储备液稀释至TOC为50,mg/L左右进行使用.
1.3 实验仪器
实验仪器包括TOC-VCPH(日本岛津)、SK-CFG-5-10实验室用臭氧发生器(济南三康)、HI19321型微电脑式酸碱度计(HANNA)、GJJ79-1磁力搅拌器(上海司乐)和SC-15数控超级恒温水槽(上海新芝).
1.4 实验装置
实验装置为自制圆柱型反应器,如图1所示,有效体积1.63,L(除去紫外灯管),高35.0,cm,内柱直径8.0,cm,保温层厚1.5,cm.其中保温层由恒温水槽控制以调节反应温度,实验所用灯源为波长274,nm、功率8~11,W的紫外灯(天津英泽),KI溶液瓶的作用为吸收尾气中的O3,碘量法测定O3浓度.根据课题组前期对天津汉沽垃圾填埋场垃圾渗滤液中腐殖酸浓度的测定[14],本次实验腐殖酸TOC浓度选择50,mg/L左右.

图1 光催化臭氧化处理腐殖酸的实验装置Fig.1 Experimental apparatus for the treatment of humic acid using photocatalytic ozonation
2 结果与讨论
2.1 工艺效果对比
在原水pH值8.54、反应温度20,℃、P25和TNTs-400投加量0.4,g/L、O3投加量0.238,g/h以及I为0.67,mW/cm2条件下,分别考察了UV/O3、UV/TNTs、P25/UV/O3和TNTs/UV/O34种工艺对腐殖酸TOC的降解效果,如图2所示.由于二氧化钛纳米管的特殊管状结构使其具有高比表面积,60,min时TNTs/UV/O3对TOC的去除率高达47.22%,相比P25/UV/O3提高了15.22%.前期实验表明,纳米管吸附能力所贡献的去除率远没达到整个去除率的增加量,去除率的增加主要是由于纳米管特殊结构引起的光解作用导致的[11].TNTs/UV/O3的增强因子f为
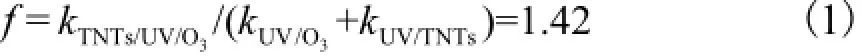
式中k为反应速率,mg/(L·min).
这说明光催化和臭氧化有明显的协同作用.故选择TNTs/UV/O3为腐殖酸的最佳降解工艺.

图2 4种工艺对TOC去除率的影响Fig.2 Effects of four technics on TOC removal
2.2 TNTs煅烧温度的影响
TNTs/UV/O3工艺中,在pH值8.54、反应温度20,℃、各煅烧温度产物TNTs投加量0.4,g/L、O3投加量0.238,g/h以及I为0.67,mW/cm2条件下,考察了煅烧温度(300、400、500、600和700,℃)对TOC去除效果的影响,如图3所示.煅烧温度为400,℃时,催化效果最好,其次是300、500、600和700,℃.分析原因主要是300,℃和400,℃煅烧产物均为内径5~7,nm,壁厚1,nm左右,长度200~300,nm的特殊管状结构,400,℃时晶型为催化效果较好的锐钛矿,300,℃时晶型以无定型及少量锐钛矿为主,随着煅烧温度的提高,500~700,℃时锐钛矿向金红石转变,纳米管受到破坏,逐渐转变为纳米棒甚至纳米颗粒,比表面积随之降低[15].故400,℃为TNTs最佳煅烧温度.
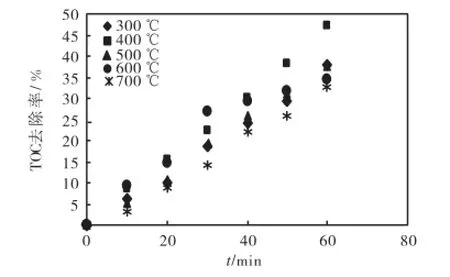
图3 TNTs煅烧温度对TOC去除效果的影响Fig.3 Effect of calcination temperature of TNTs on TOC removal
2.3 反应温度的影响
在pH值8.54、TNTs-400投加量0.4,g/L、O3投加量0.238,g/h以及I为0.67,mW/cm2条件下,通过恒温水浴控制反应温度,各温度(10、20、30和40,℃)条件下TOC的去除效果如图4所示.随着反应温度的升高,去除效果整体上升,但上升速率逐渐降低.60,min时,20,℃较10,℃时TOC去除率提高21.4%,30,℃较20,℃时提高14.7%,而40,℃较30,℃时仅提高了4.5%.故选择30,℃为最佳反应温度.2.4 初始pH值的影响
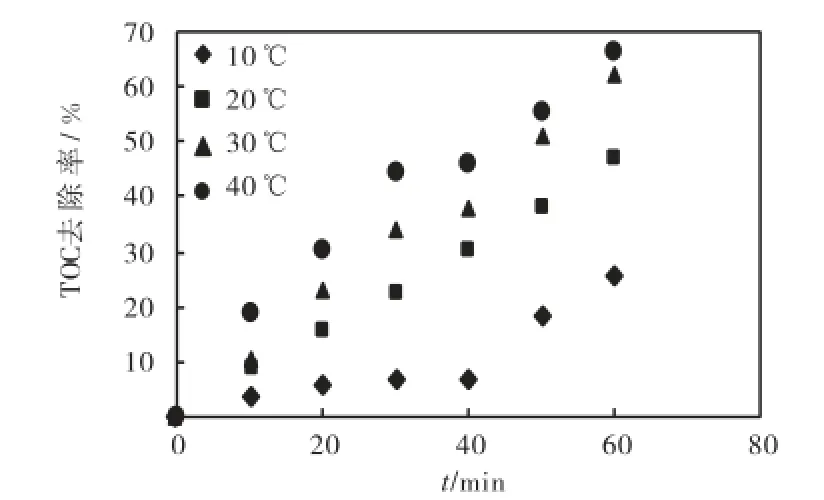
图4 反应温度对TOC去除效果的影响Fig.4 Effect of reaction temperature on TOC removal
在反应温度30,℃、TNTs-400投加量0.4,g/L、O3投加量0.238,g/h 以及I为0.67,mW/cm2条件下,分别用0.1,mol/L的NaOH溶液和H2SO4溶液调节原水pH值分别至4.42、6.32、8.54、10.76和12.36,考察其对TOC去除效果的影响,如图5所示.由图5中可以看出,前50,min,初始pH值为4.42~10.76时对TOC去除效果影响不大;60,min时,初始pH值10.76的TOC降解效果最好,但较pH值8.54时的去除率仅提高5.16%;初始pH值12.36时TOC去除效果最差.最佳初始pH值为8.5~10.7,考虑到配置的腐殖酸本身pH值为8~9,因此保持原水pH值不变即可.
分析pH值对处理效果的影响原因主要有:①如反应式(2)所示,pH值的升高有助于空穴产生羟基自由基,从而起到促进反应的效果;②pH值的降低有利于O3捕获TiO2纳米管表面电子后的产物产生羟基自由基和双氧水(如反应式(3)和(4)).因此,pH值过高或者过低均不利于羟基自由基的产生,对污染物的降解起到负面作用.

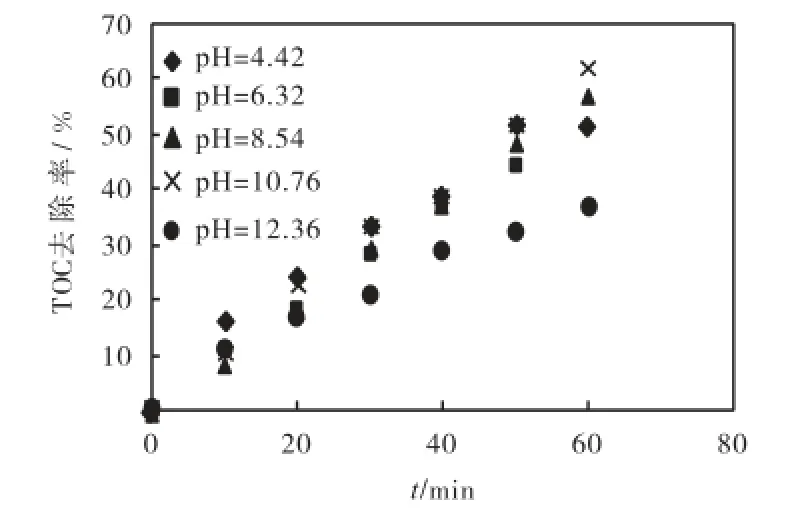
图5 初始pH值对TOC去除效果的影响Fig.5 Effect of original pH value on TOC removal
2.5 TNTs投加量的影响
在原水pH值、反应温度30,℃、O3投加量0.238,g/h以及I为0.67,mW/cm2条件下,考察催化剂投加量(0.3、0.4、0.5和0.6,g/L)对TOC去除率的影响,如图6所示.投加量0.6,g/L时TOC去除效果最好,0.3,g/L时最差.60,min时,随着催化剂量的增加,TOC去除率分别为50.13%、61.95%、62.93%和67.99%.分析原因,当催化剂量从0.3,g/L增至0.4,g/L时,体系中催化活性位置增多,有助于产生更多的·OH(如反应式(5)~(8)所示),使TOC去除率增加了11.82%;当催化剂量从0.4,g/L增至0.6,g/L时,TOC去除率仅增加6%左右,主要是由于催化剂量的进一步增加导致颗粒对紫外光的遮蔽和散射,一定程度上影响了催化性能的提高.综合处理成本考虑,选择0.4,g/L为最佳催化剂投加量.


图6 TNTs投加量对TOC去除效果的影响Fig.6 Effect of TNTs dosage on TOC removal
2.6 O3投加量的影响
在原水pH值、反应温度30,℃、TNTs-400投加量0.4,g/L以及I为0.67,mW/cm2条件下,考察了不同O3投加量(0、0.189、0.238、0.383、0.582和0.672,g/h)对TOC去除率的影响,如图7所示.当臭氧投加量为0.383,g/h时TOC去除率最佳,高达82.67%,其次为0.582、0.672、0.238和0.189,g/h时的降解效果.结果表明,当臭氧投加量从0.189,g/h增至0.383,g/h时TOC去除率有所增加;而臭氧投加量在0.383~0.672,g/h时,随着投加量的增加,去除率反而呈下降趋势.一方面,随着臭氧投加量的增加,臭氧作为电子受体可使催化剂表面的空穴与电子复合的机率降低,有助于·OH的生成(如反应式(3)和(4)).另一方面,(如反应式(9)所示),当臭氧量增加至一定程度后,臭氧本身可以与·OH反应,对·OH有一定的淬灭作用,使TOC去除率反而降低.故选择0.383,g/h为最佳臭氧投加量.
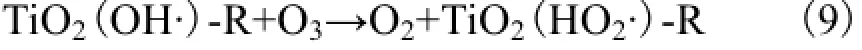

图7 臭氧投加量对TOC去除效果的影响Fig.7 Effect of ozone dosage on TOC removal
2.7 光强的影响
在pH值8.54、反应温度30,℃、TNTs-400投加量0.4,g/L以及O3投加量0.383,g/h条件下,分别考察I为0.62、0.67和0.75,mW/cm2的紫外灯光源照射下该工艺对腐殖酸TOC的去除率.由实验结果拟合得出3种反应过程均为零级反应,且有很强的相关性.如表1所示,随着光强的增加,反应速率呈上升趋势,但上升幅度有限.综合处理成本和去除效果考虑,选择I为0.62,mW/cm2的紫外灯为最佳光源.

表1 光强对TOC去除率的影响Tab.1 Effect of light intensity on TOC removal
2.8 相应应用基础研究
2.8.1 羟基自由基反应的判断
选用叔丁醇作为羟基自由基捕获剂,对TNTs/ UV/O3降解腐殖酸是否符合羟基自由基理论进行判断.叔丁醇与·OH的反应速率常数高达5×108,
L/(mol·s), 是一种很强的·OH捕获剂,也是自由基反应的有效检测剂.叔丁醇投加量对TOC去除率的影响如图8所示.从图中可以看出,投加叔丁醇后TOC去除率大幅度降低,投加0,mg/L时60,min TOC去除率高达85.72%,投加量为5.6,mg/L时60,min TOC去除率仅为25.56%,下降了60.16%;投加量为11.2,mg/L时60,minTOC去除率降至17%.说明叔丁醇的投加严重影响了TOC的去除率,主要原因是叔丁醇对反应器中的羟基自由基进行了捕获,所以TNTs/UV/O3对腐殖酸的降解遵循羟基自由基理论.
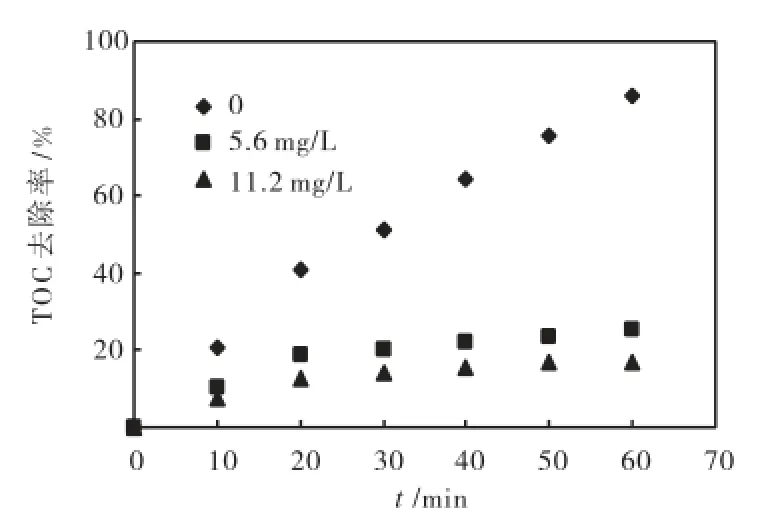
图8 叔丁醇投加量对TOC去除率的影响Fig.8 Effect of tert-butyl alcohol dosage on TOC removal
2.8.2 无机碳的影响
水中无机碳(inorganic carborn,IC)主要以CO2、形式存在,是较强的自由基清除剂,其中的抑制能力远大于H的抑制能力.所以,反应初始IC值和过程中产生的IC均会对处理效果产生严重影响.而pH值对无机碳的溶解起着关键作用,本次实验从IC角度分析了pH值对TOC降解效果的影响,如图9所示.由图9可以看出,原水pH值的增加使得更多气体CO2溶于水中,导致初始IC值的增加,pH值12.36时,IC值为21.9,远大于其他pH值条件下IC值,且此pH值条件下多以及少量存在,对·OH有很强的淬灭作用.氧化过程中,有机碳不断降解为无机碳致使反应初期IC值的增加,随着反应时间的延长,原水pH值4.42~10.76的反应在10,min后IC值由于生成CO2量的累积溢出而呈下降趋势,而原水pH值12.36的反应由于高pH值溶液易于CO2的溶解使得IC值在40,min时才开始下降,整体来说远高于其他原水pH值时反应过程中的IC值,且高pH值时多以及存在,对·OH的抑制作用较为明显.因此,强碱性原水对初始IC值的影响及反应过程中IC值的累积导致了TOC去除率的下降.
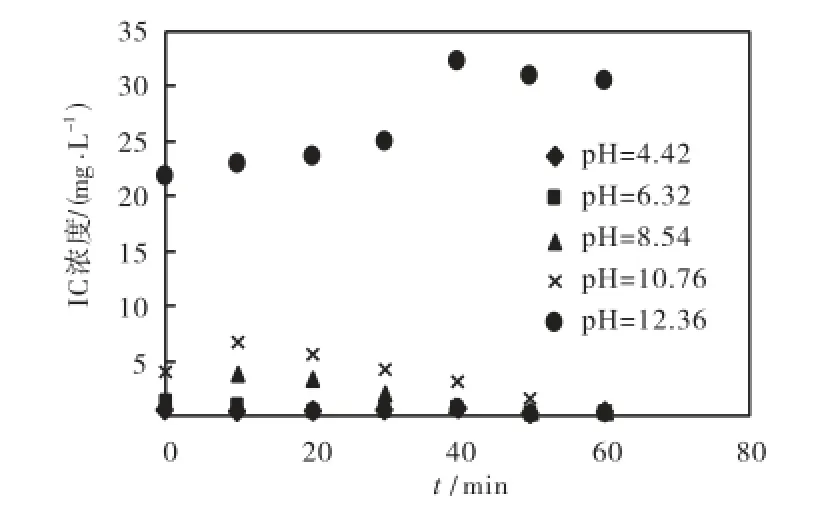
图9 原水pH值对反应过程中IC浓度的影响Fig.9 Effect of original pH value on IC concentration in reaction
2.8.3 催化剂的污染
考察催化剂的催化性能时,催化剂的抗污染能力必须作为一个重要因素来考虑,因为在处理过程中,催化剂往往容易被有机物本身、中间产物以及污染而影响催化性能.此次实验过程中,通过TOC仪器在900,℃高温条件下碳化催化剂来测量催化剂表面的总碳(S-TC).0.3,g,TNTs加入到1,L腐殖酸中磁力搅拌1,h,通过0.45,µm的膜抽滤得到被污染的催化剂,室温下晾干待测,此S-TC记作STC0,同时这个值可代表该TNTs在1,h内对腐殖酸的最大污染承受能力,以TC计.在光催化臭氧化工艺中,一定时间时取出被污染催化剂,抽滤干燥后,取0.3,g测定其S-TC,记作S-TC1.催化剂污染率可表示为

光催化臭氧化工艺中TNTs-400随反应时间的污染情况如图10所示.由图10可以看出,前10,min, TNTs-400的污染率高达70%以上,且反应初期随着反应时间的延长,催化剂污染率升高,40,min时达到最大值90%以上,此后催化剂污染情况随着时间的推移有所好转,污染率逐渐降低,60,min时污染情况和10,min时相当.说明由于反应初期溶液中有机物浓度较高,所以催化剂表面吸附污染物较多,40,min时达到最大值,基本吸附饱和,随着时间的推移,溶液中TC浓度降低,同时催化剂表面吸附有机物被羟基自由基和臭氧逐渐降解,催化剂污染情况得到改善.
图10 不同反应时间的催化剂污染情况Fig.10 Pollution condition of catalyst in different reaction times
3 结 论
(1)TNTs/UV和UV/O3有很强的协同作用,TNTs/UV/O3的增强因子f为1.42.综合TOC去除率和处理成本两者考虑,TNTs/UV/O3对腐殖酸降解的最佳工艺参数为:TNTs煅烧温度400,℃,反应温度30,℃,pH值8.5~10.7,催化剂投加量0.4,g/L,臭氧投加量0.383,g/h,光强0.62,mW/cm2,TOC去除率高达80.12%.
(2)TNTs/UV/O3对腐殖酸的降解遵循自由基原则.
(3)高pH值时,CO2易于溶解使得原水IC值增大,有助于反应过程中IC值的积累,且多以CO32−及HCO−3存在,对·OH有很强的抑制作用,致使TOC去除率下降.
(4)反应初期溶液催化剂表面吸附污染物较多,40,min时达到最大值,基本吸附饱和,随着时间的推移,催化剂污染情况得到改善.
[1] 陈现明,王成伟,董云峰. 垃圾填埋场渗滤液的组成和处理方法[J]. 舰船防化,2008(3):27-33.
Chen Xianming,Wang Chengwei,Dong Yunfeng. Components and treatment technique of landfill leachates [J]. Chemical Defence on Ships,2008(3):27-33(in Chinese).
[2] 王进安,刘学建,杜 巍,等. 北京阿苏卫垃圾卫生填埋场渗沥液处理[J]. 环境卫生工程,2006,14(3):l5-l7.
Wang Jin’an,Liu Xuejian,Du Wei,et al. Leachate treatment of Asuwei waste sanitary landfill site of Beijing [J]. Environmental Sanitation Engineering,2006,14(3):l5-l7(in Chinese).
[3] Černigoj U,Lavrenčič Štangar U,Trebše P. Degradation of neonicotinoid insecticides by different advanced oxidation processes and studying the effect of ozone on TiO2photocatalysis [J]. Applied Catalysis B:Environmental,2007,75(3/4):229-238.
[4] 姜安玺,高 洁,王化云,等. 水中腐殖酸的光催化氧化研究[J]. 哈尔滨建筑大学学报,2001,34(2):44-47.
Jiang Anxi,Gao Jie,Wang Huayun,et al. Photocatalytic oxidation of humic acid in water [J]. Journal of Harbin University of Civil Engineering and Architecture,2001,34(2):44-47(in Chinese).
[5] Sánchez L,Peral J,Domènech X. Aniline degradation by combined photocatalysis and ozonation [J]. Applied Catalysis B:Environmental,1998,19(1):59-65.
[6] Rosal R,Rodríguez A,Gonzalo M S,et al. Catalytic ozonation of naproxen and carbamazepine on titanium dioxide [J]. Applied Catalysis B:Environmental, 2008,84(1/2):48-57.
[7] Maurizio A,Vincenzo A,Elisa G L,et al. Oxidation of oxalate ion in aqueous suspensions of TiO2by photocatalysis and ozonation [J]. Catalysis Today,2005,107/108:612-618.
[8] Rajeswari R,Kanmani S. A study on synergistic effect of photocatalytic ozonation for carbaryl degradation [J]. Desalination,2009,242(1/2/3):277-285.
[9] Fernando J B,Almudena A,Juan F G. Mechanism and kinetics of sulfamethoxazole photocatalytic ozonation in water [J]. Water Research,2009,43(5):1359-1369.
[10] Farre M J,Franch M I,Malato S,et al. Degradation of some biorecalcitrant pesticides by homogeneous and heterogeneous photocatalytic ozonation [J]. Chemosphere,2005,58(8):1127-1133.
[11] 潘留明,季 民,王苗苗,等. TiO2纳米管的制备及对O3的催化性能[J]. 化工学报,2007,58(11):2787-2792.
Pan Liuming,Ji Min,Wang Miaomiao,et al. Preparation of titanium dioxide nanotube and its catalytic activity for ozonation [J]. Journal of Chemical Industry and Engineering(China),2007,58(11):2787-2792(in Chinese).
[12] Tomoko Kasuga. Formation of titanium oxide nanotubes using chemical treatments and their characteristic properties [J]. Thin Solid Films,2006,496(1):141-145.
[13] Lan Y,Gao X P,Zhu H Y,et al. Titanate nanotubes and nanorods prepared from rutile powder [J]. Advanced Functional Materials,2005,15(8):1310-1318.
[14] 刘卫华. 催化臭氧去除垃圾渗滤液中DEHP及高浓度腐殖质的机理研究[D]. 天津:天津大学环境科学与工程学院,2007.
Liu Weihua. The Mechanism of Catalytic Ozonation of DEHP and Humic Substance of High Concentration in Landfill Leachate [D]. Tianjin:School of Environmental Science and Engineering,Tianjin University,2007(in Chinese).
[15] Lee C K,Lin K S,Wu C F,et al. Effects of synthesis temperature on the microstructures and basic dyes adsorption of titanate nanotubes [J]. J Hazard Mater,2008,150(3):494-503.
[16] Lindner M,Theurich J,Bahnemann D W. Photocatalytic degradation of organic compounds:Accelerating the process efficiency [J]. Water Sci Technol,1997,35(4):79-86.
Degradation and Applied Basis of Humic Acid Treated by TiO2Nanotubes/UV/O3
PAN Liu-ming1,2,JI Min1,WANG Xiu-duo2,ZHAO Le-jun2,LU Bin1
(1. School of Environmental Science and Engineering,Tianjin University,Tianjin 300072,China;2. Tianjin Municipal Engineering Design and Research Institute,Tianjin 300051,China)
In this paper,degradation of humic acid was studied by the combined technical of photocatalysis and ozonation which was catalyzed by TiO2nanotubes (TNTs). The technological parameters were optimized and the applied bases concerned were studied. The result shows that the rate of TOC removal of humic acid by TNTs/UV/O3reaches 80.12% under the optimal condition. It proves that radical reaction played the main role in humic acid degradation by TNTs/UV/O3. The mechanism of pH value on this technic was analyzed by inorganic carbon(IC). At high pH value,CO2was easily dissolved so that the value of original IC was increased,which easily accumulated IC in the reaction. The IC mainly existed in,which had obvious inhibition to ·OH. The pollution of catalyst was increased with time extending in the reaction.After a period of time,its pollution rate would reach the maximum.Then,its pollution would be improved. The study shows that TNTs are good catalysis for TiO2/UV/O3.
titanium dioxide nanotubes;humic acid;photocatalysis;ozonation;pollution rate
X703.1
A
0493-2137(2010)04-0333-06
2009-01-06;
2009-07-13.
天津市科技发展计划资助项目(06YFGZSH06700).
潘留明(1982— ),男,博士,工程师,liumingpan@126.com.
季 民,jimin@tju.edu.cn.

