利用CO2开采海底天然气水合物影响因素分析
任德刚
(中国电力工程顾问集团公司)
利用CO2开采海底天然气水合物影响因素分析
任德刚
(中国电力工程顾问集团公司)
通过介绍气体水合物的晶体结构,从热力学方面论证了利用CO2开采海底天然气水合物的可行性,并分析了铠甲效应、温度、压力、晶体结构、晶穴充满度、多孔介质、盐度、添加剂及乳化等多种因素对CO2与CH4水合物置换反应的影响,最后指出今后研究的重点应为采取各种措施强化反应过程。该研究成果为CO2封存和海底天然气开采研究提供了一种新思路。
CO2;开采;天然气水合物;影响因素
0 引言

随着CO2捕集项目的不断投运,捕集的CO2除了少量可用于工业生产和油田回注外,大部分需要以液态形式进行地质封存和海底封存。直接进行海底封存存在影响海洋生态环境和CO2可能逸散回大气等问题[1]。气体水合物是在一定温度和压力下由气体分子填充水分子产生的晶格而形成的一种白色笼形晶体[2],是由主体分子即水分子间以氢键相互结合形成笼形空隙,并将客体分子即气体分子包络在其中所形成的非化学计量的包络化合物[3]。主、客体分子之间的作用力为范德华力[2]。 目前已知 100 多种气体如 CH4,C2H6,CO2,N2和O2等均可形成气体水合物[3]。形成天然气水合物的主要气体为CH4,通常将CH4分子含量超过99%的天然气水合物称为甲烷水合物(Methane Hydrate)。CH4水合物的构成表达式为CH4·nH2O,其中n为H2O分子和CH4分子的摩尔比,其理论最小值为5.75[4]。理论上1 m3的CH4水合物在标准条件下,可释放出164 m3的 CH4气体和 0.8 m3的水[5]。 海底存在大量天然气水合物,含量高达 1.2×1017m3[6]。因此,利用CO2开采海底天然气水合物,不仅可以解决CO2封存问题,而且可以缓解人类面临的能源危机。
1 利用CO2开采海底天然气水合物的热力学可行性
天然气水合物的形成需要具备3个基本条件:首先,温度不能太高,在0℃以上就可生成,以0~10℃为宜,而高于20℃就会分解;第二,压力要够,但也不能过大,在0℃的温度和3.03 MPa的压力下就可以生成;第三,要有足量的天然气气源[7]。因此,天然气水合物在深度为300~500 m、温度为2~4℃的海洋陆架斜坡和深海盆地沉积物中广泛存在。天然气水合物的赋存条件易于模拟,为实验研究利用CO2开采海底天然气水合物提供了条件。
1.1 热平衡
水合物的生成反应为放热反应,分解反应为吸热反应。当n=6.15时,CH4水合物的分解热为54.49 kJ/mol,CO2水合物的合成热为 57.98 kJ/mol[8]。 因此,CH4水合物分解所需的热量,完全可以由形成CO2水合物所释放出的热量提供,此时,置换反应将会自发进行。
1.2 相平衡
图1为CH4-CO2水合物相平衡及CO2的V-L关系曲线[9]。 从图 1可看出,在同一温度下,CH4平衡压力明显高于CO2平衡压力,二者间的压力差就是CO2与CH4水合物置换反应的推动力;V-L曲线则表示在某一温度下进行置换反应时,以液态或气态CO2与CH4水合物进行反应必须维持的压力下限或上限。
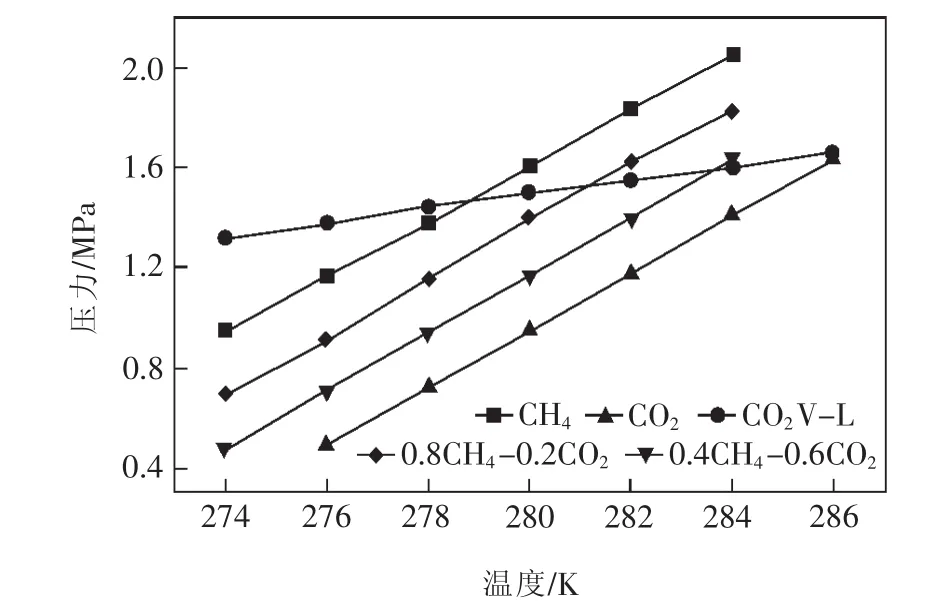
图1 CH4-CO2水合物相平衡及CO2的V-L关系曲线(据文献[9]略有修改)Fig.1 CH4-CO2hydrate phase equilibrium and CO2V-L curve
1.3 实验验证
Sivaraman[8]用实验证明了 CO2置 换 CH4水 合物的可行性。通过气相色谱分析,实验68 h后,气相中的CO2摩尔比例由100%下降到72.33%,CH4的摩尔比例由0上升到27.67%。Ohgaki等[9]发现,当置换实验在某条件下达到相平衡时,水合物中CH4的摩尔比例下降到48%,而气相中CH4的摩尔比例达到70%,即CH4在气相和水合物相中的分配系数为 1.458。 Komal[10]在精确控制压力仓中压力为3.5 MPa、温度为276±0.5 K的条件下,发现置换反应1h后,反应产物中CO2水合物和CH4水合物的比例分别为40%和45%,而且随着时间的推移,CO2水合物的比例越来越高;12 h后,置换反应基本完成。
2 影响置换反应的主要因素分析
2.1 铠甲效应
由于气体水合物为冰状晶体,因此,当CO2分子与位于晶体表面的CH4水合物接触时,置换反应的速度会变得很快。随着反应不断进行,生成的CO2水合物在晶体表面形成一层铠甲,使CO2分子向晶体内部的运动越来越困难,置换反应速度逐渐变慢。王金宝等[11]通过实验研究发现,在置换反应开始的2 h内,置换出的CH4量及进入水合物相的CO2量都会迅速增加。此后二者变化趋于平缓,置换反应速度变慢,进入平稳发展阶段,验证了铠甲效应的存在。
2.2 温度
温度对置换过程的影响十分明显,温度越高,越有利于置换反应的进行。例如,在压力为3.5MPa、置换时间为104 h的条件下,置换温度为276.15 K时的置换效率为6.90%,而置换温度为278.15 K时的置换效率为8.54%,后者比前者的置换效率提高了1.64%,如图2所示。
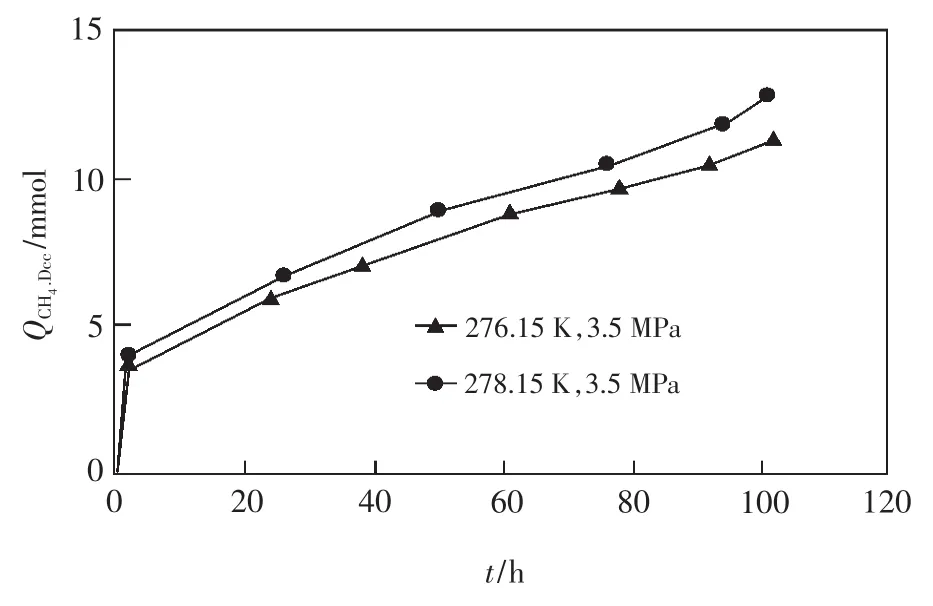
图2 不同温度条件下CH4被置换量随时间的变化(据文献[11]略有修改)Fig.2 Amount of CH4replaced change with time at different temperature
2.3 压力
压力越高,越有利于置换反应的进行,但其影响比温度要小。例如,在温度为276.15 K、置换时间为104 h的条件下,压力为3.5 MPa时的置换效率为6.90%,而压力为3.8 MPa时的置换效率为8.03%,后者比前者的置换效率提高了1.13%,如图3所示。
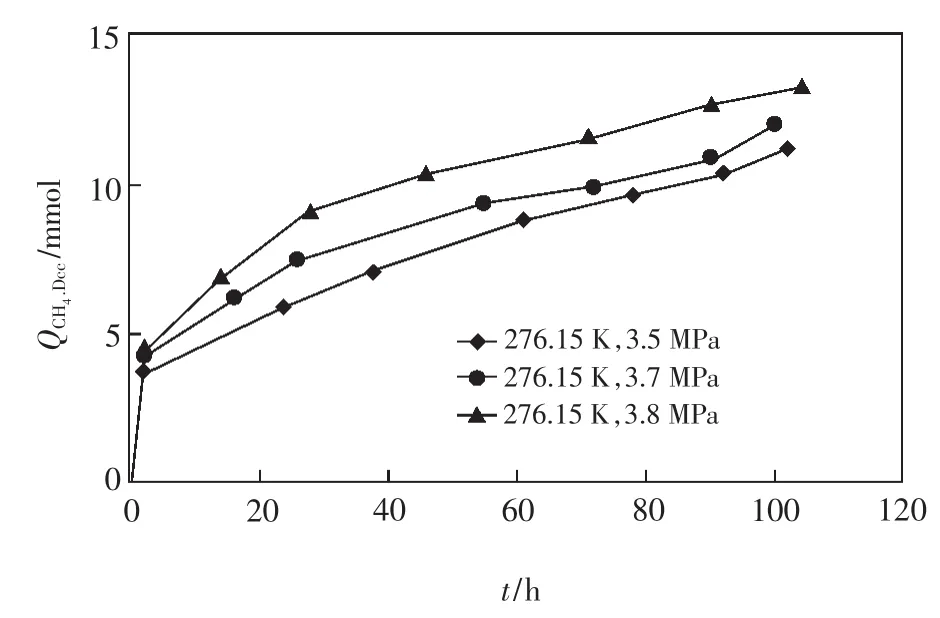
图3 不同压力条件下CH4被置换量随时间的变化(据文献[11]略有修改)Fig.3 Amount of CH4replaced change with time at different pressure
2.4 晶体结构
CH4与CO2水合物单晶均为结构Ⅰ型,由2个小晶穴和6个中晶穴组成。小晶穴为五边形十二面体(512),直径为0.510 nm;中晶穴为12个五边形和2个六边形组成的十四面体(51262),直径为0.586 nm。CH4分子的范德华直径为0.436 nm,能够填充在小晶穴和中晶穴中,而CO2分子的范德华直径为0.512nm,只能填充在中晶穴中[12]。水合物为了维持自身的稳定性,部分分解出的CH4分子重新占据小晶穴,致使CH4水合物小晶穴的分解速率远低于中晶穴的分解速率。即使CO2全部占据中晶穴,将仍有1/4的CH4分子残留在水合物晶体中[13],造成能源资源的浪费。
2.5 晶穴充满度
自然界中的甲烷水合物平均只有大约1/3的晶穴被气体分子占据,发生置换反应时有部分CO2分子会进入水合物的空晶穴,同时也有部分CO2分子会进入游离水中形成水溶液,因此,置换反应中CO2的消耗量会大于CH4的产量。实验证明,CO2消耗量和CH4产量的摩尔比最高可达到5.6[11]。
2.6 多孔介质
海底的天然气水合物存在于海底沉积带中。海底沉积带特定的温度和压力范围以及多孔介质特性会影响置换反应的热力学特性。多孔介质特性如孔径、介质材料和表面结构对置换反应均有影响,其中孔径的影响最大。孔径越小,其对置换反应的影响越大。例如,在孔径为10 nm的多孔介质中,CO2水合物的平衡温度降低5 K;在孔径为4 nm的多孔介质中,CO2水合物的平衡温度降低12 K[13]。由于多孔介质会降低CO2的扩散速度,因此,在多孔介质中置换反应速率只有大容积反应器中置换反应速率的1/2~1/4[14]。 孔径越小,CO2和 CH4的反应热差值就越大,越有利于反应进行。
2.7 盐度
盐度随海洋深度的增加而升高。盐度越高,水合物平衡温度越低。阳离子对置换反应的影响程度由大到小依次为 Mg2+,Ca2+,Na+,K+,其中只有 Mg2+影响显著。阴离子对置换反应的影响程度由大到小依次为这 3 种阴离子浓度对水合物相平衡点的影响均较显著[15]。当盐度低于4%时,其对水合物晶穴充满度的影响不明显;当盐度高于4%时,晶穴充满度会随盐度的升高而降低[16]。
2.8 添加剂
CO2在静态系统纯水体系中的形成速率非常缓慢,而注入添加剂可以提高水合物的生成速率。常见的添加剂有表面活性剂、水溶性聚合物添加剂和不溶于水的液态烃添加剂。例如,在添加质量分数为0.1%的Silwet L277后,在相同时间内CO2水合物的生成速率是纯水体系的5.3倍[17]。0.3%的十二烷基硫酸钠 (SDS)、0.3%的SDS和4%的四氢呋喃(THF)的混合物也能对CO2水合物的生成起到显著的改善效果[18]。
2.9 乳化
为了提高反应速率,McGrail等[19]提出了一种所谓强化气体水合物的回收法(EnhancedGasHydrate Recovery,简称EGHR)。该方法的要点是:首先通过一定的方法制成以液态CO2为分散相、水为连续相的乳化液,其中CO2占总体积的50%~70%;然后,在一定的压力下,将乳化液注入事先在砂层中形成的CH4水合物层,使之与水合物接触,置换出水合物中的CH4。这样充分利用了H2O-CO2混合物体系的物理和热力学性质,并结合了多孔介质中受控多相流、热量和质量传递过程的优点,使置换反应得到强化[20-24]。通过改变乳化液的温度、CO2与水的比例以及CO2作为分散相的粒度大小,可以实现对置换反应过程的控制。
3 结束语
利用CO2开采海底天然气水合物,具有环保和经济的双重意义。从热力学角度讲,用CO2置换天然气水合物中的CH4是完全可行的。CO2置换CH4的反应受多种因素的影响,目前对影响因素种类及影响程度的研究仍处于理论和实验阶段,置换反应速率还达不到工业应用的水平,因此,采取各种措施强化反应过程,应该成为今后研究的重点。
[1]石谦,郭卫东,韩宇超,等.二氧化碳海洋倾废的研究进展[J].海洋通报,2005,24(2):72-78.
[2]杨晓西,丁静,杨建平,等.水合物分离二氧化碳气体的研究[J].东莞理工学院学报,2006,13(4):51-56.
[3]王新裘,俊红.笼形水合物研究与应用[J].化工生产与技术,2004,11(3):19-22.
[4]Kvenvolden K A.李玉梅,译.天然气水合物中甲烷的地球化学研究[J].天然气地球科学,1998,9(3/4): 9-18.
[5]蒋向明.天然气水合物的形成条件及成因分析[J].中国煤炭地质,2009,21(12):7-11.
[6]Klauda J B,Sandler S I.Global distribution of methane hydrate in ocean sediment[J].Energy&Fuels,2005,19(2):459-470.
[7]吴后波,苏晓波,颜文.海底天然气水合物的微生物成因及识别[J].海洋科学,2008,32(3):96-100.
[8]Sivaraman R.The potential role of hydrate technology in sequestering carbon dioxide[J].Gas Tips,2003,9(4):4-7.
[9]Ohgaki K,Takano K,Sangawa H,et al.Methane exploitation by carbon dioxidefromgashydrates-phaseequilibriaforCO2-CH4mixed hydrate system[J].Journal of Chemical Engineering of Japan,1996,29(3):478-483.
[10]Komal T.祝斌强,译.二氧化碳和甲烷水合物再形成与置换的动力学机制[J].海洋地质,2008,(24):33-40.
[11]王金宝,郭绪强,陈光进,等.二氧化碳置换法开发天然气水合物的实验研究[J].高校化学工程学报,2007,21(4):715-719.
[12]Sloan E D.Clathrate hydrates of natural gases[M].New York:Marcel Dekker,1998.
[13]罗莎莎,刘宏菊,孙也.CO2开采海底天然气水合物的研究进展[J].中国资源综合利用,2008,26(3):19-23.
[14]周锡堂,樊栓狮,梁德青.CO2置换开采天然气水合物研究进展[J].化工进展,2006,25(5):524-527.
[15]宋永臣,杨明军,刘瑜,等.离子对甲烷水合物相平衡的影响[J].化工学报,2009,60(6):1362-1366.
[17]刘妮,张国昌,罗杰斯R E.二氧化碳气体水合物生成特性的实验研究[J].上海理工大学学报,2007,29(4):405-408.
[18]刘妮,刘道平,谢应明.水合物法高效储存二氧化碳气体的实验研究[J].中国电机工程学报,2009,29(14):36-40.
[19]McGrail B P,Zhu T,Hunter R B,et al.A New Method for Enhanced Production of Gas Hydrates with CO2[C]∥AAPG Hedberg Conference.Gas Hydrates:Energy Resource Potential and Associated Geologic Hazards.Vancouver,2004 :1-3.
[20]杜金虎,何海清,皮学军,等.中国石油近年勘探进展及未来勘探接替领域与重点区带[J].岩性油气藏,2011,23(1):1-16.
[21]李武广,邵先杰,康园园,等.油藏分类体系与方法研究[J].岩性油气藏,2010,22(2):123-127.
[22]刘云,卢渊,伊向艺,等.天然气水合物预测模型及其影响因素[J].岩性油气藏,2010,22(3):124-127.
[23]王涛.盐水层CO2埋存潜力及影响因素分析[J].岩性油气藏,2010,22(增刊):85-88.
[24]文钢锋,王智,韩军,等.地质模型反演预测隐蔽油气藏[J].岩性油气藏,2009,21(1):94-98.
Influencing factors of subsea natural gas hydrate exploitation with CO2
REN De-gang
(China Power Engineering Consulting Group Corporation,Beijing 100120,China)
This paper introduced the crystal structure of gas hydrate,discussed the feasibility on methane hydrate exploitation with CO2from thermodynamics,and analyzed the effects of different factors on the replacement reaction,including loricae effect,temperature,pressure,crystal structure,crystal cage fill fraction,porous media,salinity,additive and microemulsion.It is pointed out that reinforcement of the reaction procedure by multi measures is the research emphasis in the future,and the research provides a newthought for CO2subsea preservation and natural gas hydrate expoitation.
CO2; exploitation; natural gas hydrate; influencingfactor
TE133
A
2011-06-29;
2011-08-05
任德刚,1969年生,男,高级工程师,从事火力发电设计和管理工作。地址:(100120)北京市西城区安德路 65号。E-mail:dgren@cpecc.net
1673-8926(2011)06-0124-04
王会玲)

