加压碳化法制备碱式碳酸镁新工艺研究
, ,,,,
(河北科技大学化学与制药工程学院,河北石家庄 050018)
目前国内生产碱式碳酸镁常用的工艺方法是白云石碳化法和苦土粉-硫酸-碳酸氢铵法,但是这些传统方法生产成本较高、工艺流程长、设备庞大、工艺繁杂、产品质量较难控制,得到的产品杂质含量较高,在生产过程中造成的工业“三废”污染严重,并且还涉及到矿石的采集及加工等一系列问题。祁洪波等[1]以盐湖老卤与纯碱为原料,在40 ℃下,将纯碱液滴加到卤液中,维持1 h,生成碳酸镁,然后将碳酸镁悬浊液移入密闭反应釜中,在110~130 ℃下维持80 min,即可得到碱式碳酸镁,但收率较低。Hao Zhihua等[2]先以六水硝酸镁和碳酸钠为原料合成出光滑棒状结构的三水碳酸镁,然后将三水碳酸镁悬浊液加热至80 ℃,维持30 min即可得到Mg5(CO3)4(OH)2·4H2O。陈白珍等[3]以盐湖水氯镁石氨法一次沉镁后的母液再经碳酸氢铵二次沉镁得到的复盐MgCO3·(NH4)2CO3·H2O为原料,采用热解法制备出了符合HG/T 2959—2000 标准的碱式碳酸镁。以上3种方法使用的原料是液态镁盐,解决了碱式碳酸镁产品的杂质超标问题。但工序和操作条件较复杂,生产成本较高。A.Botha等[4]以氢氧化镁料浆为原料,控制溶液温度,向其中以190 mL/min 的速度喷射CO2气体,控制反应终点pH为7.5~9.0,然后过滤,洗涤,在100~120 ℃将产品烘干,粉碎,得到碱式碳酸镁产品。此方法可得到纯度很高的碱式碳酸镁,并且产品晶形易于控制,是制备特殊用碱式碳酸镁的一种有效方法,但是,此方法由于在常压下操作,受气液传质速率影响,CO2的利用率较低,反应时间长,生产成本较高。笔者以氢氧化镁浆液为原料,欲采用加压碳化法制备碱式碳酸镁,以解决常压碳化法CO2利用率低的问题。
1 实验部分
1.1 实验原料及仪器
氢氧化镁采用六水氯化镁和石灰乳反应制得,其中w(MgO)=63.2%。实验时将氢氧化镁固体粉末溶于一定量蒸馏水中经搅拌得到氢氧化镁浆液。纯CO2气体,CO2体积分数>99.8%。
容积为250 mL的高压反应釜。
1.2 实验步骤
取120 mL氢氧化镁浆液置于容积为250 mL高压釜内,密封釜盖并开动搅拌,转速为800 r/min,开始加热。当温度到达所设定温度时,通入CO2气体,并维持一定的CO2分压,经过一定时间后停止通气和加热,并通入冷却水将反应混合液降至室温出料,过滤洗涤,于120 ℃下干燥5 h即可得到Mg5(CO3)4(OH)2·4H2O产品。
1.3 产品表征
采用日本HITACHI S-4800型发射场扫描电镜观测颗粒的形貌;采用日本RIGAKU 公司生产的D/MAX2500PC型X射线粉末衍射仪分析产品的物相结构及其相关性质,分析条件:功率为1 200 W,选用镍滤波片滤波,CuKα辐射(λ=0.154 18 nm),扫描速度为5 (°)/min;采用德国Netzsch的STA 449C型同步热分析仪分析产品的热失重情况。
2 结果与讨论
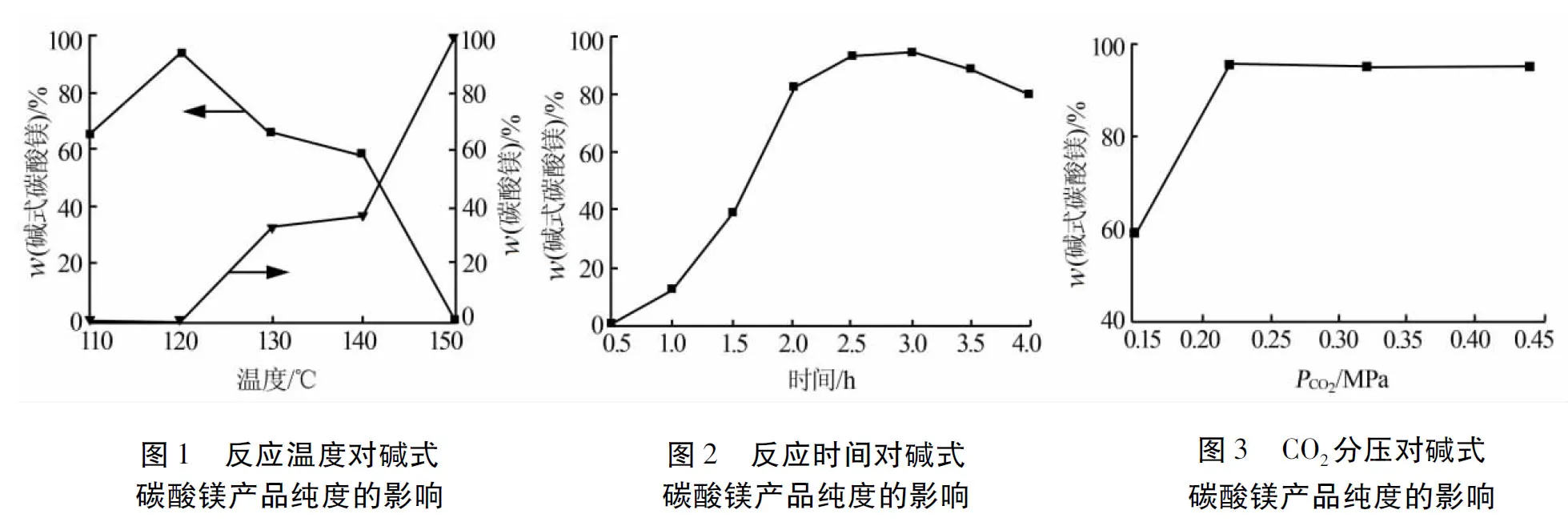
图1为固定反应时间为3 h、维持CO2气体压力在0.22 MPa,考察不同反应温度对碱式碳酸镁产品质量的影响。由图1可以看出,在温度为120 ℃时,几乎没有生成碳酸镁。随着温度的升高,产品中碱式碳酸镁含量逐渐降低,而碳酸镁含量逐渐升高。这是因为碱式碳酸镁或其他形式的含水碳酸镁盐比无水碳酸镁盐更易沉淀,碱式碳酸镁能在温度较高时进一步生成碳酸镁。而且随着温度的升高,此转变反应也会加快[5]。但是当温度低于150 ℃、CO2压力较低时,这个转变过程非常缓慢,这点从图中也可以证实。此结果与F.L.Sayles等[6]和L.Stevula等[7]报道的碱式碳酸镁经碳化转变成碳酸镁的过程是吻合的。温度为110 ℃时,反应速率较慢,反应时间达到3 h时固体产品中碱式碳酸镁的质量分数只有65.3%,其余是还未反应的氢氧化镁。在120 ℃时,产品中碱式碳酸镁质量分数高达95.2%,另外4.8%为氢氧化镁原料,产品纯度较高。因此,采用反应温度为120 ℃较好。
图2为在120 ℃下、维持CO2气体压力在0.22 MPa,考察反应时间对所制备的碱式碳酸镁产品纯度的影响。由图2看出,随着反应时间的延长,碱式碳酸镁含量逐渐升高,当反应时间为3 h时,碱式碳酸镁质量分数达到95.2%。并且产品中除原料氢氧化镁外,没有其他杂质生成。这是因为随着时间的延长,会使氢氧化镁和CO2充分反应,从而使产品中碱式碳酸镁含量逐渐升高。当时间超过3 h后,碱式碳酸镁的含量开始降低,此时,开始有碳酸镁生成。综合考虑,采用反应时间为3 h较好。
图3为在反应温度为120 ℃、反应时间为3 h时,考察CO2分压对产品纯度的影响。由图3可以看出,随着CO2分压的升高,碱式碳酸镁的含量存在升高的趋势。这是因为随着CO2分压的增加使溶解于溶液中的CO2的量增加,因此在相同的反应时间内,产品中碱式碳酸镁含量会随着CO2分压的增加而提高。但当压力大于0.22 MPa时,再提高压力,碱式碳酸镁的含量变化不大,这可能是由于压力较高时,整个过程的控制步骤由气液传递转变为液相化学反应。经过综合考虑,选用CO2分压为0.22 MPa较好。
3 产品表征
采用较佳反应条件,即:反应温度为120 ℃,CO2分压为0.22 MPa,反应时间为3 h,制得碱式碳酸镁产品,并对其进行表征。
图4为产品的XRD图。产品的衍射峰与碱式碳酸镁的标准衍射谱图PDF 00-025-0513及氢氧化镁的标准衍射谱图PDF 01-083-0114对比后检测出碱式碳酸镁的纯度为95.2%,氢氧化镁质量分数为4.8%。
图5为产品的TG-DTA曲线。碱式碳酸镁的理论热分解过程分为3部分:在250 ℃以下脱水(脱除结晶水),在250~350 ℃脱羟基[Mg(OH)2脱去羟基分解为MgO],高于350 ℃后脱除二氧化碳(MgCO3脱二氧化碳分解为MgO)[8]。碱式碳酸镁的理论总质量损失为56.9%。图5中的TG曲线基本符合碱式碳酸镁的理论热分解过程。在0~310℃质量损失为7.91%,在310~425℃,质量损失为18.39%,在425 ℃以上,质量损失为29.54%。总质量损失为55.84%。与之对应的DTA曲线中分别在264.5、410.2、440.5 ℃有较强吸热峰。产品各阶段分解温度比理论分解温度高可能与碱式碳酸镁的晶体结构有关。
图6为碱式碳酸镁的SEM图。由图6可见,产品碱式碳酸镁为规则的六方薄片状、形貌规则、分散性良好。晶体形貌是由其单晶结构及在生长过程中各晶面的生长速度决定的。Mg5(CO3)4(OH)2·4H2O的理想形貌即为六方片状[9],其(100)与(001)晶面中的键能较强,面网密度较小,因此在晶体生长过程中主要沿这2个晶面生长,得到片状的Mg5(CO3)4(OH)2·4H2O 晶体。

4 结论
1)随着温度的升高,产品中碱式碳酸镁含量逐渐降低,碳酸镁含量逐渐升高,这是因为碱式碳酸镁会转变为碳酸镁,并且随着温度的升高,转变速率加快。2)随着时间的延长,氢氧化镁和CO2充分反应,从而使产品中碱式碳酸镁含量逐渐升高。3) CO2分压的升高使溶解于溶液中的CO2的量增加,产品中碱式碳酸镁含量会随着CO2分压的升高而提高。4)在反应温度为120 ℃时,以氢氧化镁浆液为原料,CO2分压维持在0.22 MPa,反应3 h,得到质量分数为95.2%的、六方片状的碱式碳酸镁。
[1] 祁洪波,杨维强.轻质透明碱式碳酸镁生产工艺研究[J].无机盐工业,2008,40(10):36-38.
[2] Hao Zhihua,Du Fanglin.Synthesis of basic magnesium carbonate microrods with a "house of cards" surface structure using rod-like particle template[J].Journal of Physics and Chemistry of Solids,2009,70(2):401-404.
[3] 陈白珍,江剑兵,徐徽,等.热解法制备碱式碳酸镁[J].中南大学学报:自然科学版,2008,39(5):907-912.
[4] Botha A,Strydom C A.Preparation of a magnesium hydroxy carbonate from magnesium hydroxide[J].Hydrometallurgy,2001,62(3):175-183.
[5] Hanchen M,Prigiobbe V,Baciocchi R,et al.Precipitation in the Mg-carbonate system—effects of temperature and CO2pressure[J].Chemical Engineering Science,2008,63(4):1012-1028.
[6] Sayles F L,Fyfe W S.The crystallization of magnesite from aqueous solution[J].Geochimica et Cosmochimica Acta,1973,37(1):97-99.
[7] Stevula L,Petrovic J,Kubranova M.Formation of synthetic magnesite by carbonatization of hydromagnesite under hydrothermal conditions[J].Chemicke Zvesti,1978,32(4):441-443.
[8] Choudhary V R,Pataskar S G,Gunjikar V G,et al.Influence of preparation conditions of basic magnesium carbonate on its thermal analysis[J].Thermochimica Acta,1994,232(1):95-110.
[9] Yan Xiaoxing,Li Yunfei,Xue Dongfeng,et al.Bonding analysis on the crystallization of magnesium carbonate hydrates[J].Journal of Synthetic Crystals,2007,36(5):991-999.

