肾移植术后TOR-I替代CNI免疫抑制治疗的Meta分析
吴斌,吴逢波,卢静,于磊,唐尧#(.四川大学华西医院药剂科,成都市6004;2.四川大学华西药学院,成都市 6004)
自20世纪80年代以来,钙调蛋白抑制剂(Calcineurin inhibitor,CNI)成为肾移植术后免疫抑制标准治疗药物之一;但在其降低术后急性排斥反应、提高存活率的同时,也带来严重肾脏毒性风险[1]。雷帕霉素靶位抑制剂(Target-of-rapamycin inhibitor,TOR-I)是新型免疫抑制剂,研究表明TOR-I能够改善CNI造成的肾脏毒性[2,3]。为此,一些研究探讨了CNI撤除治疗方案[4,5]:Mulay等[5]发现术后CNI干预一段时间撤除后代以TOR-I治疗,虽然造成术后急性排斥反应增加,但不对近期存活率造成影响,同时改善了肾脏功能。然而,肾移植术后立即给予TOR-I替代CNI免疫抑制治疗的有效性和安全性如何,有必要进行评价。因此,本研究将采用Cochrane协作网推荐方法,对其进行系统分析。
1 资料与方法
1.1 纳入及排除标准
1.1.1 文献类型。纳入随机对照试验(Randomized controlled trial,RCT)。
1.1.2 患者类型。纳入肾移植患者。排除全身或局部感染患者;室性心律失常患者;近5年内有恶性肿瘤史患者;胃肠功能障碍影响药物吸收患者;多器官移植患者;孕妇等。
1.1.3 干预措施。试验组术后立即给予TOR-I,对照组术后立即给予CNI,即TOR-I(西罗莫司、依维莫司)vs.CNI(环孢素A、他克莫司);其余联合治疗药物2组一致。
1.1.4 结局指标。急性排斥反应;肾小球滤过率;患者存活率;移植物存活率;不良反应等。
1.2 文献检索与数据提取
在Cochrane图书馆(2009年第3期)及Medline、Embase、SCI、CBM数据库中采用主题词与自由词联合方式进行检索;手工检索重要参考文献及其他肾移植相关文献,检索时间截止至2009年9月。文献筛选及数据提取均由2名研究员独立进行后核对,发生分歧协商解决或由第三研究员协助解决。如果一个研究多次报道,最早并且数据完整的报道纳入分析。
1.3 质量评价与统计分析
该研究中除不良反应外的结局指标均为客观指标,故盲法不作为质量指标。因此,质量评价指标包括:随机方法,隐藏分配,及对丢失数据是否采用意向性(ITT)分析方法;按方法学质量由高到低分为A、B、C 3级。
效应量合并分析采用RevMan 5.0软件。先检验各研究的临床异质性,必要时划分亚组。采用Q检验统计学异质性,检验水准为α=0.10;经检验无异质性(P>0.10)的研究采用固定效应模型合并,存在异质性(P<0.10)的采用随机效应模型分析。对分类变量采用危险比(RR)或危险差(RD)、连续变量采用加权均数差(WMD)并用95%置信区间(95%CI)表示合并效应量。必要时进行敏感性分析。
2 结果
2.1 检索结果及纳入文献信息
初步检索得到文献989篇;初步排除后152篇进入第2筛选;排除非随机试验、无对照、对照不符、综述等,43篇进入第3次筛选;再排除33篇给药方式不符的研究、摘要性报道和无法获得全文的会议论文,最后纳入10篇符合标准的RCT报道[6~15],TOR-I制剂均为西罗莫司,主要信息及纳入文献质量评价结果见表1(表中,SIR代表西罗莫司;CsA代表环孢素A;S-CsA代表标准剂量环孢素A;TAC代表他克莫司)。
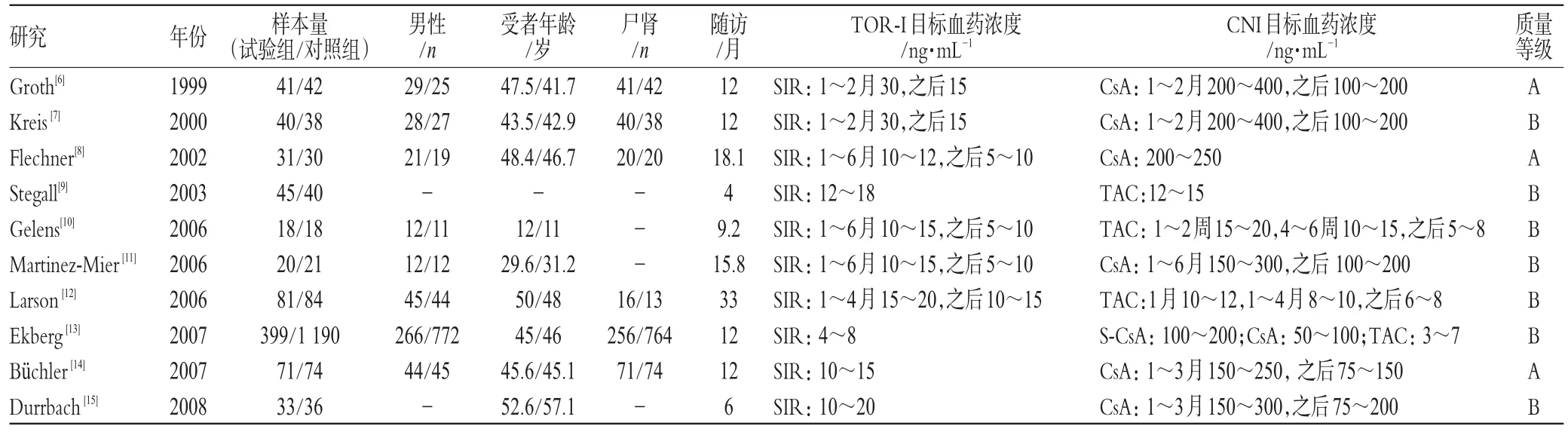
表1 纳入文献主要信息Tab 1 General information of included literatures
2.2 结局指标分析
2.2.1 有效性。对急性排斥反应、肾小球滤过率、患者存活率、移植物存活率进行Meta分析(表2):TOR-I组对比CNI组,急性排斥反应发生率升高,差异有统计学意义;肾小球滤过率升高,差异有统计学意义;患者存活率和移植物存活率差异均无统计学意义。

表2 肾移植术后TOR-I替代CNI免疫抑制治疗的有效性分析结果Tab 2 Effectiveness analysis of immunosuppressive therapy of TOR-I instead of CNI after kidney transplantation
2.2.2 安全性。各研究均有不良反应(ADR)报道,选取能合并的典型ADR进行Meta分析,分析结果见表3:其中,术后糖尿病、高血压、伤口感染和白血病在2组间的差异无统计学意义;对比CNI组,TOR-I组CMV感染降低,贫血、高胆固醇血症、高甘油三酯血症发生率增加,且差异均有统计学意义。
3 讨论

表3 肾移植术后TOR-I替代CNI免疫抑制治疗的安全性分析结果Tab 3 Safety analysis of immunosuppressive therapy of TOR-I instead of CNI after kidney transplantation
CNI在免疫抑制治疗中常导致肾脏毒性、血液系统毒性、术后糖尿病、高血压、感染和脂代谢紊乱等ADR[16];基于当前证据,TOR-I替代治疗能保护肾脏功能、降低CMV感染,但贫血、高胆固醇血症、高甘油三酯血症发生风险升高。在纳入研究中,Ekberg等[13]采用低剂量干预,结果显示低剂量西罗莫司并不具有疗效优势,且ADR发生率最高。所以,TOR-I干预效果可能与剂量相关。Meta分析发现,TOR-I与CNI相比急性排斥反应增加,这也是脱落治疗人数增加的主要原因;但不影响患者存活率和移植物存活率,这可能是肾移植患者使用TOR-I后,一方面排斥反应发生率增加,另一方面肾脏毒性降低,两方面相互作用的结果。
本次评价发现,TOR-I在肾移植后免疫抑制治疗中利弊并存。但结果主要居于短期随访研究,对长期疗效和安全性尚不能确定。另外,各研究存在临床异质性,特别在药物干预剂量上存在一定差异,可能存在潜在偏倚。
综上所述,对比CNI,TOR-I在肾移植术后免疫抑制治疗中能改善肾脏功能,不改变患者存活率与移植物存活率,并降低CMV感染发生率;但短期急性排斥反应发生率、贫血、高胆固醇血症、高甘油三酯血症发生率风险增加。期待高质量、长期随访研究报道的进一步证实。
[1] de Mattos AM,Olyaei AJ,Bennett WM.Nephrotoxicity of immunosuppressive drugs:long-term consequences and challenges for the future[J].Am J Kidney Dis,2000,35(2):333.
[2] Webster AC,Lee VW,Chapman JR,et al.Target of rapamycin inhibitors(TOR-I;sirolimus and everolimus)for primary immunosuppression in kidney transplant recipients[J].Cochrane Database Syst Rev,2006,19(2):CD004290.
[3] Morales J,Fierro A,Benavente D,et al.Conversion from a calcineurin inhibitor-based immunosuppressive regimen to everolimus in renal transplant recipients:effect on renal function and proteinuria[J].Transplant Proc,2007,39(3):591.
[4] Kasiske BL,Chakkera HA,Louis TA,et al.A meta-analysis of immunosuppression withdrawal trials in renal transplantation[J].J Am Soc Nephrol,2000,11(10):1 910.
[5] Mulay AV,Hussain N,Fergusson D,et al.Calcineurin inhibitor withdrawal from sirolimus-based therapy in kidney transplantation:a systematic review of randomized trials[J].Am J Transplant,2005,5(7):1 748.
[6] Groth CG,Bäckman L,Morales JM,et al.Sirolimus(rapamycin)-based therapy in human renal transplantation:similar efficacy and different toxicity compared with cyclosporine.Sirolimus European Renal Transplant Study Group[J].Transplantation,1999,67(7):1 036.
[7] Kreis H,Cisterne JM,Land W,et al.Sirolimus in association with mycophenolate mofetil induction for the prevention of acute graft rejection in renal allograft recipients[J].Transplantation,2000,9(7):1 252.
[8] Flechner SM,Goldfarb D,Modlin C,et al.Kidney transplantation without calcineurin inhibitor drugs:a prospective,randomized trial of sirolimus versus cyclosporine[J].Transplantation,2002,74(8):1 070.
[9] Stegall MD,Larson TS,Prieto M,et al.Kidney transplantation without calcineurin inhibitors using sirolimus[J].Transplant Proc,2003,35(3 Suppl):125.
[10] Gelens MA,Christiaans MH,van Heurn EL,et al.High rejection rate during calcineurin inhibitor-free and early steroid withdrawal immunosuppression in renal transplantation[J].Transplantation,2006,82(9):1 221.
[11] Martinez-Mier G,Mendez-Lopez MT,Budar-Fernandez LF,et al.Living related kidney transplantation without calcineurin inhibitors:initial experience in a Mexican center[J].Transplantation,2006,82(11):1 533.
[12] Larson TS,Dean PG,Stegall MD,et al.Complete avoidance of calcineurin inhibitors in renal transplantation:a randomized trial comparing sirolimus and tacrolimus[J].Am J Transplant,2006,6(3):514.
[13] Ekberg H,Tedesco-Silva H,Demirbas A,et al.Reduced exposure to calcineurin inhibitors in renal transplantation[J].N Engl J Med,2007,357(25):2 562.
[14] Büchler M,Caillard S,Barbier S,et al.Sirolimus versus cyclosporine in kidney recipients receiving thymoglobulin,mycophenolate mofetil and a 6-month course of steroids[J].Am J Transplant,2007,7(11):2 522.
[15] Durrbach A,Rostaing L,Tricot L,et al.Prospective comparison of the use of sirolimus and cyclosporine in recipients of a kidney from an expanded criteria donor[J].Transplantation,2008,85(3):486.
[16] 周燕萍.肾移植患者的免疫抑制治疗药物[J].中国药房,2002,13(10):603.

