关于滴定方式的讨论
陈鲜丽
(韶关学院医学院 广东韶关 512026)
滴定方式是分析化学课程的重要内容,贯穿于四大经典滴定中。但许多分析化学教材对于滴定方式的概念不明确,范畴不统一,容易使学生在学习时混淆,尤其是对于置换滴定和间接滴定以及置换滴定和置换反应的概念更是模糊不清。本文对此加以讨论,以增强教学的严谨性,使学生学习时更容易理解。
文献[1]把滴定方式分为两大类:直接滴定法和间接滴定法,并把间接滴定法又分为3类:①返滴定法,②置换滴定法,③其他间接滴定法。由于文献[1]在间接滴定法中又分出了其他间接滴定法,这使学生更容易混淆滴定方式,因此不是好的分类方式。
文献[2]明确地把滴定方式分为4大类:① 直接滴定法,② 返滴定法,③ 置换滴定法,④ 间接滴定法。这种分类比较可取。
即使在同一本教材中,也存在概念未贯穿始终的情况。如文献[2-3]的酸碱滴定一章,分为直接滴定法和间接滴定法两大类来讲,然后又把硼酸的测定和铵盐中氮的测定归纳在间接滴定法中来论述。这不太妥当。
1 硼酸的测定
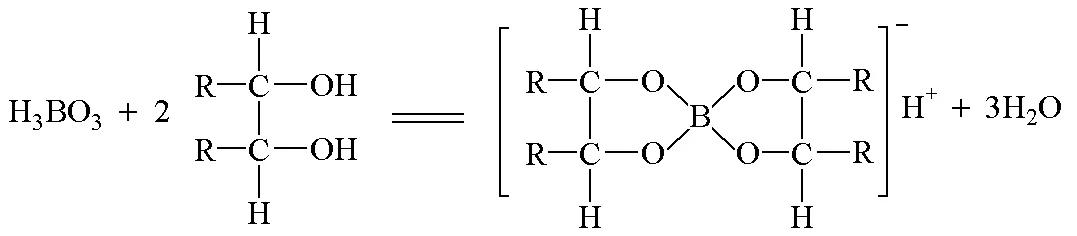
硼酸是不能用NaOH直接滴定的弱酸(pKa=9.24);但硼酸与多元醇作用生成酸性较强的络合酸(pKa=4.26)之后,可用NaOH溶液直接滴定。但这不属于间接滴定,而是属于置换滴定。
2 铵盐中氮的测定

2.1 蒸馏法
先在铵盐中加入过量的NaOH溶液,再用过量的标准酸溶液吸收NH3,然后用NaOH溶液滴定剩余的标准酸。这属于返滴定法。
2.2 甲醛法

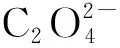
3 碘量法和高锰酸钾法的滴定方式分类
许多教材[1-3]把碘量法分为两大类:① 直接碘量法,② 间接碘量法。将间接碘量法又分为返滴定法和置换滴定法;而对同一节的高锰酸钾法,却又分为① 直接滴定法,② 返滴定法,③ 间接滴定法。这样也容易造成混乱。
4 置换反应与置换滴定
中学化学的置换反应是指一种单质与一种化合物起反应,生成另一种单质和另一种化合物。如Fe+CuSO4(aq)=FeSO4+Cu,其本质是氧化还原反应。
置换滴定已于上面提到,除了提到的例子以外,如Ag+与EDTA形成的螯合物很不稳定,用EDTA直接滴定不能得到准确的结果;但Ag+与CN-的配合物很稳定,可从Ni(CN)42-中置换出Ni2+:
然后用EDTA滴定Ni2+,根据Ni2+的量计算出Ag+的量。该反应不涉及氧化还原。置换滴定中“置换”的含义是“替换”出来,它的外延比“置换反应”更为宽泛。但是两者又容易混淆,尤其是文献[1-3]中,都是在第一次论述置换滴定法时,以K2Cr2O7测定Na2S2O3为例。反应式如下:
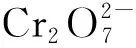
根据以上讨论,我认为最好把滴定分为以下4种方式:① 直接滴定法,② 返滴定法,③ 置换滴定法,④ 间接滴定法。在酸碱滴定、氧化还原滴定、配位滴定、沉淀滴定中,将以上4种滴定方式贯穿其中,可以避免造成不必要的混淆,增强教学的严谨性。
[1] 孙毓庆,胡育筑.分析化学.第2版.北京:科学出版社,2006
[2] 谢庆娟,杨其绛.分析化学.北京:人民卫生出版社,2010
[3] 华中师范大学,东北师范大学,陕西师范大学,等.分析化学.第3版.北京:高等教育出版社,2001

