生物样品中碘的分析方法概述
崔俐俊,范国荣,廖跃华
(1、上海医疗器械高等专科学校,上海 200093;2、第二军医大学药学院药物分析学教研室,上海 200433;3.上海市药物代谢产物研究重点实验室,上海 200433)
生物样品中碘的分析方法概述
崔俐俊1,范国荣2,3,廖跃华1
(1、上海医疗器械高等专科学校,上海 200093;2、第二军医大学药学院药物分析学教研室,上海 200433;3.上海市药物代谢产物研究重点实验室,上海 200433)
碘是具有重要生物效应的微量元素之一,与人体的生长发育、新陈代谢密切相关,自然界中碘分布广泛并以多种形式存在,对于人体、食物、药物及环境中碘含量的分析是人们极为关注的问题。本文综述了近年来有关碘特别是生物样品中碘的分析方法进展。
碘;生物样品;分析方法;综述
碘是具有重要生物效应的微量元素之一,与人体的生长发育、新陈代谢密切相关。碘缺乏会导致甲状腺肿大,引起一系列新陈代谢紊乱;而碘过量亦会引发甲状腺肿、甲状腺功能减退或亢进。同时,碘分子能够氧化或碘化巯基化合物、肽类、蛋白质、酶、脂质和胞嘧啶等生物生存所必需的分子,使微生物死亡,因而在临床上,碘又被用作杀菌剂、消毒剂而广泛使用。在自然界碘分布广泛,可以以游离的元素碘、碘化物、碘酸盐等多种形式存在,并通过大气圈、水圈、生物圈和土壤圈不断循环。因此,人体成分、食品、药物及环境中碘的分析是人们极为关注的问题。
碘的易氧化还原、易挥发和易吸附等特点使得碘的化学分析具有一定的难度,在样品处理过程中碘易挥发损失或引入污染。目前测定碘的方法很多,常用的有容量分析法、分光光度法、电化学法、中子活化法、原子吸收光谱法、色谱法等。近年来又出现了毛细管电泳、电子耦合等离子体质谱等方法。本文着重介绍近年来有关碘特别是生物样品(食品、药品、体液)中碘的分析方法进展。
1 样品预处理
碘是多价态元素(0、-1、+5、+7),在不同介质和条件下具有多种形态,其行为也大不相同。碘的不同形态以及易挥发、易污染等因素使碘的分析复杂化,针对不同的样品采用适当的预处理方法显得尤为重要。
目前有关碘样品分析的预处理方法很多,主要可分为酸消化法、碱灰化法、氧瓶燃烧法等。酸消化法通常选用氯酸、过硫酸铵作为消化剂,在控制温度的条件下对血样、尿样等生物样品进行消化,进而通过砷铈催化反应测定样品中的碘含量。王雪红等[1]对尿碘测定的氯酸消化法和过硫酸铵消化法进行了比较,认为两种方法测定尿碘在标准曲线、检出限、精密度、准确度方面差异无统计学意义,但过硫酸铵法的检测条件优于氯酸法。
碱灰化法一般选择碳酸钾等碱性物质固定碘,硫酸锌等作为助灰化剂。在马弗炉中高温灼烧,使样品中的有机物灰化,碘全部转化为碘化钾,经水提取,试样中的碘可转入溶液中。灰化温度通常控制在450~650 ℃,温度过低,有机物破坏不完全;温度过高,会造成碘的损失。刘列钧等[2]采用碳酸钾、硫酸锌、氯化钠混合碱性助剂在550 ℃下灰化牛奶样品,用水溶解灰份后取上清液进行砷铈催化分光光度法测定其中碘的含量。
氧瓶燃烧法将样品粉末点燃置入盛有吸收液(水、氢氧化钠溶液)的燃烧瓶中,通入氧气,使其充分燃烧,样品中有机物质被破坏而卤素(F、Cl、Br、I)及硫等挥发性元素释放出来,用一定的吸收液将其吸收。该方法样品分解完全,能有效净化试样的基体,从而消除试样中蛋白质、有机酸的物质对测定的干扰。
2 容量分析法
容量分析法中硫代硫酸钠滴定法和银量法是碘的经典滴定方法。其基本原理是碘化物在酸性条件下,用饱和溴水、高锰酸钾、重铬酸钾等氧化剂氧化成碘酸盐,然后加入过量碘化钾析出单质碘,以淀粉作指示剂,用硫代硫酸钠溶液或AgNO3标准溶液滴定。当样品中碘量较低时,该法灵敏度不高,测定误差大,但对于高含量碘的测定,容量分析法具有流程简单、快速、准确性好的特点,广泛应用于碘盐含碘量的分析。
3 分光光度法
分光光度法具有灵敏度较高、仪器简单、易于操作等优点,目前应用比较广泛。利用分光光度法测定碘主要有淀粉比色法、催化比色法等。其基本原理是在酸性条件下,加氧化剂将I-氧化为IO3-,再加KI析出I2,淀粉显色测定;或利用I-对一些氧化还原反应的催化作用,进行比色测定。表1为分光光度法测定食品中碘的应用。

表1 分光光度法测定食品中的碘
4 电化学法
4.1离子选择电极法 碘离子选择电极测碘是一种比较好的方法,其设备简单、测定范围宽、选择性好。碘离子电极由AgI/Ag2S膜或单纯AgI膜组成,也有由HgI2/HgS膜组成的,电极适用的pH范围为2~12,对低浓度碘的测定,最佳pH范围为2.5~3。表2为碘离子选择电极测定生物样品中碘的应用示例。

表2 碘离子选择电极法测定生物样品中的碘
4.2阴极溶出伏安法与极谱法 阴极溶出伏安法以其高灵敏度著称,有较低的检出限,常用于痕量碘的测定。与前几种方法相比,该法具有操作简便、灵敏度高、选择性好、测定范围宽、干扰离子少等特点。极谱法是采用滴汞电极或能周期性更新的电极作为工作电极的电化学分析方法。表3为阴极溶出伏安法与极谱法测定生物样品中碘的应用示例。
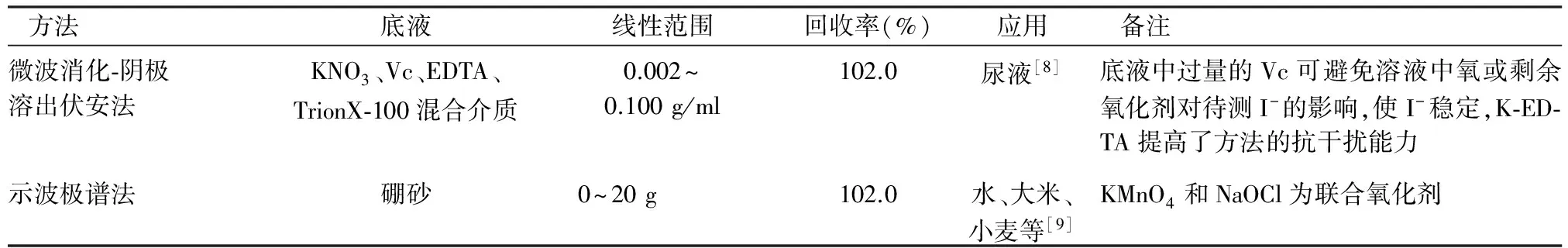
表3 阴极溶出伏安法与极谱法测定生物样品中的碘
5 中子活化法
中子活化法是一种灵敏度较高的测定碘的方法,该法不需要对样品进行繁复的预处理分离,属于非破坏性检验,所以其分析准确度较高。而对于生物或食物样品,由于其中Na、Cl、Al的含量较高,热中子活化后产生的24Na、38Cl、28Al等极大干扰I和Br的测定,故一般采用超热中子活化法或放射化学中子活化法对其中的I、Br进行测定。由于中子活化法的设备较为特殊且价格昂贵,虽然其测定灵敏度高,但应用范围有限。表4简要列举了该法在碘含量测定中的应用。

表4 中子活化法测定生物样品中的碘
6 原子吸收光谱法
原子吸收光谱法直接测定金属元素,灵敏度高,直接测定非金属元素则有困难。碘的共振吸收线是183.04 nm,处于真空紫外区,目前一般的原子吸收分光光度计难以直接测定真空紫外区的分析谱线,因此测碘需要用间接方法。孙孝祥等[12]利用[Cd(Phen)3]2+与I-可形成[Cd(Phen)3]2+(I-)2离子对原理,用硝基苯萃取,通过测定有机相中镉的含量,间接测定碘。该法用于测定食品中的碘,检测限达0.04 μg/ml。
7 色谱法
色谱法是近年来测碘较常用的方法,主要有气相色谱法、高效液相色谱法。目前色谱法广泛应用于生物样品、食品、土壤、海水等样品中碘的检测。
7.1气相色谱法 气相色谱法是以气体为流动相的色谱方法,可以分析气体试样,易挥发或可衍生化转化为易挥发的液体和固体试样。通常气相色谱法通过衍生化将I-转化为有挥发性的碘化物来间接测定I-,常用的衍生剂有烷基化试剂、五氧苄基化试剂以及酮类衍生试剂,常用的检测器有电子俘获检测器、火焰电离检测器和热导检测器。表5为气相色谱法测定食品中碘的应用示例。

表5 气相色谱法测定食品中的碘
7.2高效液相色谱法 高效液相色谱法是在经典液相色谱法的基础上,引入了气相色谱法的理论和实验技术,以高压输送流动相,采用高效固定相及高灵敏度检测器的现代液相色谱分析方法。目前应用于碘分离测定中的主要有离子色谱法、反相高效液相色谱法。
7.2.1离子色谱法 离子色谱法是将离子交换色谱与电导检测器相结合分析各种离子的方法,可以分离有机和无机阴、阳离子以及氨基酸、糖类等。离子色谱法具有快速、多离子连续检测等特点,在碘的分析中应用广泛。表6为离子色谱法测定生物样品中碘的一些基本应用。

表6 离子色谱法测定生物样品中的碘
7.2.2反相高效液相色谱法 反相高效液相色谱法采用非极性键合相为固定相,极性流动相洗脱。对于样品中的碘含量测定,通常采用反相离子对色谱法,即将离子对试剂加入到含水流动相中,使碘离子形成离子对,增加其在非极性柱上的保留,改善分离效果。表7为反相高效液相色谱法分析生物样品中碘的基本应用。

表7 反相高效液相色谱法测定生物样品中的碘
8 毛细管电泳法
毛细管电泳法需要的样品量,试剂量少,操作时间短,是一种测定碘的新方法。Zhuo等[27]用高效毛细管电泳法分离海水中的碘化物及碘酸盐。采用未涂布的石英毛细管柱,负极压力进样,检测波长226 nm(碘化物);210 nm(碘酸盐),缓冲液为12.5 mM氯化十六烷基三甲基铵(CTAC)、0.5 M NaCl(pH 2.4)。碘离子浓度在3~60 μg/L内线性关系良好,碘酸盐在40~800 μg/L内线性关系良好。最低检测限碘离子为0.23 μg/L,碘酸盐为10 μg/L。该报道中还比较了毛细管电泳与离子色谱的测定结果,证明毛细管电泳方法同样准确可靠。
9 电感耦合等离子体质谱法
电感耦合等离子体质谱(IPC-MS)技术是上世纪80年代才出现的分析技术,因其具有检出限低、动态线性范围宽、干扰少且易消除等优点,近几年在元素测定中应用广泛。由于碘的不同形态以及易挥发、易污染等因素使得IPC-MS测碘常常遇到分析信号波动大、记忆效应严重、分析精密度和准确性差等问题,如何正确处理样品以及合理选择测定溶液的介质是准确测定样品中全碘的关键。表8为IPC-MS测定生物样品中碘的应用示例。

表8 IPC-MS测定生物样品中的碘
10 结语
本文综述了近年来国内外各种测碘方法的现状和进展。碘的测定在地方病防治、生物样品分析、环境分析、临床分析中具有重要作用,因而,上述各种方法被广泛应用于各种样品碘的分析中。但是,由于经济条件不一,一些需运用大型专属仪器测碘的方法尚难普及。相信随着科学技术和经济建设的不断发展,简便、灵敏、准确度高的测碘分析技术将会不断产生、完善和推广。
[1] 王雪红, 招 莉, 卢经凤. 尿碘测定的氯酸消化法和过硫酸铵消化法比较[J]. 预防医学情报杂志, 2007, 23(4):507.
[2] 刘列钧, 李秀维, 李淑华,等. 碱灰化砷铈催化分光光度法测定鲜奶及奶粉中碘含量[J]. 中国地方病防治杂志, 2006, 21(2):79.
[3] 王 勇, 倪永年. 动力分光光度法测定食用碘盐中碘酸根[J]. 光谱学与光谱分析, 2008, 28(6):1387.
[4] 申湘忠, 李宪平, 刘志成. 阻抑动力学光度法测定乳品中的痕量碘[J]. 分析试验室, 2007, 26(5):103.
[5] 张东霞, 杜宝中. 食物中微量碘的离子选择性电极测定法[J]. 西安理工大学学报, 2007, 23(2):212.
[6] 李 磊. 碘离子选择电极测定食盐中的碘含量[J]. 沈阳医学院学报, 2007, 9(4):225.
[7] 雷艳秋, 姚伟东. 离子选择电极法测定尿中碘的干扰实验[J]. 黑龙江环境通报, 2005, 29(2):41.
[8] 李吉学, 卢 洁, 骆望美,等. 微波消化-阴极溶出伏安法测定尿碘[J]. 南京军医学院学报, 2000, 22(1):50.
[9] 丁建文, 丁建武, 付克万,等. 示波极谱法测定大米等样品中的碘[J]. 中国预防医学杂志, 2002, 36(1):47.
[10] 王雪飞, 张 芳, 徐 清,等. 超热中子活化法研究补碘大鼠甲状腺碘水平[J]. 核化学与放射化学, 2003, 25(1):6.
[11] 陈如松, 刘国栋, 王 珂,等. 我国成年人甲状腺碘含量的检测——微堆超热中子活化法测碘[J]. 广东微量元素科学, 2000, 7(2):35.
[12] 孔孝祥, 修长泽, 孔秀云,等. 火焰原子吸收光谱法间接测定食品中碘[J]. 理化检验-化学分册, 2001, 37(11):521.
[13] 庞民好, 刘颖超, 张利辉,等. 衍生气相色谱法测定奶粉中的微量碘[J]. 河北农业大学学报, 2006, 29(4):98.
[14] 王福军, 雷 军, 董宝琴,等. 顶空毛细管气相色谱法测定水中碘化物[J]. 色谱, 2005, 23(3):326.
[15] Malongo TK, Patris S, Macours P,etal. Highly sensitive determination of iodide by ion chromatography with amperometric detection at a silver based carbon paste electrode[J]. Talanta, 2008, 76(3):540.
[16] Han J, Liang LN, Mou SF,etal. Determination of trace iodide in saturated brine using ion chromatography[J]. Chin J Anal Chem, 2008, 36(2)187.
[17] 柴成文, 刘克钠, 牟世芬. 安培检测-离子色谱法测定乳品中的微量碘[J]. 色谱, 2001, 19(1):94.
[18] Bruggink C, Rossum WJM, Spijkerman E,etal. Iodide analysis by anion-exchange chromatography and pulsed amperometri detection in surface water and adsorbable organic iodide[J]. J Chromatogr.A, 2007, 1144:170.
[19] Liang LN, Cai YQ, Mou SF,etal. Comparisons of disposable and conventional silver working electrode for the determination of iodide using high-performance anion-exchange chromatography with pulsed amperometric detection[J]. J Chromatogr.A, 2005, 1085:37.
[20] Cataldi TRI, Rubino A, Laviola MC,etal. Comperison of silver,gold and modified platinum electrodes for the electrochemical detection of iodide in urine samples following ion chromatography[J]. J Chromatogr.B, 2005, 827:224.
[21] Chen J, Jandik P, Avdalovic N. Pulsed amperometric detection of sulfide, cyanide, iodide, thiosulfate, bromide and thiocyanate with microfabricated disposable silver working electrodes in ion chromatography[J]. Analytica Chimica Acta, 2005, 536:267.
[22] 潘 峰, 路 菊, 孙 伟,等. 反相离子对色谱法分析交联淀粉碘的碘[J]. 理化检验-化学分册, 2004, 40(4): 210.
[23] 胡家炽, 慕容敬章. 高效液相色谱法测定聚维酮碘中的总碘含量[J]. 广东药学院学报, 2006, 22(1): 48.
[24] Andersson S,Forsman U. Determination of total iodine in biological material by alkaline ashing and column-switching ion-pair liquid chromatography[J]. J Chromatogr.B, 1997, 692: 53.
[25] Rong L, Lim LW, Takeuchi T. Determination of iodide and thiocyanate in seawater by liquid chromatography with poly(ethylene glycol) stationary phase[J]. Chromatographia, 2005, 61:371.
[26] Sajonz P, Bookalam J, Miller RA. Separation of periodate, iodate and iodide on a C18stationary phase. Dependence of the retention on the temperature and solvent composition. Monitoring of an oxidative cleavage reaction[J]. Chromatographia, 2006, 64:635.
[27] Huang Z, Ito K, Timerbaev AR,etal. Speciation studies by capillary electrophoresis-simultaneous determination of iodide and iodate in seawater[J]. Anal Bioanal Chem, 2004, 378:1836.
[28] Reid HJ, Bashammakh AA. Goodall PS,etal. Determination of iodine and molybdenum in milk by quadrupole IPC-MS[J]. Talanta, 2008, 75:189.
[29] Liu W, Yang HX, Li B,etal. Speciation stabillties of iodine in underground water by high performance liquid chromatography-inductively coupled plasma mass spectrometry[J]. Chin Anal Chem, 2007, 35(4):571.
2011-01-17
[修回日期]2011-07-07
Reviewoftheanalysismethodsofiodineinbiologicalmatrix
CUI Li-jun1, FAN Guo-rong2,LIAO Yue-hua1
(1. Shanghai medical instrumentation college, Shanghai 200093, China; 2. Department of Pharmaceutical Analysis, School of Pharmacy, Second Military Medical University, Shanghai 200433, China;3.Shanghai Key Laboratory for Pharmaceutical Metabolite Research, Shanghai 200433, China)
Iodine was one of the most important trace elements in human nutrition. It was essential for the biosynthesis of thyroid hormones, which was closely related with the mental development, growth and basic metabolism. Iodine spead and exist widely in many forms. The analysis methods of iodine in human body, food, medicine and environmental
many attentions. The analysis methods of iodine in biological matrix were reviewed to give some references for the further research.
iodine; biological matrix; analysis method; review
崔俐俊(1984-),女,硕士,助教.Tel:(021)6548555-3420,E-mail:cuilijun620@yahoo.com.cn.
TQ460.7+2
A
1006-0111(2011)06-0408-05

