亚甲兰注射治疗椎间盘源性腰痛的临床观察
杨 洪,高春华,庞晓东,李端明,彭宝淦
椎间盘源性腰痛是指椎间盘内各种病变刺激椎间盘内疼痛感受器所引起的腰痛,不伴有神经根性症状,无神经受压或节段活动过度的放射学证据,可引起功能的丧失,是慢性腰痛的最多见类型,约占40%[1]。引起椎间盘源性疼痛的机制还不完全清楚。最近组织学研究发现:椎间盘源性腰痛患者的疼痛椎间盘的病理学特征是沿着后方纤维环的放射性裂隙形成的伴有广泛神经分布的血管化肉芽组织条带区,此条带区是腰椎椎间盘造影术时疼痛复制和椎间盘源性腰痛的产生部位[2-3]。据此,椎间盘内注射亚甲蓝,灭活沿着裂隙长入椎间盘内的痛性神经纤维,将达到治疗椎间盘源性腰痛的目的。回顾性分析本院2010 年8 月~2011 年12 月行亚甲蓝椎间盘内注射治疗的椎间盘源性腰痛的病例资料,疗效满意,报告如下。
1 资料与方法
1.1 一般资料
回顾性分析武警总医院2010 年8 月~2011 年12 月行亚甲蓝椎间盘内注射治疗的90 例椎间盘源性腰痛病例。患者年龄为19~70 岁,其中男42 例,平均40 岁;女48 例,平均43 岁。
1.2 临床特点
持续或反复发作腰痛>6 个月,对各种非手术治疗无效,腰痛以脊柱区域为中心,部分患者伴有臀部、腹股沟区、大腿内外侧的放射痛或酸胀不适感。除腰部压痛外无神经根定位体征,直腿抬高试验阴性。腰椎CT 或MRI 无腰椎椎间盘突出等神经受压表现,但MRIT2 加权像可见“黑间盘”,即椎间盘低信号改变,部分伴有纤维环后方有点状高信号区。
1.3 手术方法
腰椎椎间盘造影阳性(见图1)患者通过腰椎椎间盘造影针立即注入1%亚甲蓝1 mL (10 mg),术后卧床24 h,3 周内避免剧烈腰部活动。
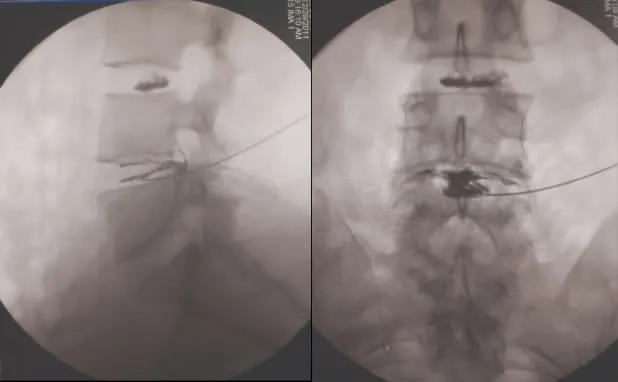
图1 椎间盘造影术中正侧位影像显示L4/L5 椎间盘破裂,疼痛诱发实验阳性Fig.1 Anteroposterior and lateral images during discography show L4/L5 disc disruption and concordant pain response
术前、术后腰痛症状采用疼痛视觉模拟量表(visual analog scale,VAS)评分[4],同时根据Oswestry 功能障碍指数(Oswestry disability index,ODI)[5]评价每个患者手术前后的腰椎功能。
1.4 统计学分析
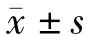
2 结 果
90 例亚甲兰注射患者术后随访时间为3~6 个月。术后1 周VAS 评分由术前平均8.4 分下降为平均2.8 分;ODI 由术前平均54.8 下降为平均21.5,差异有统计学意义(P<0.01,见表1)。90 例患者中,有5 例腰痛症状术后有轻度改善,但3 个月后基本恢复至术前水平;另有2 例腰痛症状无明显改善,术后VAS 评分较术前降低<2 分;其余83 例中,腰痛症状完全消失者10 例,有显著改善者60例,最后随访时VAS<2 分,另外13 例有明显改善,其VAS 评分至少比术前降低2 分。术后90 例患者中,80 例腰椎功能均明显改善。
共有54 例患者随访>3 个月。末次随访时的VAS 评分和ODI 与术后1 周时进行比较,观察其疼痛症状和腰痛功能是否随时间延长而有所改变,结果发现亚甲蓝注射后>3 个月的疗效与1 周时比较差异无统计学意义(P >0.05)。
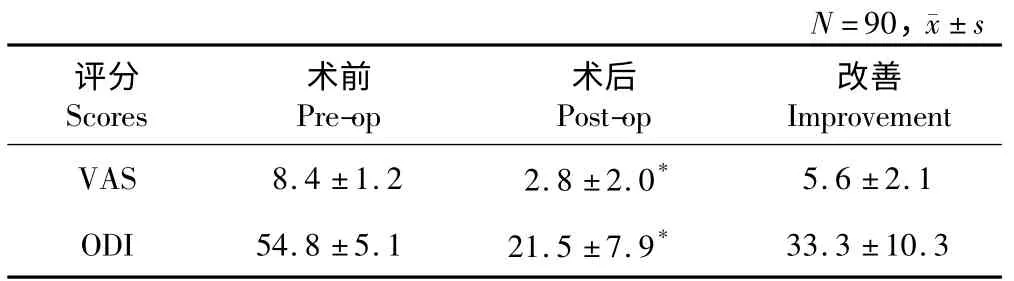
表1 手术前后患者VAS 和ODI 评分Tab.1 Pre-and post-operative VAS and ODI scores
3 讨 论
慢性椎间盘源性腰痛的治疗是目前困扰脊柱外科医生的一个难题。对于疼痛程度轻,发病时间短的患者,可采取非手术治疗,包括功能锻炼、局部封闭、非甾类抗炎药、止痛药、短期卧床休息、物理治疗及针灸等方法,但非手术治疗适应证有限,治疗时间长,有效率低且复发率高[6]。经皮穿刺腰椎椎间盘激光汽化减压术(percutaneous laserdisc decompression,PLDD)[7]是近年来发展很快的一种治疗腰椎椎间盘突出症、椎间盘源性腰痛的方法,损伤小、恢复快、不影响后续治疗、易被患者接受。此术式适用于纤维环未破裂,且不合并隐窝狭窄,后纵韧带钙化或关节突畸形等病变者,可能产生神经根、血管损伤,以及周围组织热损伤等并发症。椎间盘内热疗[8]是一种微创、非手术的椎间盘源性腰痛的治疗方法,低功率激光低温理疗治疗椎间盘源性腰痛产生的温度低,对周围组织产生的损伤小,安全性高,可行多次手术,低温对椎间盘只起到理疗的作用,对脊柱的刚度影响小,在达到治疗效果的同时维持了脊柱的稳定性。但激光作为一种理疗,一般需要多次手术,手术后可能会出现一过性的症状加重或腰部肿胀,可能与手术多次穿刺有关,故术后常规的消炎、脱水等治疗不可少。髓核成形术[9-10]又称椎间盘射频消融术,具有穿刺孔更小、基本无渗血、术后能即刻下床行走、无热损伤所致的明显疼痛等优点,禁忌证有椎间盘脱出、髓核游离、侧隐窝狭窄、椎间隙狭窄等。
椎间盘源性腰痛的手术治疗经历了几十年的发展,治疗方法目前尚无一致意见,临床疗效报道差异较大[11]。近年来,许多学者应用BAK、TFC 等椎体间金属融合器技术,尤其是腹腔镜下椎体间融合术,具有创伤小、手术时间短的优点。但是椎体间融合术后仍然存在问题,最早的问题包括取骨处疼痛和假关节形成,而后会在融合处的近端或远端相邻运动节段出现退行性改变。另外,融合术后应力的屏蔽作用会导致废用性骨质疏松症。椎间盘源性腰痛是假体置换的最佳适应证,假体置换术包括人工椎间盘置换和髓核置换术,它是利用人工假体恢复椎间隙的高度和病变椎间盘的生物力学结构和负载能力,以达到节段性稳定和节段性运动,恢复腰椎自然负重及运动功能,减轻负荷,解除疼痛等症状;不增加相邻节段的应力载荷;彻底清除椎间盘组织,消除了炎性刺激和自身免疫性反应,是治疗椎间盘疾病的理想方法。人工腰椎椎间盘使用中仍有一些问题需要解决:①假体活动度过大而稳定性不够;②有滑动核脱出的现象;③金属盖板缺乏表面处理,因而与骨表面的互相长入欠佳。目前脊柱外科的新技术还不能用于替代传统的腰椎椎间盘切除术和融合术,临床应用要严格掌握手术适应证,并注意长期随访观察。
疼痛椎间盘在MRI 和椎间盘造影片上的异常表现类型与无症状的退变椎间盘相比无明显差异,唯一的不同是疼痛椎间盘在椎间盘造影术过程中推注造影剂时诱发疼痛复制反应。分析椎间盘源性腰痛的病理本质,文献[12]显示:一些退变椎间盘原本无神经分布的内纤维环和髓核出现了神经分布,这为椎间盘源性腰痛提供了一个形态学基础。文献[13]显示,46%慢性腰痛患者的血管和神经末稍长人内层纤维环,22%长入髓核。椎间盘源性腰痛患者的疼痛椎间盘内部髓核表达生长相关蛋白-43(growth-associated protein-43,GAP-43)和P 物 质(substance P,SP),而对照组椎间盘中没有神经结构,这支持了神经内生长在慢性腰痛致痛机制中的作用。Peng 等[14]研究经椎间盘造影证实为椎间盘源性腰痛患者的手术切除椎间盘标本,发现疼痛椎间盘组织学的显著特征表现为形成一条自髓核至纤维环外层的血管化肉芽组织条带区,其间伴有一个或多个裂隙,并且肉芽组织条带区与椎间盘造影术后CT 显示的纤维环裂隙一致;免疫组化染色显示SP、神经丝蛋白和血管活性肠肽等3 种神经肽阳性,神经纤维分布数量和比例均较正常对照组椎间盘和生理老化组椎间盘明显增多;因此推断,在椎间盘造影期间,造影剂由髓核向后方流出至纤维环外层,造影剂所产生的压力作用于肉芽组织并分布于其中的神经纤维,是产生腰痛复制的基础。疼痛椎间盘的病理学特征是炎性血管化肉芽组织和神经纤维沿着纤维环裂隙自外层向内层长入,长入椎间盘内部的炎性肉芽组织可以产生多种炎性介质和化学因子,刺激纤维环甚至髓核内部的疼痛感受器使其痛阈降低,在轻微机械压力作用下就可引起腰痛。动物实验发现,亚甲兰作为鸟苷酸环化酶抑制剂,可通过降低组织局部鸟苷酸浓度,阻断缓激肽诱导的痛觉过敏,表明亚甲兰可以消除局部组织炎症引起的痛觉过敏反应[3]。
本研究中将亚甲兰用于椎间盘内注射治疗椎间盘源性腰痛,取得了很好的临床治疗效果。本研究中,几乎所有患者的腰痛症状和下肢牵涉痛症状都有明显改善。在本组患者的随访过程中,患者的腰痛症状在开始的3 个月逐渐改善,然后稳定维持在这一水平。椎间盘内注射亚甲蓝为难治性椎间盘源性腰痛提供了一种安全有效的微创治疗手段。
[1]Schwarzer AC,Aprill CN,Derby R,et al.The prevalence and clinical features of internal disc disruption in patients with chronic low back pain[J].Spine (Phila Pa 1976),1995,20(17):1878-1883.
[2]Peng B,Wu W,Hou S,et al.The pathogenesis of discogenic low back pain[J].J Bone Joint Surg Br,2005,87(1):62-67.
[3]庞晓东,徐展,彭宝淦,等.亚甲蓝治疗椎间盘源性下腰痛机制的动物实验研究[J].中国疼痛医学杂志,2011,17(5):274-279.
[4]Huskisson EC.Measurement of pain[J].Lancet,1974,2(7889):1127-1131.
[5]Chow JH,Chan CC.Validation of the Chinese version of the Oswestry Disability Index[J].Work,2005,25(4):307-314.
[6]Nakamura SI,Takahashi K,Takahashi Y,et al.The afferent pathways of discogenic low-back pain.Evaluation of L2 spinal nerve infiltration[J].J Bone Joint Surg Br,1996,78(4):606-612.
[7]都芳涛,尚博,张劼,等.经皮激光椎间盘减压术治疗椎间盘源性腰痛疗效观察[J].颈腰痛杂志,2008,29(2):138-140.
[8]罗光平,刘洪,肖业生,等.激光低温理疗治疗椎间盘源性腰痛[J].中国微创外科杂志,2009,9(7):648-650.
[9]吴叶,侯树勋,吴闻文,等.射频消融髓核成型术治疗盘源性腰痛疗效观察[J].中国疼痛医学杂志,2006,12(3):135-137.
[10]Lipsky MS,Sharp LK.Exploring the mission of primary care[J].Fam Med,2006,38(2):121-125.
[11]陈金栋,彭宝淦,侯树勋.椎间盘源性下腰痛治疗方法进展[J].国外医学骨科学分册,2005,26(6):336-338.
[12]周昊嵬,侯树勋,商卫林,等.椎间盘源性下腰痛与椎间盘内神经生长[J].国外医学骨科学分册,2005,26(6):339-341.
[13]Freemont AJ,Peacock TE,Goupille P,et al.Nerve ingrowth into diseased intervertebral disc in chronic back pain[J].Lancet,1997,350(9072):178-181.
[14]Peng B,Wu W,Hou S,et al.The pathogenesis of discogenic low back pain[J].J Bone Joint Surg Br,2005,87(1):62-67.

