添加混合菌剂对石油污染土壤的降解
陈丽华 ,马金珠,雒晓芳,杨琴
(1.西北民族大学 实验中心,甘肃 兰州,730030;
2.兰州大学 西部环境与气候变化研究院,甘肃 兰州,730000;
3.长庆油田公司 油气工艺研究院,陕西 西安,710012)
治理石油污染土壤的修复技术主要有物理修复、化学修复、生物修复以及综合修复等[1-3]。其中,物理修复(如热处理)可破坏土壤中的大部分污染物,但同时破坏了土壤组分和结构,而且价格昂贵;化学修复有较好的除油效果,但所用的化学试剂会产生二次污染,限制其应用范围[4]。近年来,石油烃的生物降解受到越来越多的关注,在石油污染的生物处理中,石油降解菌以石油烃为碳源而将其降解[5-7]。石油降解微生物的资源研究已经成为一个重要研究方向,国际上已建成专门的降解微生物菌种资源库[8]。污染土壤的石油组分复杂,单一的细菌或真菌产生酶的种类较少、浓度较低,一般只能降解少数特定烃类或者只降解到某一阶段,某些复杂烃类的彻底降解往往需要多种微生物协同作用[9]。研究表明:加入高效降解菌能有效地强化生物修复速度和程度。如韩慧龙等[10]利用细菌和真菌在生长以及对石油类物质降解途径方面的互补性,构建了以真菌和细菌组成的真菌-细菌混合菌剂,大大地提高了石油类物质的生物降解。另外,碳、氮和磷等主要营养元素缺乏也会限制微生物的生长,降低修复效率[11-13]。生物菌剂在我国处于研发阶段,处理油污土壤的初始含量还处于低范围(质量分数小于2%),尤其是细菌、霉菌、放线菌混合的降油菌体系对油污土壤的生物修复未见报道。而降解研究大多针对具体石油组分含量的测定,未从物质构型转化及石油组分群的生物演化参数方面去进行全面的降解演化研究。本文以甘肃陇东地区含油土壤为菌源,以原油为唯一的碳源进行筛选分离得到石油降解菌,分别为细菌,霉菌和放线菌。把5种菌属的菌混合在一起制成混合菌剂,投加到5%油污染土壤中,将滞留的污染物快速降解和转化。通过分析脱氢酶活性的变化,不同量有机肥中的氮、磷对石油类污染物降解的影响,研究土壤中微生物对石油污染物的修复性能的影响。同时,采用GC-MS分析混合菌对石油各组分群的降解演化规律,以期为后期的现场修复提供重要的实验依据。
1 材料与方法
1.1 试验材料
1.1.1 土壤及原油
所用的土样和原油取自甘肃陇东地区,西峰市郊某油井及附近农田中未污染土样;用西-27#原油作为微生物的唯一碳源。由于研究区油田散布于黄土塬农业区中,土壤中速效钾是肥力的重要表征参数,总氮、有效磷、有机质既是土壤肥力表征参数,又是油污土壤微生物降解所需氮源、磷源、碳源的背景土壤。表1所示为背景土壤与生物降解有关的信息。
从背景土壤整体情况来看,陇东油区由于降雨量偏少,采样时又为冬季,土壤含水率较低(5%左右);pH为7.8左右,弱碱性,有利于微生物降解;总氮量较低0.180 g/kg,有机质含量低(1%左右),土壤较为贫瘠;有效磷、速效钾由于人工施肥背景值比荒地的高,但远远低于微生物降解所需要的氮磷含量;电导率普遍小于0.2 mS/cm,表现出土壤盐度低的特点。
1.1.2 混合菌剂
以甘肃陇东地区西峰市油田附近的含油土壤为菌源,以原油为唯一碳源进行筛选分离,得到高效石油降解菌。经大连宝生物工程有限公司鉴定分别为:A6菌株属于铜绿假单胞菌(Pseudomonas aeruginosa)菌属,D4菌株归属于蒙氏假单胞菌(P.monteilii)菌属,A5菌株属于鲁菲不动杆菌(Acinetobacter lwoffii)菌属,F1 菌株属于黄色类诺卡氏菌(Nocardioides luteus)菌属,F2菌株属暗黑微绿链霉菌(Streptomyces atrovirens)菌属。把这5种菌属的菌混合在一起制成混合菌剂。

表1 背景土壤基本信息Table1 Information of background soil
1.2 实验方法
1.2.1 模拟生物原位修复处理方法
取1 kg没有被石油污染过的土壤浇透水1次后自然风干,分别按照 0,2%,4%和8%的比例加入混合菌剂和有机肥,混合均匀后在室温下培养,每隔1 d浇1次,保持含水率在20%左右。每个处理设置 2个平行。分别于第 1,4,7,12,17,20,27,34,41,48和63天测定石油类污染物降解率、脱氢酶活性、土壤中的氮、磷含量以及电导率。
1.2.2 混合菌剂的制备
混合菌剂的培养采用的是三级扩大培养法,在37 ℃的恒温箱中培养24 h,经平板稀释法检查菌落数大于1×1010个/mL后,以蚯蚓肥为载体将菌液吸附于载体上(载体与菌液的质量比为2.5:1)制备成菌剂,在室温下保存。
1.2.3 分析方法
土壤中石油类物质的测定采用紫外分光光度法。用索式提取法提取土壤中石油类物质,在紫外分光光度计下测出相对应的吸光度,计算每千克干土中石油类物质含量,进而按下式计算石油类物质降解率R:

其中:w1为第1天土壤中石油类物质含量,mg/kg;wi为第i天土壤中石油类物质含量,mg/kg。
紫外分光光度法测得原油的标准方程为:

其中:相关系数R2为0.999 3。
为方便计算,将其转变为250 mL样品中所含的石油类总量和吸光度之间的关系式为:

其中:D为用250 mL石油醚萃取含油土样得到萃取液的有效吸光度,无量纲;M为样品所含石油类污染物总量,mg。
土壤样品中脱氢酶活性的测定采用的是TTC分光光度法。通过把土壤溶液离心后加入TTC和Tris溶液并萃取后测定其吸光度,根据测得的吸光度和绘制的标准曲线计算出土壤中脱氢酶活性,脱氢酶活性系数表示土壤中微生物降解石油能力。
土壤中全氮的测定采用的是凯氏定氮法;土壤中有效磷用0.5 mol/L NaHCO3浸提-钼锑抗比色法测定;土壤中电导率采用电导法测定。
1.2.4 GS-MC测定降解后石油各组分
将混合菌株接入20 mL含10 mg原油的无机盐培养基的三角烧瓶,于28 ℃摇床震荡培养7 d,取出加入氯仿10 mL,放入超声波仪器中破乳15 min,倒入滴液漏斗中萃取出氯仿相。如此反复3次,将萃取液收集一起,放入水浴中将氯仿蒸发殆尽,剩下的残油准确称量后定容10 mL,即为GS-MC测试降解油样。同时不添加混合菌剂设置对照组。降解油样各组分分析条件为:气化温度 260 ℃;载气He;柱温200 ℃;柱SE-30(50 m);质谱条件为:电子能量70 eV,质量范围40~450。
2 结果与讨论
2.1 各菌株生长曲线
将实验所需的5种菌种活化24 h后分别接种于营养肉汤中,每1种菌接种于11个单独的小试管中。另外,接种1组包括5种菌剂的混合菌剂。将接种后的菌放置于温度为37 ℃、转速为80 r/min的振荡培养箱中培养。每隔3 h取出每1种菌剂和混合菌剂的1组菌悬液,置于波长600 nm处测定光密度,用菌悬液光密度随时间变化表示菌种的生长曲线,如图1所示。
根据图1,单个细菌的生长周期很明显,有调整期、对数生长期、稳定期和衰退期。混合菌在调整期后都生长良好。但5种单菌的稳定期都很短,有的很快就到达衰减期。在混合菌的生长曲线中,接种后几乎没有调整期出现,很快适应新的环境并开始呈指数增长,可以看出其生长良好,调整期较短,对数期较长,各种菌的性能都达到最佳状态,有利于提高石油的降解速率。
2.2 不同浓度的混合菌株对降油率的影响
不同浓度菌剂处理下的石油烃降解率的变化情况如图2所示。从图2可见:随着培养时间的增长,各种处理下的石油类物质降解率不断增加,中间阶段时升时降,直至49 d后变化速率渐趋于稳定。前12 d几种处理石油烃物质的降解率均较小,这是由于菌剂中的微生物加入土壤后需要一段时间适应土壤环境,加入的菌剂还没有完全发挥其高效降解作用。14 d后石油降解速率加快,细菌在适应新环境之后开始迅速生长繁殖,使石油烃的降解率逐渐升高。其中加入有机肥与菌剂的土壤中石油的降解率与没有添加任何组分(CK)相比要高的多。因为加入的有机肥本身含有大量容易被微生物利用的氮、磷元素,能够刺激土著微生物的生长,同时,加入的菌剂与土著微生物的联合作用提高降解效果。在第63天时,2%,4%和8%菌剂对5%油污土壤的降解率分别达到67.49%,80.18%和77.03%,是CK的1.67,1.98和1.90倍;而4%和8%菌剂的石油类物质降解率相差不明显,4%菌剂的降解率略高于8%菌剂的降解率。这可能是加入菌剂量过多时,土壤自身环境条件对菌剂容纳量有限而影响其存活率;有机肥中丰富的有机质可以促进土壤中的不同微生物的生长繁殖,但是,有机质的浓度过高,会抑制降油菌对石油的降解作用,导致降解率下降。
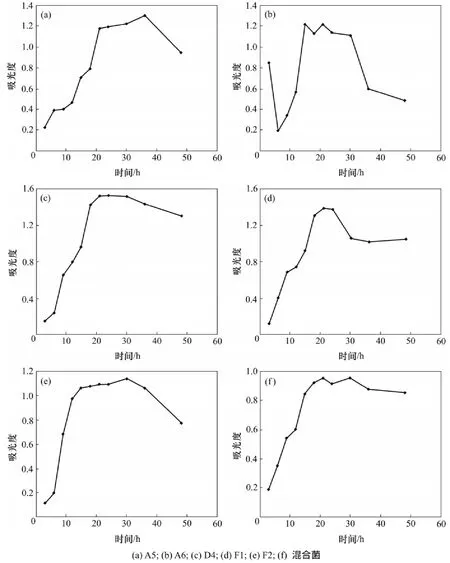
图1 菌株生长曲线Fig.1 Curves of strain growth
2.3 混合菌降解石油主要组分规律研究
从原油GC-MS图谱分析可知,该地区原油正构烷烃的碳数主峰靠前为nC15,高碳数正构烷烃降解明显,奇数碳优势已不够明显,霍烷和甾烷的异构化现象明显,均说明成烃环境微生物发育,原油演化程度高,成熟度高。非烃和多环芳烃在成烃环境中热、压力能量和微生物作用下,已多数演化为类异戊二烯烷烃等烃类物质,在离子流图中较难提取,含量很少。故以氯仿提取混合菌降解后原油进行GC-MS分析,其组分亦主要包括饱和烃(正构烷烃、霍烷、甾烷系列),芳烃、非烃含量很少。对降解后主成分正构烷烃、霍烷系列的分析,结果见表2和表3。2系列总离子流图见图3和图4。
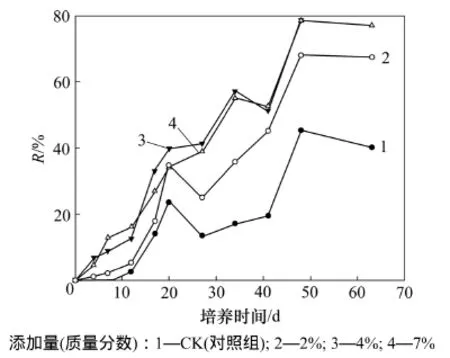
图2 添加不同浓度菌剂下的石油降解率RFig.2 Degradation rates of different contents of oil degradation bacteria
2.3.1 正构烷烃、类异戊二烯烷烃降解规律
原始油样和经混合菌作用7 d的原油正构烷烃的碳数分布相同均为C14~C39,但经混合菌作用7 d的原油正构烷烃的主峰碳明显前移,是混合菌具有选择性对高碳数正构烷烃有较强烈的去甲基作用的反映。w(∑C21-)/w(∑C22+)参数显示混合菌在降解正构烷烃时高碳数烷烃的降解速率明显大于低碳数烷烃。原始油样的成熟度高因而OEP变化不太明显,但原始油样的OEP比经混合菌作用7 d的原油样品的大,表明混合菌在降解正构烷烃时奇数碳烷烃的降解速率大于偶数碳烷烃的降解速率。姥植比(w(Pr)/w(Ph))是利用类异戊二烯烷烃中常见的姥鲛烷与植烷的比值,研究样品有机质氧化还原程度的有意义的参数。一般认为原油遭受混合菌不太强烈的降解时,类异戊二烯烷烃不受降解的影响。本研究发现:经受混合菌对原油作用7 d后其w(Pr)/w(Ph)比为0.644,明显大于原油的0.578,反映出原油中类异戊二烯烷烃在混合菌7 d的作用过程中发生了明显的降解,使部分植烷(C20H42相对分子质量M=282)脱去1个甲基转化为姥鲛烷(C19H40,M=268)。w(Pr)/w(C17)和w(Ph)/w(C18)是姥鲛烷(Pr)与其相邻的C17烷烃以及植烷(Ph)与其相邻的C18烷烃的相关性参数,该值越大表明原油受混合菌作用时烷烃降解的速率越高。由表3可知:经受混合菌对原油作用7 d后其w(Pr)/w(C17)和w(Ph)/w(C18)均呈明显的增大趋势,表明原油受混合菌7 d作用过程中烷烃受到较明显的降解,混合菌可以广泛利用从C14~C39正构烷烃为碳源,降解率为42.8%~89%,类异戊二烯烷烃则比较稳定。w(∑hop)/w(∑)烷烃是反映藿烷在原油总离子流中相对强度的参数,经混合菌作用7 d的原油样品该值明显比原始油样的大,表明混合菌在降解原油时环状萜类化合物比烷烃系列稳定得多。
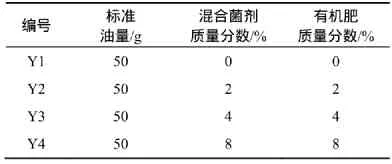
表2 各组试验处理措施Table2 Each experimental treatment or measures
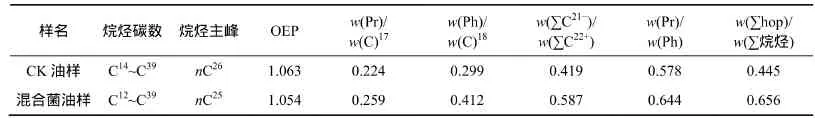
表3 降解后烷烃组分分析Table3 Analysis of alkane component after degradation %
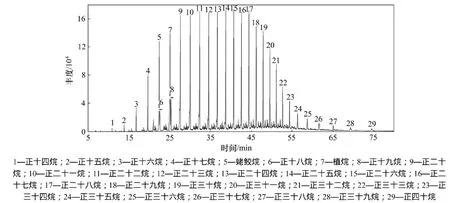
图3 降解后正构烷烃、类异戊二烯烷烃离子流图Fig.3 TIC of remaining n-alkanes and isoprenoid alkanes after degradation
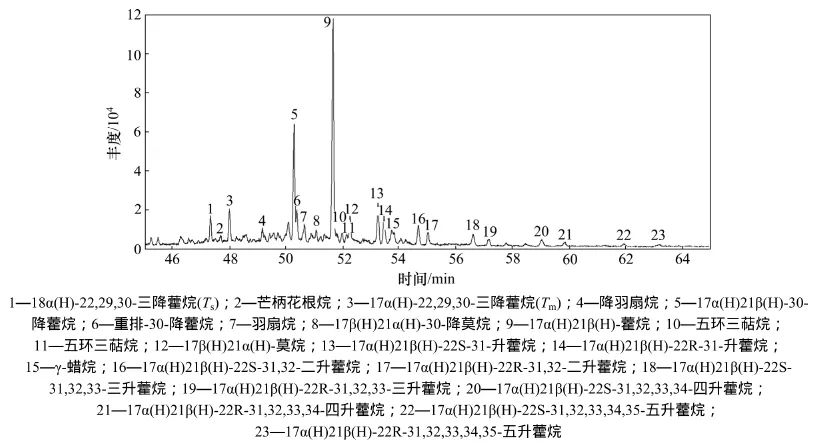
图4 降解后霍烷离子流图Fig.4 TIC of remaining hopane after degradation
2.3.2 霍烷降解规律
原始原油和经历混合菌作用7 d的原油的藿烷系列碳数分布相同均为C27~C35(C28缺失),主峰相同均为C30-αβ藿烷。w(Ts)/w(Tm)是石油地质领域常用的有机质演化程度参数,Ts为18α(H)-22,29,30-三降藿烷,Tm为17α(H)-22,29,30-三降藿烷。在生物体原生质中只有Tm构型是没有Ts构型的,当这类生物进入地质体后在热作用、微生物作用、压力及矿物催化作用下三降藿烷将由Tm立体构型逐渐向更稳定的Ts立体构型转化,因而w(Ts)/w(Tm)越大既反映了有机质受外作用力的程度越强。研究样品主要改变的外作用力是混合菌作用,所以,w(Ts)/w(Tm)越大,则混合菌对有机质的降解越强烈。从表4可以看出:经混合菌作用过的样品w(Ts)/w(Tm)均比原始油样的大,因而混合菌作用能促使五环三萜类化合物立体构型中不稳定构型向稳定性构型转化。大于31个碳的17α(H)和21β(H)构型的藿烷其第22位碳原子成为手性碳,因而会出现一对镜像异构体(22S+22R)。由于在生物体中22R异常高而22S异常低,通常将22R构型称作生物构型,将22S构型称作生地质构型。当这类生物进入地质体后,在热作用、微生物作用、压力及矿物催化等外力作用下,22R将逐渐向22S转化,其转化终点值为w(22S):w(22R)=6:4。地球化学研究中常用C31αβ-22S/22(S+R)和C32αβ-22S/22(S+R)作为判识有机质演化程度的参数(该值大于0.400为成熟有机质,该值小于0.200为未熟有机质,介于0.200~0.400之间为低成熟有机质)。研究的原始油样为成熟有机质,其C31αβ-22S/22(S+R)和C32αβ-22S/22(S+R)分别为0.591和0.577即将接近转化终点值(0.600),受外力作用变化不会很大。从表4可以看出经混合菌作用过的样品C31αβ-22S/22(S+R)和C32αβ-22S/22(S+R)均大于原始油样的该值,到达终点。因而,混合菌作用能促使五环三萜类化合物的手性碳R构型向更稳定的S构型转化。
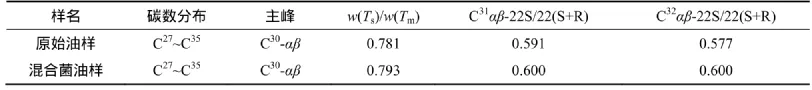
表4 降解后霍烷组分分析Table4 Analysis of hopane component after degradation
2.4 影响石油降解的因素分析
2.4.1 脱氢酶活性的变化
用752紫外分光光度计在波长486 nm处测得TTC标准曲线,得到标准曲线方程为:
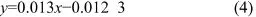
其中:相关系数R2为0.993;y为不同浓度的TTC对应的吸光度;x为TTC质量浓度,μg/mL。
脱氢酶活性可以作为微生物氧化还原系统的指标,被认为能很好地估计土壤中微生物的氧化能力,土壤肥力和施肥方式可直接影响土壤脱氢酶活性。如图5所示,随着培养时间的增加,脱氢酶活性逐渐增大,说明在生物修复过程中微生物的活性在逐渐增强,这也与图2中石油烃降解率变化趋势大体相同。在培养过程中,0~4 d的脱氢酶活性变化曲线表明:向土壤加入菌剂的初期,一方面,有机肥的加入促进了土著微生物的生长;另一方面,外加菌剂进入新环境需要一定的适应时间的,上升趋势平缓。随着混合菌在土壤中适应性增强,细菌开始迅速增长,微生物活性明显增加,在17 d时达到了最高峰,此时微生物降解土壤中石油烃物质效率最高;此后,微生物的活性逐渐降低,34 d后逐渐达到平衡,修复后期随着石油烃类污染物的不断消耗,难降解物质的大量积累以及代谢产物的积累导致微生物活性降低。实验中由于添加的有机肥的含量不同,CK是没有加任何菌剂和有机肥的对照组,但是,它的石油降解率的变化趋势和2%的变化趋势没有很明显的区别,说明加入少量菌剂和有机肥对石油降解速率的提高没有明显的作用。4%添加量的石油降解率的变化趋势与8%的变化趋势相比,4%添加量略大于8%的添加量,这是因为过量的有机肥会抑制细菌的增长。
2.4.2 氮磷含量与石油降解率的关系
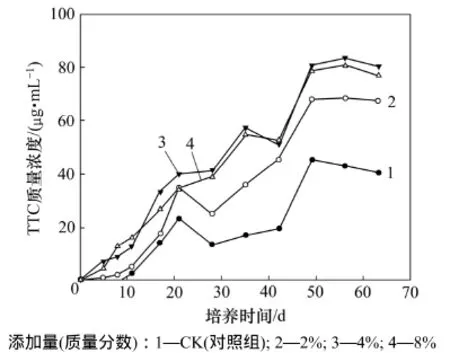
图5 添加不同浓度菌剂下的TTC质量浓度变化Fig.5 TTC concentration change of different concentrations of bacteria
微生物细胞的化学组成主要是碳、氢、氧、氮、磷和各种矿质元素,石油污染物提供的主要是碳、氢元素。本实验中氮、磷由加入的蚯蚓肥提供。氮、磷营养物质是影响土壤中石油污染物生物降解的一个主要原因。不同菌剂下氮、磷质量分数与降解率的关系如图6所示。由图6可见:氮、磷的消耗量随着石油降解率的增大而逐渐减少,说明石油降解菌在添加一定量的氮、磷时对石油烃的微生物降解均有明显的促进作用。但是存在一个较经济合理的添加量范围。在本实验菌剂量和土壤环境下,4%的有机肥添加量使降解效果达到最好。
2.4.3 降解率与电导率的关系
降解率与电导率的关系如图7所示。从图7可见:土壤中石油的降解率与土壤溶液中的电导率呈反比例关系。土壤溶液中的电导率主要受土壤全盐含量。土壤含水量的影响,而本实验中土壤的含水量保持在20%左右,对电导率的影响不大,本实验电导率的主要影响因素是全盐含量,图5中由于有机肥是按照0,2%,4%和8%的量加入石油污染土壤中的,所以,对降解率的影响也不同。图7(a)中由于没有加入菌剂和有机肥,石油的降解主要是靠土壤中土著微生物的作用,开始由于石油的加入,提供了碳源,以及土壤中本身的矿物含量提供了氮磷等微生物生长所需的营养物质,微生物迅速增长,石油的降解率有所提高,但当土壤中的矿物含量慢慢减少时,电导率也呈下降趋势。由于缺少生长所需营养物质,微生物的量开始下
降,石油的降解速率也下降。图7(b)中由于加入的有机肥的含量少,所以,变化趋势和图7(a)的变化趋势相似。图7(c)和(d)中,由于加入的有机肥的量满足微生物的生长需要,所以,微生物大量生长,石油的降解率明显高于图7(a)和(b)中的石油降解率。营养盐的消耗使得土壤中的电导率呈下降趋势,所以,石油降解率升高时,土壤电导率下降。
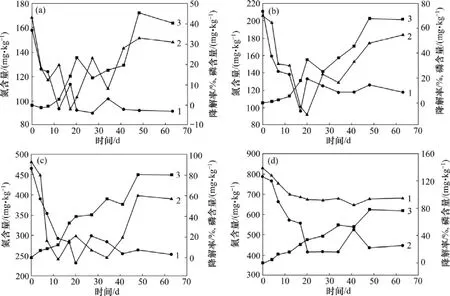
图6 不同菌剂下氮、磷含量(质量分数)与降解率的关系Fig.6 Change of Nitrogen phosphorus and degradation rate under action of different concentrations of bacteria
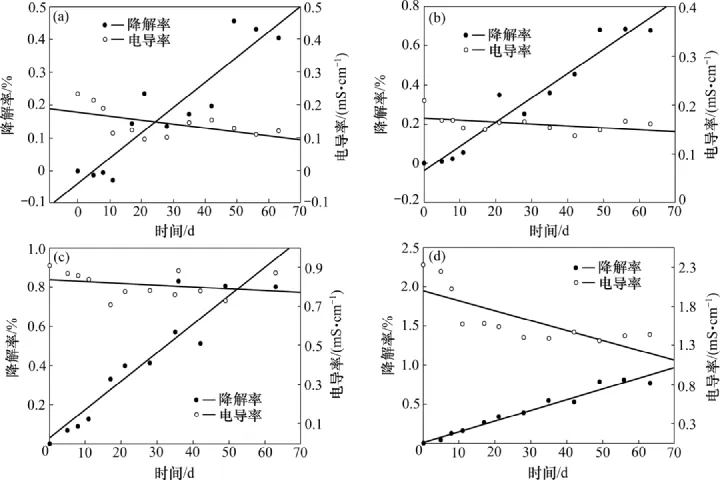
图7 不同菌剂下的降解率与电导率的关系Fig.7 Change of degradation rate and electrical conductivity under action of different contents of bacteria
3 结论
(1)由于只添加2%有机肥的菌剂,脱氢酶活性变化趋势与未添加有机肥的变化趋势相似。分别添加4%和8%有机肥的脱氢酶活性变化趋势相差不大,添加4%有机肥的降解细菌含量有时略大于添加8%有机肥的细菌含量。这是因为添加的有机肥的含量不同决定的。但总的说来,添加一定量菌剂的石油降解率要比不添加或者添加少量菌剂量的石油降解率高,并且添加菌剂量不同其降解效率也不同。
(2)实验中由于添加的有机肥的含量不同,导致石油降解率也不同。不加有机肥和加过量的有机肥都不能促进石油降解细菌更好地降解石油,只有添加适量的有机肥才能使降解细菌的降解效果最好。
(3)土壤溶液中电导率与石油降解率呈反比例关系,石油的降解率增加则土壤中的电导率下降。
(4)混合菌株降解石油规律是先降解高碳数正构烷烃为低碳数正构烷烃,高碳数正构烷烃中奇数碳向偶数碳正构烷烃演化;经受混合菌对原油作用7 d后其w(Pr)/w(Ph)为0.644,明显大于原油的0.578,反应出原油中类异戊二烯烷烃在混合菌7 d的作用过程中发生了明显降解,使部分植烷(C20H42,M=282)脱去1个甲基转化为姥鲛烷(C19H40,M=268)。此外,菌株还能较好地促使五环三萜类化合物立体构型中不稳定构型向稳定性构型转化。
[1]何良菊, 魏德洲, 张维庆.土壤微生物处理石油污染的研究[J].环境科学进展, 1999, 7(3): 110-115.HE Liang-ju, WEI De-zhou, ZHANG Wei-qing.Research of microbial treatment of petroleum contaminated soil[J].Advances of Environmental Science, 1999, 7(3): 110-115.
[2]Margesin R, Schinner F.Bioremedation (Natural Attenuation and Biostimulation)of diesel-oil-contaminated soil in an alpine glacier sking area[J].Appl Environ on Microbio, 2001, 67(7):3127-3133.
[3]李春荣, 王文科, 曹玉清, 等.石油污染物的微生物降解[J].地球科学与环境学报, 2007, 29(2): 214-216.LI Chun-rong, WANG Wen-ke, CAO Yu-qing, et al.Petroleum pollutions degraded by microorganisms[J].Journal of Earth Sciences and Environment, 2007, 29(2): 214-216.
[4]Kishore E D, Ashis K M.Crude petroleum-oil biodeg-radation efficiency of Bacillus subtilis and Pseudomonas aeruginosa strains isolated from a petroleum-oil contami-nated soil from North-East India[J].Bioresource Tech-nology, 2007, 98(7):1339-1345.
[5]Alejandro R G, Mar A C, Ferre-R O, et al.Bioremediation of crude oil polluted seawater by a hydrocarbon-degrading bacterial strain immobilized on chitin and chitosan flakes[J].International Biodete-rioration & Biodegradation, 2006, 57(4): 222-228.
[6]Ayotamuno M J, Kogbara R B, Ogajs O T, et al.Bioremediation of a crude-oil polluted agricultural-soilat PortHarcourt,Nigeria[J].Applied Energy, 2006, 83(11): 1249-1257.
[7]Mark A S, James S B, Cheryl A P, et al.Evaluat ion of two commercial bio-augmentation products for enhanced removel of petroleum from a wet land[J].Ecological Engineering, 2004, 23:263-277.
[8]Sorkhoh N A, Ghannoum M A, Ibrahim A S, et al.Crude oil and hydrocarbon degrading strains of Rhodococcus rhodochrous isolated from soil and marine environments in Kuwait[J].Environ Pollut, 1990, 65(1): 1-17.
[9]顾传辉, 陈桂珠.石油污染土壤生物降解生态条件研究[J].生态科学, 2000, 1(4): 67-71.GU Chuan-hui, CHEN Gui-zhu.Research of bioremediation condition of petroleum contaminated soil[J].Ecological science,2000, 1(4): 67-71.
[10]韩慧龙, 陈镇, 杨健民, 等.真菌-细菌协同修复石油污染土壤的场地试验[J].环境科学, 2008, 29(2): 454-461.HAN Hui-long, CHEN Zhen, YANG Jian-min, et al.Field scale demonstration of fungi-bacteria augmented remediation of petroleum contaminated soil[J].Environment Science, 2008,29(2): 454-461.
[11]丁克强, 尹睿, 刘世亮, 等.石油污染土壤堆制微生物降解研究[J].应用生态学报, 2002, 13(9): 1137-1140.DING Ke-qiang, YIN Rui, LIU Shi-liang, et al.Bioremediation for petroleum-contaminated soil by composting technology[J].Chinese Journal of Applied Ecology, 2002, 13(9): 1137-1140.
[12]何良菊, 李培杰, 魏德洲.石油类物质微生物降解的营养平衡及降解机理[J].环境科学, 2004, 25(1): 91-94.HE Liang-ju, LI Pei-jie, WEI De-zhou.Nutrient balance and mechanism of biological degradation of oil[J].Environment Science, 2004, 25(1): 91-94.
[13]乔俊, 陈威, 张承东.添加不同营养助剂对石油污染土壤生物修复的影响[J].环境化学, 2010, 29(1): 6-11.QIAO Jun, CHEN Wei, ZHANG Cheng-dong.Bioremediation of petroleum contaminated soil by various nutrient amendments[J].Environment Chemistry, 2010, 29(1): 6-11.

