Sr2MgSi2O7∶Tb3+,Li+荧光粉的合成和发光机理
陈 茜 史元元 陈宁远 赵君风 荣春英 余丽萍 廉世勋
(湖南师范大学化学化工学院,化学生物学及中药分析教育部重点实验室;资源精细化与先进材料湖南省高校重点实验室,长沙 410081)
Sr2MgSi2O7∶Tb3+,Li+荧光粉的合成和发光机理
陈 茜 史元元 陈宁远 赵君风 荣春英 余丽萍 廉世勋*
(湖南师范大学化学化工学院,化学生物学及中药分析教育部重点实验室;资源精细化与先进材料湖南省高校重点实验室,长沙 410081)
采用高温固相法合成Sr2-mMg1-nSi2O7∶mTb3+,nLi+(m=0.03~0.50,n=m)系列荧光粉。使用X射线衍射仪和荧光光谱仪对样品的物相和发光性质进行了表征。在377 nm紫外光激发下,荧光粉的发射光谱呈多谱带发射,主峰位于490 nm,542 nm,590 nm和613 nm处,分别对应于Tb3+的5D4→7FJ(J=6,5,4,3)跃迁发射。调节Tb3+离子掺杂浓度,可实现荧光粉的发光颜色从蓝到白、黄、绿的可调发射;名义组成为Sr1.95Mg0.95Si2O7∶0.05Tb3+,0.05Li+的荧光粉在紫外光(377 nm)激发下发白光,其色坐标(0.322,0.317)接近纯白光(0.33,0.33),是一种潜在的LED用单基质白光荧光粉。
Sr2MgSi2O7∶Tb3+;紫外光激发;LED;白光荧光粉
与传统的白炽灯、荧光灯相比,白光LED具有节能、寿命长、高亮度及环保无污染等优点,可用于照明、显示等领域。1993年日本日亚化学公司首先在蓝光GaN发光二极管上取得技术突破[1],并于1996年采用光转换技术实现了白光LED。目前,白光LED的实现方法有光转换型和芯片组合型。从工艺、成本及技术现状等因素考虑,光转换法优于芯片组合法。
光转换法是指通过在近紫外或蓝光LED芯片上涂覆具有光致发光性能的荧光粉来实现白光。根据芯片的不同,光转换法又有两种方式:一种是蓝光芯片加黄色荧光粉InGaN/Y3Al5O12∶Ce3+(YAG∶Ce)[2],另一种是紫外芯片涂覆单一白色[3-5]或三基色荧光粉[6]。由于YAG∶Ce体系缺乏红光导致显色性不高、三基色荧光粉之间存在颜色再吸收和配比调控困难等问题[7],紫外芯片激发的单一基质白光荧光粉引起了广泛关注。近年来,国内外对紫外或近紫外激发的全色单一基质荧光粉的研究很多,并且取得了相当大的进展。例如,碱土磷灰石M5(PO4)3Clx∶Eu2+(M=Ca,Sr,Ba),铟酸盐CaIn2O4∶Eu3+,硫化物( Ca1+x-yEuy)Ga2S4+x,硅酸盐Li2SrSiO4∶Eu2+,Ce3+、Sr2SiO4∶Eu2+、Ba3MgSi2O8∶Eu2+,Mn2+、Sr2MgSiO5∶Eu2+、Ca2SiO3Cl2∶Eu2+,Mn2+、Ca2-x-yAl2SiO7∶Ce3+,Tb3+等[8-15]。 但是,以Sr2MgSi2O7为基质的白光发射荧光粉还未见报道。我们发现Tb3+掺杂Sr2MgSi2O7可以获得白光现象,本文报道了Sr2MgSi2O7∶Tb3+荧光粉的合成和发光性质,并对白色发光机理进行了讨论。
1 实验部分
1.1 试剂与仪器
所用试剂SrCO3,MgO,LiNO3和H2SiO3均为分析纯,Tb4O7的纯度为99.99%。日本理学 D/max-2500型X射线衍射仪 (Cu靶,40 kV,300 mA),F-4500荧光分光光度计(150 W氙灯光源,R928型号光电倍增管,电压400 V,滤光片为UV390)。
1.2 实验过程
按照化学式Sr2-mMg1-nSi2O7∶mTb3+,nLi+(m=0.03~0.50,n=m)的计量比合成系列荧光粉。准确称取原料 SrCO3(AR),MgO(AR),H2SiO3(AR),LiNO3(AR)和Tb4O7(99.99%),置于玛瑙研钵中充分研磨均匀,并装入氧化铝坩埚,置于箱式炉中在1 200℃灼烧6 h。自然冷却至室温,取出后研磨即得荧光粉样品。
2 结果与讨论
2.1 结构表征
图1为合成样品的X射线衍射图。衍射峰与Sr2MgSi2O7标准卡片(PDF No.75-1736)一致,表明合成样品均为纯相,属于四方晶系,空间群为P421m (No.113)。这表明 Tb3+和 Li+离子的加入并未对Sr2MgSi2O7晶体结构产生影响。
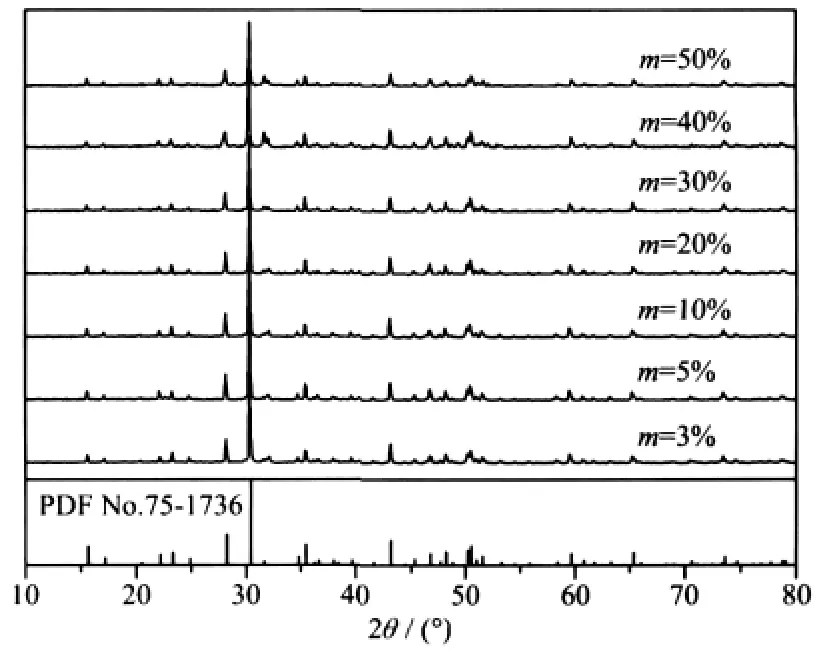
图1 样品Sr2-mMg1-nSi2O7∶mTb3+,nLi+(m=0.03~0.50,n=m)的XRD图Fig.1 XRD patterns of Sr2-mMg1-nSi2O7∶mTb3+,nLi+(m= 0.03~0.50,n=m)samples
2.2 Sr2-mMg1-nSi2O7∶mTb3+,nLi+的光谱特性
图 2(a)是 Sr2-mMg1-nSi2O7∶mTb3+,nLi+(m=0.03~0.50,n=m;简写成SMS∶Tb3+,Li+)系列样品在377 nm激发下的发射光谱。发射光谱表明Tb3+在SMS基质中呈现多谱带发射,490 nm、542 nm、590 nm和613 nm 发射峰分别对应于 Tb3+离子5D4→7FJ(J= 6,5,4,3)跃迁。图2(b)列出了490 nm、542 nm、590 nm和613 nm处发射峰强度与Tb3+离子掺杂浓度变化的关系。由图2(b)可知,Tb3+离子浓度变化不改变样品的发射光谱分布,但影响了红、绿和蓝光的相对发光强度,红光和绿光强度变化显著,红光和绿光发射强度比值(R/G)见图2(c)。随着Tb3+离子浓度增加,R/G值呈现先增大后减小的变化趋势。当m=0.05时,红、绿光强度相近,R/G值等于0.88。增大Tb3+离子浓度m=0.10,此时红光强度增大至绿光的2倍,R/G值达到最大为2.34,但红、绿光均未达到最强。继续增大Tb3+离子浓度m=0.20,红、绿光强度达到最高且强度相当,R/G值降低近似等于1。当Tb3+离子浓度大于0.30时,红光强度逐渐降低,绿光显著增强,R/G值小于1。
根据图2(a)发射光谱数据,采用色坐标软件CIE计算了SMS∶mTb3+系列样品的色坐标,结果如表1所示。由表1可知,在377 nm紫外光激发下,样品的色坐标随Tb3+离子浓度的变化而变化。其色坐标如图3所示,随Tb3+离子掺杂浓度逐渐增大,荧光粉发光颜色从蓝到白、到黄、再到绿变化,颜色可调。点b、c和e分别对应于样品S2、S3、和S5,色坐标均落在白光区,且样品S2(m=0.05)的色坐标 (0.322,0.317)与1931年国际照明委员会给出的纯白光色坐标W(0.33,0.33)接近。
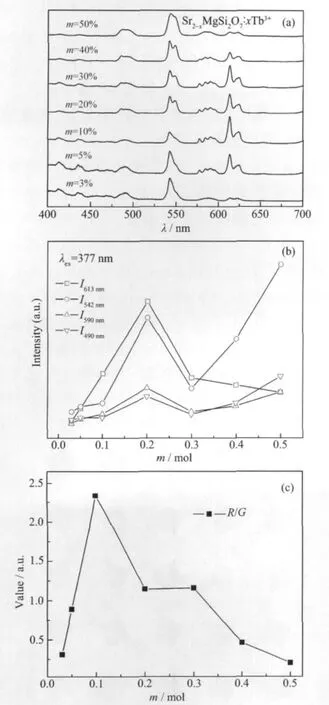
图2 377 nm激发下,Sr2-mMg1-nSi2O7∶mTb3+,nLi+(m=0.03~0.50,n=m)的发射光谱(a)、Tb3+离子浓度与样品发光强度(b)和R/G比值(c)的关系Fig.2 Emission spectra for Sr2-mMg1-nSi2O7∶mTb3+,nLi+(m= 0.03~0.50,n=m) (a)Relationship between the emission intensities of Sr2-mMg1-nSi2O7∶mTb3+,nLi+ (m=0.03~0.50,n=m)samples and the Tb3+ concentration(b)and the relationship between the concentration of Tb3+and R/G value of Tb3+under excitation at 377 nm(c)
2.3 Tb3+和Eu3+在Sr2MgSi2O7中发光性质的差异
在377 nm紫外光激发下,SMS∶0.05Tb3+可同时发射红、绿和蓝光并复合得到白光,其色坐标与纯白光点接近。一般地,单掺Tb3+离子荧光粉的红光发射强度较低,多以蓝光发射和绿光发射为主[16-19]。在SMS基质中,Tb3+离子的红光发射强度与绿光发射强度相当甚至更高。Eu3+离子的特征发射在590 nm或613 nm处,为排除Eu3+的干扰,我们在同样的实验条件下合成了SMS∶0.05Eu3+荧光粉,并研究了其光谱性质。图4是样品SMS∶0.05Tb3+和SMS∶0.05Eu3+的激发和发射光谱。图4(a)表明,SMS∶0.05Tb3+的激发光谱由 4f8→4f75d1允许跃迁激发的宽吸收带(200~280 nm)、4f→4f电子跃迁吸收带340~400 nm和484 nm窄吸收带三部分构成,其中377 nm处的激发峰最强,484 nm处的激发峰强度略低于377 nm。荧光粉可被紫外光 (350~380 nm)和蓝光(484 nm)有效激发,但目前缺乏484 nm蓝光LED芯片,所以SMS∶0.05Tb3+是一种适用于UVLED管芯激发的荧光粉。在377 nm激发下,发射光谱如图4(b)所示。荧光材料呈多峰发射,4个主要发射峰分别位于490,542,590和613 nm处,且绿光发射与红光发射强度相当。受SMS晶体场的影响,Tb3+离子5D4→7FJ(J=6,5,4,3)跃迁对应发射峰产生劈裂、峰值左右波动。5D4→7F6(489 nm)发射峰劈裂为485 nm和490 nm 2个尖峰,位于613 nm处的尖峰也是由于5D4→7F3(620 nm)发射峰劈裂所致。而5D4→7F4(586 nm)跃迁发射出现了三峰劈裂现象,分别位于576 nm、584 nm和590 nm处。观察图4(b)可以发现,红光区613 nm处发射类似于Eu3+离子的5D0→7F2跃迁发射。与单掺Tb3+离子样品红光区的最高发射峰相比,单掺Eu3+离子的发射峰向左偏移,且激发光谱中397 nm处并未发现Eu3+离子的特征激发峰。在377 nm和397 nm紫外光激发下,SMS∶0.05Eu3+发射光谱中均未发现Tb3+离子542 nm特征发射。结果表明,SMS∶0.05Tb3+中613 nm处红光发射属于Tb3+离子的跃迁发射。

表1 Tb3+不同掺杂浓度的样品色坐标Table 1 CIE chromaticity coordinate of Sr2-mMg1-nSi2O7∶mTb3+,nLi+(m=0.03~0.50,n=m)
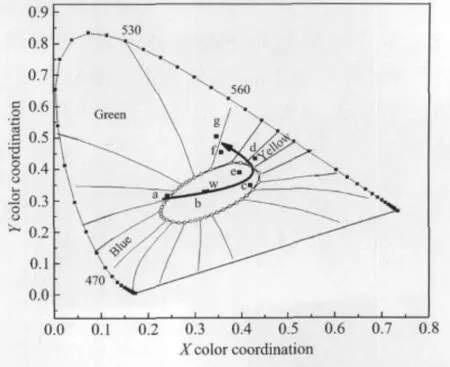
图3 377 nm激发下,Sr2-mMg1-nSi2O7∶mTb3+,nLi+(m=0.03~0.50,n=m)S1~S7样品的色坐标Fig.3 CIE chromaticity diagram for Sr2-mMg1-nSi2O7∶mTb3+, nLi+(m=0.03~0.50,n=m)from S1to S7excited by λex=377 nm Point a,S1;Point b,S2;Point c,S3;Point d,S4;Point e,S5;Point f,S6;Point g,S7

图4 Sr1.95MgSi2O7∶0.05Tb3+和Sr1.95MgSi2O7∶0.05Eu3+荧光粉的激发光谱(a)和发射光谱(b)Fig.4 Excitation spectra(a)and emission spectra(b)of Sr1.95Mg0.95Si2O7∶0.05Tb3+,0.05Li+and Sr1.95Mg0.95Si2O7∶0.05Eu3+,0.05Li+phosphors
2.4 Tb3+在Sr2MgSi2O7中的白色发光机理
Sr2MgSi2O7和Ca2MgSi2O7晶体结构相似,存在八配位(SrⅠ)格位[20-21],其晶体结构如图5所示。当半径较小的Tb3+离子 (0.118 nm)取代Sr2+离子(0.126 nm)格位,晶格产生扭曲,导致Mg-O键长发生变化,基质中有可能产生六配位(SrⅡ)格位,并且Tb3+离子将优先占据Sr2+离子的八配位晶体场格位,形成稳定结构[22-23]。由于Tb3+离子取代Sr2+离子电荷价态不匹配,对合成材料的发光性能产生影响,因此,引入Li+离子作为电荷补偿剂[24]。图6是SMS∶0.05Tb3+荧光粉的发光衰减曲线。如果荧光粉中有一种发光中心,衰减函数可以使用一阶拟合。若有两种发光中心,衰减函数则使用二阶拟合,以此类推[25]。SMS∶0.05Tb3+荧光粉中存在两种发光中心,拟合后计算可知Tb3+离子5D4→7F3(613 nm)、5D4→7F4(590 nm)、5D4→7F5(542 nm)和5D4→7F6(490 nm)的衰变寿命τ分别为1.18 ms,1.80 ms,2.75 ms和2.44 ms。根据衰变寿命τ,可以发现5D4→7F5(542 nm)衰减时间最长,5D4→7F3(613 nm)衰减时间最短。因此,5D4→7F6,5,4跃迁发射比5D4→7F3跃迁发射更易稳定存在,这也是大多数单掺Tb3+离子荧光粉发蓝绿光的主要原因。
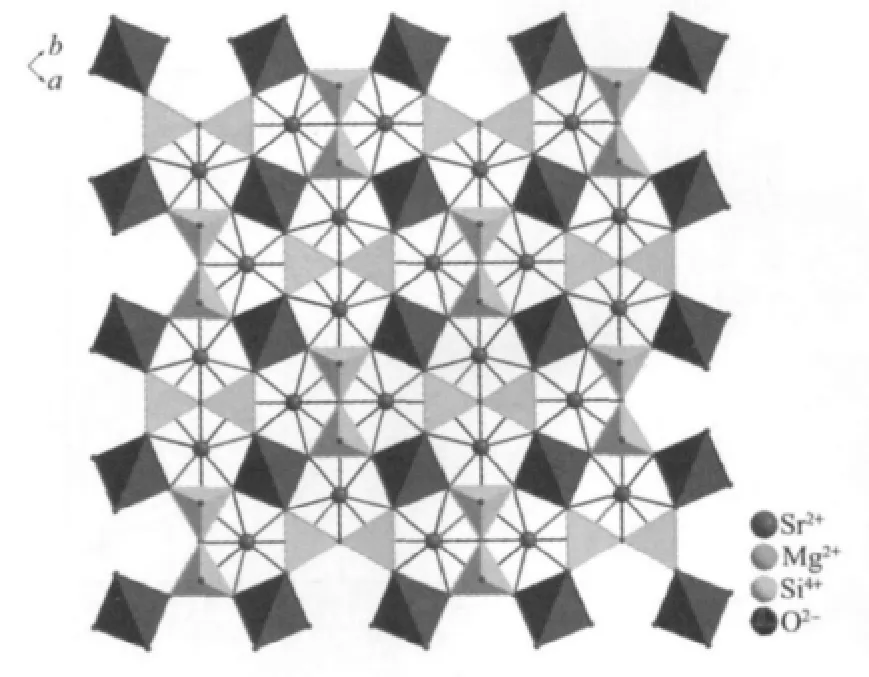
图5 Sr2MgSi2O7晶胞部分结构Fig.5 A portion of the structure of Sr2MgSi2O7
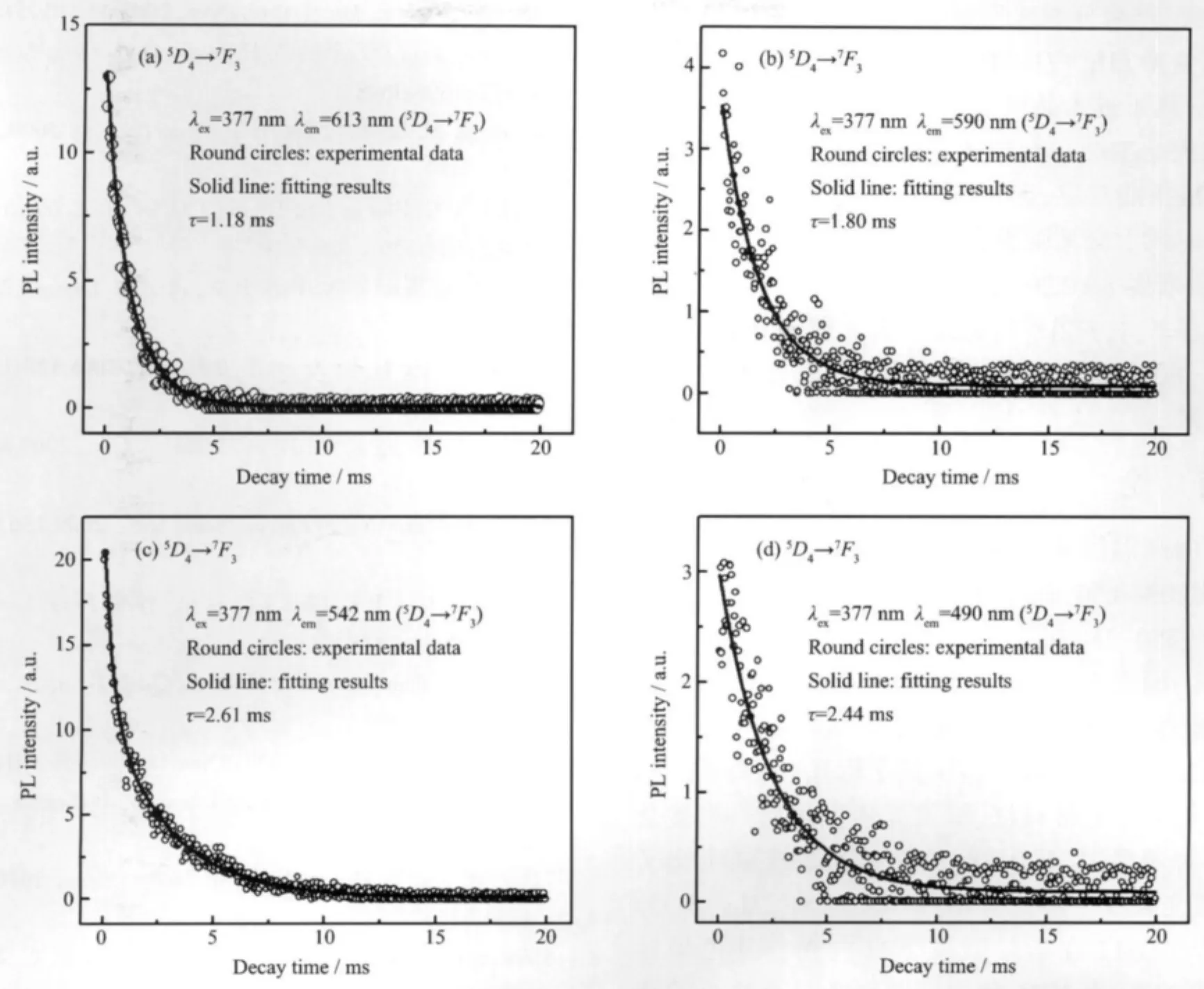
图6 Sr1.95MgSi2O7∶0.05Tb3+中Tb3+离子发光衰减曲线Fig.6 Luminescence decay curves for Tb3+in Sr1.95Mg0.95Si2O7∶0.05Tb3+,0.05Li+
当SMS基质中掺杂Tb3+离子的物质的量百分含量为0.03mol%时,多数掺杂离子倾向于取代SrⅠ格位形成稳定结构,产生5D4→7FJ(J=6,5,4,3)跃迁,主要以蓝、绿光(5D4→7F6,5)发射为主。在SMS基质中,虽然Tb3+离子取代SrⅡ格位几率较低,但只要占据SrⅡ格位,就将产生5D4→7F3(613 nm)跃迁,发射红光。保持电荷补偿剂物质的量百分含量不变,增大Tb3+离子的掺杂浓度,材料将产生更多晶格缺陷[26],分别为带正电荷的阳离子空穴和带负电荷的氧离子空穴。当两种空穴浓度接近,材料可稳定存在。随着Tb3+离子浓度增大,阳离子空穴将逐渐增加。根据电荷互补原理,材料中也将产生更多的氧空穴[27],从而提高了Tb3+离子的跃迁发射几率,材料发光强度明显增强。同时,也增强了Tb3+离子取代Sr2+离子六配位格位几率,具体表现为5D4→7F3红光跃迁发射增强。即Tb3+离子含量增大至0.20mol%,红绿光强度达到最强。而继续增大Tb3+离子浓度,红光强度逐渐降低。这是由于激活剂Tb3+离子浓度过高,晶格发生畸变,导致Tb3+离子取代SrⅡ格位几率减小,表现为红光强度减弱。因此,Tb3+离子取代Sr2+离子不同格位几率是决定材料红、绿强度比率的关键。也就是说,当Tb3+离子浓度为0.05mol%,0.10mol%,0.30mol%,掺杂离子占据六配位格位和八配位格位几率相当,则红、绿光强度相近,R/G比值近似等于1,如图2所示。结合图3中点b、c和e的色坐标可知,除红、绿光发射强度对样品白光区色坐标位置的影响外,蓝光相对发射强度也是影响因素之一。
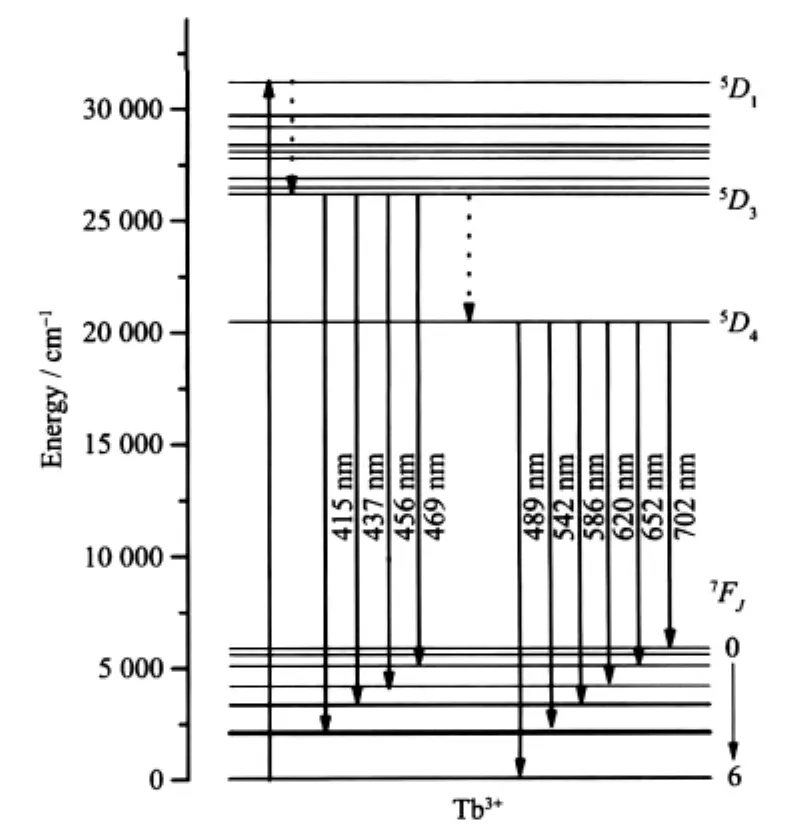
图7 Tb3+离子能级跃迁机理Fig.7 Schematic energy level diagram of the Tb3+ showing possible energy transfer mechanisms
在Tb3+离子能级中,由于5D3和5D4能级之间的能隙 (~5600 cm-1)与7F6和7F0之间的能隙 (~5800 cm-1)相近,其能级跃迁机理如图7所示。因此,当Tb3+离子掺杂含量大于0.20mol%,高能级发射将很容易猝灭,产生低能级发射[17],激活剂Tb3+离子间发生交叉弛豫:Tb3+(5D3)+Tb3+(7F6)→Tb3+(5D4)+Tb3+(7F0)。大量Tb3+离子进入晶格,晶格扭曲与交叉弛豫同时发生。SMS∶mTb3+(m=0.20~0.30)中离子间的交叉弛豫强于晶格扭曲效应,蓝光强度降低。当m>0.30,晶格扭曲效应强于交叉弛豫,蓝光强度小幅度增强。反之,掺杂浓度m<0.20时,交叉弛豫现象减弱,出现5D3→7FJ(J=5,4,3,2)系列蓝光发射。即SMS∶0.05Tb3+样品中,红光和绿光发光强度相当,混合蓝光产生白光发射。
3 结 论
采用高温固相法制备的Sr2-mMg1-nSi2O7∶mTb3+,nLi+(m=0.03~0.50,n=m)(0.03≤m≤0.50)荧光粉可被紫外光 (350~380 nm)有效激发,同时发射蓝绿光(490 nm)、绿光(542 nm)、红橙光(590 nm)和红光(613 nm)。随Tb3+离子掺杂浓度增大,红光与绿光发射强度比(R/G)先增大后减小,Tb3+离子取代Sr2+离子不同格位的几率决定材料红、绿发光强度比值。当掺杂浓度相对较高(大于0.30),晶格扭曲效应强于交叉弛豫,蓝光强度先降低后增强。发现Sr1.95Mg0.95Si2O7∶0.05Tb3+,0.05Li+在紫外激发下发白光,其色坐标(0.322,0.317)与1931年国际照明委员会给出的纯白光(0.33,0.33)非常接近,是一种潜在的适用于近紫外芯片的LED用白光荧光材料。
致谢:张漫波副教授(博士)在晶体结构方面提出了有益的建议并帮助绘制了晶胞结构图。
[1]Nakamura S,Mukai T,Senoh M.Appl.Phys.Lett.,1994,64 (13):1687-1689
[2]Nakamura S,Fasol G.The Blue Laser Diode:GaN Based Light Emitters and Lasers.Berlin:Springer Verlag,1997: 230-233
[3]Guo N,Huang Y,You H,et al.Inorg.Chem.,2010,49(23): 10907-10913
[4]MaW,ShiZ,Wang R.J.AlloysCompd.,2010,503(1):118-121
[5]Chen X,Zhao J,Yu L,et al.J.Lumin.,2011,131:2697-2702
[6]LiuCH,WuRK.Jpn.J.Appl.Phys.,2003,42(4B):2284-2287
[7]Kim J S,Jeon P E,Park Y H,et al.Appl.Phys.Lett.,2009, 85(17):3696-3698
[8]Zhang X M,Li W L,Seo H J.Phys.Lett.A,2009,373(38): 3486-3489
[9]Zhang X G,Zhang J L,Huang J Q,et al.J.Lumin.,2010, 130(4):554-559
[10]Choi N S,Park K W,Park B W,et al.J.Lumin.,2010,130 (4):560-566
[11]Zhang X,He H,Li Z,et al.J.Lumin.,2008,128(12):1876-1879
[12]Zhang X,Wang J,Wu H,et al.Mater.Lett.,2009,63(2):340 -342
[13]Jiao H,Wang Y.J.Electrochem.Soc.,2009,156(5):J117-J120
[14]Kim J S,Jeon P E,Choi J C,et al.Appl.Phys.Lett.,2004, 84(15):2931-2933
[15]Sun X Y,Zhang J,Zhang X,et al.Chin.J.Lumin.,2005,26 (3):404-
[16]WANG Miao(王淼),HUANG Qing-Li(黄庆利),CHEN Xue-Tai(陈学太).Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao), 2007,23(9):1550-1554
[17]Xie M,Tao Y,Huang Y,et al.Inorg.Chem.,2010,49(24): 11317-11324
[18]Zhang C,Hou Z,Chai R,et al.J.Phys.Chem.C,2010,114 (15):6928-6936
[19]ZHANG Hai-Yan(张海燕),CAO Liang-Jun(曹亮军),WANG Lin-Kun(王琳琨),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2010,26(5):822-826
[20]Endo T,Doi Y,Wakeshima M,et al.Inorg.Chem.,2010,49 (23):10809-10814
[21]He D,Shi Y,Zhou D,et al.J.Lumin.,2007,122-123:158-161
[22]Schaper A K,Schosnig M,Kutoglu A,et al.Acta Cryst., 2001,57:443-448
[23]Bindi L,Bonazzi P,Dusek M,et al.Acta Cryst.,2001,57: 739-746
[24]LIAN Shi-Xun(廉世勋),LIN Jian-Huan(林建华),SU Mian-Zeng(苏勉曾).Chin.J.Rare Earths(Xitu Xuebao),2001,19 (6):602-605
[25]Furusho H,Holsa J,Laamanen T,et al.J.Lumin.,2008,128 (5/6):881-884
[26]Tian L,Mho S.Solid State Commun.,2003,125(11):647-651
[27]Holsa J,Aitasalo T,Jungner H,et al.J.Alloys Compd., 2004,374(1/2):56-59
Synthesis and Luminescent Mechanism of Sr2MgSi2O7∶Tb3+,Li+Phosphor
CHEN XiSHI Yuan-Yuan CHEN Ning-Yuan ZHAO Jun-Feng RONG Chun-Ying YU Li-Ping LIAN Shi-Xun*
(Key Laboratory of Chemical Biology&Traditional Chinese Medicine Research(Ministry of Education); Key Laboratory of Resource Fine-Processing and Advanced Materials,Universities of Hunan Province; College of Chemistry and Chemical Engineering,Hunan Normal University,Changsha410081,China)
The phosphors designed as Sr2-mMg1-nSi2O7∶mTb3+,nLi+(m=0.03~0.50,n=m)were prepared by the high temperature solid state reaction.Crystallization and optical properties were investigated by using powder X-ray diffraction and fluorescence spectrophotometer,respectively.Under the excitation of ultraviolet(377 nm),the emission spectra of these phosphors exhibit sharp multi-emission lines peaked at about 490 nm,542 nm,590 nm and 613 nm corresponding to the5D4→7FJ(J=6,5,4,3)typical transitions of Tb3+,respectively.The luminescence color can be tuned from blue to white,yellow and green by adjusting the doping concentration of Tb3+ions.It had been found that the nominal composition Sr1.95Mg0.95Si2O7∶0.05Tb3+,0.05Li+phosphor provides a white emission (0.322,0.317)that is very close to the standard white(x=0.33,y=0.33),which shows that it is a potential singlephased white phosphor for LED-based UV-chip.
Sr2MgSi2O7∶Tb3+;ultraviolet light excitation;LED;white phosphor
O482.31;O614.23+2
A
1001-4861(2012)02-0233-06
2011-07-01。收修改稿日期:2011-09-14。
国家自然科学基金(No.20971042),湖南省教育厅重点项目(No.10A070)和国家大学生创新性实验计划(No.101054230)资助项目。*
。E-mail:lianshixun@yahoo.com.cn;会员登记号:S060014830M。

