Au负载OMS-2催化剂的制备及其低温催化氧化性能
叶 青,闫立娜,罗才武,霍飞飞,程水源,康天放 (北京工业大学环境与能源工程学院环境科学系,北京100124)
Au负载OMS-2催化剂的制备及其低温催化氧化性能
叶 青*,闫立娜,罗才武,霍飞飞,程水源,康天放 (北京工业大学环境与能源工程学院环境科学系,北京100124)
通过前掺杂法(QI),浸渍法(IM)和沉积-沉淀法(DP)3种方法制备了Au负载氧化锰八面体分子筛(OMS-2)Au/OMS-2催化剂,研究了制备方法和制备条件对其催化氧化CO活性的影响.采用X射线衍射(XRD)和BET比表面积测定等技术对所制样品进行表征.结果表明,沉积-沉淀法制备的Au/OMS-2-DP催化剂活性明显高于前掺杂法和浸渍法制备的催化剂,这与Au/OMS-2-DP催化剂比表面积较大和负载Au颗粒较小有关.制备条件(沉淀剂种类、制备溶液pH、Au负载量和催化剂焙烧温度)明显影响Au/OMS-2-DP催化剂的催化活性.对于各种不同的沉淀剂,以KOH为沉淀剂制备的催化剂活性最高,这可能与其无钝化作用,而且形成的Au颗粒较小有关;制备溶液的为最佳,当pH值过高或过低容易导致Au颗粒的聚集和Au沉淀量较少;XRD结果表明,当Au负载量为5wt%催化剂和催化剂焙烧为300℃时,所制备的催化剂颗粒最小,所得的催化剂活性最高.最佳条件制备的Au/OMS-2-DP催化剂活性较好,CO完全转化(100%)的温度为67℃.
Au/OMS-2;低温催化氧化;制备方法;制备条件
CO主要来自于于含碳物质不完全燃烧.CO催化氧化反应已在很多领域得到了广泛的应用如封闭式内循环CO2激光器、CO气体探测器、室内空气净化以及密闭空间微量 CO的消除等领域[1].近年来,在富H2气氛下CO的优先催化氧,化(CO-PROX)也得到广泛的研究和应用[2].此外,由于 CO催化氧化反应的简单性,其常被作为催化研究中的探针反应之一[3].
自从1987年Haruta等[4]报道金负载催化剂对CO低温催化氧化具有很高的活性以来,人们对纳米金负载催化剂的CO催化氧化性质进行了广泛的研究.金负载催化剂的催化性质与Au颗粒大小,载体性质和催化剂制备工艺密切相关[5-6].目前普遍认为,高分散态纳米金对低温CO催化氧化反应具有极好的催化活性[5,7-8].当金高度分散在半导体氧化物(例如TiO2、α-Fe2O3和Co3O4)时,可以获得高的CO低温氧化活性[9].
氧化锰八面体分子筛(OMS-2),作为一种新型的绿色催化剂,成为继沸石型四面体分子筛之后又一新的研究方向[10].前期对 OMS-2的研究主要侧重于制备及结构,近期才逐渐开始应用于催化领域.目前OMS-2在催化上的应用主要侧重于催化氧化和催化还原方面:如催化脱氢和选择性催化氧化[11-12].本研究基于纳米 Au的催化氧化特性,将Au与OMS-2组成复合催化剂,并研究其结构和催化氧化CO的特性.
1 材料与方法
1.1 催化剂的制备
Au/OMS-2催化剂采用3种不同的方法制备.前掺杂法:在搅拌条件下,将 0.065mol/L的HAuCl4·4H2O(AR)溶 液加 入 1.73mol/L 的MnSO4(AR)溶液中,缓慢滴加浓 HNO3(AR)至pH2~3,再将 0.37mol/L KMnO4(AR)溶液滴加到上述溶液中,回流、抽滤,并洗涤至无 Cl-(用0.1mol/L AgNO3(AR)检测),120℃干燥12h,300℃焙烧4h,制得Au/OMS-2-QI.浸渍法:在搅拌条件下,缓慢将浓HNO3滴加至1.73mol/L MnSO4溶液,至pH 2~3,随后再将0.37mol/L KMnO4溶液滴加到上述溶液中,回流,抽滤,洗涤至无 Cl-(用0.1mol/L AgNO3检测),120℃干燥12h,400℃焙烧2h,制 得 OMS-2,随 后 将 0.065mol/L 的HAuCl4·4H2O加入到上述 OMS-2固体中,搅拌24h,抽滤,洗涤至无Cl-(用0.1mol/L AgNO3检测), 120℃干燥 12h,300℃焙烧 4h,制得 Au/OMS-2-IM.沉积-沉淀法:将0.065mol/L的HAuCl4·4H2O溶液加入到OMS-2固体中,用KOH(AR)溶液调节 pH 9后搅拌 2h,随后过滤,120℃干燥 12h, 300℃焙烧4h,制得Au/OMS-2-DP.
不同条件下使用沉积-沉淀法制备的Au/OMS-2-DPX:将 计 算 量 浓 度的 HAu Cl4·4H2O溶液(溶液浓度的量为获得1wt%, 3wt%, 5wt%, 7wt%和10wt% Au负载量)加入到OMS-2固体中,加入尿素,并将溶液加热到 70℃(或加入(KOH或NaOH)碱溶液,调节pH9),搅拌2h,过滤,洗涤、120℃干燥 12h,300℃焙烧 4h时,制得Au/OMS-2-DP(X),其中X为不同条件的标识.
1.2 催化剂的表征
BET:用Micromeritics公司的ASAP 2010测试仪在液氮温度下测得.测试前样品先于 200℃, 0.1Pa条件下进行脱气处理.在相对压力 P/P0= 0.05~0.2范围内,设定一个N2分子的横截面积为0.162nm2,用 BET法计算比表面积.X 射线粉末衍射(XRD)测试仪器为 Bruker-axs公司 D8-ADVANCE射线衍射仪,入射光源为 CuKα辐射,入射波长为 0.15405nm,管电压 50kV,管电流30mA,扫描范围2θ=10~80°,扫描速率3.5°/min.
1.3 活性评价
催化剂的评价在常压固定床流动石英管反应器(6mm内径)中进行,催化剂添装量为 100mg (过40~60目筛),反应器内插入热电偶测量内部温度,混合气(北京普莱克斯气体有限公司)组成为1%(体积分数) CO+空气.反应气总流量50mL/min,空速 30,000mL/(g·h),进样气体和出口混合气采用Shimadzu GC-8A气相色谱在线分析,反应原料气O2,N2和CO采用TDX-01柱状分子筛进行分离.分别取反应前和反应后气体进行进样分析,根据CO峰面积百分比计算反应转化率.
2 结果与讨论
2.1 制备方法对Au/OMS-2催化氧化CO活性影响
图1为OMS-2载体及3种不同方法制备的Au负载催化剂Au/OMS-2(Au负载量=3wt%)的XRD 谱图.结果表明,所有样品在 2θ =28.9°, 37.5°,42°和50°处出现具有典型四方晶型结构的OMS-2化合物(JCPDS PDF#29-1020),表明不同方法制备的Au/OMS-2催化剂中Au的负载并未影响OMS-2的晶型结构.进一步分析表明,制备方法明显影响 Au/OMS-2催化剂中 Au在OMS-2载体上的存在状态,浸渍法制备的Au/OMS-2-IM(图1d)的样品,在2θ =38°和44.5°处明显出现对应 Au0(111)和(200)晶面的衍射峰(JCPDS PDF# 04-0784).根据 Au(200)的晶面参数,利用Scherrer′s方程计算出Au/OMS-2-IM中金颗粒平均大小为29.21nm.而沉积-沉淀法制备的 Au/OMS-2-DP和前掺杂法制备的Au/OMS-2-QI,其对应 Au的峰形较弱,表明 Au颗粒较小,高度分散在OMS-2中.不同方法制备Au颗粒大小的差异可能是由于金的熔点(1063℃)较低,而高度分散的纳米Au具有明显的量子效应,熔点可低至 327℃[13].通过浸渍法制备的样品,其Au仅仅负载在载体OMS-2的表面,在焙烧过程中,Au颗粒受热易聚集成大颗粒.而沉积-沉淀法制备的样品,由于Au在溶液中形成Au(OH)nδ-,通过与载体的相互作用沉积在载体上,这个沉积是个慢过程,难以形成大颗粒,而且 Au牢固结合在载体表面,所以在焙烧过程中,载体可以阻止Au颗粒的聚集,从而得到更小的Au颗粒.前掺杂法制备的Au/OMS-2-QI样品上对应Au的XRD峰形也较弱(图1b),表明颗粒较分散,这可能是由于使用前掺杂制备Au/OMS-2过程中,部分Au进入到OMS-2孔道或骨架中,使得Au主要分布在OMS-2中.
另外,从表1的Au/OMS-2样品的BET比表面积数据也可以看出不同制备方法对催化剂的影响,Au/OMS-2-DP(74.61m2/g)和 Au/OMS-2-QI(64.9m2/g)的比表面积大于 Au/OMS-2-IM(50.80m2/g),这可能是由于浸渍法制备的 Au颗粒较大,阻塞了OMS-2的部分孔道,从而使比表面积减少,而沉积-沉淀法和前掺杂法制备的Au/OMS-2-DP和Au/OMS-2-QI样品,Au颗粒较小,未阻塞孔道[14].
由图2可见,本底OMS-2本身对CO催化氧化具有一定的活性,其T100(CO转化率为100%时的温度)约为190℃.对于负载Au催化剂,沉积-沉淀法制备的Au/OMS-2-DP催化氧化CO效果最佳,其 T100为 125℃,前掺杂法制备的Au/OMS-2-QI催化剂活性稍好于载体,其T100为180℃.浸渍法制备的 Au/OMS-2-IM 活性最差,其T100高达220℃,甚至低于载体活性.即它们活性顺序为: Au/OMS-2-DP >> Au/OMS-2-QI>Au/OMS-2-IM.
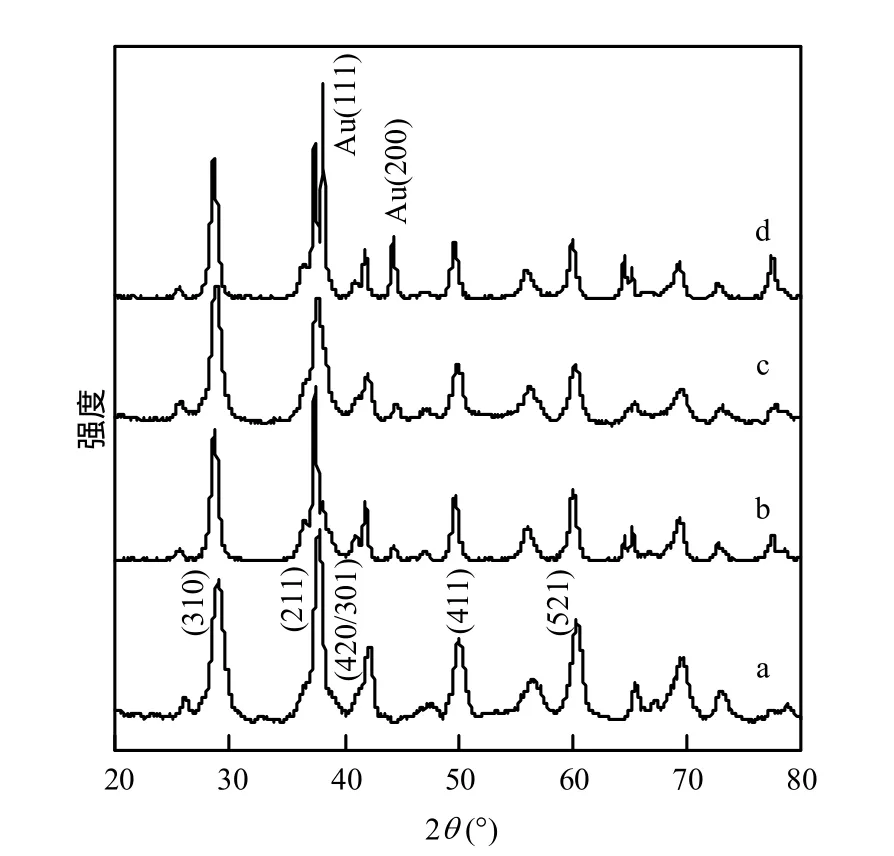
图1 不同方法制备Au/OMS-2的XRD谱图Fig.1 XRD patterns of Au/OMS-2 prepared by different methods
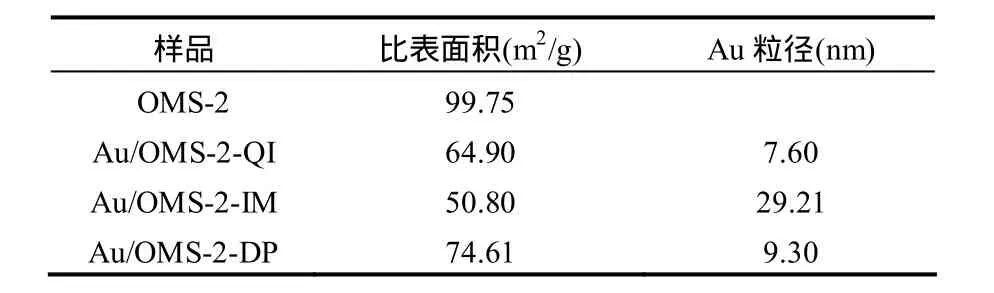
表1 Au/OMS-2催化剂比表面积及Au平均粒径Table 1 BET surface areas and average Au particle sizes of the Au/OMS-2 catalysts
对于以上不同方法制备的Au/OMS-2催化剂催化活性的差别,可能主要来自于 Au颗粒的大小及Au活性位数量.XRD(图1)和BET(表1)结果表明,Au/OMS-2-DP具有最大的比表面积和较小的 Au颗粒大小,而浸渍法制备的Au/OMS-2-IM 比表面积最小,Au颗粒最大. Au/OMS-2-QI的 Au颗粒虽然不大,但其与Au/OMS-2-DP活性相差较大,这可能是由于在前掺杂制备催化剂的过程中,Au进入OMS-2的骨架,部分的Au颗粒包裹在载体之间,难以与CO和 O2接触发生催化作用,而沉积-沉淀法制备的Au颗粒较小而且均匀分布在OMS-2载体表面上,因而 Au/OMS-2-DP的活性高于 Au/OMS-2-QI.
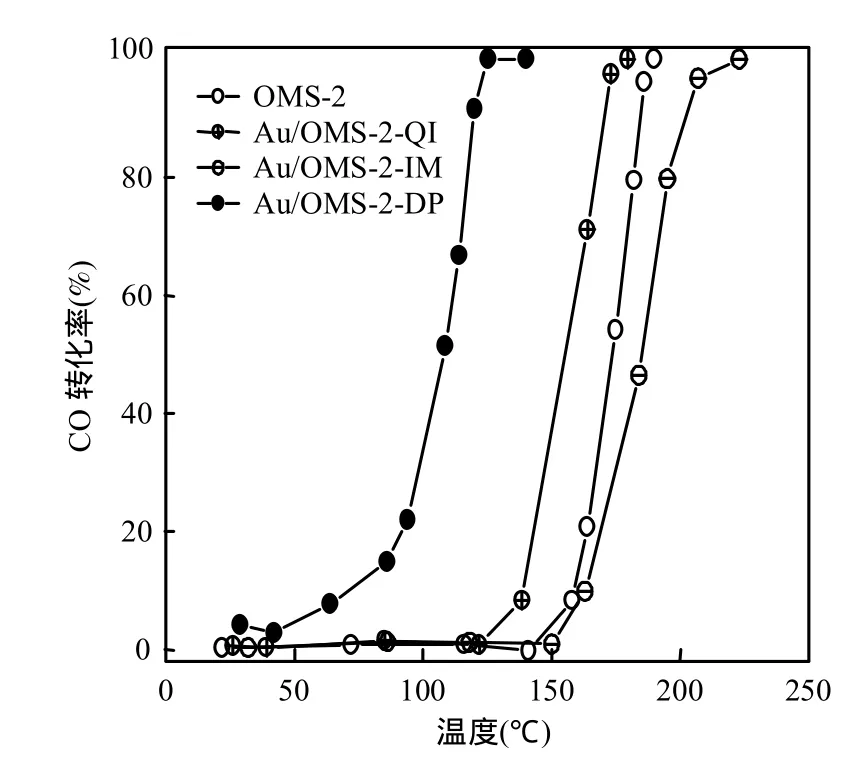
图2 制备方法对催化剂活性的影响Fig.2 Effect of preparation methods on the catalytic activity
2.2 制备条件对Au/OMS-2-DP催化活性的影响
沉积-沉淀法制备的催化剂具有最高的活性,为此以下研究各种制备条件对沉积-沉淀法制备的Au负载样品(Au/OMS-2-DP(X))催化活性的影响.
2.2.1 沉淀剂种类对催化活性的影响 对于沉积-沉淀法,沉淀剂种类对负载 Au催化剂的活性会产生一定的影响.本研究分别以 KOH、NaOH和尿素为沉淀剂制备Au/OMS-2-DPX催化剂,并对其活性进行评价(图3).结果表明,沉淀剂种类对催化活性影响较大.其活性顺序为: Au/OMS-2-DP(KOH)>Au/OMS-2-DP(NaOH)>Au/OMS-2-DP(Urea)即,以KOH为沉淀剂制备的 Au/OMS-2-DP(KOH)催化剂活性最高,而使用尿素为沉淀剂制备的Au/OMS-2-DP(Urea)活性最低.对于强碱沉淀剂来说,KOH为沉淀剂制备的催化剂活性明显优于以NaOH为沉淀剂制备的催化剂活性,这与 Haruta[15]和邹旭华等[16]研究Fe2O3负载Au催化剂上的结果相似.这可能是由于在使用NaOH或KOH为沉淀剂制备催化剂过程中,OMS-2表面上吸附了微量Na+或K+,而Na+通常会钝化Au催化剂的催化活性,微量K+对Au催化剂的催化活性影响不大;另一方面,对于OMS-2来说,K+位于OMS-2分子筛孔道中,当以NaOH为沉淀剂制备催化剂时,在制备过程中难免会有少量的Na+取代OMS-2孔道中的K+,形成间距较短Na—O键,从而引起OMS-2孔道发生错位,而使孔道结构发生稍微畸变,致使OMS-2结构发生微变,影响催化剂活性.
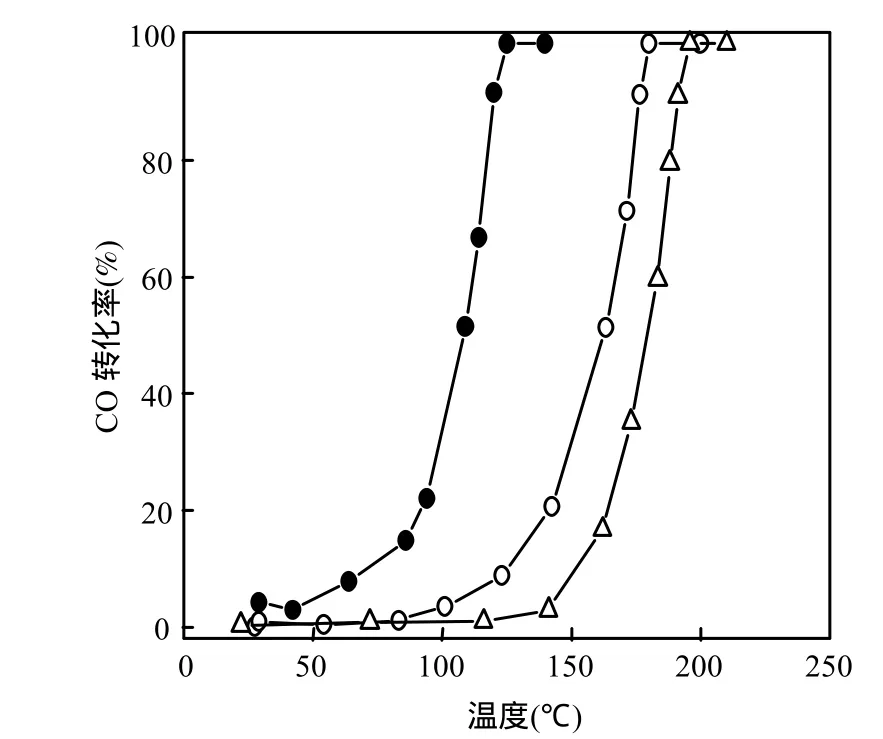
图3 沉淀剂种类对催化剂活性的影响Fig.3 Effect of precipitants on the catalytic activity
实验结果(图3)还表明,以尿素为沉淀剂制备的催化剂活性明显低于NaOH和KOH为沉淀剂制备催化剂.这可能与采用尿素作为沉淀剂时,虽其逐渐水解产生 OH-能使 Au3+均匀沉淀(CO(NH2)2+3H2O=2NH4++CO2↑+2OH-),但在加热分解过程中,pH值逐渐升高[17],当pH值较低时,所有沉积的金以较大胶体形式沉积在正电荷的表面上,随着pH值的增加,金胶体重排成小颗粒,导致金颗粒分布不均匀,而KOH和NaOH作为沉淀剂,pH值一直维持不变,沉积和重排过程同时发生,产生均匀的小颗粒金;另一方面,尿素水解过程产生的NH4+离子半径与OMS-2孔道中的K+相似,容易将孔道中 K+置换出来,经焙烧处理可能得到氢型 H-OMS-2[12],导致晶格发生扭曲变形,影响催化活性.所以在该实验条件下, KOH更适于作制备金催化剂的沉淀剂.
2.2.2 pH值对催化活性的影响 大量研究表明[18],制备溶液的pH值对于纳米Au催化剂的活性较为重要.图4为以KOH为沉淀剂,制备溶液pH值对Au/OMS-2-DP催化氧化CO活性的影响.结果表明,当溶液的 pH值由 2增加到 9时,Au/OMS-2-DP催化活性在增加,当进一步增加pH值时,其催化活性在下降.这可能与HAuCl4在不同 pH值条件下具有不同水解形式,致使负载Au颗粒大小或Au的有效负载量差别.Moreau等[19]研究认为,当 pH2,5,7,9,11时溶液中主要存在的络合Au离子分别是AuCl4-,AuCl2(H2O)OH, [AuCl2(OH)2]-,[AuCl(OH)3]-和[Au(OH)4]-,而OMS-2的零点位(IEP)约为6.2[20],故当pH2时,溶液中的Au以阴离子形式(AuCl4-)存在,催化剂表面上的正电荷与AuCl4-相结合,加速了金颗粒的团聚,因而分布在活性位上的 Au很不均匀,催化活性较低;随 pH值的增加,金沉积的速度逐渐减慢,Au的粒径变小,且分布较均匀,所以活性增加;随 pH值进一步增加,当pH12时, OMS-2表面为负电荷,排斥溶液中的带负电荷的金离子,导致金的沉积量减小,Au颗粒较大,所以活性较低.另一方面,对于OMS-2而言,溶液pH值较低时,溶液中的H+可能会置换出OMS-2孔道中部分K+,产生的裁剪拉力作用于晶格中[21],牵拉 Mn-O键,使得OMS-2晶系由原来的四方型扭曲成单斜型,引起晶格中适合于单斜结构的 Mn3+数目的增加,从而导致催化活性下降[22].从催化反应结果看,反应溶液的最佳pH值为9.
2.2.3 金负载量对催化活性的影响 以 KOH为沉淀剂和反应液的pH值固定为9.0,从图5可以看出,当Au负载量低于5wt%,催化活性随Au负载量的增加而增加,当含Au量大于5wt%负载量时,其催化活性反而降低.
由图6可见,随着Au负载量的增加,对应Au的特征衍射2θ = 38.2°,44.4°,64.5°和77.6°逐渐增强.根据Au(200)的晶面参数,利用Scherrer′s方程 计算出 3wt%,5wt%,7wt%和 10wt%的Au/OMS-2中 Au颗粒平均大小分别为9.30,11.71,15.24,22.87nm.随Au含量增加,Au颗粒大小明显增加,结合以上催化反应结果,可以认为,随Au增加,虽然Au活性中心量在增加,但是由于Au颗粒较大,金微粒容易发生聚集,使得暴露在外的活性中心数减少,从而导致其催化活性降低.
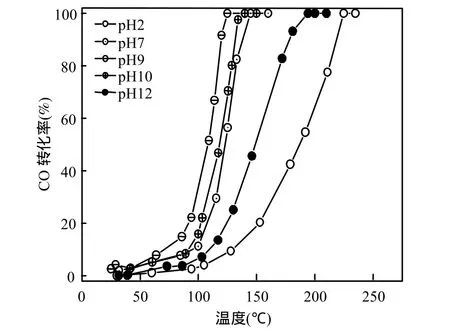
图4 pH值对催化剂活性的影响Fig.4 Effect of pH values on the catalytic activity

图5 金负载量对催化活性的影响Fig.5 Effect of Au loading on the catalytic activity
2.2.4 催化剂焙烧温度对催化活性的影响 焙烧是活化催化剂的重要步骤之一,通常焙烧温度对催化剂的结构和活性有很大影响.为此,将沉积-沉淀法最佳条件制备的Au/OMS-2催化剂样品分别在100, 200, 300, 400, 500℃不同的焙烧条件下处理,并评价其对CO催化氧化活性,结果如图7所示.结果表明,焙烧温度对Au/OMS-2催化活性影响很大,在300℃以下,随焙烧温度升高,催化活性明显提高;当焙烧温度 300℃时,T100为67℃,催化活性达最大;当温度进一步增加,高于300℃时,催化活性逐渐降低.
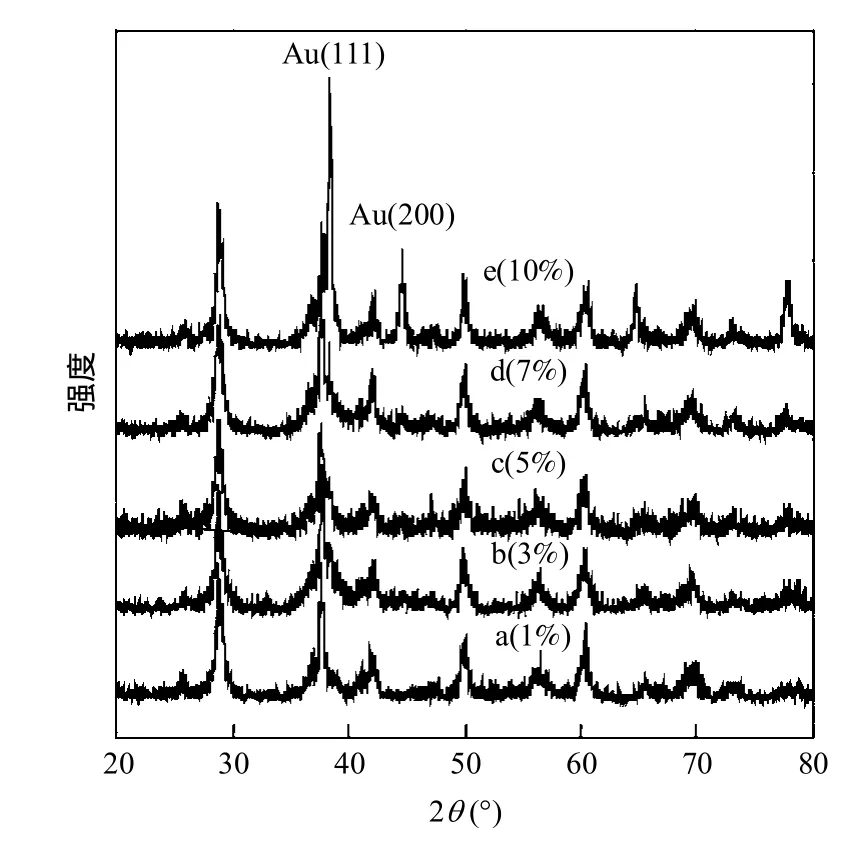
图6 不同金负载量的Au/OMS-2-DP的XRD谱图Fig.6 XRD patterns of Au/OMS-2 with various Au loading
由图8可见,当焙烧温度低于300℃时,其XRD谱图未观察到明显对应Au的衍射峰.当焙烧温度为300℃时,出现了弱的对应Au0的衍射峰,当温度进一步升高(>300℃)时,在2θ=38.2°和44.4°处明显出现了对应Au0(111)和(200)晶面的衍射峰,并且随温度升高,对应 Au0的峰强增加.表明当温度低于300℃时,沉淀物种Au(OH)3较稳定,未分解,当温度高于300℃时,沉淀物种Au(OH)3自还原或分解成金属Au[23-24].其分解方程如下所示:

对于 Au负载样品中 Au颗粒大小,根据Au(200)的晶面参数,利用 Scherrer′s方程计算出400℃和500℃焙烧样品的Au0颗粒大小分别为10.47,19.70nm.这表明,Au的颗粒大小随焙烧温度增加而增大,这可能是由于在焙烧过程中,纳米Au的低熔点导致颗粒粒径增加,300℃焙烧催化剂具有最小颗粒,所以,300℃焙烧的样品显示出最高的催化活性,这可能是由于在 200℃焙烧时沉淀物种没有完全分解成金属 Au物种,而当焙烧温度高于 300℃时,由于纳米 Au的量子效应, Au会聚集成较大的颗粒,从而导致活性下降.

图7 催化剂成型焙烧温度对催化活性的影响Fig.7 Effect of calcination temperatures of catalysts on the catalytic activity

图8 不同焙烧温度下Au/OMS-2的XRD谱图Fig.8 XRD patterns of Au/OMS-2 by calcined at different temperatures
另外,从文献报道来看,目前催化氧化CO催化剂的类型上,主要集中在金属氧化物负载 Au催化剂,Haruta 等[25-26]认为将 Au负载在可还原性的金属氧化物上(如:α-Fe2O3,Co3O4,TiO2和NiO),可以获得了较好的低温催化氧化 CO活性,Hoflund等[27-28]进一步研究了锰氧化物(MnOx)负载Au型催化剂催化氧化CO活性,他们通过改变条件(如;Au和Mn的比例等)制备出的具有最佳活性的Au/MnOx催化剂,其催化氧化CO最佳活性为:55℃时,CO转化率为85%,而本研究最优催化剂在此温度可以获得近90%的CO转化率,而且其所用空速和Au负载(10 wt%)高于本研究,所以本研究锰八面体氧化物分子筛负载Au型催化剂具有较好的催化氧化CO活性.
3 结论
3.1 沉积-沉淀制备的 Au/OMS-2-DP催化剂,比表面积最大,负载的Au颗粒最小,催化氧化CO最高.这可能是由于在沉积沉淀法过程中,溶液中的 Au(OH)nδ-牢固地结合在载体表面,在焙烧过程中,载体可以阻止Au颗粒的聚集,从而得到更小的Au颗粒,获得最优的催化性能.
3.2 对于沉积-沉淀法,沉淀剂的种类明显影响催化活性,以 KOH为沉淀剂制备的催化剂活性较NaOH为沉淀剂制备的活性更高.这可能是因为在催化剂的制备过程中, OMS-2表面上吸附了微量Na+或K+,Na+钝化了Au/OMS-2-DP催化剂的催化活性,另外,少量Na+可能会取代OMS-2分子筛孔道中的 K+,形成间距更短的 Na-O键,从而引起孔道发生错位,微量改变OMS-2结构.
3.3 对于沉积沉淀法,反应液最佳pH值为9.在不同 pH值下金前身化合物的水解程度不同,导致活性中心金颗粒的大小或金的有效负载比(活性中心的数目)不尽相同,从而影响催化剂的活性.当pH值适中时,Au颗粒平均粒径较小且分布较均匀,活性较高.
3.4 对于沉积沉淀法,Au最佳负载量为5wt %.当Au负载量低于5wt%,催化活性随Au负载量的增加而增加,当含 Au量大于 5wt%负载量时,其催化活性反而降低.这可能是由于催化剂活性与表面金微粒活性中心数有关,随着金负载量的提高,活性中心数逐渐增多,催化剂活性提高;金负载量过高时,金微粒容易发生聚集,使得活性中心数减少,催化活性降低.
3.5 对于沉积沉淀,最佳的焙烧温度为300℃.低于此温度,沉淀产生的Au(OH)3没有完全分解,高于此温度,分解后的 Au颗粒随着焙烧温度的升高,颗粒增大,导致活性下降.
[1] Gardner S D, Hoflund G B, Schryer D R, et al. Catalytic behavior of noble metal/ reducible oxide materials for low-temperature carbon monoxide oxidation.1. Comparison of catalyst performance [J]. Langmuir, 1991,7(10):2135-2139.
[2] 李巧霞,周小金,李金光,等.Pt-Ru合金薄膜的电沉积制备及其电化学表面增强红外吸收光谱 [J]. 物理化学学报, 2010, 26(6):1488-1492.
[3] 刘英骏,张继军,李 能,等.CO2对 Cu-Ce-O催化剂催化氧化CO活性的影响 [J]. 物理化学学报, 1999,15(2):97-100.
[4] Haruta M, Kobayashi T, Sano H, et al. Novel gold catalysts for the oxidation of carbon monoxide at a temperature far below 0oC [J]. Chem. Lett., 1987,16(2):405-408.
[5] Zhang X, Shi H, Xu B Q. Comparative study of Au/ZrO2catalysts in CO oxidation and 1,3-butadiene hydrogenation [J]. Catal. Today, 2007,122(3/4):330-337.
[6] Haruta M, Yamada N, Kobayashi T S, et al. Gold catalysts prepared by coprecipitation for low-temperature oxidation of hydrogen and carbon monoxide [J]. J. Catal., 1989,115(2):301-309.
[7] 邵建军,张 平,宋 巍,等.预处理条件对Au/ZnO催化剂CO氧化性能的影响 [J]. 化学学报, 2007,65(18):2007-2013.
[8] Haruta M. Catalysis of gold nanoparticles deposited on metal oxides [J]. CATTECH, 2002,6(3):102-115.
[9] Haruta M, Tsubota S, Kobayashi T, et al. Low-temperature oxidation of CO over gold supported on TiO2, α-Fe2O3, and Co3O4[J]. J. Catal., 1993,144(1):175-192.
[10] Suib S L. Sorption, catalysis, separation design [J]. Chem. Innov., 2000,30(3):27-33.
[11] Krishnan V V, Suib S L. Oxidative Dehydrogenation of 1-Butene over Manganese Oxide Octahedral Molecular Sieves [J]. J. Catal., 1999,184(2):305-315.
[12] Makwana V D, Garces L J, Liu J, et al. Selective oxidation of alcohols using octahedral molecular sieves: influence of synthesis method and property-activity relations [J]. Catal. Today, 2003, 85(2-4):225-233.
[13] Buffat P, Borel J P. Size effect on the melting temperature of gold particles [J]. Phys. Rev. A, 1976,13(6):2287-2298.
[14] Ivanova S, Petit C, Pitchon V. A new preparation method for the formation of gold nanoparticles on an oxide support [J]. Appl. Catal. A, 2004,267(1/2):191-201.
[15] Haruta M. Size and support-dependency in the catalysis of gold [J]. Catal. Today, 1997,36(1):153-166.
[16] 邹旭华,齐世学,贺红军,等.不同方法制备的 Au/Fe2O3催化剂对CO的催化氧化 [J]. 烟台大学学报(自然科学与工程版), 2000, 13(3):171-175.
[17] Radnik J, Wilde L, Schneider M, et al. Influence of the precipitation agent in the deposition-precipitation on the formation and properties of Au nanoparticles supported on Al2O3[J]. J. Phys. Chem. B, 2006,110(47):23688-23693.
[18] 王东辉,程代云,郝郑平,等.纳米金催化剂及其应用 [M]. 北京:国防工业出版社, 2006.
[19] Moreau F, Bond G C, Taylor A O. Gold on titania catalysts for the oxidation of carbon monoxide:control of pH during preparation with various gold contents [J]. J. Catal., 2005,231(1): 105-114.
[20] Kosmulski M. pH-dependent surface charging and points of zero charge II. Update [J]. J. Colloid Interface Sci., 2004,275(1):214-224.
[21] Liu J, Makwana V, Cai J, et al. Effects of alkali metal and ammonium cation templates on nanofibrous cryptomelane-type manganese oxide octahedral molecular sieves (OMS-2) [J]. J. Phys. Chem. B, 2003,107(35):9185-9194.
[22] Jothiramalingam R, Wang M K. Synthesis,characterization and photocatalytic activity of porous manganese oxide doped titania for toluene decomposition [J]. J. Hazar Mater., 2007,147(1/2): 562-569.
[23] Okumura M, Tanaka K, Ueda A, et al. The reactivities of dimethylgold (III) β-diketone on the surface of TiO2:A novel preparation method for Au catalysts [J].Solid State Ion., 1997, 95(1/2):143-149.
[24] Yuan Y Z, Asakura K, Wan H L, et al. Preparation of supported gold catalysts from gold complexes and their catalytic activities for CO oxidation [J]. Catal. Lett., 1996,42(1/2):15-20.
[25] Haruta M, Tsubota S, Kobayashi T, et al.Gold catalysts prepared by coprecipitation for low-temperature oxidation of hydrogen and of carbon momoxide [J]. J. Catal., 1989,115:301-309.
[26] Haruta M, Tsubota S, Kobayashi T, et al.Low-temperature oxidation of CO over gold supported on TiO2,α-Fe2O3and Co3O4[J]. J. Catal., 1993,144:175-192.
[27] Gardner S D, Hoflund G B,Schryer D R, et al. Catalytic behavior of noble metal reducible oxide materials for low-temperature carbon monoxide oxidation. 1. Comparison of catalyst performance [J]. Langmuir, 1991,7:2135-2139.
[28] Hoflund C B, Gardner S D, Schryer D R, et al. Au/MnOx catalytic performance characteristics for low-temperature carbon monoxide oxidation [J]. Appl. Catal. B Environ., 1995,6:117-126.
Low-temperature CO oxidation over Au-doped OMS-2 catalysts: preparation and catalytic activity.
YE Qing*, YAN Li-na, LUO Cai-wu, HUO Fei-fei, CHENG Shui-yuan, KANG Tian-fang (Department of Environmental Science, College of Environmental and Energy Engineering, Beijing University of Technology, Beijing 100124, China). China Environmental Science, 2012,32(4):609~616
Au/OMS-2 catalysts were prepared by pre-incorporation (QI), typical wet impregnation (IM) and deposition-precipitation (DP) methods. The influences of prepared methods and conditions on the catalytic activity of CO oxidation were studied. The samples were characterized by X-ray diffraction (XRD) and Brunaner-Emmett-Teller (BET). As compared with pre-incorporation and typical wet impregnation methods, Au/OMS-2-DP prepared from deposition-precipitation (DP) method revealed the highest activity, due to the largest surface area and the smallest Au particle size. A study was conducted on the effects of different preparation conditions (i.e., precipitating agents, pH of solution, Au loading and calcinations temperature) on the catalytic oxidation of CO over Au/OMS-2-DP. Effects of precipitating agents on catalytic activity were obvious. The best catalytic activity was shown by the Au/OMS-2-DP catalyst prepared with KOH as a precipitating agent, which could be explained in terms of the smallest Au particle size. A pH of 9 generated greater amounts of Au loading and smaller Au particles on OMS-2 than other pH value. The sample calcined at 300℃ showed the highest activity, which may be due to the sample’s calcined at 200℃ inability to decompose completely to metallic gold while the sample calcined at 400℃ had larger particles of gold deposited on the support. Au/OMS-2-DP prepared from a gold solution with KOH as a precipitating agent, pH of 9, Au loading at 5 wt%, and a calcination temperature of 300℃ provides the optimum catalytic activity for CO oxidation, i.e. 100% CO conversion at 67℃.
Au/OMS-2;low temperature catalytic oxidation;preparation methods;preparation condition
2011-07-01
国家自然科学基金项目(20777005);北京市自然科学基金资助项目(8082008)
* 责任作者, 副教授, yeqing@bjut.edu.cn
X701
A
1000-6923(2012)04-0609-08
致谢:本研究在催化剂的表征过程中,得到了北京工业大学固体微结构与性能研究所的帮助,在此表示感谢.
叶 青(1969-),女,江西萍乡市人,副教授,博士,主要从事环境催化化学研究.发表论文60余篇.

