电膜过程中膜面水解离的数学模型
刘玉玲,陆 君,马晓云,李 艳,王宇新
(1.江苏科技大学生物与化学工程学院,江苏镇江212003)(2.天津大学 化工学院,天津300072)
几乎所有的电膜过程中(如电渗析ED,电去离子EDI和电解电渗析EED等)都存在膜面水解离,水解离对电膜过程的性能有着重要的影响.当离子交换膜存在于电解质溶液中时,膜中的离子交换活性基团便会发生解离,解离的离子(反离子)可在膜内和溶液中自由移动.离子交换膜对反离子的选择渗透系数要远高于同离子,因此当电流通过膜的时候,反离子在膜内承担了几乎所有的电流传递.膜外溶液反离子的浓度远低于膜中反离子的浓度,因此膜内反离子的传递通量大于膜外溶液中反离子传递通量.这使得离子膜的两侧表面迅速建立起浓差极化,膜的一侧形成离子富集区,另一侧形成离子耗竭区(见图1,其中cm为离子交换膜的交换容量,cb为本体溶液浓度,δ为浓差极化边界层的厚度).浓差极化的程度由电流密度和对流传递通量控制,当电流密度逐渐增大,耗竭区的反离子浓度降低到一定程度时,剧烈的浓差极化使得膜面的耗竭区反离子浓度足够的低,膜面发生水解离,水解离的产物H+和OH-充当了电流的载体,一部分的电流由水解离产物H+和OH-运载.
1956年文献[1-2]首次发现阴阳离子交换膜表面的水解离现象.自由溶液中水解离的反应式为:


图1 浓差极化和水解离示意图Fig.1 Schematial view of concentration polarization and water dissociation at the membrane′s surface.
水解离产生的离子传递的电流最大值为Fk1cH2Oδ,其中k1为自由溶液中水解离的速率常数,cH2O为膜表面的水分子浓度,δ为水解离层的厚度.长期以来学者认为水解离发生在膜表面大约1~10 nm的区域内[3].假设自由溶液中水分子的浓度约为10 000 mol·m-3,k1为2 ×10-5s-1,由此计算出水解离产生的离子传递电流约为2×10-4A·m-2.但在电膜过程中,实际测得阴离子交换膜表面水解离产生的离子传递的电流约为50 A·m-2,大约为自由溶液中的250 000倍[3].这意味着在电膜过程中,必定有促进水解离的效应存在.
对于促进水解离效应的一个可能的解释是第二 Wien 效应 (the second wien effect,SWE),Wien发现处于高电场强度下的弱电解质有更高的解离度.文献[4]对这种效应进行了详细地讨论.电膜表面耗竭区内的电场强度极高,大约108~109V/m,Onsager认为此高电场对水解离的正方向速率常数k1有加强作用,而对逆方向速率常数k-1没有影响.此促进水解离机理对于阴膜和阳膜同样适用,即在同一条件下,电场对于阴膜和阳膜表面的水解离有着相同的加速作用.该理论比较简洁直观,也曾得到实验证实.其局限性在于Onsager理论只适用于E=107~108V/m场强的情况,不适用于更高场强情况.而且第二Wien效应关于电场加速正反应速率的模型,缺乏物理机制上的解释.
文献[5-6]从不可逆热力学的角度对水解离反应中物质电化学势的变化进行了研究,得出了一个基于不可逆热力学的水解离反应的催化模型.在离子交换膜的耗竭面,水解离反应层中的水分子解离成H+和OH-,这两种离子在电场力的作用下,分别迁移进入不同的相.文中将在此不可逆热力学水解离催化模型的基础上,建立用于电去离子和电渗析过程的膜面水解离催化过程数学模型[7].
1 膜面水解离的数学模型
1.1 电场对膜面水解离反应的增强作用
取阴离子交换膜为例,膜面水解离反应式为

根据化学反应热力学,使得反应向正方向进行的必要条件是




式(3)中(μH2O)σ为反应层中水分子的电化学势.
把式(5)和(6)代入式(3)可得

式中:Δφσ为反应层两侧边界上的电势降,即反应产物H+和OH-之间的电势降为

由此可见,反应层内的电场对水解离反应的推动力的影响,表现在反应前后反应物和产物的电化学势的变化对反应推动力的影响上,即水解离反应层两侧的电势差降低了反应Gibbs自由能,从而加速了水解离反应.
在阴膜表面,水解离产生的H+在电场下进入溶液相,OH-则进入膜相(图1).反应产物分别处于不同的相,反应产物的电势相对于反应物的电势发生了变化.以阴膜的耗竭表面为例,图2,3分别为在存在外电场和不存在外电场的条件下,阴离子交换膜表面附近的盐离子浓度和电势分布.
当不存在外电场时,离子交换膜内部的离子浓度和其周围溶液中本体的离子浓度达到Donnan平衡(图2).在离子交换膜表面形成一个连续的Donnan电势分布,分布的跨度为从膜内部1/κ到膜外部溶液1/κ处,约为2/κ宽的区域(κ为德拜休克尔系数).水解离反应在此Donnan电势区域中发生,将此区域的厚度表示为σ.
当存在外电场时,膜和溶液相中出现离子传递的电流,离子交换膜表面形成的浓差极化(浓差极化边界层的厚度为δ,且δ≫σ)和膜界面区域内的体电荷使得膜表面的Donnan电势分布偏离不存在外电场时的电势分布[6].具体表现为外加电场越大(即盐离子传递的电流密度越大),界面上Donnan 电势的梯度越大[8].

图2 阴离子交换膜表面附近的盐离子浓度的分布Fig.2 Concentration distribution of salt ion at the surface of the anion exchange membrane

图3 阴离子交换膜表面电势的分布Fig.3 Potential distribution at the surface of anion exchange membrane
当不存在外电场的时候(图2,3中曲线iw=0),由于离子交换膜的选择透过性,反应层两侧会出现 Donnan平衡电位,即,此时,Donnan平衡电势使得膜表面反应层内的水解离反应的推动力(iw)大于自由溶液中的推动力[6].因此,相对于自由溶液中的水解离反应,即使盐离子传递的电流密度为0时(图2,3中曲线iw=0),膜界面上水解离反应也会被Donnan平衡电势形成的电场加速.当有外电场存在时(图2,3中曲线iw>0),离子交换膜内有电流通过,离子交换膜表面形成一个高梯度的电势分布(梯度高于Donnan电势分布),这使得水解离反应的推动力(iw)增加,从而加速了水解离反应.
自由溶液中水解离反应的速率为


式中:if和ib分别为水解离反应的正方向和反方向的水解离电流.
图4为水解离反应电化学自由能和反应状态的关系[5-6]。实线表示反应层两边电势差为0时(即不存在电场,iw=0)时,反应物和产物的能态;虚线表示在反应层两边存在电势差(iw>0)的情况下产物的能态[5-6].其中为自由溶液中正反应方向的活化能为逆反应方向的活化能.(H+)s+为 Δφσ=0 时 H+和 OH-的能级状态为 Δφσ> 0 时 H+和OH-的能级状态.从图中可见,当反应层两侧存在电势差的时候,反应产物的能级降低了,这使得正方向的活化能降低了 ξFΔφσ,逆反应方向的活化能提高了(1-ξ)FΔφσ.决定正逆方向活化能改变大小的分配参数为电化学传递系数ξ,它由能垒的形状决定.阴离子膜表面水解离反应层两侧的电势差使得正方向反应的活化能降低,正方向反应速率为[5-6]

负方向水解离反应的活化能被提高,故负方向反应的速率减慢,负方向反应速率为

对于整个水解离反应,总体趋势为正方向反应被加速,负方向反应被减慢,电场加速下的水解离的电流密度为式中:反应层两侧的电势差 Δφσ等于Donnan电势,即

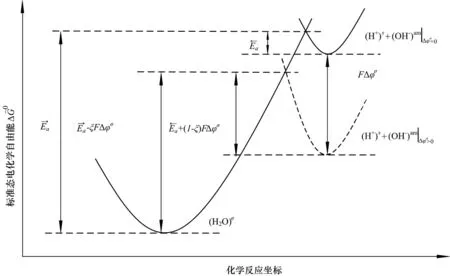
图4 水解离反应电化学自由能和反应状态的关系[5-6]Fig.4 Schematic diagram of the standard state electrochemical free enthalpyΔ~G0vs the reaction co-ordinateof the water dissociation reaction in the reaction layer[5-6]

式中:γi和γami分别为i离子(膜中的反离子)在溶液相和阴膜相中的活度系数.假设活度系数都为1,式(15)可以写为

把式(16)代入式(13,14)得阴膜界面水解离电流密度为
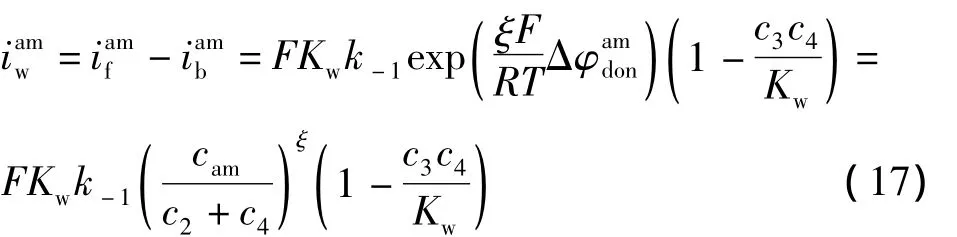
同理,阳膜界面水解离密度为

式中:Kw为自由水溶液的离子积常数.
以上提出的电场对水解离加速作用对阴膜和阳膜同样适用,但在实验中[3],同样浓差极化程度下阴膜表面的水解离度要远远高于阳膜表面.因此可以认为除电场对水解离的加速作用以外,还有另外一种催化作用.
1.2 催化基团对膜面水解离反应的增强作用
季铵型强碱性阴离子交换膜和阴树脂被广泛应用于电膜过程.阴离子膜和阴树脂上的季铵基团会在一定条件下发生降解,降解产生的叔胺基团对水解离有催化作用.文献[3]提出了一个质子化/去质子化的反应机理,此机理又被称为化学反应模型(CHT).以B表示弱碱基团,水解离反应由一步反应变为如下弱碱基团的质子化和去质子化的两步反应[9]:

在上述反应式中,弱碱基团B在反应前后没有发生结构的变化,第一步是可逆的弱碱基团质子化的反应,弱碱基团和反应层中的水分子结合生成质子化的弱碱基团和OH-;第二步反应是可逆的去质子化过程,质子化的弱碱基团和水分子反应,使得质子化的弱碱基团去质子化成弱碱基团和H+,其中第二步为控制步骤.当B为叔胺基团时,式(19)和(20)可写为

在电场下,质子化和去质子化过程分别产生的OH-和H+在电场下发生电迁移并形成电流,即水解离电流.由此可看出,在季铵型阴离子交换膜或树脂表面,电场对水解离反应的催化作用表现为对第二步去质子化反应的加速.Simons[3]发现,在107~108V/m的强电场作用下,质子化反应的正反应速率常数k2比该反应在自由溶液中进行时增大了1 000倍以上.
第1步的质子化反应相对较快,可以作为平衡反应来处理,其反应平衡常数为[9]

因为第2步去质子化反应是速度控制步骤,根据第2步反应可推导出无电场催化作用下的水解离电流密度,即

在加入电场催化因素后,第2步去质子化反应的正方向被加速,负方向被减缓,正负反应的水解离电流密度为

由式(25)和(26)可得阴膜界面上两种催化作用下的水解离电流密度

根据文献[3],质子化和去质子化过程的正逆反应常数存在如下关系

式中:pKb=-logKb.把式(23,28,29)代入式(27),得阴离子交换膜表面水解离电流密度此时可认为阴膜上催化基团的浓度等于离子的交换容量,即

1.3 电膜过程中的膜面水解离模型
在电渗析(ED)过程中,阳膜上的膜面水解离仅仅由电场加速,其模型可用式(18)表示.在阴膜上膜面水解离由电场和催化基团同时加速,其模型可用式(30)表示.
在电去离子(EDI)过程中,虽然阳膜上不存在能催化水解离的基团,但是若和阳膜接触的是阴树脂,除了电场的催化,阴树脂上催化基团同样能催化阳膜界面上水解离.因此对于不同树脂填充方式的床层,其阳膜上水解离的机理有一定的差别.
CRbed为仅仅填充阳离子交换树脂的淡室床层.在CRbed中,和阳膜接触的只是阳树脂,因此此时的水解离仅仅被电场催化.阳膜上水解离电流可由式(18)得到,即

ARbed为仅仅填充阴离子交换树脂的淡室床层.在ARbed中,和阳膜接触的是阴树脂,阳膜上的水解离将会被和其接触的阴树脂上的催化基团催化.因此,阳膜上水解离将同时被两种方式催化.但是只有阴树脂和阳膜接触的区域的水解离才能被阴树脂的催化基团催化.这里为了简化模型,对阳膜和树脂的接触面上催化基团的浓度进行平均化处理.即认为和阳膜接触的阴树脂上催化基团是均匀分布在阳膜表面.对于粒径为0.5mm的不同柔软度的离子交换树脂颗粒,树脂和壁面接触面积占壁面面积的0.15~0.21.本模型中,接触面积占阳膜总面积的比取平均值即0.18.因此催化基团的平均浓度表达式为

式中:cAR为阴树脂的交换容量.因此,和ARbed接触的阳膜的水解离电流密度为
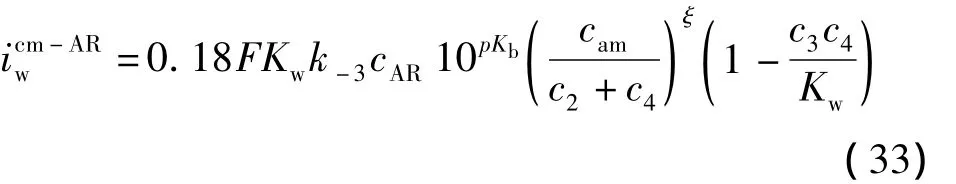
Mixbed为填充有混合阴阳离子交换树脂的淡室床层.在Mixbed中,和阳膜接触的是混合树脂,且阴阳树脂比例是1∶1,因此可得到催化基团的平均浓度为

由此,Mixbed—阳膜界面上的水解离电流密度为

2 结论
由以上数学分析所推导出的膜面水解离数学模型,包括膜面电场和膜面催化基团对水解离反应的加速作用,可以较准确地描述电渗析和电去离子过程中的膜面水解离过程,适用于所有电膜过程的膜面水解离反应.
电场对膜面水解离速率的加速机理为电场改变了水解离反应正反向活化能,使得正方向水解离反应被加速,负方向水解离反应减缓.对于阴离子交换膜,除了电场对水解离反应的加速作用以外,阴离子交换膜上的催化基团对膜面水解离反应有一定的增强作用.故对于阳离子交换膜,其膜面水解离反应仅仅由膜面电场加速;对于阴离子交换膜,其膜面水解离反应由膜面电场和水解离催化基团同时加速.
References)
[1]Frilette.Preparation and characterization of bilayered ionexchange membranes[J].Journal of Physical Chemistry,1956,60:435-441.
[2]Tye,Kressman T R E.The effect of current density on the transport of ions through ion-selective membranes[J].Discussions of the Faraday Society,1956,21:185-192.
[3]Simons R.Strong electric field effects on proton transfer between membrane bound amines and water[J].Nature,1979,280:824-826.
[4]Onsager L.Deviations from Ohm′s Law in weak electrolytes[J].Journal of Chemical Physics,1934(2):599-615.
[5]Hurwitz H D,Dibiani R.Investigation of electrical properties of bipolar membranes at steady state and with transient methods[J].Electrochimica Acta,2001,47(3):759-773.
[6]Hurwitz H D,Dibiani R.Experimental and theoretical investigations of steady and transient states in systems of ion exchange bipolar membranes [J].Journal of Membrane Science,2004,228(1):17-43.
[7]Lu J,Wang Y X,Zhu J.Numerical simulation of the electrodeionization(EDI)process accounting for water dissociation[J].Electrochimica Acta,2010,55(8):2673-2686.
[8]Zabolotskii V I,Nikonenko V V,Korzhenko N M,et al.Mass transfer of salt ions in an electromembrane system with violated electroneutrality in the diffusion layer:the effect of a heterolytic dissociation of water[J].Russian Journal of Electrochemistry,2002,38(8):810-818.
[9]Danielsson C O,Dahlkild A,Velin A,et al.Nitrate removal by continuous electropermutation using ion-exchange textile I modeling[J].Journal of the Electrochemical Society,2006,153(4):51-61.

