舒尼替尼治疗晚期肾癌临床疗效的初步评价
李延帅赵立王亚林李建涛曲楠黄晨麦海星李学超陈立军
1.解放军总医院,北京 100853;
2.军事医学科学院附属医院泌尿外科,北京 100071
舒尼替尼治疗晚期肾癌临床疗效的初步评价
李延帅1,2赵立2王亚林2李建涛2曲楠2黄晨2麦海星2李学超2陈立军2
1.解放军总医院,北京 100853;
2.军事医学科学院附属医院泌尿外科,北京 100071
背景与目的:舒尼替尼治疗肾癌已取得显著疗效,本研究旨在初步探讨舒尼替尼治疗晚期肾癌的有效性及安全性。方法:晚期肾癌患者36例,其中单发转移16例,其余为全身多发转移病灶,均经穿刺病理证实为肾癌。采用标准4/2治疗方案:舒尼替尼50 mg,每天1次。口服,服药4周停药2周为1个周期,持续至患者疾病进展或出现不可耐受的不良反应,至少2个周期进行1次疗效评价。结果:随访截止至2012年7月,可评价疗效病例29例,疾病进展(progressive disease,PD)5例、部分缓解(partial response,PR)6例、完全缓解(complete response,CR)1例,疾病稳定(stable disease,SD)17例,疾病控制率(DCR=CR+PR+SD)为82.8%(24/29),客观反应率(ORR=CR+PR)为24.1%(7/29),因疾病进展死亡5例(17.2%),中位无进展生存期(progression-free survival,PFS)与总生存期(overall survival,OS)尚未达到。常见不良反应主要有乏力21例(58.3%)、皮肤黄染17例(47.2%)、手足皮肤反应18例(50%)、高血压16例(44.4%)、甲状腺功能减退8例(22.2%)、腹泻10例(27.8%)、贫血9例(25%)、中性粒细胞减少9例(25%)、血小板减少7例(19.4%),3、4级不良反应有手足皮肤反应2例(6%),高血压1例(3%),中性粒细胞减少3例(8%),血小板减少2例(6%)。多数为轻度不良反应,经对症治疗后均可缓解。结论:舒尼替尼治疗晚期肾癌有效,严重不良反应较少,耐受性及安全性良好。
肾癌;转移癌;舒尼替尼;不良反应
舒尼替尼能明显改善肾癌患者预后,2010年美国国家癌症综合网(National Comprehensive Cancer Network,NCCN)肾癌治疗指南中将其推荐为晚期肾细胞癌的一线治疗药物,为了进一步总结舒尼替尼治疗晚期肾癌的临床经验,本研究回顾性分析了2009年6月—2012年7月军事医学科学院附属医院泌尿外科应用舒尼替尼治疗晚期肾癌患者的临床资料,总结该药的有效性及安全性。
1 资料和方法
1.1 一般资料
本组患者36例。男性31例、女性5例,平均年龄58岁。其中单发转移16例,其余均为多发转移,所有患者均经病理证实,病理类型分透明细胞癌(clear renal cell carcinoma,CRCC)、乳头细胞癌(papillary renal cell carcinoma,PRCC)、混合细胞癌(hybrid renal cell carcinoma,HRCC),各类型转移情况见表1。ECOG行为状态评分为0~1分。
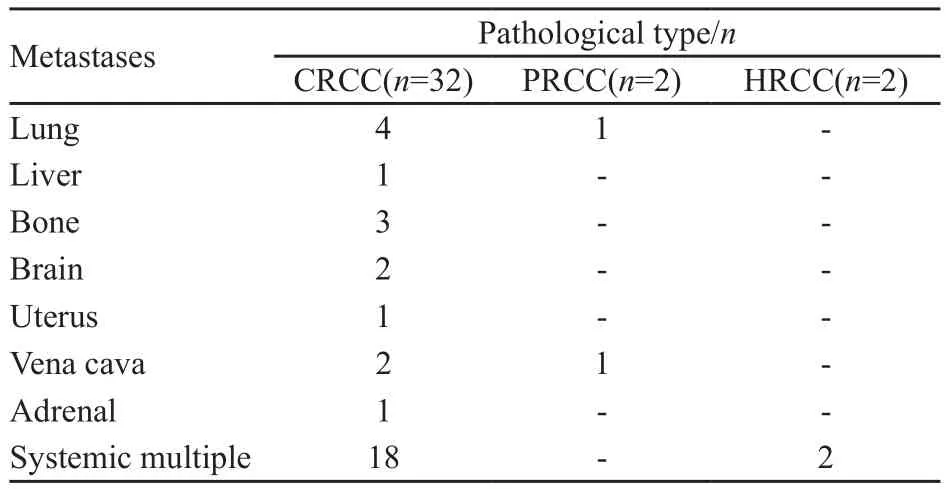
表 1 转移病灶及病理类型相关情况Tab. 1 Metastases and pathological type
1.2 服药方法
标准4/2治疗方案:舒尼替尼50 mg每天1次口服,服药4周停药2周为1个周期。如出现3、4级不良反应酌情减量或停药。手术患者于术后2周开始服药。按以上方案给药至肿瘤进展或出现难以控制的严重不良反应。
1.3 评价标准
采用实体肿瘤疗效评价标准(Response Evaluation Criteria in Solid Tumors,RECIST)评估疗效。完全缓解(complete response,CR):所有靶病灶消失,无新病灶出现,且肿瘤标志物指标正常,至少维持4周。部分缓解(partial response,PR):靶病灶最大径之和减少≥30%,至少维持4周。疾病进展(progressive disease,PD):靶病灶最大径之和至少增加≥20%,或出现新病灶。疾病稳定(stable disease,SD):靶病灶最大径之和缩小未PR,或增大未达到PD。如仅一个靶病灶的最长径增大≥20%,而记录到的所有靶病灶的最长径之和增大未达20%,则不评价为“PD”。
总生存期(overall survival,OS)从随机化开始至因任何原因引起死亡的时间。无病生存期(disease-free survival,DFS)或者无疾病生存时间是从随机入组开始到第1次复发或死亡的时间。无进展生存期(progression-free survival,PFS)是从入组开始到肿瘤进展或死亡的时间。疾病控制率(disease control rate,DCR)为CR+PR+SD。客观缓解率(objective response rate,ORR)指肿瘤缩小达到一定量并且保持一定时间的患者的比例,包括CR+PR的病例。不良反应按照国际不良反应标准(National Cancer Institute Common Terminology Criteria for Adverse Events, version 3.0,NCI-CTC 3.0)进行分级。
1.4 不良反应观察指标及方案
观察指标包括患者生命体征、体力状态评分、不良反应等级、院外对症治疗方案等。
本组患者在服药第1个周期均住院观察,定期复查血常规、肝肾功及甲状腺功能,在出现异常的早期即给予对症处理。根据患者第1周期治疗情况,决定第2周期是否住院观察,如患者无严重不良反应或通过药物可以控制,可院外服药并定期复查相关生化指标及不良反应等;对于第1个周期出现3、4级不良反应者,或经药物控制才可以结束第1周期者,建议继续留院观察,直至缓解;院外服药患者每服药满2个周期后返院复查评估,以服药前2周内靶病灶的CT或MRI等影像结果为基线,每个周期CT或MRI复查1次,间隔2个周期对比影像学检查进行疗效评估。每周至少复查血常规1次,出现骨髓抑制者应缩短复查时间;如院外出现严重不良反应要立刻返院治疗。
2 结 果
2.1 疗效评价
患者随访3~28个月。36例患者实际可评价疗效29例,5例因疾病进展死亡或出组。目前仍在服药的患者中PD 5例、PR 6例、CR 1例,SD 17例,ORR为24.1%(7/29),DCR为82.8(24/29),因疾病进展死亡5例(17.2%),尚不能评价本组患者的PFS与OS。
2.2 不良反应
本组患者在服用舒尼替尼后常见不良反应主要有乏力、皮肤黄染、手足皮肤反应及高血压等。3、4级不良反应有手足皮肤反应、高血压、中性粒细胞减少及血小板减少(表2)。
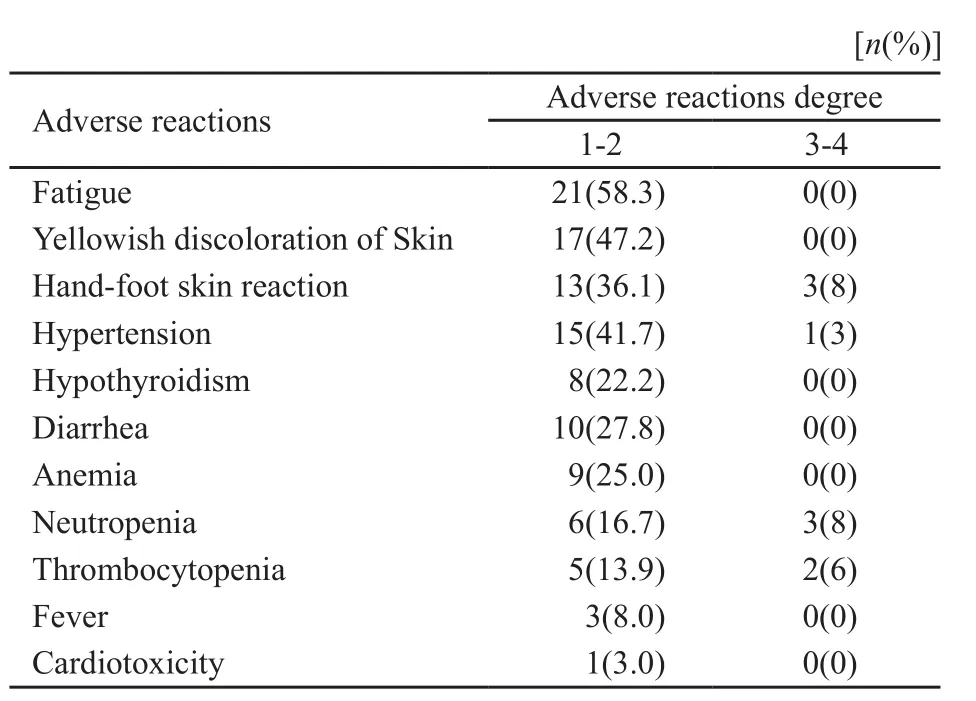
表 2 患者服药后不良反应情况Tab. 2 The adverse reactions of all patients after taking the degree
3 讨 论
随着靶向药物时代的到来,相继出现多种靶向药物如索拉非尼、舒尼替尼、替西罗莫司(temsirolimus)、贝伐珠单抗、依维莫司、帕唑帕尼(pazopanib)及阿西替尼(axitinib)等被批准用于晚期肾癌的治疗。值得提出的是,在二线治疗细胞因子治疗失败的转移性肾癌的Ⅱ期临床试验中,DCR达到40%[1],OS最长达到23.9个月[2],明显优于既往的其他二线治疗药物,并且在Ⅲ期对比试验中OS超过2年[3]。随后大量的文献数据也显示舒尼替尼对肾癌靶向治疗效果良好[4-5]。国内有关数据显示,ORR为26.5%~53%,DCR为87%~97%[6-7]。本研究ORR为24.1%,DCR为82.8%,与报道数据相比稍有差距,其原因可能有多种因素:部分病理类型为非透明细胞癌,瘤体较大,Furman分级多为 3、4级,MSKCC风险分级多为中-高危,样本例数少等。
乏力为服药后常见的不良反应,多为1、2级,发生率为37%~54% ,而3、4级不良反应为8%~11%[8-9],本研究为58.3%,较国外报道数据稍高,可能与国人体质有关。5例患者伴有中度贫血,给予纠正贫血后精神状态好转;2例食欲差者建议少食多餐,给予高热量、高蛋白、高维生素、易消化的软食,均能保持较好的体力;1例患者晚间睡眠障碍,限制白天睡眠并建议做些康复、推拿、按摩等非药物干预治疗后,晚间睡眠时间延长,乏力明显缓解。
本组皮肤黄染主要表现为皮肤及巩膜黄染,多在服药2周后出现,停药后会逐渐缓解,均未影响服药。出现严重手足皮肤反应3例(10.3%),均伴有明显疼痛,给予对症治疗可缓解,不影响治疗,随着服药周期结束症状可逐渐缓解。有研究报道,高血压发生率30%~50%,严重不良反应发生率为5%~10%[10]。在本研究中,出现高血压者16例,未出现难以控制的高血压。本组腹泻多为1、2级。轻度腹泻早期给予饮食指导(避免食用辛辣、高脂肪、油炸食物及大量水果);较严重者则给予止泻药物及补液治疗。3、4级骨髓抑制反应[中性粒细胞和(或)血小板减少]发生率约为17%,高于国外报道的10%[11],给予小剂量升白细胞、血小板药物,即可缓解。
本组患者中多数伴有肿瘤多发转移,病情较重,预后不良,而患者及家属对靶向药物的治疗持怀疑态度,再加上药物价格昂贵,巨大的经济及心理压力很容易形成消极的治疗态度,本科医护人员及时给予充分的沟通和交流,耐心讲解药物的作用、疗效、不良反应、注意事项及应对措施等,鼓励患者及家属增加治疗信心,绝大多数患者能够坚持治疗,且对不良反应的耐受性也增加。本组临床结果进一步提示舒尼替尼治疗晚期肾癌严重不良反应少,疗效、耐受性及安全性良好。
[1] MOTZER R J, MICHAELSON M D, REDMAN B G, et al. Activity of SU11248, a multitargeted inhibitor of vascular endothelial growth factor receptor and platelet-derived growth factor receptor, in patients with metastatic renal cell carcinoma[J]. J Clin Oncol, 2006, 24(1): 16-24.
[2] MOTZER R J, MICHAELSON M D, ROSENBERG J, et al. Sunitinib efficacy against advanced renal cell carcinoma[J]. J Urol, 2007, 178(5): 1883-1887.
[3] MOTZER R J, HUTSON T E, TOMCZAK P, et al. Sunitinib versus interferon alfa in metastatic rena1-cell carcinoma[J]. N Engl J Med, 2007, 356(2): 115-124.
[4] 吴翔, 李学松, 何志嵩, 等. 舒尼替尼治疗转移性肾癌的进展[J]. 中华临床医师杂志(电子版), 2012, 6(3): 655-658.
[5] OUDARD S, BEUSELINCK B, DECOENE J, et al. Sunitinib for the treatment of metastatic renal cell carcinoma[J]. Cancer Treat Rev, 2011, 37(3): 178-184.
[6] 程树林, 曾浩, 李响, 等. 舒尼替尼治疗转移性肾癌的疗效及安全性评价[J]. 中华泌尿外科杂志, 2010, 5(31): 304-307.
[7] 吴翔, 李学松, 黄立华, 等. 舒尼替尼治疗转移性肾癌的疗效和安全性分析:单中心37例总结[J]. 中华泌尿外科杂志, 2011, 32(4): 278-281.
[8] MOTZER R J, HUTSON T E, TOMCZAK P, et al. Overall survival and updated results for sunitinib compared with interferon alfa in patients with metastatic renal cell carcinoma[J]. J Clin Oncol, 2009, 27: 3584-3590.
[9] GORE M, SZCZYLIK C, PORTA C, et al. Safety and efficacy of sunitinib for metastatic renal-cell carcinoma: an expandedaccess trial[J]. Lancet Oncol, 2009, 10: 757-763.
[10] ZHOU A P. Management of sunitinib adverse events in renal cell carcinoma patients: the Asian experience[J]. Asia-Pacific J Clin Oncol, 2012, 8: 132-144.
[11] UEMURA H, SHINOHARA N, YUASA T, et al. A phaseⅡstudy of sunitinib in Japanese patients with metastatic renal cell carcinoma: insights into the treatment, efficacy and safety[J]. Jpn J Clin Oncol, 2010, 40: 194-202.
The preliminary evaluation of sunitinib’s clinical efficacy for the advanced kidney cancer
LI Yanshuai1,2, ZHAO-Li, WANG Ya-lin2, LI Jian-tao2, QU Nan2, HUANG Chen2, MAI Hai-xing2, LI Xue-chao2, CHEN Li-jun2(1.The General Hospital of Chinese People’s Liberation Army, Bejing 100853, China; 2.Department of Urology, Affiliated Hospital of the Academy of Military Medical Sciences, Beijing 100071, China)
CHEN Li-jun E-mail: chenlj829@163.com
Background and purpose: There is significant efficacy in the treatment of renal cell carcinoma for sunitinib. This article aimed to investigate preliminarily the efficacy and safety of advanced renal cell carcinoma treated with sunitinib. Methods: A total number of 36 patients with advanced renal cell carcinoma were enrolled, including 16 cases of solitary metastases and the rest of systemic multiple metastases, all the patients were confirmed by biopsy. Sunitinib was administered in standard 4/2 regimens: 50 mg once a day orally, taking 4 weeks, stopping 2 weeks, 6 weeks per 1 cycle, and continued until disease progression or occurrence of intolerable adverse reactions, and had an efficacy evaluation at least 2 cycles. Results: The follow-up ended in Jul. 2012, 29 patients could be evaluated efficacy, 5(17.2%) patients dead, 5 patients developed progressive disease, 6 patients achieved partial remission, 1 patient achieved complete remission, 17 patients demonstrated stable disease, the disease control rate was 82.8% (24/29), objective response rate was 24.1% (7/29). The median progression-free survival and overall survival has not yet reached. The follow-up time was ranged from 3 to 28 months. Common adverse reactions were mainly fatigue,yellowish discoloration of skin, hand-foot skin reaction, hypertension, hypothyroidism, diarrhea, anemia, neutropenia, thrombocytopenia, 3-4 adverse events were hand-foot skin reaction (11.5%), hypertension, thrombocytopenia and neutropenia. Mostly mild adverse reactions after symptomatic treatment could be alleviated, did not affect the medication. Conclusion: Sunitinib was efficacious in the treatment of advanced kidney cancer, had fewer serious adverse reactions and good tolerability and safety.
Renal cell carcinoma; Metastatic; Sunitinib; Adverse event
10.3969/j.issn.1007-3969.2013.03.014
R737.11
:A
:1007-3639(2013)03-0235-04
2012-12-17
2013-02-16)
《中国癌症杂志》2013年1~6期继续教育栏目课程表
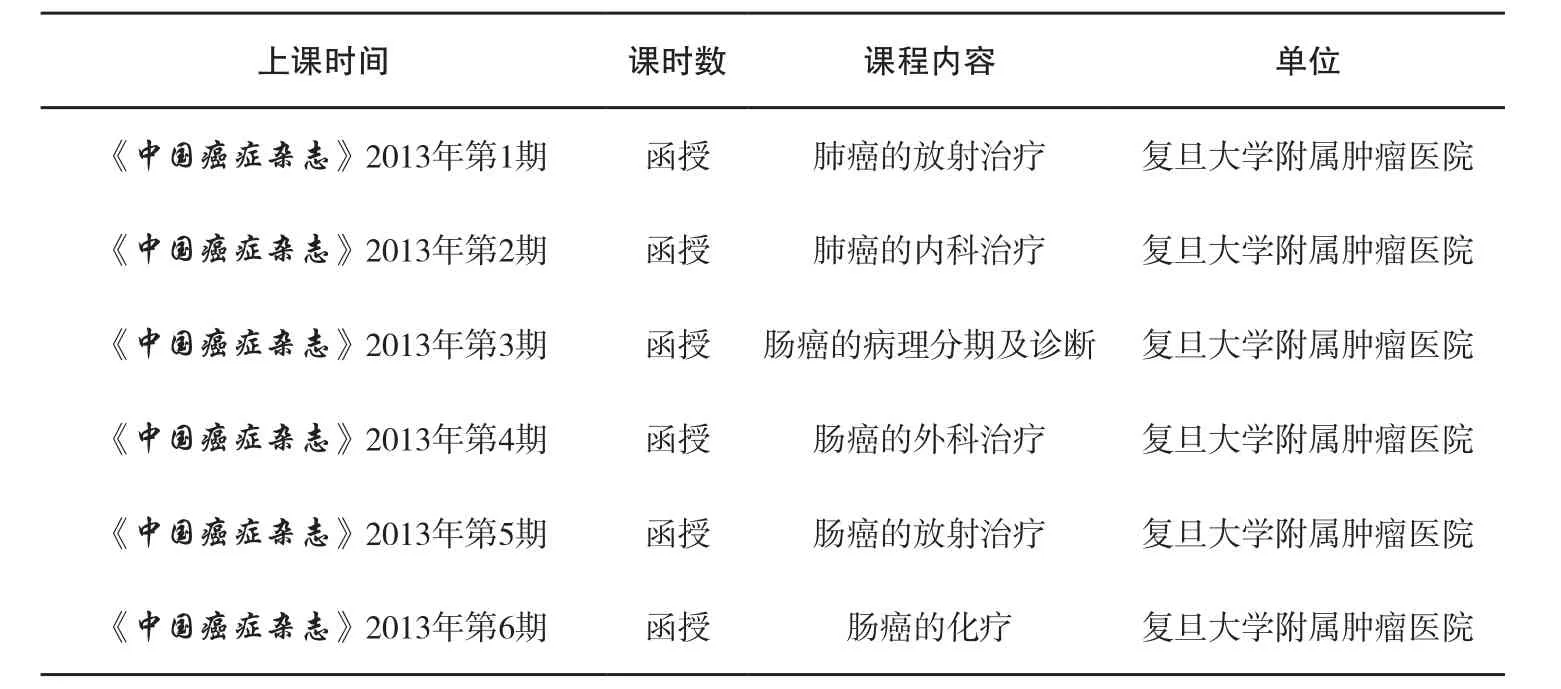
上课时间课时数课程内容单位《中国癌症杂志》2013年第1期函授肺癌的放射治疗复旦大学附属肿瘤医院《中国癌症杂志》2013年第2期函授肺癌的内科治疗复旦大学附属肿瘤医院《中国癌症杂志》2013年第3期函授肠癌的病理分期及诊断复旦大学附属肿瘤医院《中国癌症杂志》2013年第4期函授肠癌的外科治疗复旦大学附属肿瘤医院《中国癌症杂志》2013年第5期函授肠癌的放射治疗复旦大学附属肿瘤医院《中国癌症杂志》2013年第6期函授肠癌的化疗复旦大学附属肿瘤医院
陈立军 E-mail:chenlj829@163.com

