尿素对甲酸盐体系三价铬电沉积的作用机理
李烨,高云芳*,徐新,姚秋实
(浙江工业大学化学工程与材料学院,浙江 杭州 310014)
传统镀铬工艺采用以硫酸根为催化剂的六价铬镀液,但Cr(VI)具有强氧化性,是一种强致癌物质,严重污染环境,各国政府均加强了含Cr(VI)产品应用的立法管理,开始限制并逐步淘汰Cr(VI)的应用[1-2]。Cr(III)镀液体系毒性较小且有良好的电镀性能,成为 近年来研究的热点[3-6]。
Cr(III)电镀最早于1854年由B.Robert 提出,但是相关的工艺研究进展却十分缓慢[7]。20世纪70年代,英国Albring & Wilson 公司开发了甲酸镀液体系三价铬电沉积的新工艺并应用于工业中[8],Cr(III)镀液体系的研究取得了较快的发展[9-12],众多不同体系Cr(III)镀液相继研究成功,如氨基乙酸体系、乙酸体系、乙二胺四乙酸(EDTA)体系等。但Cr(III)镀液体系制得的镀层性能仍无法与Cr(VI)镀液体系相比[13]。20世纪90年代,A.A.Watson 等[14-15]通过大量实验发现,在Cr(III)-甲酸盐体系中加入尿素和甲醇可大幅提高Cr(III)的沉积速率,镀层厚度也高达200 μm。近年来,众多镀铬新工艺均采用了添加尿素和甲酸的Cr(III)镀液体系[16-17],如V.S.Protsenko、F.I.Danilov 等从含甲酸和尿素的Cr(III)镀液中沉积得到纳米晶铬镀层。但目前国内外有关尿素在Cr(III)-甲酸盐镀液体系电沉积过程中作用机理的研究相对较少。
本文结合Cr(III)-甲酸盐镀液体系的一些研究结果,通过紫外-可见光(UV-vis)吸收光谱、线性电位扫描曲线(LSV)、恒电位沉积试验、扫描电子显微镜(SEM)等检测技术,对Cr(III)-甲酸盐镀液体系电沉积时尿素所发挥的作用机理进行探讨,以获得较深入、准确的Cr(III)阴极反应信息,促进Cr(III)电沉积铬工艺技术的发展。
1 实验
1.1 工艺流程
抛光─超声除油(无水乙醇,20 min)─热水洗(80 °C)─浸蚀[φ(HNO3)= 20%,30 min]─水洗─吹干─电镀─水洗─吹干。
1.2 镀液组成与工艺
Cr2(SO4)30.3 mol/L
NH4COOH 1.0 mol/L
CO(NH2)20.3 mol/L
H3BO30.6 mol/L
Na2SO40.4 mol/L
十二烷基硫酸钠(SDS) 0.01 g/L
硫酸铬、甲酸盐、H3BO3等试剂均为分析纯,溶液采用去离子水配制。
1.3 性能检测
1.3.1 镀液组分
采用紫外吸收光谱法,用岛津UV-2600 紫外-可见光分光光度计(UV-vis),扫描范围为200~800 nm,扫描速率为中速。
1.3.2 线性极化曲线
采用上海辰华CHI660D 电化学工作站,工作电极为2 cm × 1 cm 的紫铜片,参比电极为饱和Hg/Hg2SO4电极(SSE),辅助电极为铂片,扫描电位区间为-0.4~-2.0 V,扫描速率为10 mV/s,在室温[(25 ± 1)°C,下同]下进行。
1.3.3 恒电位沉积试验
采用上海辰华CHI1200B 型恒电位仪,在-1.0~-2.0 V 内选择合适的恒电位,在室温下沉积10 min。采用自制三电极电解槽,工作电极为2 cm × 2 cm 的黄铜片,辅助电极为石墨电极,参比电极为饱和Hg/Hg2SO4电极。实验前通入99.99%的氩气20 min 以除去溶液中的氧气,使电沉积试验在氩气氛围下进行。阴极电流效率按式(1)计算:

式中,Δm 为电沉积后阴极的增重量(g);Q 为电沉积过程中的总电量(C);k 为Cr3+的电化当量(g/C)。
1.3.4 镀层形貌
在电位-1.8 V、室温下,对2 cm × 2 cm 的黄铜片恒电位沉积30 min,采用日立S4700 扫描电子显微镜观察所得镀层的表面微观形貌。
2 结果与讨论
2.1 镀液中三价铬配合物的结构
图1为未加配位剂的三价铬基础镀液和采用不同配位剂时三价铬镀液的UV-vis 谱图。由图1a可知,Cr2(SO4)3基础镀液的最大吸收波长λ1= 419 nm、λ2= 581 nm;加入1.0 mol/L HCOO-后,最大吸收波长变为λ1= 415 nm、λ2= 572 nm,与基础镀液相比,其λ1蓝移了4 nm,λ2蓝移了9 nm,且λ1和λ2处的吸光度有较大幅度的升高。此现象可解释为:Cr2(SO4)3溶液的 pH <3 时,Cr(III)主要以[Cr(H2O)6]3+形式存在[18]。基础镀液中不含任何配合物,所以 Cr(III)主要以[Cr(H2O)6]3+形式存在。加入1.0 mol/L HCOO-后,由于HCOO-与[Cr(H2O)6]3+发生配位取代反应,生成了[Cr(H2O)n(HCOO-)m]3-m(m + n = 6,m = 1、2、3),结合相关文献[19-20],其取代机理如下:
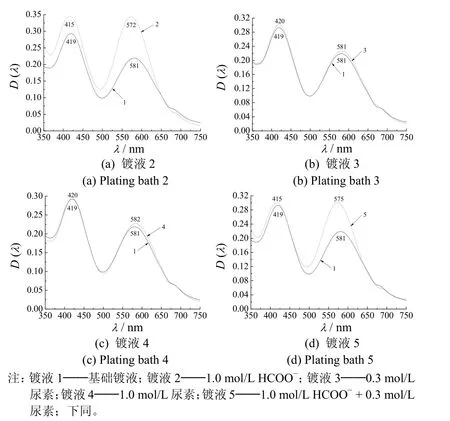
图1 不同配位体系Cr(III)镀液的UV-vis 谱图Figure 1 UV-vis spectra for Cr(III) plating baths with different complexing agents
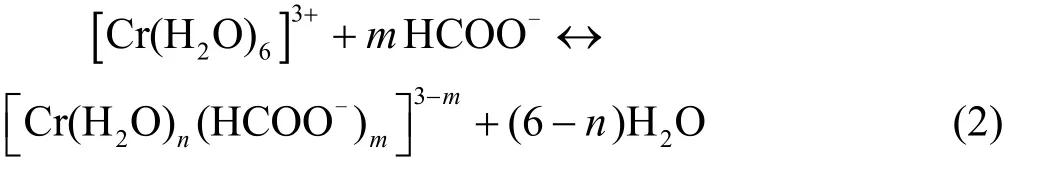
由图1b和图1c可知,尿素的添加量对Cr2(SO4)3镀液的最大吸收波长影响不大,说明加入不同含量的尿素后,镀液中的Cr(III)仍主要以[Cr(H2O)6]3+存在。由图1d可知,同时加入1.0 mol/L HCOO-和0.3 mol/L 尿素后,即镀液5 的最大吸收波长为λ1= 415 nm、λ2= 575 nm,比镀液1 的λ2蓝移了6 nm,比镀液2 的λ2红移了3 nm,说明此镀液5 中的Cr(III)配合物组成不同于镀液1 和镀液2。根据Cr(III)配合物的相关研究结果[9],尿素分子和甲酸根离子对Cr(III)均有掩蔽作用,且尿素的掩蔽作用要强于甲酸根离子,这是因为尿素与Cr(III)的配合作用比甲酸根离子更加稳定。当引入尿素、甲酸根离子双配体时,尿素与Cr(III)- 甲酸盐体系的活性配合物发生配位取代反应,生成了分子体积更大的[Cr(H2O)n(CON2H4)k(HCOO-)m]3-m(m + n + k = 6;m = 1、2、3),其取代机理推测如下:
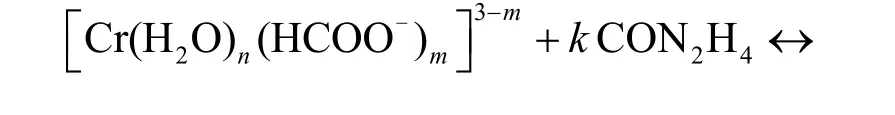
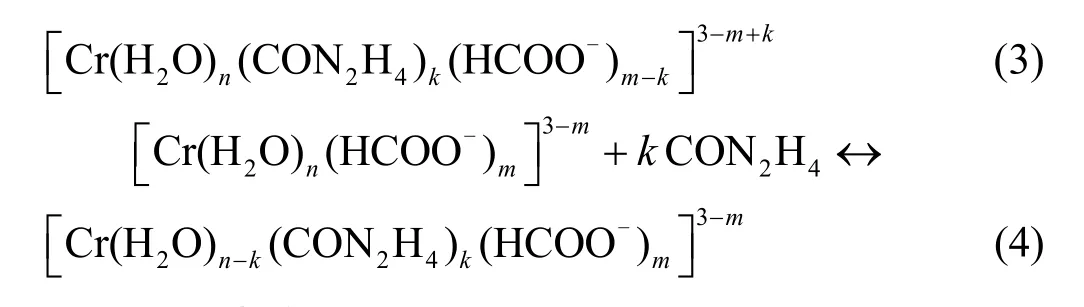
2.2 线性极化曲线
图2为铜电极在添加不同成分配合物Cr(III)镀液体系的线性极化(LSV)曲线。在电位阴极极化扫描过程中,主要的阴极反应是Cr(III)的电还原和析氢反应。
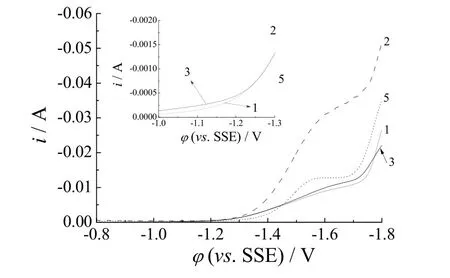
图2 铜电极在不同配位体系镀液中的LSV 曲线Figure 2 LSV curves for copper electrode in plating baths with different complexing agents
由图2可知,电位为-1.5 V 时,镀液2 和镀液5的电流增长速率均有所减缓,镀液1 和镀液3 的电流最小。结合V.Protsenko 等关于Cr(III)-甲酸盐镀液体系电沉积机理的相关研究,推测是因为镀液2 和镀液5的阴极表面被电还原中间产物Cr(II)配合物所覆盖,抑制了析氢反应的发生,镀液5 由于阴极表面吸附有尿素,使电流变化的减缓趋势更强;镀液1 和镀液3则由于发生析氢反应,阴极附近 pH 迅速升高,[Cr(H2O)6]3+发生水解并发生羟桥联反应,阻碍Cr(III)的电还原;随电位进一步负移,所有镀液的电流都迅速增长,这是因为富集在阴极表面的Cr(II)活性配合物开始发生电沉积反应,对析氢反应的阻碍作用也逐渐消失。
2.3 恒电位电解及其电流效率
根据2.2 节的相关结论推测,在电位区-1.0~-2.0 V内,整个电沉积过程的总电流I 主要包括3 个部分。
(1) 析氢电流 2HI :2H++ 2e-→ H2。
(2) 沉积电流I1:Cr3++ 3e-→ Cr。
(3) 电沉积中间产物电流I2:Cr3++ e-→ Cr2+。
整个电沉积过程的沉积电流效率如式(5)所示:

分别对镀液1、镀液2、镀液3 和镀液5 进行恒电位沉积。结果表明,当电位控制在-1.5~-1.9 V 时,含1 mol/L HCOO-和含1 mol/L HCOO-+ 0.3 mol/L尿素的镀液中铜电极表面均出现光亮的银白色Cr 镀层,而含0.3 mol/L 尿素的Cr2(SO4)3镀液和不含配体的Cr2(SO4)3基础镀液的铜电极表面只形成一层易脱落的深绿色沉淀物。
图3为镀液2 和镀液5 在不同电位下恒电位沉积时的η-φ 曲线。从图3可知,阴极电位为-1.5 V 时,Cr(III)-甲酸盐镀液中加入0.3 mol/L 尿素后,铬沉积的电流效率约降低4%;阴极电位低于-1.6 V 时,含0.3 mol/L 尿素的Cr(III)-甲酸盐镀液,其铬沉积电流效率均高于Cr(III)-甲酸镀液体系。结合LSV 曲线和UV-vis 测试结果,原因可分析如下:Cr(III)-甲酸盐镀液中加入尿素后,尿素与Cr(III)配合物配位取代,使镀液电还原所需活化能提高,Cr(III)沉积过电位负移,电位为-1.5 V 时的电流效率较低,随电位负移,尿素在阴极表面发生吸附,使析氢反应对沉积层的破坏减少,电流效率提高。
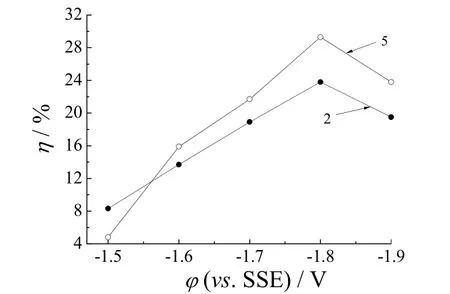
图3 不同配位体系中Cr(III)恒电位沉积的电流效率Figure 3 Current efficiency of Cr(III) deposition in plating baths with different complexing agents at constant potential
当阴极电位达-1.8 V 时,2 组镀液中对应的铬沉积电流效率均达到最大,随阴极电位进一步负移,铬沉积电流效率降低。这主要是因为剧烈的析氢反应会破坏沉积层,大量析出的氢气泡会阻碍Cr(III)-甲酸盐镀液体系中的活性配合物与阴极接触,并对阴极表面尿素的吸附造成破坏。
2.4 电沉积层表面微观形貌
镀液2 和镀液5 在-1.8 V 下恒电位沉积30 min 所得镀层的SEM 照片见图4。从图4a和图4b可知,Cr(III)-甲酸盐镀液中不含尿素时,所得镀层表面存在明显的气孔和裂痕,晶粒尺寸较大,实验发现此时镀层厚度为4.2 μm,继续增长困难。Cr(III)-甲酸盐镀液中加入0.3 mol/L 尿素后,所得镀层晶粒尺寸大多为1~2 μm,且表面无明显裂痕和气孔,沉积层晶粒分布密度差异较大,实验发现此时镀层仍处于增厚阶段,最厚可达12.7 μm。另外,观察镀层外观发现,镀液2 沉积所得镀层光泽度较差,呈暗黑色;而镀液5 所得镀层则为光亮的银白色。

图4 不同配位体系所得镀层的SEM 照片Figure 4 SEM images of the coatings prepared from plating baths with different complexing agents
上述结果可解释如下:由恒电位沉积试验可知,尿素可提高Cr(III)-甲酸盐镀液体系中铬沉积的过电位。结合金属电沉积的相关理论[21],金属沉积过电位越高,则沉积层晶粒尺寸越小。另外,尿素会吸附于阴极表面,导致阴极电流密度分布不均匀,造成沉积层的晶粒尺寸大小和分布密度也不够均一。
3 结论
(1) Cr(III)基础镀液中只加入尿素时,尿素很难与[Cr(H2O)6]3+发生配位取代反应,甲酸对尿素与三价铬的配位起促进或诱导作用。
(2) Cr(III)-甲酸盐镀液体系电沉积铬的过程中,尿素通过参与Cr(III)配合物的配位取代反应及其在阴极的吸附来提高Cr 沉积的过电位,并抑制析氢反应。
(3) 尿素对Cr(III)-甲酸盐镀液体系的沉积层晶粒有细化作用,可有效提高镀层的厚度和改善镀层外观。
[1]MANDICH N V.Chemistry & theory of chromium deposition: part I— Chemistry [J].Plating and Surface Finishing,1997,84 (5): 108-115.
[2]EDIGARYAN A A,SAFONOV V A,LUBNIN E N,et al.Properties and preparation of amorphous chromium carbide electroplates [J].Electrochimica Acta,2002,47 (17): 2775-2786.
[3]PROTSENKO V S,DANILOV F I,GORDIIENKO V O,et al.Electrodeposition of hard nanocrystalline chrome from aqueous sulfate trivalent chromium bath [J].Thin Solid Films,2011,520 (1): 380-383.
[4]PHUONG N V,KWON S C,LEE J Y,et al.Mechanistic study on the effect of PEG molecules in a trivalent chromium electrodeposition process [J].Microchemical Journal,2011,99 (1): 7-14.
[5]PROTSENKO V S,GORDIIENKO V O,DANILOV F I,et al.Unusually high current efficiency of nanocrystalline Cr electrodeposition process from trivalent chromium bath [J].Surface Engineering,2011,27 (9): 690-692.
[6]SAFONOVA O V,VYKHODTSEVA L N,POLYAKOV N A,et al.Chemical composition and structural transformations of amorphous chromium coatings electrodeposited from Cr(III) electrolytes [J].Electrochimica Acta,2010,56 (1): 145-153.
[7]屠振密.三价铬镀铬的国内外研究和发展[J].哈尔滨工业大学学报,1980 (1): 109-121.
[8]EL-SHARIF M,MCDOUGALL J,CHISHOLM C U.Electrodeposition of thick chromium coatings from an environmentally acceptable chromium (III)-glycine complex [J].Transactions of the Institute of Metal Finishing,1999,77 (4): 139-144.
[9]方景礼.电镀配合物: 理论与应用[M].北京: 化学工业出版社,2008.
[10]方景礼.多元络合物电镀[M].北京: 国防工业出版社,1983.
[11]WARD J J B,BARNES C.Trivalent chromium plating baths: US,4157945 [P].1979-06-12..
[12]姚守拙,李克平.用EDTA 为络合剂的三价铬镀铬工艺研究[J].电镀与环保,1985,5 (6): 1-4.
[13]李家柱,林安.三价铬电镀研究进展[J].材料保护,2003,36 (3): 8-11.
[14]WATSON A,SU Y J,EL-SHARIF M R,et al.The electrodeposition of zinc chromium alloys and the formation of conversion coatings without the use of chromate solutions [J].Transactions of the Institute of Metal Finishing,1993,71 (1): 15-20.
[15]WATSON A,ANDERSON A M H,EL-SHARIF M R,et al.The role of chromium II catalysed olation reactions in the sustained deposition of chromium and its alloys from environmentally acceptable chromium III electrolytes [J].Transactions of the Institute of Metal Finishing,1991,69 (2): 26-32.
[16]EUGÉNIO S,RANGEL C M,VILAR R,et al.Electrochemical aspects of black chromium electrodeposition from 1-butyl-3-methylimidazolium tetrafluoroborate ionic liquid [J].Electrochimica Acta,2011,56 (28): 10347-10352.
[17]DANILOV F I,PROTSENKO V S,GORDIIENKO V O,et al.Nanocrystalline hard chromium electrodeposition from trivalent chromium bath containing carbamide and formic acid: Structure,composition,electrochemical corrosion behavior,hardness and wear characteristics of deposits [J].Applied Surface Science,2011,257 (18): 8048-8053.
[18]PHUONG N V,KWON S C,LEE J Y,et al.The effects of pH and polyethylene glycol on the Cr(III) solution chemistry and electrodeposition of chromium [J].Surface and Coatings Technology,2012,206 (21): 4349-4355.
[19]PROTSENKO V,DANILOV F.Kinetics and mechanism of chromium electrodeposition from formate and oxalate solutions of Cr(III) compounds [J].Electrochimica Acta,2009,54 (24): 5666-5672.
[20]ZENG Z X,SUN Y L,ZHANG J Y.The electrochemical reduction mechanism of trivalent chromium in the presence of formic acid [J].Electrochemistry Communications,2009,11 (2): 331-334.
[21]何新快.羧酸盐-尿素体系脉冲电沉积纳米晶铬镀层的工艺优化[J].材料保护,2009,42 (3): 44-47.

