培美曲塞单药或联合铂类治疗非小细胞肺癌86例分析
张冠中,焦顺昌,杨纪华
1解放军总医院 肿瘤内科,北京 100853;2沈阳军区总医院 肿瘤科,辽宁沈阳 110016
非小细胞肺癌(non-small cell lung cancer,NSCLC)约占肺癌总数的80%,其中75%~85%在确诊时已为晚期,5年生存率不足5%[1-2]。晚期非小细胞肺癌的首选治疗方法为铂类(platincum)为基础的联合化疗(铂类联合吉西他滨、多西他赛、紫杉醇、长春瑞宾),一线化疗能延长患者生存期,改善患者生存质量,但有效率仅为30%~40%,中位生存期仅7~12月[3-4]。当前对于晚期NSCLC的二线治疗包括选择单药多西他塞、培美曲塞及厄罗替尼。培美曲塞是一种多靶点抗叶酸制剂,2004年8月被美国FDA批准用于晚期NSCLC的二线治疗,2005年12月在中国上市[5]。本研究回顾性研究培美曲塞单药或联合铂类治疗局部进展或复发转移NSCLC患者的近远期疗效和不良反应。
资料和方法
1 资料 2008年12月-2011年5月解放军总医院应用培美曲塞单药或联合铂类治疗局部进展或远处转移的非小细胞肺癌患者86例,均为经病理和(或)细胞学证实的局部进展或复发转移的晚期非小细胞肺癌患者,既往治疗中未曾应用过培美曲塞。所有患者预计生存期>3月,ECOG评分0~2分,均有可测量及评价病灶。86例中男性64例,女性22例,年龄34~79岁,中位年龄54岁,其中腺癌51例,鳞癌(squam)26例,支气管肺泡癌6例,大细胞癌2例,腺鳞混合癌1例。一线化疗9例,二线化疗48例,三线化疗23例,四线化疗6例。既往化疗为吉西他滨、多西他赛、紫杉醇、长春瑞滨与顺铂或卡铂等不同方案的联合治疗。培美曲塞单药治疗29例,联合铂类治疗57例。非鳞癌患者60例(69.8%);鳞癌患者26例(30.2%)。患者资料详见表1。
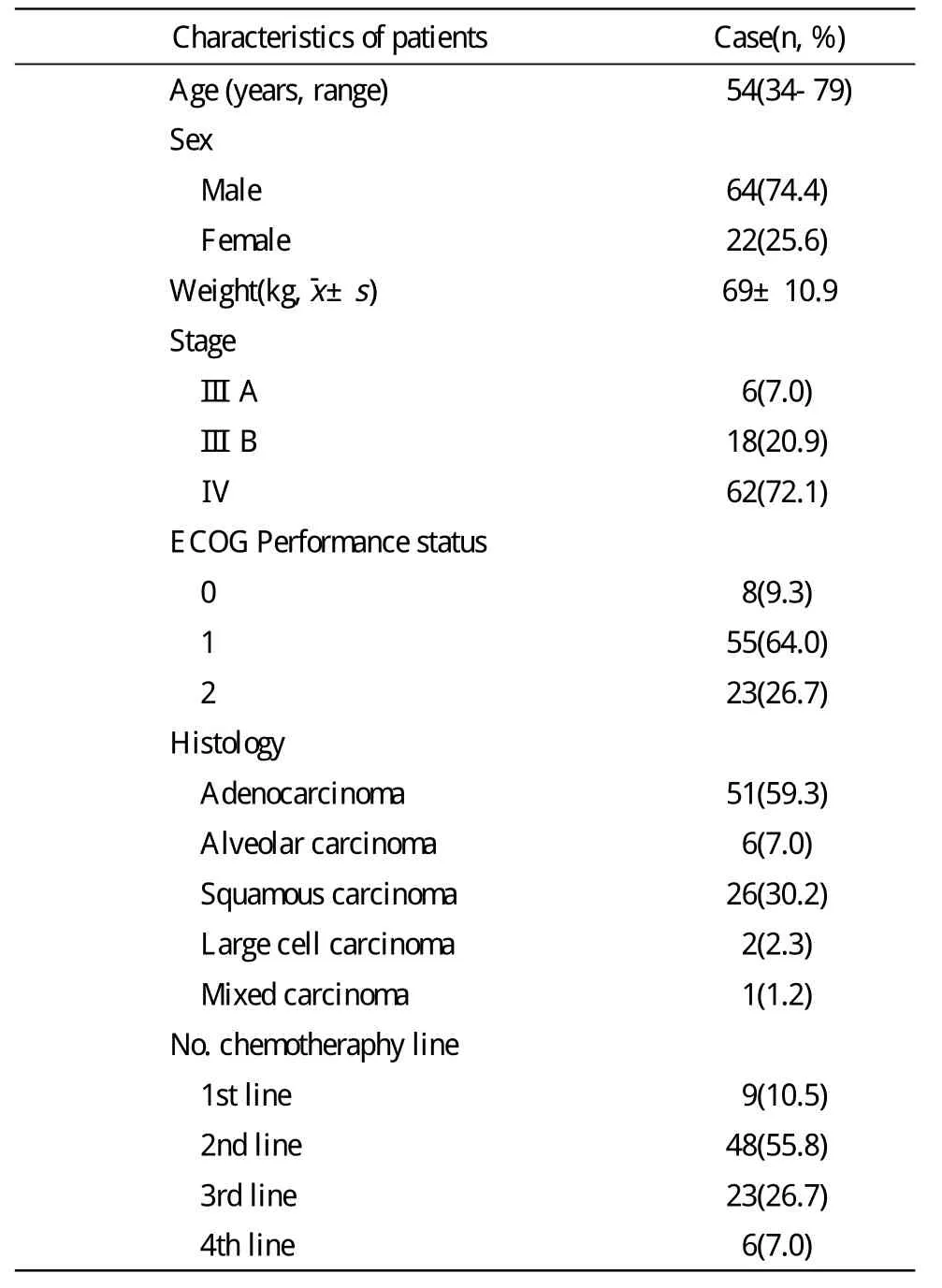
表1 患者资料Tab.1 Parameters of patients included in this study(n=86)
2 治疗方法 培美曲塞单药:培美曲塞500 mg/m2d1,每21 d为1周期。29例(33.7%)接受单药治疗。培美曲塞联合铂类(顺铂或卡铂):培美曲塞500 mg/m2+顺铂75 mg/m2d1;或培美曲塞500 mg/m2+卡铂AUC=5 d1,每21 d为1个周期。57例(66.3%)接受联合治疗。所有患者用药前1周口服多维元素片(含叶酸400 μg/片)1片,1/d至少5 d直至最后一次应用培美曲塞后21 d;第1周期化疗开始前给予维生素B12 1 000 μg肌注1次,每3周期治疗开始前重复;用药前晚、当天早晚和第2天早口服地塞米松3.75 mg,预防过敏反应发生。化疗前查血常规、肝肾功能、心电图均无明显异常开始化疗,化疗2周期后评价疗效,疾病进展或不良反应不能耐受停止治疗。
3 疗效评价及不良反应 肿瘤基线检查在治疗开始前2周内进行,治疗结束后采用相同的影像学检查手段进行疗效评价。近期疗效评价按照实体瘤疗效评定标准(response evaluation criteria in solid tumors,RECIST)分为完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(PD)。客观缓解率(objective response rate,ORR)为CR+PR占所有病例的百分比,疾病控制率(disease control rate,DCR)为CR+PR+SD占所有病例的百分比。远期疗效评价的无进展生存时间(progression-free survival time,PFS)指治疗开始至疾病未进展的生存时间。总生存时间(overall survival time,OS)指治疗开始至任何原因引起的死亡时间。不良反应按照WHO抗癌药物毒性反应评价标准进行评价。分析病人的ORR、DCR、PFS、OS和不良反应,并比较培美曲塞单药与联合铂类治疗的疗效和不良反应以及非鳞癌及鳞癌患者疗效的差异。
4 统计学分析 采用SPSS17.0软件进行统计学分析。近期疗效及不良反应分析采用χ2检验或Fisher精确检验;PFS及OS采用Kaplan-Meier方法分析,并经Log-rank检验。P<0.05为差异有统计学意义。
结 果
1 随访情况 86例从诊断到应用培美曲塞治疗的中位时间为8个月,均至少完成1周期化疗,总化疗周期数285个,中位化疗周期数3(1~10)个。治疗中因不良反应5例(5.8%)进行了剂量调整,14例(16.3%)化疗时间被延迟。中位随访时间10.9(1~42)月。截止至2012年5月随访结束,3例失访可进行疗效及不良反应评价, 10例无进展,31例仍存活。
2 疗效 86例中CR 0例,PR 10例(11.6%),SD 53例(61.6%),PD 23例(26.7%),ORR 11.6%,DCR 73.3%;PFS 7.3(5.8~8.7)月,OS 14.6(12.2~16.9)月,1年生存率45.1%(39.1%~51.1%)。培美曲塞单药和联合铂类治疗组及非鳞癌和鳞癌患者的疗效分析见表2。统计学分析显示,培美曲塞联合铂类的DCR优于培美曲塞单药(P<0.05),ORR无统计学差异(P>0.05);两组的PFS及OS无统计学差异(P>0.05),见图1、表2。非鳞癌与鳞癌的近期疗效(ORR及DCR)无统计学差异(P>0.05);两组的PFS及OS无统计学差异(P>0.05),见表2、图2。
3 不良反应 主要不良反应为Ⅰ/Ⅱ度消化道反应和白细胞减少(表3)。培美曲塞联合铂类治疗组的主要不良反应发生率高于单药组(P<0.05)。Ⅳ度腹泻1例,Ⅳ度肾功改变1例,Ⅲ度恶心呕吐1例,均发生在联合铂类组。Ⅲ度皮疹4例,单药组及联合铂类组各2例。

表2 疗效评价Tab.2 Assessment of curative effect
图1 培美曲塞单药与联合铂类治疗后非小细胞肺癌患者的PFS及OSFig.1 PFS and OS of patients with non-small cell lung cancer after treatment with pemetrexed and in combination with platinum
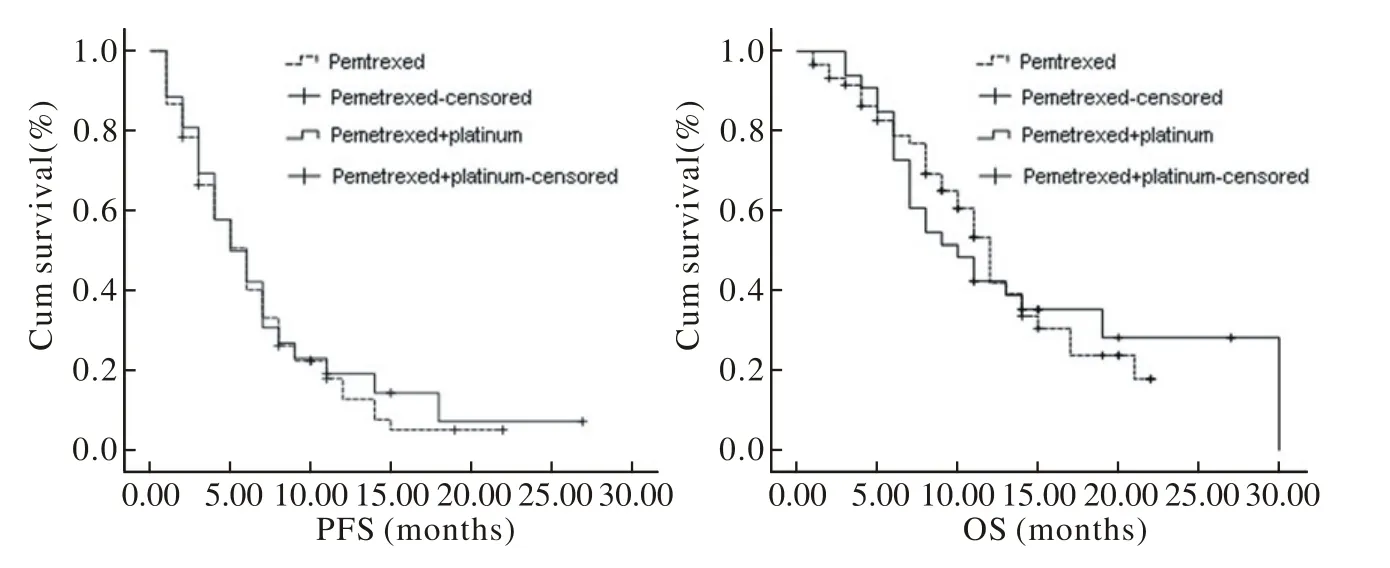
图2 非鳞与鳞状细胞肺癌患者化疗后PFS及OSFig.2 PFS and OS of patients with non-squamous and squamous cell lung cancer after Chemotherapy

表3 不良反应Tab.3 Adverse reactions(n, %)
讨 论
化疗是晚期非小细胞肺癌的主要治疗手段,一线化疗失败的患者,如果其一般状况良好,积极的二线治疗较最佳支持治疗更能让患者获益[6]。培美曲塞的两项Ⅲ期临床试验-JMDB、JMEI表明:培美曲塞一线联合顺铂疗效与吉西他滨联合顺铂相当;二线单药与多西他赛疗效相当,并且培美曲塞的安全性和耐受性更好[7-9]。本研究ORR为11.6%,远低于一线治疗JMDB试验的30.6%,略高于二线JMEI试验的9%,可能与本组数据大部分为二线以后治疗有关。本研究的PFS和OS分别为7.3月和14.6月,较JMDB的4.8月和10.3月和JMEI的2.9月和9.0月显著延长,考虑存在培美曲塞在亚裔人群中有更好的远期疗效的可能性,但本研究的样本量较小,还须以大样本的临床试验证实。在不良反应方面,主要为Ⅰ/Ⅱ度的消化道反应和白细胞降低。Ⅲ/Ⅳ度不良反应主要见于白细胞及血小板减少,发生率较低,分别为9.3%和8.2%,经过对症治疗后恢复正常。我们的研究显示培美曲塞或培美曲塞联合铂类在亚裔人群的非小细胞肺癌治疗中疗效确切,且耐受性及安全性良好。
本研究中培美曲塞联合铂类与培美曲塞单药治疗相比,DCR前者好于后者,但不良反应显著增高,并且PFS及OS无统计学差异。本组病人中接近90%为二线以后治疗,研究提示单药可能是二线以后非小细胞肺癌治疗的更好选择,相对于联合治疗在生存期相似的情况下可有更小的不良反应及更高的生活质量。JMDB试验中,非鳞癌患者的OS显著长于鳞癌患者,因此培美曲塞联合铂类推荐用于非鳞状细胞肺癌患者的治疗。有研究显示TS表达与培美曲塞敏感性呈负相关[10]。在我们的研究中,非鳞癌与鳞癌的近期及远期疗效均未见明显差异,这种差异可能与病人的种族不同相关,也不能排除样本量相对较小因素,得出结论尚需进一步的研究。
1 Paz-Ares L, de Marinis F, Dediu M, et al. Maintenance therapy with pemetrexed plus best supportive care versus placebo plus best supportive care after induction therapy with pemetrexed plus cisplatin for advanced non-squamous non-small-cell lung Cancer(Paramount): a double-blind, phase 3, randomised controlled trial[J]. Lancet Oncol, 2012, 13(3): 247-255.
2 刘哲峰,赵宏,焦顺昌.培美曲塞与吉西他滨联合顺铂治疗晚期非小细胞肺癌比较[J].军医进修学院学报,2009,30(3):320-322.
3 D'addario G, Früh M, Reck M, et al. Metastatic non-small-cell lung Cancer: ESMO Clinical Practice Guidelines for diagnosis,treatment and follow-up[J]. Ann Oncol, 2010, 21 Suppl 5(suppl 5): v116-v119.
4 Azzoli CG, Temin S, Giaccone G. 2011 focused update of 2009 American society of clinical oncology clinical practice guideline update on chemotherapy for stage IV Non-Small-Cell lung Cancer[J].J Oncol Pract, 2012, 8(1): 63-66.
5 Zhang GZ, Jiao SC, Meng ZT. Pemetrexed plus cisplatin/carboplatin in previously treated locally advanced or metastatic non-small cell lung cancer patients[J]. J Exp Clin Cancer Res, 2010, 29 :38.
6 吴玉婷,余秉翔,李芸.培美曲塞治疗30例晚期非小细胞肺癌患者疗效观察[J].军医进修学院学报,2009,30(1):53-55.
7 Scagliotti GV, Parikh P, von Pawel J, et al. Phase III study comparing cisplatin plus gemcitabine with cisplatin plus pemetrexed in chemotherapy-naive patients with advanced-stage non-small-cell lung cancer[J]. J Clin Oncol, 2008, 26(21):3543-3551.
8 Hanna N, Shepherd FA, Fossella FV, et al. Randomized phase III trial of pemetrexed versus docetaxel in patients with non-smallcell lung Cancer previously treated with chemotherapy[J]. J Clin Oncol, 2004, 22(9): 1589-1597.
9 Passaro A, Cortesi E, de Marinis F. Second-line treatment of nonsmall-cell lung cancer: chemotherapy or tyrosine kinase inhibitors?[J]. Expert Rev Anticancer Ther, 2011, 11(10):1587-1597.
10 Takezawa K, Okamoto I, Okamoto W, et al. Thymidylate synthase as a determinant of pemetrexed sensitivity in non-small cell lung Cancer[J]. Br J Cancer, 2011, 104(10): 1594-1601.

