镁粉投加对剩余污泥碱性发酵的影响
苏高强,王淑莹,汪传新,袁悦,彭永臻
(北京工业大学 北京市水质科学与水环境恢复工程重点实验室,北京市污水脱氮除磷处理与过程控制工程技术研究中心,北京,100124)
中国是世界上金属镁的主要生产国,2010年,金属镁的生产量达到 138.87万 t[1]。金属镁在生产和加工过程中,产生了大量的金属镁废弃物,特别是在材料加工过程中产生的一些金属镁粉,它不仅会造成大气污染,而且镁粉在空气中遇到火源时会发生爆炸[2]。因此,为了减少资源浪费,防止环境污染和保障人身安全,有必要对其进行回收和利用。中国目前处理污水的工艺主要是生物法,在污水处理过程中能产生大量的剩余污泥(WAS),污泥的处理处置费用占到污水厂运行和管理费用的50%~60%[3]。因此如何实现污泥的减量化、稳定化、无害化和资源化是污水厂亟待解决的问题。WAS中含有大量的蛋白质和多糖,微生物在厌氧的环境条件下能利用这些有机物产生挥发性脂肪酸(VFA),且产生的VFA能被用作碳源进行脱氮除磷。和酸性,中性环境条件下相比,碱性条件能促进污泥的水解并且能抑制产甲烷细菌的活性,因此在碱性条件下污泥的产酸量能得到大幅度的提升,且在碱性条件下污泥的减量率能得到提升[4]。因此污泥在碱性条件下发酵是一种可持续的工艺。镁离子是多种激酶或合成酶的激活剂,会对产酸过程产生影响[5]。文献[6−7]中考察了镁离子对微生物产甲烷和产氢气的影响,但镁离子对剩余污泥碱性条件下水解产酸的影响鲜见报道。由于镁离子在碱性条件下会生成沉淀,不利于控制镁离子浓度。而镁粉为零价金属,不仅能够降低反应系统的氧化还原电位(ORP), 给产酸提供较好的环境[8];且在投加量不同时可以造成反应系统内不同的镁离子浓度。为此,本文作者考察了碱性条件下投加不同量的镁粉对剩余污泥水解产酸的影响。
1 试验的材料与方法
1.1 试验的装置与运行方法
污泥碱性发酵试验在20 ℃的恒温培养箱中进行,反应器为6个1 L的广口试剂瓶,各反应器中分别添加900 mL的WAS,而后每克干污泥中分别添加0,0.01,0.05,0.10和0.20 g的镁粉,最后使用2 mol/L的NaOH调节剩余污泥的pH为10[4]。曝氮气2 min排出反应器顶部的空气,而后使用橡胶塞密闭。橡胶塞中开3个孔,其中一个用于插入pH电极或ORP电极用于检测pH和ORP,一个插入玻璃棒用于取样,另外一个用于投加NaOH控制反应器的 pH。反应过程中使用2 mol/L的NaOH和2 mol/L的HCl控制反应器的pH为10±0.2。反应过程使用磁力搅拌器进行搅拌,搅拌速率为(100±10) r/min。反应器共运行14 d,取样周期为2 d。
1.2 污泥的来源与性质
试验使用的 WAS取自本实验室的中试间歇式活性污泥法反应器,而后在4 ℃的条件下浓缩沉淀24 h。污泥的各项指标如下:pH 6.90,总悬浮固体质量浓度(TSS)10.688 g/L,挥发性悬浮固体质量浓度(VSS)9.103 g/L,溶解性化学需氧量59 mg/L,总化学需氧量(TCOD)11.688 g/L,溶解性蛋白质26 mg/L,溶解性多糖13.5 mg/L,上清液氨氮3 mg/L,上清液正磷酸盐47 mg/L,VFA 0 mg/L。
1.3 测定方法
取样后样品在4 000 r/min的转速下离心20 min,之后使用0.45 μm孔滤膜过滤,滤液用来分析SCOD、氨氮、正磷酸盐、蛋白质、多糖、VFA以及钠离子和镁离子,滤渣用来分析TSS和VSS。pH,氧化还原电位(ORP),TSS,VSS,SCOD,TCOD,氨氮和正磷酸盐测量均采用标准方法[9];蛋白质采用福林酚试剂法测定;多糖采用苯酚−硫酸法测定;VFA使用安捷伦7 890 N气相色谱仪测定;钠离子和镁离子采用离子色谱仪 (761 Compact IC /瑞士万通) 测量。污泥的蛋白酶和淀粉酶的活性根据Goel等的方法测定[10]。每个指标测量2次,取平均值为试验数据。
2 结果与讨论
2.1 污泥溶解情况
污泥在碱性条件下发酵过程中,污泥中的有机物如蛋白质和多糖不断被溶解,污泥的溶解情况可以用SCOD表示[11],图1所示为不同镁粉投加量下剩余污泥SCOD的溶出情况。由图1可知:SCOD的溶出可以分为3个阶段,(Ⅰ) 0~4 d,快速溶出阶段;(Ⅱ) 4~8 d,慢速溶出阶段;(Ⅲ) 8~14 d,下降阶段。第4天时,在镁粉投加量分别为0,0.01,0.05,0.10和0.20 g/g时污泥溶出的SCOD的量为最大溶出量的97%,91%,97%,90%和93%。从图1还可以发现:除第2天时,镁粉投加量为0.01和 0.05 g/g时WAS的SCOD溶出量较低。其他时间内无论镁粉投加量为多少,WAS的SCOD溶出量基本相同。这可能是因为随着时间的延长,调节 pH使用的氢氧化钠和污泥反应的越来越充分,导致镁粉的投加不会对污泥 SCOD的溶出产生影响。

图1 镁粉投加对剩余污泥溶解的影响Fig.1 Effect of magnesium powder addition on WAS solubilisation
2.2 蛋白酶和淀粉酶的活性
污泥在溶解过程中会释放出大量的蛋白质和多糖。2 d时镁粉投加量为0,0.01,0.05,0.10,0.20 g/g时污泥发酵液中蛋白质分别为1 317,288,932,670,900和1 267 mg/L,多糖的质量浓度分别为143,211,68,169和143 mg/L。蛋白质和多糖是产酸的主要底物,在产酸过程中蛋白质和多糖首先被蛋白酶和淀粉酶水解成氨基酸和单糖,而后被产酸细菌用于产挥发性脂肪酸,因此,蛋白酶和淀粉酶的活性直接影响着产酸效率。以不投加镁粉的剩余污泥的蛋白酶和淀粉酶的活性作为对照,测定了第8天不同镁粉投加量条件下剩余污泥的蛋白酶和淀粉酶的活性,如表1所示。
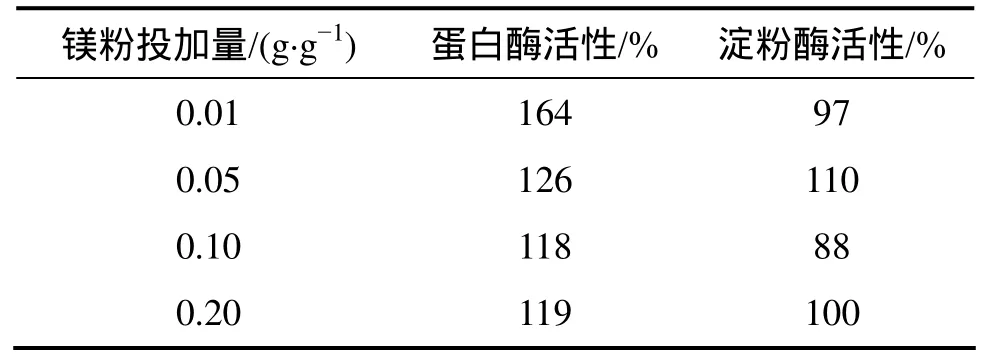
表1 镁粉投加量对蛋白酶和淀粉酶活性的影响Table 1 Effect of magnesium powder addition on activity of protease and α-glucosidase
由表1可知:镁粉的投加可以提高蛋白酶的活性,且在镁粉投加量为0.01 g/g时,蛋白酶的活性增加的最多。原因为第8天时镁粉投加量为0,0.01,0.05,0.10和0.20 g/g时,发酵液中镁离子的质量浓度分别为8,43,61, 134和288 mg/L,镁离子是多种酶的激活剂,较高的镁离子浓度激活了蛋白酶的活性[5];而促进微生物生长所需镁离子的浓度有一个最佳的范围,超过这个范围镁离子的促进作用会降低甚至会抑制微生物的生长[4]。镁粉的投加对淀粉酶的活性影响不大。
2.3 污泥的产酸情况
剩余污泥碱性发酵过程中能溶出大量的蛋白质和多糖,这些蛋白质和多糖被水解成氨基酸和单糖,而后被产酸细菌用于产挥发性脂肪酸。这些挥发性脂肪酸主要由乙酸、丙酸、异丁酸、丁酸、异戊酸和戊酸组成,将其浓度换算为COD,而后相加和为总挥发酸(TVFA)。图2所示为镁粉投加对WAS产酸的影响。
由图2可知:不同镁粉投加量条件下TVFA的含量在0~12 d时均随时间增加而呈不断上升的趋势,且在12 d后TVFA含量开始稳定。12 d时,镁粉投加量为0,0.01,0.05,0.10和0.20 g/g时,相应的WAS的产酸量(以 COD 计)为 2.693,2.948,3.019,2.759和2.838 g/L。由图2还可知:投加镁粉后剩余污泥的产酸量大部分时间内要比不投加镁粉的要多。原因如下:(1) 镁粉的投加提高了发酵液中镁离子的浓度,而镁离子增强了蛋白酶的水解活性。发酵液中蛋白质的浓度要高于多糖的浓度(2 d,镁粉投加量为0,0.01,0.05,0.10和0.20 g/g时污泥发酵液中蛋白质分别为1 317,288,932,670,900和1 267 mg/L,多糖的浓度分别为143,211,68,169和143 mg/L),是产酸的主要基质,因此蛋白酶活性的提高能增强污泥的产酸量。(2) 由于零价镁粉具有较强的还原能力,2~6 d时投加镁粉的反应器中的氧化还原电位均在−500~−700 mV之间,而未投加镁粉的反应器氧化还原电位在−200~−400 mV之间,较低的氧化还原电位能够促进产酸过程中各种还原反应的进行[8]。(3) 镁粉在发酵过程中会释放出镁离子,镁离子是参与产酸过程中多种酶如己糖磷酸化酶、磷酸果糖激酶、磷酸转移酶、磷酸水解酶和异柠檬酸脱氢酶的激活剂,能够促进产酸[5,12]。辛亮[7]也指出当镁离子质量浓度为100和200 mg/L时,与质量浓度为10 mg/L相比,使用玉米秸秆作为基质乙酸和丁酸的产量能够增加。由图2还可知:当镁粉投加量为0.01和0.05 g/g时,TVFA的含量较多,这是因为这2种条件下蛋白酶的活性均较高。从运行成本上考虑,镁粉投加量为0.01 g/g时最佳。
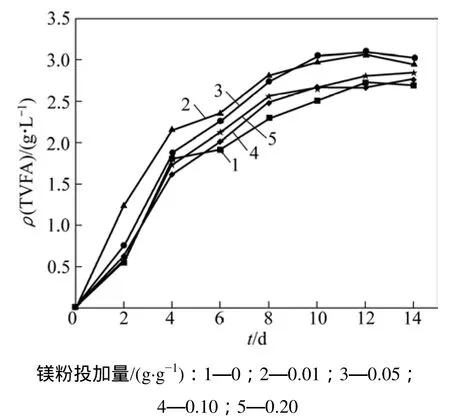
图2 镁粉投加对剩余污泥产酸的影响Fig.2 Effect of magnesium powder addition on acid production of WAS
2.4 产酸组成情况
剩余污泥发酵产生的挥发酸主要有乙酸、丙酸、异丁酸、丁酸、异戊酸和戊酸。在生物脱氮除磷过程中较易被利用的酸主要为短链脂肪酸,如乙酸和丙酸[13−14]。而在生物除磷过程中,微生物合成 PHV 主要靠利用长链脂肪酸,如戊酸[15]。因此TVFA的组成对其利用有重要的影响。不同镁粉投加量情况下,发酵时间为12 d时TVFA的组成如图3所示。
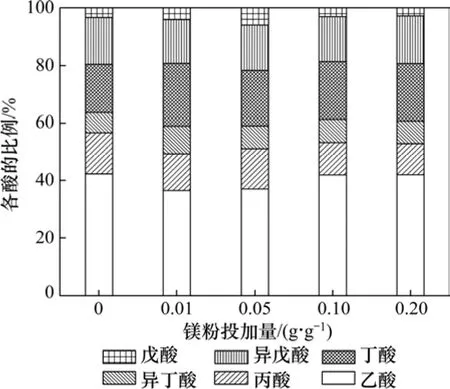
图3 镁粉投加对产酸组成的影响Fig.3 Effect of magnesium powder addition on composition of VFA
从图3可知:无论镁粉的投加量为多少,乙酸所占的比例总是最大,而戊酸所占的比例最小。镁粉投加量为0,0.01,0.05,0.10和0.20 g/g时,乙酸的比例分别为 42%,36%,37%,42%和 42%,而戊酸的比例分别为3%,4%,6%,3%和3%。且各种镁粉投加量情况下,各挥发酸比例由大到小顺序均为乙酸,丁酸,异戊酸,丙酸,异丁酸,戊酸。从图3可以发现:镁粉投加量为0.01和0.05 g/g时,长链脂肪酸(异丁酸、丁酸、异戊酸和戊酸)所占的比例较高。这是因为这2种条件下蛋白酶的活性较高,消耗的蛋白质较多,而长链脂肪酸主要依靠代谢蛋白质脱氨基以及斯提克兰反应产生[16]。
2.5 氨氮和正磷酸盐的释放情况
在污泥碱性发酵过程中,由于蛋白质的水解以及微生物磷脂双分子层被破坏以及胞内多聚磷酸盐的释放,污泥会释放出大量的氨氮和磷酸盐[17]。而氨氮和正磷酸盐的释放势必会影响发酵液作为碳源进行脱氮除磷,因此考察了污泥碱性发酵过程中发酵液中氨氮和正磷酸盐的浓度。图4所示为不同镁粉投加量情况下,发酵液中氨氮和正磷酸盐的浓度。
从图4可知:无论镁粉投加量为多少,发酵液中氨氮的浓度均随时间呈现不断上升的趋势。这是因为越来越多的蛋白质被水解。且在镁粉投加量为0.01 g/g时发酵液中氨氮的浓度最高,原因为该条件下蛋白酶的活性最高。而不加镁粉时,蛋白酶的活性较低,导致氨氮的浓度最低。其他条件下氨氮的浓度基本相同。而对于正磷酸盐,除了不投加镁粉时,发酵液中正磷酸盐的浓度呈现先上升后下降的趋势,其他条件下正磷酸盐的浓度从开始就呈现出不断下降的趋势。14 d时,镁粉投加量为0.05,0.10和0.20 g/g,污泥发酵液中正磷酸盐的质量浓度仅为1~4 mg/L。这是因为镁粉会产生镁离子,而镁离子能和正磷酸盐反应生成磷酸镁沉淀。发酵液中较低的正磷酸盐的浓度可以大大减轻发酵液作为生物除磷碳源时的所带来的磷负荷,因此在镁粉投加量为0.05,0.10和0.20 g/g时,发酵液较适合用作除磷的碳源。随着镁粉的投加量的增多,正磷酸盐的浓度呈不断下降的趋势。原因为随着镁粉的投加量的增多,发酵液中镁离子的浓度也逐渐增大,镁离子和正磷酸盐生成了磷酸镁沉淀。
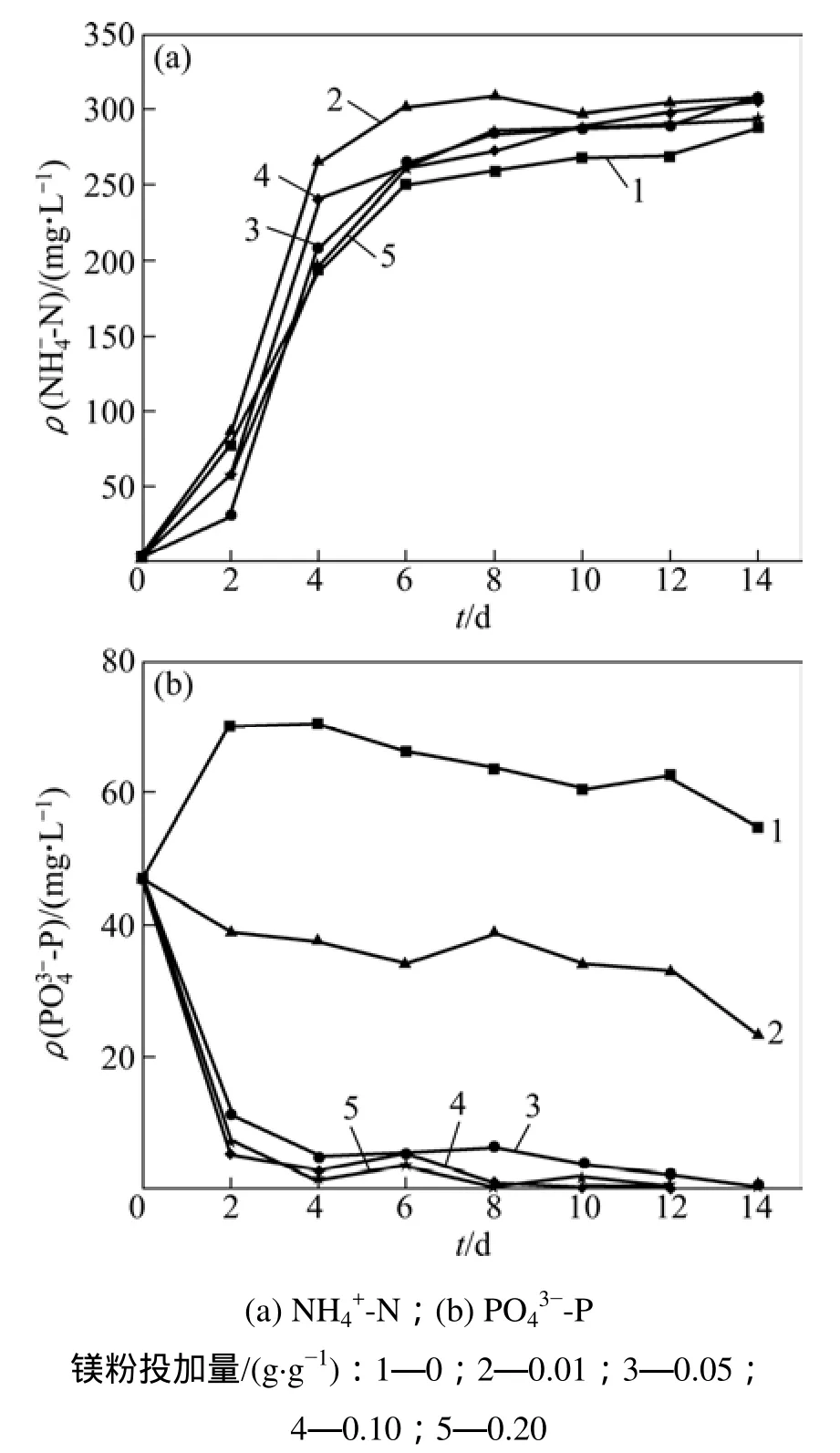
图4 镁粉投加对氨氮和正磷酸盐释放的影响Fig.4 Effect of magnesium powder addition on ammonia and phosphorus release
3 结论
(1) 镁粉投加不会影响WAS溶出SCOD的量,但可以增强蛋白酶的活性,投加量为0.01 g/g时,蛋白酶的活性能增加64%。
(2) 镁粉投加可以增加剩余污泥的产酸量,最佳投加量为0.01 g/g,该条件下12 d时产酸量为2.948 g/L。
(3) 各种镁粉投加量情况下,产酸组成由大到小顺序均为乙酸(36%~42%),丁酸,异戊酸,丙酸,异丁酸,戊酸(3%~6%)。在镁粉投加量为0.01和0.05 g/g时,长链脂肪酸(异丁酸、丁酸、异戊酸和戊酸)所占的比例较高。
(4) 不投加镁粉时氨氮释放量最低,而镁粉投加量为0.01 g/g时氨氮释放量最高。正磷酸盐随着镁粉投加量的增加而降低。
[1]李树林.我国“十一五”期间金属镁生产发展述评[J].轻金属,2011(12): 3−5.LI Shulin.Review of magnesium production and development in the 11th five-year plan[J].Light Metals, 2011(12): 3−5.
[2]付羽, 陈宝智, 李刚.粒径对镁粉爆炸特性的影响[J].工业安全与环保, 2009, 35(8): 36−38.FU Yu, CHEN Baozhi, LI Gang.The influence of particle size on explosive characteristics of magnesium dust[J].Industrial Safety and Environmental Protection, 2009, 35(8): 36−38.
[3]Li H, Jin Y Y, RasoolBux M, et al.Effects and model of alkaline waste activated sludge treatment[J].Bioresource Technology,2008, 99 (11): 5140−5144.
[4]Chen Y G, Jiang S, Yuan H Y, et al.Hydrolysis and acidification of waste activated sludge at different pHs[J].Water Research,2007, 41(3): 683−689.
[5]沈萍, 陈向东.微生物学[M].北京: 高等教育出版社, 2009:92−93.SHEN Ping, CHEN Xiangdong.Microbiology[M].Beijing:Higher Education Press, 2009: 92−93.
[6]彭震.新型自热式抗结壳沼气反应器发酵特性研究[D].重庆:重庆大学动力工程学院, 2011: 51−69.PENG Zhen.Fermentation characteristics of the new type autothermal anaerobic digester for anti-crusting device[D].Chongqing: Chongqing University.College of Power Engineering, 2011: 51−69.
[7]辛亮.菌株X9利用玉米秸秆的产氢能力及影响因素研究[D].哈尔滨: 哈尔滨工业大学市政环境工程学院, 2007: 30−33.XIN Liang.Research on hydrogen production and influential factors using straw by X9[D].Harbin: Harbin University of Technology.School of Municipal and Environmental Engineering, 2007: 30−33.
[8]刘轶文.零价铁强化厌氧废水处理的研究[D].大连: 大连理工大学环境学院, 2011: 37−38.LIU Yiwen.The research on enhancement of anaerobic digestion using adding of zero valent iron[D].Dalian: Dalian University of Technology.School of Environmental Science and Technology,2011: 37−38.
[9]APHA.Standard methods for the examination of water and wastewater[M].19th ed.Washington, DC: American Public Health Association, 1995: 1−1325.
[10]Goel R, MinoT, Satoh H, et al.Enzyme activities under anaerobic and aerobic conditions in activated sludge sequencing batch reactor[J].Water Research, 1998, 32(7): 2081−2088.
[11]Andreasen K, Petersen G, Thomsen H, et al.Reduction of nutrient emission by sludge hydrolysis[J].Water Science and Technology, 1997, 35(10): 79−85.
[12]刘士清, 刘伟伟, 马欢, 等.不同金属离子对生物质发酵产氢的影响[J].农业工程学报, 2010, 26(10): 290−296.LIU Shiqing, LIU Weiwei, MA Huan, et al.Effects of metallic ions on hydrogen fermentation in mixed anaerobic culture system[J].Transactions of the CSAE, 2010, 26(10): 290−296.
[13]Elefsiniotis P, Wareham D G, Smith M O.Use of volatile fatty acids from an acid-phase digester for denitrification[J].Journal of Biotechnology, 2004, 114(3): 289−297.
[14]Chen Y G, Andrew A R, Terrence M.The efficiency of enhanced biological phosphorus removal from real wastewater affected by different ratios of acetic to propionic acid [J].Water Research,2004, 38 (1): 27−36.
[15]Lemos P C, Serafim L S, Reis M A M.Synthesis of polyhydroxyalkanoates from different short-chain fatty acids by mixed cultures submitted to aerobic dynamic feeding[J].Journal of Biotechnology, 2006, 122(2): 226−238.
[16]Liu X L, Liu H, Chen Y Y, et al.Effects of organic matter and initial carbon-nitrogen ratio on the bioconversion of volatile fatty acids from sewage sludge[J].Journal of Chemical Technology and Biotechnology, 2008, 83(7): 1049−1055.
[17]Tong J, Chen Y G.Recovery of nitrogen and phosphorus from alkaline fermentation liquid of waste activated sludge and application of the fermentation liquid to promote biological municipal wastewater treatment[J].Water Research, 2009,43(12): 2969−2976.

