基于Microtox技术(微毒测试)的中药综合毒性快速评价
赵军宁 鄢良春
(四川省中医药科学院药理毒理研究所,国家中医药管理局中药质量生物评价重点研究室,四川省道地药材系统开发工程技术研究中心,中药品质评价与创新中药研究四川省重点实验室,成都,610041)
基于Microtox技术(微毒测试)的中药综合毒性快速评价
赵军宁 鄢良春
(四川省中医药科学院药理毒理研究所,国家中医药管理局中药质量生物评价重点研究室,四川省道地药材系统开发工程技术研究中心,中药品质评价与创新中药研究四川省重点实验室,成都,610041)
Microtox技术(微毒测试)是以一种非致病的明亮发光杆菌作指示生物,以其发光强度的变化为指标,测定环境中有害有毒物质的生物毒性的一种方法,现已成为一种简单、快速的生物毒性检测手段。本文综述了Microtox技术(微毒测试)的研究现状,并就该技术在中药毒性评价应用的技术方法、技术路线、关键问题以及应用范围等方面开展研究,为建立一种新的中药毒性快速检测、安全性评价以及风险分级评定的的综合评价体系奠定基础。
中药;Microtox技术;发光细菌;毒性;生物评价
中药毒性和安全性评价已经成为关系人民群众的用药安全、我国民族医药产业健康持续发展和中医药国际化的重大科学问题[1-2]。中药(尤其是有毒中药),是中医临床用药的重要组成部分,其毒性也给临床安全用药带来一定风险。由于中药成分的复杂性、易变性和现时人们对其认知的程度,决定了仅依赖于现今对已知有效成分的分析测定尚远不能满足作为一个药物质量控制的最低要求,赵军宁等提出基于“功效-毒性-物质”并行性中药质量控制与评价的新型方法体系,对于保证中药临床安全性和有效性具有重大的现实意义[3]。中药毒性是一项非常重要的生物学参数,它是衡量中药样品对活性生物体所产生的影响,大多必须在条件苛刻实验室使用整体动物,甚至高等生物进行,不完全符合中药复杂体系安全性测试的实际情况,存在耗时、费钱、条件高、可重复性较低等不足,目前尚存众多争议[4-5]。Microtox技术(Microtox technology,微毒测试)是以一种非致病的明亮发光杆菌作指示生物,以其发光强度的变化为指标,测定环境中有害有毒物质的生物毒性的一种方法,也是目前我国国家标准GB/T 15441-1995和国际标准(ISO11348)认证的急性毒理测试。自1672年R.Boyle观察到发光的菌体所发出的光易被化学物质抑制后,许多科学家相继对细菌的发光效应进行了大量的研究。本世纪70至80年代初,国外科学家首次从海鱼体表分离和筛选出对人体无害,对环境敏感的发光细菌,用于检测水体生物毒性,现已成为一种简单、快速的生物毒性检测手段[6]。80年代初我国引进了这项技术,并先后分离出海水型和淡水型的发光细菌,用以检测环境污染物的急性生物毒性。近年来还分离出明亮发光杆菌暗变种检测环境污染物致突变性,扩大了检测范围[7]。本文综述了Microtox技术(微毒测试)的研究现状,并就该技术在中药毒性评价应用的技术方法、技术路线、关键问题以及应用范围等方面开展研究,为建立一种新的中药毒性以及毒性分级、配伍解毒等的综合评价体系奠定基础。
1 发光细菌及Microtox技术基本原理
1.1 发光细菌及其代谢特征 发光细菌(lnminescent bacteris或luminousbacteria)是一类在正常的生理条件下能够发射可见荧光的细菌,这种可见荧光并不发热,属于冷光,波长在450~490nm之间,在黑暗处肉眼可见。发光细菌为革兰氏阴性,兼性好氧化能自养型细菌。按传统分类,根据细菌表型特征,即细菌的形态、生理生化特征等方面的相对性,目前已发现并收入《伯杰氏细菌手册》的发光细菌有以下几种:1)属于异短杆菌属(Xenorhabdus)的有发光异短杆菌(Xenorhabdus luminescens);2)属于发光杆菌属(Photobacterium)的有明亮发光杆菌(Photosbacterium phosphoreum)和鳆发光杆菌(P.1eiognathi);3)属于希瓦氏菌属(Shewanella)的有羽田希瓦氏菌(Shezoanella hanedai),以前也曾经把它归类为交替单胞菌属(Alteromonas)的海氏交替单胞菌(Alteromonas hanedia);4)属于弧菌属(Vibrio)的有哈维氏弧菌(Vibrio harveyi)、美丽弧菌生物型I(V.splendidus biotype I)、费氏弧菌(V.fischeri)、火神弧菌(V.1ogei)和东方弧菌(V.orientalis)。霍乱弧菌(V.cholerae)和地中海弧菌(V.mediterranei)中的某些菌株有发光现象,曾有报道易北河弧菌(V.albensis)有发光现象,后将其重新分类归人霍乱弧菌(V.cholerae)[8]。其中,发光杆菌属、希瓦氏菌属以及弧菌属中的大多数发光细菌均为海洋细菌,而霍乱弧菌则是少数被发现的淡水发光细菌之一。我国学者朱文杰也从青海湖中分离得到一个淡水发光细菌新种并命名为青海弧菌[7]。
发光细菌的发光现象是其正常的代谢活动,在一定条件下发光强度是恒定的。虽然发光细菌的种类有很多,但发光机理是相同的,属于酶促氧化反应。细菌发光反应主要参与的物质包括荧光酶、FMN、NAD(P)H、长链脂肪醛(RCHO)、分子氧等。发光细菌合成的荧光酶可以催化还原型的黄素单核苷酸(FMNH2)和长链脂肪醛(RCHO,至少含8个C),并在O2的参与下发生氧化反应,产生的能量并不被生物体储存,而是通过光的形式释放出来。发光的代谢过程及原理见图1[7]。
有研究表明,发光基因(lux gene)系统中包括结构基因luxC,D,A,B,E和调节基因luxI和luxR等。从不同发光细菌中分离得到的发光基因其种类和数量有所差异,例如luxF仅发现于明亮发光杆菌,但以上五个结构基因luxC,D,A,B,E是普遍存在于已知的所有发光细菌中的。编码菌荧光素酶的基因是luxA和luxB,在lux操纵子中,luxA和luxB是紧密相连的。luxA luxB分别编码荧光酶的α(40 kD)和β(37 kD)亚基,形成的异二聚体即为具有产光能力的细菌荧光酶。而luxCDE分别编码依赖NADPH的醛蛋白还原酶(54 kD)、酰基转移酶(33 kD)和ATP合成酶(42 kD),三者共同构成脂肪酸还原酶复合体,产生长链脂肪醛作为发光反应的电子供体[8]。
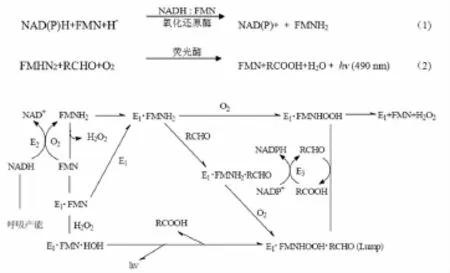
图1 发光细菌发光的代谢过程和原理图[9]
E1:细菌荧光素酶,由α、β 2个亚基组成,α为40000~42000D,β为37000~39000D。单独α、β亚基均无发光活性,只有α、β共存时才有活性。E2:NADH:FMN氧化还原酶,分子量为3000D,对FMN有高度特异性。E3:脂肪酸还原酶。
1.2 Microtox技术原理 发光细菌的发光现象是其正常的代谢活动,在一定条件下发光强度是恒定的。外来受试物(无机、有机毒物、抑菌、杀菌物等)与发光细菌接触时会使细胞的状态(包括细胞壁、细胞膜、电子的转移系统、酶及细胞质的结构)发生改变,其发光强度即有所减弱。变化的大小与受试物的浓度及毒性呈相关关系,浓度越高,毒性越强,抑制代谢作用越强,发光抑制率也就越高。通常认为外来受试物通过下面两个途径抑制细菌发光:1)直接抑制参与发光反应的酶类活性;2)抑制细胞内与发光反应有关的代谢过程(如细胞呼吸等)。利用发光细菌和LumiFox为检测系统可以检测样品的综合毒性。发光菌毒性测试是在20世纪70年代后兴起的一种微生物监测环境污染及检测污染物毒性的新方法。1978年美国Beckman公司即推出功能完备的生物发光光度计“Microtox”。自此这一急性毒性测试技术在世界范围内迅速推广。因此人们也将发光菌毒性测试称为Microtox测试。目前,市场上有许多测光仪器可供选择。国产的测光仪,大多适用于一般化学发光检测。由于发光细菌的发光是一种生物活体的发光,与单纯的化学反应导致的发光有所不同,如果不是处于最佳的响应波长范围内,就会大大影响检测的灵敏度和稳定性。故用专为发光细菌毒性检测用的测光仪,能保证结果的可靠性。专为发光细菌毒性检测用的测光仪一般都有配套的发光菌冻干粉,主要为进口仪器,如美国Bechman仪器公司Microtox、CheckLight公司ToxSreen、Merck公司ToxA-lert、荷兰SKaler公司ToxTracer、美国SDI公司Deltatox、芬兰BioTox、美国哈希LUMIStox300等。近年来,国内的北京滨松光子技术股份有限公司也研制出专门用于发光细菌急性毒性检测法的BHP9511检测仪[7]。其主要操作流程图如下:

图2 Microtox测试主要操作流程图[10]
2 适合于中药研究的Microtox技术测试方法及应用
2.1 实验方法 大多数中药本身颜色或者水不溶性可能对实验结果产生较大影响。我们通过实验认为,对于一些浑浊或具有颜色的样品,可选用具有色度和浊度的自动补偿功能的检测仪。
2.1.1 待测样品溶液制备 在1%~100%抑制率所落在的浓度范围内根据需要再增配6~12个浓度。将样品用蒸馏水稀释到各浓度,再将淡水样品与渗透压调节液以17∶3的比例混合,配制成待测样品溶液。样品每个浓度都设3个平行样(即3个测试管),分别取各浓度待测样品溶液1 mL到对应的干净的测试管中。
2.1.2 零标管(空白对照管)溶液制备 取1 mL复苏稀释液加入到每一个干净的测试管中,共3个测试管。
2.1.3 发光细菌冻干粉复苏 以费氏弧菌冻干粉(CS234)为例,根据费氏弧菌冻干粉的活性大小以及待测样品浓度的个数(零标管15 min测量的发光值在900在光值之间为宜),从冰箱冷冻室取3~5支冻干粉置于室温(20℃左右)平衡15 min。按每个测试管加0.05 mL冻干粉溶液,取合适量的复苏稀释液加入到平衡后的费氏弧菌冻干粉试剂瓶中,溶解后的冻干粉溶液应合并到一起,置于室温下10 min后用于测定样品。
2.1.4 样品发光度测定 用移液枪向各测试管中依次加入0.05 mL复苏后的冻干粉溶液,轻轻振荡,使之充分混匀,放置15 min后选择LU模式测定发光值(若样品有颜色干扰,则需开启色度校正功能),计算抑制率。
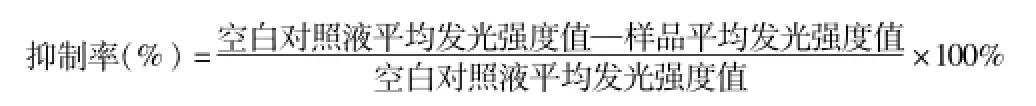
2.1.5 毒性参数的表示方法 1)标准毒物(如重铬酸钾、氯化汞、苯酚、硫酸锌等)浓度表示:当未经稀释的样品(即样品稀释度为100%)的抑光率在5%~95%时,也即相对发光强度在95%~5%范围内,可以用相同抑光率时标准毒物的浓度来表示样品的毒性。
2)EC50/IC50值表示:EC50/IC50值是指受试物对发光菌作用后,发光强度下降为对照组的50%时(即相对发光强度或抑光率为50%时)的受试物浓度。EC50/IC50值是评价化合物生态毒性的重要参数,也是评价毒物对生物体毒理学效应的常用参数,常用于表征受试物对发光菌的作用结果。EC50/IC50值越小表明受试物的毒性越大。
3)毒性剂量-效应动力曲线:可以直观反应药物的毒性效应动力学过程和作用特点。
4)毒性表达方法还应注明样品与发光菌作用的时间,因为作用时间也影响数值大小。发光菌作用时间10 min和作用15 min的数值是不同的,有时差异还很大,故必须表明作用的时间。一般可在数值表达后用括号加注作用时间,例如:EC50=0.10%(15 min),或抑光率45%(15 min),表明是15 min时实测数据。
2.2 Microtox技术在中药毒性生物评价的应用
2.2.1 中药、有毒中药毒性评价 我们提出一种基于Microtox技术的快速检测中药综合毒性的生物测试方法,包括如下步骤:1)制备测试用菌液:取发光细菌冻干粉,用氯离子浓度为0.1~1.0 mol/L的溶液复苏,得测试用菌液;2)检测:取待检中药样品,用测试用菌液检测,确定发光强度抑制率为50%的样品浓度以及浓度-效应动力曲线。本发明方法检测准确度和灵敏度均较高,操作简单。通过对雷公藤、苍耳子、吴茱萸、蛇床子、醋甘遂、醋商陆、贯众、马钱子、天南星、重楼等中药水提取物进行综合毒性测试,结果表明:1)本发明方法可以有效检测中药的综合毒性,获得定量化的IC50(抑制率为50%的样品浓度)、标准毒物参比值(如氯化汞参比,适合无法测试IC50的中、低毒性物质)、毒性剂量-效应动力曲线,可重复性好,再现性好,准确度高。2)不同中药IC50值差异较大,本发明方可以测出不同中药的毒性大小,可基于毒性剂量-效应动力曲线为中药的质量控制及安全性评价提供参考[11]。
2.2.2 在中成药、中药注射剂毒性评价 以中药注射剂为例,近年来随着中药注射剂临床应用的日趋广泛,不良反应报道亦日渐增多。从2006年“葛根素事件”“鱼腥草事件”到2008年的“刺五加事件”“茵栀黄事件”,再到2009年的“双黄连事件”和“清开灵事件”,让整个中药注射剂行业陷入信任危机。2006年之后,国家对中药注射剂安全问题的关注达到了前所未有的高度。2009年7月,国家食品药品监督管理局下发《关于做好中药注射剂安全再评价工作的通知》,全面开展生产及质量控制环节的风险排查切实控制中药注射剂安全隐患。目前,中药注射剂质量控制检测的项目包括:性状、鉴别、pH值、重金属、灼炽残渣、有关物质(蛋白质、鞣质、树酯、草酸盐、钾离子)、热原或细菌内毒素、无菌、装量、不溶性微粒、可见异物、含量测定、降压物质、异常毒性、过敏反应检查、溶血与凝聚、渗透压、有害元素、聚山梨酯80、5-HMF、指纹图谱、大分子蛋白检查等。但是,这些检测指标仍然无法有效的保证其药效的一致性和降低其不良反应的发生率。因此,有必要引入新的质量控制方法。我们提出一种基于Microtox技术的快速检测中药注射剂综合毒性的生物测试方法,确定发光强度抑制率为50%的稀释度以及浓度-效应动力曲线。通过鱼腥草注射液、红花注射液的实验说明,对于用传统方法检测质量均合格的中药注射液,我们的发明方可以测出其毒性有大有小,能够较好地解释现有中药注射液不良反应不一致的现象。可见,本发明毒性检测方法的检测速度快,操作简单,反应灵敏,准确度高,可以检测中药注射液的毒性,为中药注射液的质量控制提供依据,应用前景良好[12-14]。
2.2.3 药物联合作用 当待测生物暴露在混合污染物中时,由于混合物中各组分相互影响,会产生联合毒性作用,表现为加和作用、协同作用和拮抗作用。为了深入了解重金属混合物的联合毒性对发光细菌的作用,利用淡水发光细菌——青海弧菌Q67(Vibrio qinghaiensis sp.nov-Q67)发光值的测定方法,采用联合毒性单位法,在测定了硝酸镉、重铬酸钾和硝酸铅单一毒性EC50的基础上,对硝酸镉+重铬酸钾、硝酸镉+硝酸铅、硝酸铅+重铬酸钾3种重金属二元混合物的联合毒性进行了评价。结果表明,硝酸镉+重铬酸钾、硝酸铅+重铬酸钾是拮抗作用,硝酸铅+硝酸镉是协同作用[15]。采用二次二因子回归通用旋转组合实验设计,以明亮发光杆菌(photobacterium phosphoreum)T3变种作为毒性测试物种,研究了多菌灵+氟硅唑、甲氨基阿维菌素+阿维菌素和二氯喹啉酸+莎稗磷等二元农药混合物的联合毒性和主因子作用,建立了3个相应的数学模型。结果表明,多菌灵、氟硅唑、甲氨基阿维菌素、阿维菌素、二氯喹啉酸和莎稗磷等农药对明亮发光杆菌的毒性有显著的正效应[16]。3个二元农药混合物的联合毒性作用不同,总体上,多菌灵与氟硅唑以拮抗作用为主,而甲氨基阿维菌素与阿维菌素以相加作用为主,二氯喹啉酸与莎稗磷以协同作用为主。从单因子作用效应的角度看,对相对发光强度的影响:多菌灵大于氟硅唑、阿维菌素大于甲氨基阿维菌素,莎稗磷大于二氯喹啉酸。发光细菌法作为一种快速、操作方便、成本低廉的生物监测方法,将在农产品污染物毒性评价和农产品安全快速检测中有着广泛的应用前景[17]。有用明亮发光杆菌分别检测甘草及其配伍药物的抑光率、川乌及其配伍药物的抑光率、藜芦及其配伍药物的抑光率。结果三组配伍药的抑光率均相等或低于单味药物的抑光率。证实“十八反”的药物配伍后的毒性没有增加或有所减低[18]。运用了“明亮发光杆菌502测定”“十八反”药物的毒性,研究结果支持“十八反”配伍毒性并不增加,相反有些毒性有所降低的结论[19]。
3 方法学评价与前景展望
1)目前,物质毒性的常规检测还是以理化指标检测方面为主,而对综合毒性的考虑较少;若要回答对人群健康的影响,则必须用生物医学的方法对毒性进行分析判断,而传统的医学毒理学实验是以受试生物的死亡数来判断毒性的大小,一般需要几天的时间才能有结果,而且个体差异大,影响因素多,导致动物消耗量过大、测定结果在不同国家不同实验室存在很大波动等问题。
2)Microtox技术用于中药毒性检测具有以下特点:a.发光细菌同高等动物有着类似的物理化学特性和酶作用过程等特点,凡能干扰或破坏发光细菌呼吸、生长、新陈代谢等生理过程的有毒有害物质等都可以运用发光细菌法检测生物毒性,故是一种综合毒性检测方法;b.方法客观、可靠、快速,国际公认,操作简单方便,结果易于重复;c.对毒物反应灵敏(要比一般生物细胞反应灵敏几个数量级);d.试验所用的细菌数量大(达数百万),个体差异可以忽略不计;e.可同时获得多个定量参数,IC50(抑制率为50%的样品浓度)、标准毒物参比值(如氯化汞参比,适合无法测试IC50的中、低毒性物质)、毒性剂量-效应动力曲线等,既可以作为受试药物毒效生物指纹图谱,又可以测试其毒性效能和效强,综合表征药物毒性特点;f.特别适用有毒中药、中药注射剂以及药物联合毒性作用的快速评价。
3)探索和应用快速、敏感、可靠的新型毒性测试技术已经成为中药毒性和安全性评价领域的技术瓶颈和大势所趋。现行的美国ASTM标准(D-5660)《通过对海洋发光细菌进行毒性试验而对遭化学污染的水和土壤进行微生物解毒予以评估的标准试验方法》,美国环保局(EPA)饮用水毒性测试协议(WET)认可,欧盟ISO11348-3《水质测定——水样对于发光细菌的抑制效应测定》,中国国标GB/T15441-1995《水质急性毒性的测定发光细菌法》均提示Microtox技术作为高效的毒性测试方法的广泛应用前景。我们有理由相信,未来在进一步改善和完善专门针对中药的Microtox技术系统基础上,这种任何人都能简单地用这种技术而且只需要很短时间完成标准化检测,将可能是复杂成分中药毒性和安全性快速检测、安全性评价以及风险分级评定的重大突破。
[1]赵军宁,叶祖光.传统中药毒性分级理论的科学内涵与《中国药典》(一部)标注修订建议[J].中国中药杂志,2012,37(15):2193-2198.
[2]赵军宁,杨明,陈易新,等.中药毒性理论在我国的形成与创新发展[J].中国中药杂志,2010,35(7):922-927.
[3]赵军宁,鄢良春,宋军.建立以"功效"为核心的新型中药质量评价模式[J].中药药理与临床,2010,26(5):158-161.
[4]赵军宁,叶祖光.中药毒性理论与安全性评价[M].北京:人民卫生出版社,2012.
[5]赵军宁,朱家谷,叶祖光.中药毒性和安全性试验方法,见:陈奇主编.中药药理研究方法学[M].3版,北京:人民卫生出版社,2011:107-109.
[6]Girotti S,Ferri EN,Fumo MG,et al.Monitoring of environmental pollutants by bioluminescent bacteria[J].Analytica Chimica Acta,2008,608(1):2 -29.
[7]朱文杰,郑天凌,李伟民.发光细菌与环境毒性检测[M].北京:中国轻工业出版社,2009.
[8]Meighen EA.Molecular biology of bacterial bioluminescence[J].Microbiological Review,1991,55(1):123-142.
[9]大连理工大学环境与生命学院.发光细菌法急性毒性的测定.http://netclass.dlut.edu.cn/uploads/063/files,2010-08-06.
[10]北京滨松光子技术股份有限公司.发光细菌.http://www.bhphoton. com/product/pdf/fgxjy,2010-07-10.
[11]赵军宁,鄢良春,郑晓秋,等.一种快速检测中药综合毒性的生物测试方法[P],中国:201310572953.0,2013-11-18.
[12]赵军宁,鄢良春,郑晓秋,等.一种快速检测中药注射液综合毒性的生物检测方法[P],中国:201310210195.8,2013-05-31.
[13]赵军宁,鄢良春,郑晓秋,等.一种快速检测鱼腥草注射液综合毒性的生物检测方法[P],中国:201310369652.8,2013-08-23.
[14]赵军宁,鄢良春,郑晓秋,等.一种快速检测红花注射液综合毒性的生物检测方法[P],中国:201310572952.X,2013-11-18.
[15]熊蔚蔚,吴淑杭,徐亚同,等.等毒性配比法研究镉、铬和铅对淡水发光细菌的联合毒性[J].生态环境,2007,16(4):1085-1087.
[16]吴淑杭,周德平,徐亚同,等.二元农药混合物对发光细菌的联合毒性研究[J].农业环境科学学报,2008,27(5):2028-2032.
[17]董玉瑛,邹学军,陈峥,等.三种药品联合毒性作用及其环境风险分析[J].环境化学,2013,32(7):1257-1262.
[18]杨安泰,张丽英,金彩琪,等.用发光细菌研究中药”十八反”[J].上海中医药杂志,1989,(6):2-4.
[19]沈光稳.采用发光细菌研究探讨“十八反”配伍药物的临床毒性[J].中医药研究,1998,14(1):10.
(2014-01-06收稿 责任编辑:洪志强)
Microtox-based fast Testing Method of Comprehensive toxicity of Traditional Chinese Medicine
Zhao Junning,Yan Liangchun
(Sichuan Academy of Traditional Chinese Medicine,Chengdu 610041,China)
Microtox technology is one of the fastest testing methods for determining the poisonous or toxic substances which use Luminous bacteria as a indicator organism.Our research reviews the development of microtox technology,and application for testing toxicity of Chinese medicinal materials,including technical methods,technical maps,key issues and scope of work.Our research serves as foundation for establishing a new safety and risk analysis system by providing a fast test method of TCM toxicity.
Traditional Chinese Medicine;Microtox Technology;Luminous bacteria;Toxicity;Biological evaluation
R285.5
A
10.3969/j.issn.1673-7202.2014.02.003
国家重点基础研究发展计划(973计划)项目(编号:2009CB522801),国家支撑计划项目(编号:2012BAI29B10),“重大新药创制”科技重大专项项目(编号:2011ZX09401-304),国家自然基金面上项目(编号:81073047),四川省科技支撑计划项目(编号:2013sz0115)
赵军宁,研究员,博士,博士生导师,从事中药药理(毒理)、中药质量生物控制以及道地药材系统研究开发,Tel:(028)85226120,E-mail:zarmy@189.cn

