不同浸提介质对医用护理垫体外细胞毒性评价的影响
刘春丽 苏小军 方菁嶷 苏锋 宁萍
1 苏州大学卫生与环境技术研究所(苏州 215123)
2 苏州大学医学部(苏州 215123)
医用护理垫因具有超强吸收力,透气性能好,柔软舒适,保持床单整洁干净,预防并发症等优点广泛应用于临床,同时其生物安全性也逐渐引起人们的注意。体外细胞毒性实验是生物安全性评价的重要组成部分,是评价直接或间接接触人体组织和细胞的医疗器械和材料的通用方法。浸提液实验是目前用于检测医疗器械和材料的细胞毒性比较广泛的一种方法,选择不同的浸提介质可能对实验结果有直接的影响。目前标准推荐的浸提介质有:含血清培养基、无血清培养基、生理盐水溶液以及其他适宜的溶剂。本实验根据ISO 10993-5:2009[1]的试验原则和评价标准,采用不同的浸提介质制备了医用护理垫浸提液,用MTT 比色法评价不同的浸提介质对细胞L929 毒性的影响。
1.材料与方法
1.1 试验材料
L929 小鼠成纤维细胞株,购自中国科学院上海细胞所,CO2细胞培养箱(Thermo Forma),倒置相差显微镜(Lecia),酶标仪(Bio-tek),含/不含酚红MEM 培养液(Gibco),胎牛血清(Gibco),胰酶(Gibco),青链酶素(Gibco),MTT(Sigma),异丙醇(国药集团化学试剂有限公司)。
1.2 试验方法
1.2.1 实验设计与分组
A 浸提介质组,含10%胎牛血清的MEM 培养基;B 浸提介质组,MEM 培养基,浸提结束补充10%的胎牛血清;C 浸提介质组,MEM 培养基,浸提结束用含20%胎牛血清的2×MEM 做1:1稀释;D 浸提介质组,0.9%NaCl 注射液,浸提结束用含20%胎牛血清的2×MEM 做1:1 稀释。浸提结束立刻用于实验,浸提液浓度设100%、75%、50%、25%四个剂量。每组均设实验组、阴性对照组(高密度聚乙烯)、阳性对照组(含0.4% 苯酚的相应浸提介质)和空白对照组,各组设5 个平行孔。
1.2.2 浸提液的制备
护理垫厚度为1mm,根据ISO 10993-5:2009和ISO 10993-12:2009[2],护理垫按3 cm2/ml 分别浸入A、B 浸提介质;护理垫按1.5 cm2/ml 分别浸入C、D 浸提介质,置于37˚C 浸提24h 后备用。同法制备阴性对照和阳性对照。
1.2.3 MTT 比色法
将L929 细胞培养在含10%胎牛血清和抗生素(青霉素100 U/ml,链霉素100 µg/ml)的MEM 培养液中,取对数生长期的细胞,用胰酶消化制备成单细胞悬液,离心(200g,3min),将细胞重新分散于培养基中,调整细胞密度为1×105个/ml;接种上述细胞悬液到96 孔培养板中,每孔100 µL,置37˚C,5% CO2培养箱中培养24h;待细胞贴壁后吸出原来的培养液,分别加入100 µl 不同浓度护理垫浸提液(100%、75%、50%、25%)、空白对照液、阳性对照和阴性对照液(100%),培养24h 后,取出96 孔板置倒置显微镜下观察细胞形态。吸出原来的培养液,每孔加50μL MTT(1mg/ml),继续培养2h 后弃去孔内液体,加入100 μL 异丙醇,置振荡器上振荡10min,在酶标仪上以570nm 为主吸收波长,650nm 为参考波长测定吸光度值。按以下公式计算细胞存活率:Viab.%=试验组(阴性、阳性组)吸光度值×100/空白组吸光度值。
1.2.4 数据处理
数据以平均值±标准差(mean±SD)表示,采用SPSS 11.0 统计软件包对数据进行分析,数据的比较采用单因素方差分析,P<0.05 差异有统计学意义。
1.2.5 评价标准
根据ISO 10993-5:2009,样品50%浸提液的细胞存活率应大于或等于100%浸提液的细胞存活率,试验成立,否则应重复试验。试验品100%浸提液的细胞存活率小于空白组70%,说明样品具有潜在的细胞毒性。
2.结果
2.1 细胞形态学结果
加样后24 h 镜下观察空白组和阴性对照组,细胞形态呈长条梭形或不规则多边形,细胞贴壁良好,无空泡,细胞大量增殖。阳性对照组细胞变圆、胞核固缩或裂解死亡,细胞数量无明显增加。护理垫A 浸提介质组(100%浸提液)细胞部分变圆,细胞数量明显低于阴性对照组,细胞生长受到明显抑制。B、C、D 浸提介质组(100%浸提液)细胞数量和阴性对照组与空白组比较无明显差异,见图1。
2.2 MTT 比色法结果
MTT 比色法测定加样后24h 的细胞存活率见表1。各阳性对照组细胞存活率为7.5%左右,阴性对照组细胞存活率均大于95%,各实验组50%浸提液组细胞存活率均高于同组100%浸提液组细胞存活率,说明本实验体系适用于该试验样品细胞毒性的判定。从表1 看出,A 浸提介质组细胞存活率为68.6%,与空白组和阴性对照组比较,细胞存活率明显降低,差异有统计学意义(P<0.05)。B、C、D 浸提介质组细胞存活率差别不大,都在90%左右,差异无统计学意义(P>0.05)。以上结果说明用不同的浸提介质浸提医用护理垫,对其体外细胞毒性结果有直接影响。
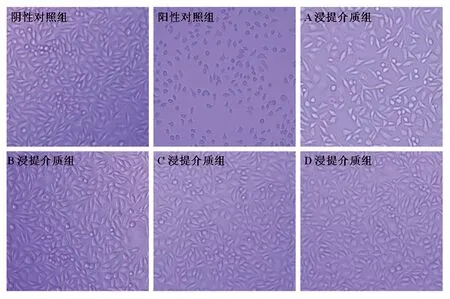
图1.L-929 细胞与4种浸提介质及对照组共培养24 h 的细胞形态(倒置相差显微镜,×100)
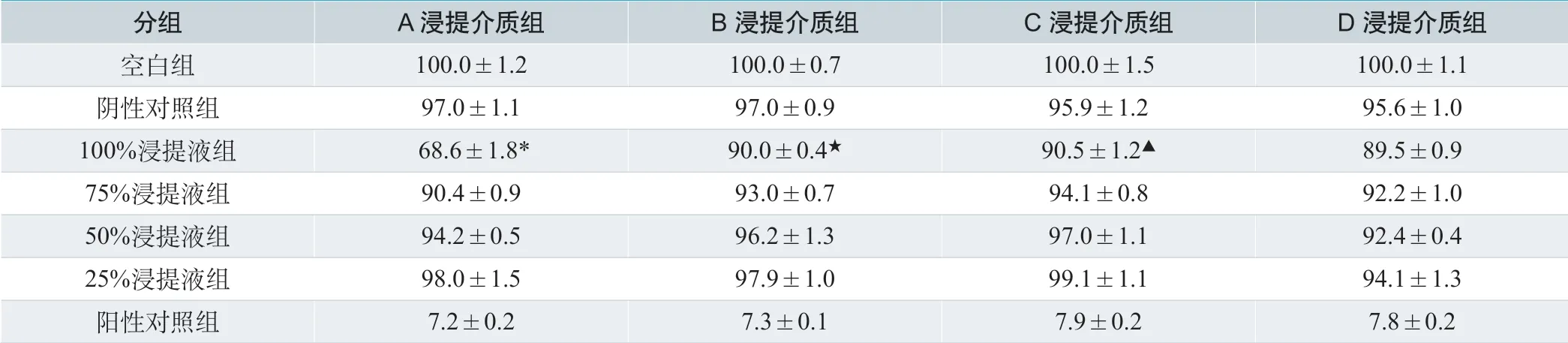
表1.护理垫各组加样后24h 的细胞存活率(mean±SD,n=5)
3.讨论
目前医用护理垫广泛地应用于临床,适用于医院手术,瘫痪病人,大小便失禁,产妇护理等。为保证其使用的安全性,选择合适的方法进行生物学评价是必要的步骤。体外细胞毒性实验具有操作简单、易标准化、周期短、敏感性强且能定量分析等优点,是医疗用品生物安全性评价体系中最重要的检测指标之一。目前GB/T16886.5-2003[3]和ISO 10993-5:2009 中规定了3 类试验方法,即浸提液试验、直接接触试验以及间接接触试验。浸提液实验是将样品材料浸提液直接加入到细胞培养器皿,与细胞共培养一段时间,观察浸提液中的溶出物对细胞毒性的影响。研究者认为医用材料中一些易溶出物质是引起毒性反映的主要原因。根据国内外评价标准,浸提介质可选择含/不含血清培养基、生理盐水等。
在医用材料生物学评价的具体实践中,浸提介质的选择对细胞毒性评价结果的影响是否存在差异目前相关文献报道不多。为探索不同浸提介质对评价结果的影响,本实验采取浸提试验,制备不同浸提介质的浸提液,用ISO 10993-5:2009附录C 规定的MTT 比色法来评价护理垫的细胞毒性。我们在试验中发现,A 浸提介质组使细胞生长受到明显抑制,细胞存活率相对于空白组仅为68.6%,根据ISO 10993-5:2009 的判断标准,样品具有潜在细胞毒性,而B、C、D 浸提介质组与各自空白组比较,细胞大量增殖,生长状态良好,细胞存活率均在90%左右。以上结果说明护理垫用不同的浸提介质处理,对评价其细胞毒性结果存在差异。分析可能的原因是血清在浸提前、后加入导致:A 浸提介质组为含血清培养基,在浸提时加入和护理垫相互作用;B 浸提介质组是不含血清的培养基,浸提结束补加入10%的血清。C、D 浸提介质组分别是不含血清培养基和生理盐水,浸提结束后用含20%血清的2×MEM培养基等比稀释。血清的主要作用是提供氨基酸、维生素等细胞生长必须的营养物质;提供激素和各种生长因子;提供结合蛋白;提供促接触和伸展因子使细胞体壁免受机械损伤。因此血清在一定程度上可促进细胞增殖[4]。护理垫一般由三部分组成,顶层是亲水无纺布,吸水层是木浆棉和高分子吸水树脂,底层是防漏PE/PP 膜。我们推测护理垫在浸提过程中,吸水层的木浆棉和高分子吸水树脂吸附了部分血清中的促细胞生长因子,使细胞增殖能力降低。而B、C、D 浸提介质组血清在浸提结束后补充加入,其成分和浓度不受浸提过程的影响而发生变化,仍能促进细胞生长。对于医用护理垫,不同浸提介质其细胞毒性结果不一致,是否是血清和吸水层造成的差异还需要进一步实验验证。
Oshima[5]认为不同的浸提条件和浸提方式所制备的材料溶出物在细胞敏感程度上并无显著差异。邝辉等[6]评价了不同的浸提介质对一次性使用球囊扩张导管体外细胞毒性的影响,发现不同浸提液之间的OD 值虽然存在差异,但不影响该产品的细胞毒性分级。浸提是一个复杂的过程,受时间、温度、表面积与体积比、浸提介质以及材料的相平衡的影响。由于医用材料的多样性,直接或间接接触人体引起体内环境的变异性,材料与机体作用的复杂性等,因此根据医用材料本身的理化特性及其用途,正确选择试验方法及相关参数是十分重要的。本试验认为,在评价医用材料的细胞毒性时,一定要注明所选择的试验参数和浸提介质,对于医用护理垫,如何更科学、更准确地评价其细胞毒性有待进一步研究。
[1]ISO 10993-5:2009,Biological evaluation of medical devices – Part 5:Tests for in vitro cytotoxicity[s].
[2]ISO 10993-12:2009,Biological evaluation of medical devices – Part 12:Sample preparation and reference materials[s].
[3]中华人民共和国国家质量监督检验检疫总局.GB/T16886.5-2003 医疗器械生物学评价第5 部分体外细胞毒性试验[S].
[4]司徒镇强,吴军正,细胞培养[M].世界图书出版社,2007:2009.
[5]Oshima H,Nakamura M.A study on reference standard for cytotoxicity assay of biomaterials[J].Biomed Mater Eng,1994,4(4):327.
[6]邝辉,刘尧,曹苹,等.不同浸提介质对一次性使用球囊扩张导管体外细胞毒性评价的影响[J].生物医学工程研究,2011,30(2):113-115.

