黄连解毒汤不同组分群对热毒血瘀证大鼠的影响
杜巧辉,谢晓芳,彭成,曹小玉,龚小红,贺抒,周彦希
·药理毒理·
黄连解毒汤不同组分群对热毒血瘀证大鼠的影响
杜巧辉1,2,谢晓芳1,2,彭成1,2,曹小玉2,龚小红1,2,贺抒1,2,周彦希1,2
目的:探讨黄连解毒汤各组分群对热毒血瘀证大鼠的影响。方法:采用内毒素与角叉菜胶联合制备大鼠热毒血瘀模型,分别灌胃黄连解毒汤水提物、总生物碱、总黄酮和总环烯醚萜后,观察不同组分群对热毒血瘀模型大鼠一般状态、血象和血液流变学的影响。结果:造模后大鼠一般状态差,有便溏等表现,白细胞有升高,全血粘度、红细胞压积、全血低切相对指数均明显升高(P<0.05或P<0.01);各预防给药组可明显改善大鼠的一般状态,使模型大鼠的血液全血粘度、压积明显降低,总生物碱还能明显降低全血高切还原粘度(P<0.05或P<0.01)。结论:黄连解毒汤水提物、总生物碱、总黄酮和环烯醚萜均对热毒血瘀证大鼠具有一定治疗作用,可改善其热毒症状,改善血液流变性,其中总生物碱是主要活性组分群。
黄连解毒汤;热毒血瘀;有效成分群
黄连解毒汤由黄连、黄芩、黄柏、栀子组成,处方首载于葛洪《肘后备急方》而无方名,至唐代王焘在《外台秘要》引崔氏方始冠以此名。本方为治疗外感邪气入里化火之实热证的清热解毒代表方。现代药理研究发现黄连解毒汤具有抗炎、抗菌、抗氧化、降血糖和血脂、抗脑缺血和抗肿瘤等作用[1~4]。中医认为热蕴血分容易造成血瘀,是引起血瘀证的主要病因之一。热盛伤津耗液使血液黏稠,热盛灼伤脉络使血行不利,热盛迫血妄行使血液离经,热盛阻遏气机以致气滞,这些过程均表明热毒可致血瘀。因此,笔者认为除抗菌、抗炎、解热等药理作用外[5],黄连解毒汤清热解毒的本质还可能表现在对血液系统的调节。因此,本文采用角叉菜胶和脂多糖联合诱导的大鼠热毒血瘀证模型[6],探讨黄连解毒汤对热毒血瘀证大鼠的治疗作用。
1 材料
1.1 仪器
全自动血球仪MEK-6318K(日本光电株式会社);分析天平(上海舜宇恒平科学仪器有限公司,JA1003);恒温水浴锅;凡士林等。
1.2 药物及试剂
黄连解毒汤总生物碱,黄连解毒汤总黄酮,黄连解毒汤总环烯醚萜,黄连解毒汤水提物,含生药量分别为90 g.g-1,80 g.g-1,50 g.g-1,5 g.g-1,均由中国中医科学院中药研究所提供。分别用蒸馏水配成6.1 g.L-1,6.9 g.L-1,11 g.L-1,110 g.L-1的混悬液保存备用;阿司匹林泡腾片(Astrazeneca公司,产品批号:1101083)用生理盐水配成0.02 g.mL-1;内毒素(Escherichia coli O55:B5,Sigma公司,L8880)用生理盐水稀释成50 mg.L-1;角叉菜胶(Carragenan,Sigma公司,产品批号:1001245633)用生理盐水配成10 g.L-1,沸水浴使之完全溶解后使用。
1.3 动物
SD大鼠,SPF级,全雄,体重(200±20)g, 由成都中医药大学实验动物研究中心提供,动物质量许可证号SCXK(川)2008-11。实验环境:成都中医药大学国家中医药管理局中药药理科研三级实验室,编号:TCM-2009-315,环境温度18-22℃。
2 方法
2.1 分组及给药
取健康、合格SPF级雄性大鼠56只,随机分成正常对照组、模型对照组、阿司匹林组、总生物碱组、总黄酮组、总环烯醚萜组和水提物组,每组8只。禁食不禁水12 h后,各组开始灌胃相应药液,给药剂量均为10 mL.kg-1,其中黄连解毒汤水提物和各组分群给药量均相当于黄连解毒汤5.5 g.kg-1;正常对照组和模型对照组均灌胃生理盐水,每日1次,连续5天。
2.2 模型建立
末次给药5 h后,除正常对照组外其余各组开始造模,即先腹腔注射角叉菜胶溶液2.5 mL.kg-1,8 h后尾静脉注射LPS溶液1 mL.kg-1;正常对照组均注射等剂量生理盐水。以注射LPS时为造模0 h,以尾部出现明显,肉眼可见的血栓为造模成功。
2.3 指标测定
从造模开始观察大鼠的一般状态。造模2 h时,眼眶采血测定血常规;造模6 h后,对各组大鼠股动脉取血测定血液流变学。
2.4 统计学分析
以上数据均采用SPSS17.0 统计软件包建立实验结数据库并进行分析,定量资料以均值±标准差()表示,多样本均数的比较采用one-way ANOVA分析,P<0.05为差异有统计学意义。
3 实验结果
3.1 对一般情况的影响
造模后大鼠主要表现为:耸毛,扎堆,闭目少动,反应迟钝,张口呼吸,精神萎靡,或有二便失禁,便溏稀,四肢瘫软无力。症状多在注射LPS后5~10 min出现,逐级加重。模型组大鼠尾部均出现明显血栓,长度1-15cm不等,严重者全尾均呈明显黑色血栓,各给药组大鼠在预防给药5天后,以上症状有所缓解,尾部血栓出现时间延迟,且血栓长度相对短。
3.2 对大鼠血常规的影响
由表1可见,模型大鼠在造模2 h后表现为WBC升高,主要以Lymph和Gran升高为主,而PLT、RBC呈下降趋势;经治疗后阿司匹林组大鼠PLT进一步减少(P<0.05),但其余各组对血常规无明显影响。
表1 黄连解毒汤各组分群对热毒血瘀证大鼠血常规的影响()
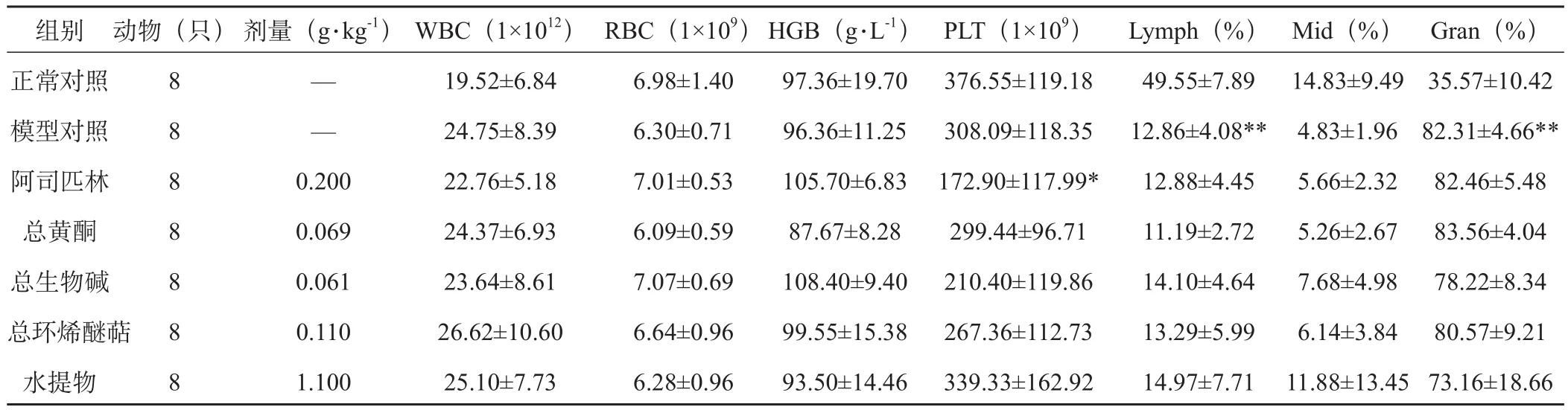
表1 黄连解毒汤各组分群对热毒血瘀证大鼠血常规的影响()
注:与模型对照组比较,*P<0.05,**P<0.01
组别 动物(只) 剂量(g.kg-1) WBC(1×1012) RBC(1×109) HGB(g.L-1) PLT(1×109) Lymph(%) Mid(%) Gran(%)正常对照 8 — 19.52±6.84 6.98±1.40 97.36±19.70 376.55±119.18 49.55±7.89 14.83±9.49 35.57±10.42模型对照 8 — 24.75±8.39 6.30±0.71 96.36±11.25 308.09±118.35 12.86±4.08** 4.83±1.96 82.31±4.66**阿司匹林 8 0.200 22.76±5.18 7.01±0.53 105.70±6.83 172.90±117.99* 12.88±4.45 5.66±2.32 82.46±5.48总黄酮 8 0.069 24.37±6.93 6.09±0.59 87.67±8.28 299.44±96.71 11.19±2.72 5.26±2.67 83.56±4.04总生物碱 8 0.061 23.64±8.61 7.07±0.69 108.40±9.40 210.40±119.86 14.10±4.64 7.68±4.98 78.22±8.34总环烯醚萜 8 0.110 26.62±10.60 6.64±0.96 99.55±15.38 267.36±112.73 13.29±5.99 6.14±3.84 80.57±9.21水提物 8 1.100 25.10±7.73 6.28±0.96 93.50±14.46 339.33±162.92 14.97±7.71 11.88±13.45 73.16±18.66
3.3 对大鼠血液流变性的影响
由表2可见,经造模后模型对照组大鼠全血粘度、压积、和全血低切相对指数均明显升高,与正常对照组比较有显著性差异(P<0.05);与模型对照组比较,黄连解毒汤水提液及总生碱、总黄酮均明显降低全血粘度,总生物碱、总黄酮和总环烯醚萜明显降低压积,且总生物碱和总黄酮还降低全血高切还原粘度,阿司匹林亦明显降低全血粘度和压积,均有显著性差异(P<0.05)。
表2 黄连解毒汤各组分群对热毒血瘀证大鼠血液流变性的影响()
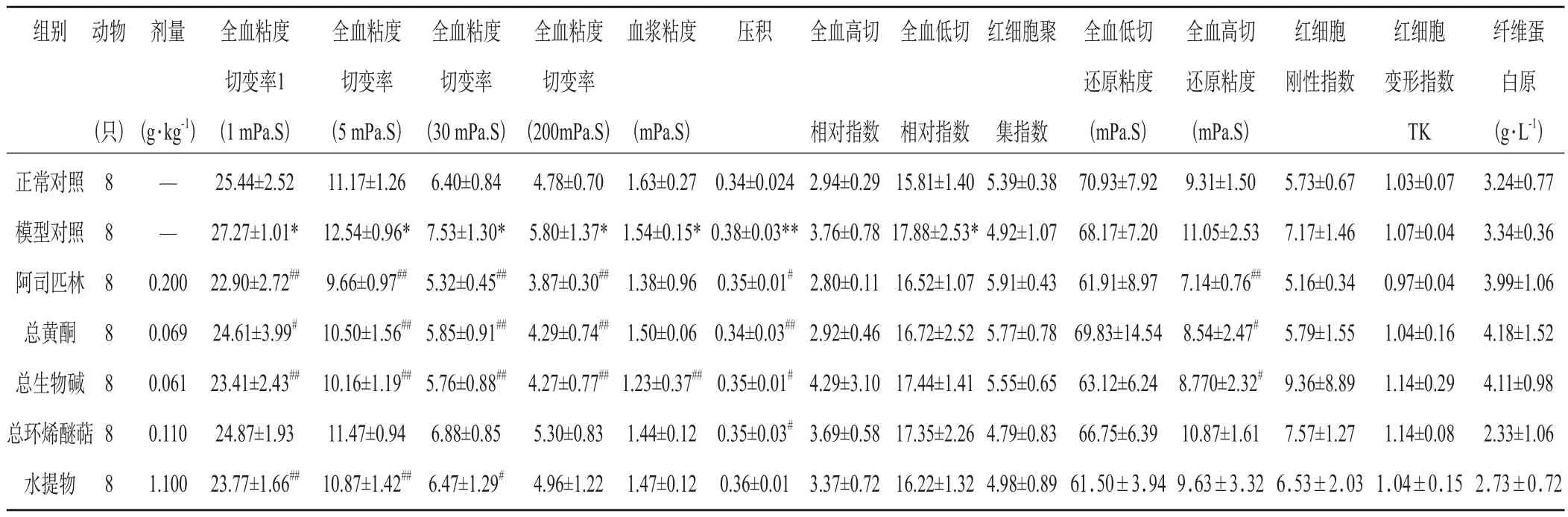
表2 黄连解毒汤各组分群对热毒血瘀证大鼠血液流变性的影响()
注:与正常对照组比较,*P<0.05,**P<0.01;与模型对照组比较,#P<0.05,##P<0.01
组别 动物 剂量 全血粘度 全血粘度 全血粘度 全血粘度 血浆粘度 压积 全血高切 全血低切 红细胞聚 全血低切 全血高切 红细胞 红细胞 纤维蛋切变率1 切变率 切变率 切变率 还原粘度 还原粘度 刚性指数 变形指数 白原(只) (g.kg-1) (1 mPa.S) (5 mPa.S) (30 mPa.S) (200mPa.S) (mPa.S) 相对指数 相对指数 集指数 (mPa.S) (mPa.S) TK (g.L-1)正常对照 8 — 25.44±2.52 11.17±1.26 6.40±0.84 4.78±0.70 1.63±0.27 0.34±0.024 2.94±0.29 15.81±1.40 5.39±0.38 70.93±7.92 9.31±1.50 5.73±0.67 1.03±0.07 3.24±0.77模型对照 8 — 27.27±1.01* 12.54±0.96* 7.53±1.30* 5.80±1.37* 1.54±0.15* 0.38±0.03** 3.76±0.78 17.88±2.53* 4.92±1.07 68.17±7.20 11.05±2.53 7.17±1.46 1.07±0.04 3.34±0.36阿司匹林 8 0.200 22.90±2.72##9.66±0.97##5.32±0.45##3.87±0.30##1.38±0.96 0.35±0.01#2.80±0.11 16.52±1.07 5.91±0.43 61.91±8.97 7.14±0.76##5.16±0.34 0.97±0.04 3.99±1.06总黄酮 8 0.069 24.61±3.99#10.50±1.56##5.85±0.91##4.29±0.74##1.50±0.06 0.34±0.03##2.92±0.46 16.72±2.52 5.77±0.78 69.83±14.54 8.54±2.47#5.79±1.55 1.04±0.16 4.18±1.52总生物碱 8 0.061 23.41±2.43##10.16±1.19##5.76±0.88##4.27±0.77##1.23±0.37##0.35±0.01#4.29±3.10 17.44±1.41 5.55±0.65 63.12±6.24 8.770±2.32#9.36±8.89 1.14±0.29 4.11±0.98总环烯醚萜 8 0.110 24.87±1.93 11.47±0.94 6.88±0.85 5.30±0.83 1.44±0.12 0.35±0.03#3.69±0.58 17.35±2.26 4.79±0.83 66.75±6.39 10.87±1.61 7.57±1.27 1.14±0.08 2.33±1.06水提物 8 1.100 23.77±1.66##10.87±1.42##6.47±1.29#4.96±1.22 1.47±0.12 0.36±0.01 3.37±0.72 16.22±1.32 4.98±0.89 61.50±3.94 9.63±3.32 6.53±2.03 1.04±0.15 2.73±0.72
4 讨论
本课题所选用的角叉菜胶联合LPS引起的热毒血瘀模型由梁爱华等[6]创建,以尾部血栓出现为模型表征,并在急性期(2-8 h)TNF-α、IL-6的表达明显升高和凝血酶原时间、白细胞、全血粘度、白细胞粘附分子CD11b、CD18、TXB2等指标的明显改变,类似于中医热毒瘀证[7~8]。本实验中模型组大鼠尾部均出现显著的血栓,结合实验中所测的指标表明模型建立成功。现代药理研究表明,黄连解毒汤对β-内酰胺类抗生素耐药的大肠杆菌和埃希菌均有一定程度的逆转作用[9],并对LPS引起的发热有一定的解热作用[10~12]。而对于LPS等外源性致热源引起的发热中,TNF和IL家族的细胞因子起着重要作用[13~14]。可直接刺激血管内皮细胞或影响内皮素等释放而引起血液流变性异常。本研究结果显示,黄连解毒汤不同组分群预防给药,可减轻LPS所致大鼠热毒症状,并能改善其血液流变性,表明各提取物均有清热活血作用,机制有待进一步研究。总体来看,总生物碱和总黄酮均为有效组分群,又以总生物碱为主。
[1] 王利津,徐强. 黄连解毒汤的抗炎作用机理研究[J]. 中国中药杂志,2000, 25(8):493.
[2] 汪长中,程惠娟,徐颖,等. 黄连解毒汤及其单味药对体外白念珠菌生物膜影响的比较[J].上海中医药杂志,2008,42(2):63.
[3] 孙冬梅,邝枣园,李岩,等.黄芩苷对耐药性金黄色葡萄球菌的抑菌作用研究[J].吉林医学,2011,32(13):2587.
[4] 宋珏,路通,谢林,等.以血清药理学方法研究黄连解毒汤对小鼠的药效动力学[J].中草药,2005,36(5):709.
[5] 赵保胜,刘永刚,王秀丽.黄连解毒汤解热、抗炎作用研究[J].中国实验方剂学杂志,2009,15(11):55.
[6] 梁爱华,刘婷,李春英,等. 一种热毒诱导的血栓形成动物模型的建立[J].中国中药杂志,2008,33(18):2124.
[7] 梁爱华,于长安,李春英,等.内毒素与角叉菜胶联合诱导的血栓形成模型的动物差异性比较[J].中国中药杂志,2006,31(1):57.
[8] 梁爱华,丁晓霜,李文,等.血瘀证与血栓形成病证结合动物模型的研究[J].中国中药杂志,2005,30(20):1613.
[9] 芦亚君,程宁.3种中药方剂逆转大肠杆菌耐药性的实验观察[J].西北药学杂志,2007, 22(6):309.
[10] 朱兆荣,刘娟,杨敏,等.黄连解毒汤对大肠杆菌内毒素致仔鸭发热的影响[A].中国《活兽慈舟》学术研讨会论文集[C],2013.
[11] 郭月,于庆海,张毅.黄连解毒汤实验药理研究[J].中成药, 1993,15(8):29.
[12] 曹于平,皋聪,孙继红.黄连解毒汤提取物的药理作用研究[J].中国药科大学学报,1996,27(10):605.
[13] Conti B, Tabarean I, Andrei C, Bartfai T. Cytokines and fever[J]. Front Biosci, 2004,1(9): 1433.
[14] 韩旭华,牛欣,阎妍,等.龙答草喷雾剂的解热作用及对肿瘤坏死因子的影响[J].中华中医药杂志,2005,20(8):469.
(责任编辑:陈思敏)
Study of the infuence of active components groups extracted from Huanglian Jiedu decoction on rats with pattern of toxic heat-induced blood stasis
DU Qiao-hui1,2, XIE Xiao-fang1,2, PENG Cheng1,2, CAO Xiao-yu2, GONG Xiao-hong1,2, He-
Shu1,2, ZHOU Yan-xi1,2//(1. Pharmacy College, Chengdu University of Traditional Chinese Medicine; The Ministry of Education Key Laboratory of Standardization of Chinese Herbal Medicine; State Key Laboratory Breeding Base of Systematic Research, Development and Utilization of Chinese Medicine Resources Co-founded by Sichuan Province and MOST, Chengdu 611137, China; 2. Chengdu University of Traditional Chinese Medicine, Chengdu 610075)
Objective:To investigate the effects of constituents groups extracted from Huanglian Jiedu decoction (HLJDD) on rats of toxic heat-induced blood stasis pattern.Method:Sprague-Dawley rats were randomly divided into control group, model group, aspirin group and HLJDD constituents groups. The rats model were established after the drugs were administered orally for 5 days. Except the control group, the model rats of toxic heat-induced blood stasis pattern were established with carragheen and LPS. The general conditions, blood routine examination, marks of blood stream change were observed to evaluate the antipyretic and blood activating activity.Result:The levels of WBC, whole blood viscosity, hematocrit and whole blood low shear rate were all improved while the general conditions were worse in model rats. HLJDD components groups had a therapeutic effect on heat and blood stasis model to improve the general conditions and remarkably decrease the whole blood viscosity and hematocrit. The total alkaloids can even decrease whole blood high shear reductive viscosity (P<0.05 or P<0.01).Conclusion:The investigation reveals that HLJDD water extract, total alkaloids, total favonoids and iridoid has therapeutic effect on the model rat to amend the heat-toxic syndrome, increase the hemorrheology characteristic. And the total alkaloids may be the possible material basis of this effect.
Huanglian Jiedu decoction; toxic heat-induced blood stasis;active components group
R 285.5
A
1674-926X(2014)04-004-03
国家科技支撑计划(中药有效成分群功效关联性评价技术研究,2008BAI51B02)
1. 成都中医药大学药学院 中药材标准化教育部重点实验室 中药资源系统研究与开发利用省部共建国家重点实验室培育基地,四川 成都 611137;2.成都中医药大学,四川 成都 610075
杜巧辉,硕士研究生,主要从事中药有效性研究 Email:elvis_do@126.com
谢晓芳,博士,助理研究员,主要从事中药复方药理与毒理研究 Email:xxf14544@163.com;曹小玉,教授,主要从事中药研究信息管理工作Email:cdzycxy@126.com
2013-11-11

