球状交联壳聚糖树脂的制备及对金属离子吸附研究
郝金丽,吴 艳
内蒙古自治区第三地质矿产勘查开发院中心实验室,呼和浩特 010010
甲壳素和壳聚糖是一种天然可再生资源,环境不造成二次污染,可进行生物降解,因而在很多方面得到了应用。但由于受到溶解性的限制,也就限制了壳聚糖在更广泛的领域,尤其在附加值较高的生物和医药领域的应用[1-4]。随着人们对环境保护意识的提高以及我国环境问题日益凸显严重,壳聚糖在处理工业废水的独特性受到重视。以日本为例,1994年壳聚糖的生产量达到800 t,用于废水处理 作为阳离子絮凝剂的壳聚糖则占44%。但是壳聚糖在吸附离子后的可再生性、选择性、吸附性能以及在强酸性条件下的使用还不够完善[5-6]。
近几年来,壳聚糖衍生物作为金属离子吸附剂的研究相当活跃,主要原因有两个:一是原料来源比较广泛,有良好的生物降解性能;二是壳聚糖衍生物对金属离子有比较好的吸附性能。但在壳聚糖和其衍生物的制备过程中,还存在着一定的二次污水处理的问题,因此,还要继续改善壳聚糖的生产技术,以便充分利用。 本文以戊二醛为交联剂,利用悬浮聚合法合成了新型壳聚糖树脂,并对壳聚糖树脂与金属离子的吸附能力做了初步表征。
1 实验部分
1.1 试剂
壳聚糖∶上海伯奥生物科技有限公司。
甲苯∶国药集团化学试剂有限公司 化学纯CP。
Span20∶上海化学试剂采购供应站经销(旅顺),上海行知中学校办工厂分装。
冰乙酸∶上海精化科技研究所 分析纯 AR。
戊二醛∶国药集团化学试剂有限公司 生化试剂BR。
乙醇∶国药集团化学试剂有限公司 分析纯AR。
邻苯二甲酸酐∶上海试剂厂。
氢氧化钠∶国药集团化学试剂有限公司 分析纯AR。
硫酸铜∶国药集团化学试剂有限公司 分析纯AR。
5%乙酸溶液:用移液管吸取5mL冰乙酸,加纯水(本实验所用水均为纯净水)至100mL,用时现配。
Cu2+标准溶液:
(1)标液A:称取0.393 3 gCuSO4.5H2O加入50mL水溶解并以水定容至100mL容量瓶中,摇匀此时溶液Cu2+质量浓度为1.001 g/L。
(2)标液B:从标液A中移取50.0mL溶液稀释至1 000mL容量瓶中,以水稀释至刻度摇匀,此溶液Cu2+质量浓度为50.0mg/L。
(3)标液C:从标液B中移取10.0mL溶液稀释至1 000mL容量瓶中,以水稀释至摇匀,此时溶液Cu2+质量浓度为0.5mg/L。
1.2 仪器
数显恒温水浴锅:HH-2 国华电器有限公司 ;
电热恒温鼓风干燥箱:上海新苗医疗器械制造有限公司。
SHZ—Ⅱ型循环水真空泵:上海亚荣生化仪器厂。
IKA—顶置式搅拌机:广州仪科实验室技术有限公司(德国 IKA广州)。
CX41系统显微镜:日本;
JVC CVC 摄像头×10:OLYMPUSU—CMAD3 JAPAN;
AE100电子分析天平:梅特勒-托利多仪器(上海)有限公司。
雷磁pHS-3C 精密pH计:上海精密科学仪器有限公司。
WSZ-100A Orbital Shaler:上海一恒科技有限公司。
SOLLAAR-929原子吸收分光光度计:(UNICAM)。
1.3 实验和测定方法
1.3.1 壳聚糖与戊二醛反应的凝胶化时间测定
称取3份2.0.0 g壳聚糖分别放入250mL烧杯中,用5%的乙酸溶液溶解,待溶解后分别加入6.30%、12.5%、25.0%的戊二醛溶液5.0mL,待烧杯中出现类似果冻状物质为止,测定其凝胶化时间。
1.3.2 交联壳聚糖树脂的制备
首先将一定量的壳聚糖溶解在体积分数为5%的乙酸溶液中备用, 向装有搅拌器及温度计的三口瓶内依次加入甲苯溶液和少许Span20,待Span20完全溶解后,加入上述壳聚糖溶液, 开动搅拌将壳聚糖溶液分散成均匀液珠, 维持15min左右, 再加入25%戊二醛溶液,将体系升温至50 ℃并维持1~2 h; 用2%氢氧化钠碱溶液调pH值至弱碱性大概为9左右, 升温至80 ℃, 固化4 h, 此时得到珠状壳聚糖产品, 经乙醇提取及水洗后, 置于烘箱中80℃烘干1~2 h。
1.3.3 壳聚糖树脂的显微镜照片制作
洗净若干玻片(大概6~8片)晾干,将不同时期制作好的壳聚糖树脂混匀分成3~4组,用干净的玻璃棒沾取少量的球状树脂于玻片上,滴上少量75%酒精,然后用玻璃棒摊开成一个平面(注意要均匀,不能有堆积)。然后待酒精挥发干后,置于显微镜下观察拍照(拍照时注意应该选取颗粒数目适中具有代表性的区域进行拍照3~5张)。
制作壳聚糖树脂的显微镜照片应注意事项:
第一、湿润的试剂最好为75%以上的酒精溶液,不能用纯水,因为纯水的表面张力很大,而酒精首先是其表面张力比较小,而且易于挥发。
第二、涂片时应尽量均匀,不要有重叠,全部置于同一个平面上,保证观察时所有壳聚糖树脂处于同一焦距上。
第三、待酒精挥发完全后,进行观察照相。(如果玻片上还有大量的溶液势必存在比较大的表面张力,影响分散效果;而且由于溶液的折射效应,会造成观察失真。)
1.3.4 交联壳聚糖树脂的稳定性检验
将已合成好的交联壳聚糖树脂分别放置于 5%、10%、50%、100%的乙酸溶液中,静置1 h、1 d、5 d、10 d观察其稳定性。
1.3.5 交联壳聚糖树脂粒径大小的测定
将已制作好的交联壳聚糖颗粒(未过筛)照片随机选中一片有20个颗粒的区域,用量尺测出其粒径大小,得到平均粒径大小,再除于照片的放大倍数,得到其粒径大小。重复此实验3次,求得平均颗粒的粒径xx。
1.3.6 交联壳聚糖树脂离子吸附能力
(1)Cu2+标准曲线的制作分别移取标液C:5.0,10.0,15.0,20.0mL置于1~4号25mL容量瓶中,以水定容至25mL,摇匀备用(5号为标液C)。开启FAAS,将Cu灯预热0.5 h至稳定,分别测定其吸光度,制作Cu2+标准曲线。其工作条件按如下:
Cu:灯电流:5.0mA ;负高压:300 V; 燃烧器高:7.0mm ;空气流量:5.0 L/min1;乙炔流量:1.5 L/min ; 光谱带宽:0.2 nm;波长等于:324.8 nm。
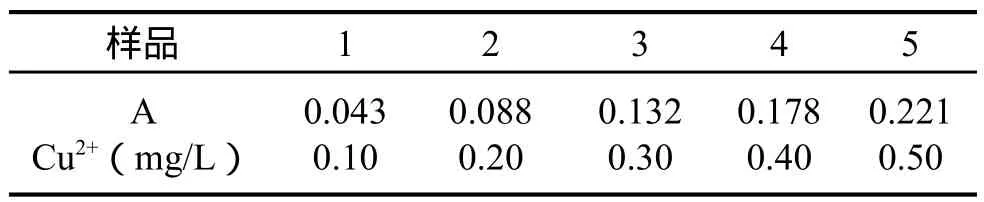
表1 Cu2+ 标准溶液的A(吸光度)测定Table 1 A (absorbance)measured of Cu2+ standard solution
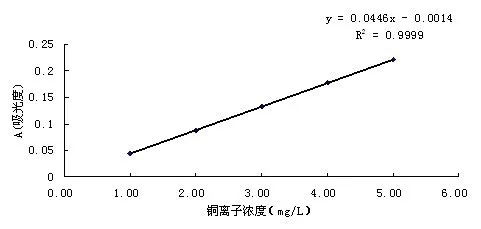
图1 铜离子标准曲线Fig.1 Cu2+ standard curve
标准线性回归方程为:y=0.044 6x–0.001 4;R2=0.999 9
(2)Cu2+的静态吸附测定:准确称取一定量交联壳聚糖树脂于250mL锥形瓶中,分别加入一定量铜离子,调节其pH,控制一定的体积,将其置于振荡器上振荡一定时间后,取滤液于原子吸收上测定,并按下式Q和A计算其吸附容量与吸附率。

式中,Q:吸附容量,mg/g
C0:处理前溶液中的金属离子的质量浓度,mg/L;
CC:处理后溶液中残留的金属离子的质量浓度,mg/L;
V:被处理的金属离子溶液的体积,mL;
W:球状交联壳聚糖的质量,mg。
A=(C0-C1)/C0
式中,A: 吸附率,%;
C0:铜离子起始质量浓度,mg/L;
C1:吸附后残留离子质量浓度,mg/L。
2 结果与讨论
2.1 反应条件对壳聚糖成球的影响
实验过程中发现影响壳聚糖树脂成球质量及粒径大小、粒径分布的因素有很多,诸如有机溶剂的种类,油/水比例,搅拌速度以及壳聚糖的浓度等等。
2.1.1 壳聚糖浓度的影响
实验表明,壳聚糖的浓度对成球有较大影响当浓度低于2%时,不能形成很多好的球,且机械强度很差;当浓度大于4%时,成球率在95%以上,且粒度分布比较均匀,强度较好。这主要时由于当壳聚糖的浓度很低时,则反应包里的壳聚糖浓度就很低,交联度自然也相应降低,以致于不能很好成球。

表2 壳聚糖浓度对壳聚糖成球性能影响Table 2 In fl uence of chitosan concentration on the performance of chitosan balling
2.1.2 搅拌速度对成球性能影响
在用反相悬浮聚合法制备交联壳聚糖树脂过程中搅拌的剪切力和液滴与分散介质间的界面张力对成球作用的影响相反。在一定的搅拌强度和界面张力下,大小不等的液滴通过一系列分散和合并的过程,构成一定的动态平衡,最后达到一定的平均粒度,但大小仍有一定的分布,主要是因为反应容器内的各部分受到的搅拌强度时不均匀造成的。
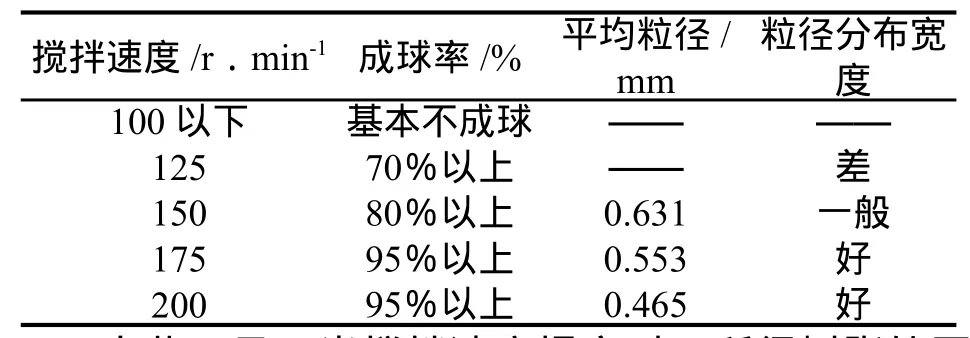
表3 搅拌速度对壳聚糖成球性能影响Table 3 In fl uence of stirring speed on the performance of chitosan balling
由此可见:当搅拌速度提高时,所得树脂的平均粒径减小,但成球率有所提高,说明搅拌速度的提高导致分散在介质中的壳聚糖小液滴粒径变小,液滴数目增多,比表面积增大。
2.1.3 油/水比例对成球性能影响
当油水比例为1∶1时基本无球状颗粒出现,此时无法进行反相悬浮交联,产品出现黄褐色絮状物质。当油水比例达到2:1时,开始出现较好的球状颗粒。
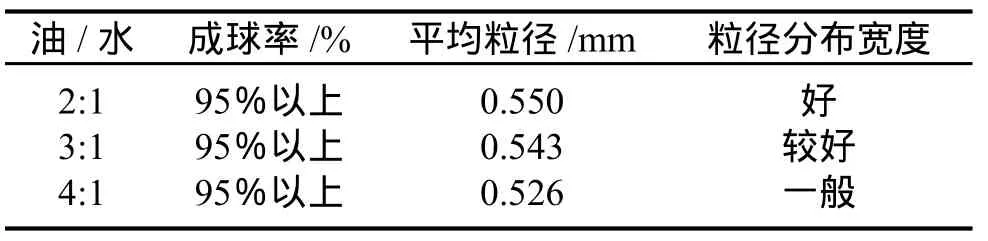
表4 油/水比例对壳聚糖成球性能影响Table 4 In fl uence of oil/water ratio on the performance of chitosan balling
由表4可见随着分散介质的增加树脂粒径有所降低,而粒径分布明显加宽。这是由于随着油/水比例的增加,反应相小液滴被有机相包裹越紧密,所受的压力也越大,因此粒径也就越小。此外由于三口瓶内边缘和中心的所受搅拌的剪切力大小不等,并且有机相越多,这种大小不等的程度越大,因此造成粒径分布加宽。
2.1.4 Span20对成球性能的影响
Span20主要是作为一种表面活性剂,因为反相悬浮法合成壳聚糖树脂,分散介质时油,反应相是水,而水表面张力比较大,容易聚在一起,不利于分散,而Span结构中含有亲水基团也含有疏水基团,它可以将一个个反应液滴包裹起来,在分散相中能够更加稳定的存在,有利于水相的分散。
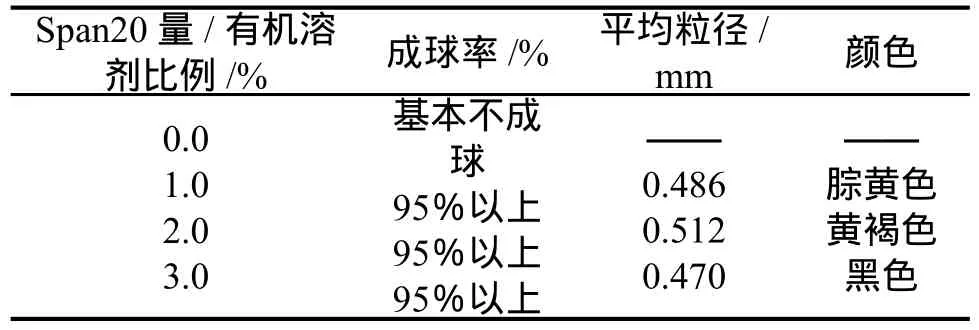
表5 Span20对壳聚糖成球性能的影响Table 5 In fl uence of Span20 on the performance of chitosan balling
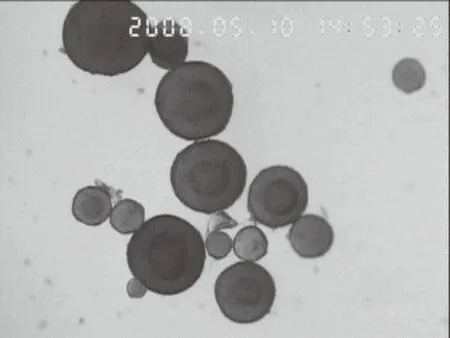
图2 交联壳聚糖树脂/Span20量适中图 ×30Fig.2 Cross-linked chitosan resin/Span20moderate quantity *30

图3 交联壳聚糖树脂/Span20过量图 ×30Fig.3 Cross-linked chitosan resin/Span20 over-dose quantity *30
由图表可见Span主要是影响交联壳聚糖的色泽,当Span20过量时,交联壳聚糖颜色发黑,当Span20大致为有机溶剂量的1%时,其颜色为黄琥珀色,显微镜下颗粒有较好的透明度。这主要是因为当Span过量时,反应包周围被包裹的非常紧密甚至有些进入反应包,从而呈现Span的黑色。
2.2 交联壳聚糖树脂的稳定性检验
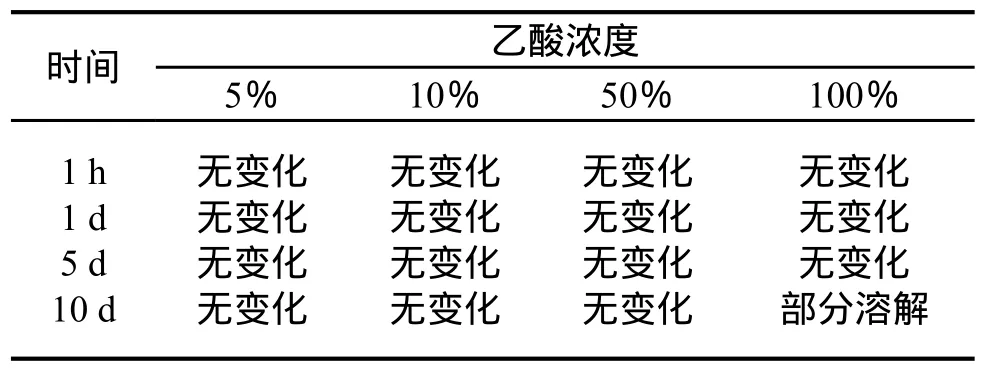
表6 CCTS在不同乙酸浓度及时间条件下的稳定性Table 6 CCTS stability under different acetic acid concentration and time conditions
由表6 可见交联壳聚糖树脂能构稳定的存在于酸性环境中,虽然壳聚糖在酸性环境会溶解,但是交联壳聚糖树脂却能够在酸性条件下稳定存在。壳聚糖能够溶解在酸性溶液中是因为胺基质子化的结果,而交联壳聚糖树脂由于交联后导致胺基基团减少并且形成了复杂的空间结构,其质子化不足于破坏其空间结构,所以交联壳聚糖树脂能够稳定存在于酸性环境中。
2.3 不同条件下交联壳聚糖对Cu2+静态吸附的影响
2.3.1 酸度对Cu2+吸附的影响
分别移取5mLCu2+的B标液(50mg/L)于50mL容量瓶,取5份分别调节pH值为3.0、4.0、5.0、6.0、7.0,以水定容,摇匀,与已称好的0.1 g CCTS一同置于100mL锥形瓶中振荡4 h以上后同时取出,干过滤,取10.0mL滤液置于100mL容量瓶里,以水定容,摇匀,用原子吸收测定。溶液中金属离子残余量(mg/L)如表7。

表7 酸度对Cu2+吸附的影响Table 7 Effects of acidity on the adsorption of Cu2+
由表7和图4可知,静态条件下,可知交联壳聚糖对铜离子的吸附性能随pH值的变化而变化,当pH=5.0时,其吸附性能达到最大值,根据1.3.6中式A可以计算出此时吸附率为95.4%。这是由于交联壳聚糖与重金属离子的作用,不是简单的物理吸附,而是既有物理吸附又有螯用,形成不同的螯合物[7-11],这种螯合作用又受到介质pH值的影响。当pH>6.0时,交联壳聚糖对金属离子的吸附性能又降低交联壳聚糖的游离氨基在水溶液中存在下列平衡:
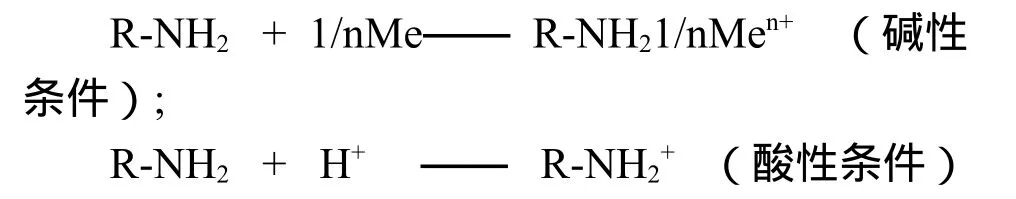
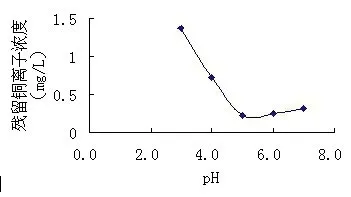
图4 残余金属离子浓度(mg/L)与pH值曲线Fig.4 Concentration of residualmetal ions (mg / L)and pH value
可见,在酸性条件下,氨基被酸化成NH4+,失去了对金属离子的螯合性,因而在酸性条件下,对金属离子的吸附量降低;在碱性条件下,氨基以游离(-NH2)的形式存在,有利于对金属离子的螯合,但碱性太高,又会使金属离子生成沉淀,使吸附量降低。
由于该交联壳聚糖不溶于酸、碱且在酸性溶液中有较好的刚性、不溶胀、不流失,在pH=5.0时,对铜金属离子有较好的吸附性能。且吸附了重金属离子的交联壳聚糖,在酸性条件下,可发生解吸作用,因而该交联壳聚糖可以重复利用。
2.3.2 饱和吸附时间的选择

表8 饱和吸附时间的选择Table 8 Selection of the saturated adsorption time
移取5份5.0mL Cu2+的标液B(50mg/L)于50mL容量瓶,调节pH 为5.0,以水定容,摇匀,与已称好的0.1 g 交联壳聚糖树脂一同置于100mL锥形瓶中振荡分别反应1.0 ,1.5,2.0,2.5,3.0 h后,干过滤于干烧杯中,取10.0mL滤液以水定容于100mL容量瓶中,摇匀,用原子吸收测定。溶液中金属离子残余量(mg/L)如表8。
由表8和图5可知,交联壳聚糖对铜离子的吸附速率很快,可以认为3 h时达到平衡。且随着时间的延长,吸附容量变化不大,根据1.3.6中式A可以计算出饱和吸附率为93.4%。
2.3.3 交联壳聚糖树脂饱和吸附量的测定
移取3份5 .0mL Cu2+的标液B(50mg/L)于50mL容量瓶,调节pH 值为5.0,以水定容,摇匀,与已称好的0.1 g交联壳聚糖树脂一同置于100mL锥形瓶中振荡反应2 h后,干过滤于干烧杯中。取10.0mL滤液以水定容于100mL容量瓶, 原子吸收测定。溶液中金属离子残余量(mg/L)如表9。

图5 残余金属离子浓度(mg/L)与振荡时间曲线Fig.5 Concentration of residualmetal ions (mg / L) and the oscillation time curve

表9 CCTS饱和吸附量的测定Table 9 Determination of saturated adsorption capacity of CCTS
通过1.3.6 Q式和A式可以计算出Cu2+的静态吸附容量为2.39mg/g,吸附率为95.3%,此种树脂虽然吸附容量比较低但其吸附率却很高,在处理浓度较低的废水方面能具有较好的效果。
3 结论
3.1 合成交联壳聚糖树脂的最佳条件
本文采用反相悬浮交联法合成了交联壳聚糖树脂,比较系统的考察了影响成球性能的各种因素,结果表明可以通过调节壳聚糖浓度、交联剂的用量(戊二醛量)、搅拌速度、和油/水比例等反应条件而得到合适的树脂。
通过实验可进一步得知当壳聚糖(g)与戊二醛(mL)为4∶1,最佳转速为175 r/min,最佳油水比例为2∶1时合成的交联壳聚糖树脂效果是最好。
3.2 交联壳聚糖树脂的静态吸附容量
通过树脂对铜离子的吸附实验可见吸附的最佳pH约为5,最佳吸附时间为3.0 h,静态吸附容量为2.39mg/g,吸附率为95.3%。此交联壳聚糖树脂虽然吸附容量很小,但其吸附率很高,在处理浓度较低的废水方面具有较好的效果。
[1] 余艺华,孙 彦,何炳林.交联壳聚糖树脂的制备工艺及性能表征[J].天津大学学报,2000,(01):68-72.
[2] 孙昌梅,曲荣君,王春华,等.基于壳聚糖及其衍生物的金属离子吸附剂的研究进展[J].离子交换与吸附,2004,(02).
[3] 刘 峥,田兴乐,蒋光明.Cu(Ⅱ)模板法合成交联壳聚糖缩和水杨醛鳌合树脂[J].应用化学,1999,(03).
[4] 白林山,冯长根,任启生.三甲胺修饰戊二醛交联壳聚糖树脂的制备及其吸附性能[J].现代化工,2003,(08):12-16.
[5] 罗道成,易平贵,刘俊峰.聚糖对电镀废水中重金属离子的吸附[J].材料保护,2002,(01).
[6] 彭长宏, 阳卫军,唐谟堂,等.壳聚糖冠醚合成及表征[J].高分子材料科学与工程,2003 (02):89-93.
[7] 程珊珊,杨锡洪,章超桦,等.壳聚糖对Cd2+和Pb2+的吸附作用[J].水产学报,2011(03).
[8] 贺小进,谭天伟,戚以政.球形壳聚糖树脂制备方法及吸附性能研究[J].离子交换与吸附 ,2000,(01).
[9] 曹小红,刘云海,朱 政,等.壳聚糖及其衍生物对铀的吸附研究[J].化学研究与应用,2006,(07).
[10] 赖声礼,曹佐英,葛华才. 微波辐射下模板交联壳聚糖的制备及其对Cu2+吸附性能的研究[J]. 华南理工大学学报(自然科学版),2000 ,(08):53-58.
[11] 袁彦超,陈炳稔,王瑞香,等.新型交联壳聚糖树脂的制备及其对苯甲酸的吸附行为研究[J].化学学报,2004,62.

