正交试验优选羧甲基壳聚糖-醋甲唑胺纳米微球的制备方案*
张桂贤,陈 斌,王晓辉,李 楠,刘佩莉,李光远,祝君梅
(天津市医药科学研究所,天津300020)
正交试验优选羧甲基壳聚糖-醋甲唑胺纳米微球的制备方案*
张桂贤,陈 斌,王晓辉,李 楠,刘佩莉,李光远,祝君梅
(天津市医药科学研究所,天津300020)
目的:制备羧甲基壳聚糖载药纳米微球,醋甲唑胺为模型药物,测量药物的包封率和纳米微球形态。方法:采用乳化交联法,在微乳液的基础上制备载药纳米微球,对可能影响药物包封率的处方因素进行优化设计,筛选出最优配方。结果:羧甲基壳聚糖溶液的浓度对包封率有显著性影响,三聚磷酸钠溶液浓度和醋甲唑胺药量对包封率未见影响。优化方案的载药纳米微球包封率为49.36%,其电镜下为较规整的球型纳米微球,平均粒径386.0 nm。结论:采用乳化交联法,可形成较高包封率的羧甲基壳聚糖-醋甲唑胺纳米微球。
羧甲基壳聚糖,纳米微球,醋甲唑胺,乳化交联
以壳聚糖及衍生物为载体材料的纳米给药系统常用于眼科局部给药的研究[1]。该系统有控制药物释放、协助药物向组织渗透和滞留等优点[2]。羧甲基壳聚糖生物相容性好,水溶解性优于壳聚糖,以其为载体的载药纳米微球可与角膜前表面黏附,延长药物滞留时间,便于药物透过角膜[3]。醋甲唑胺是醋酸酐酶抑制剂,眼科用药减少房水生成,临床用于降眼压治疗,也可用于治疗黄斑水肿[4]。但醋甲唑胺水溶性较差,口服给药,有毒副作用[5]。载有醋甲唑胺的纳米微球,可通过局部给药降低家兔眼压。本研究用乳化交联法直接使亲水载体羧甲基壳聚糖包裹醋甲唑胺形成纳米微球,探讨纳米微球的制备工艺和载药能力。
1 材料及仪器
1.1 材料醋甲唑胺原料药(武汉大华伟业医药化工有限公司),醋甲唑胺对照品(中国食品药品检定研究院,含量测定用,纯度为99.4%,批号100589-200501),羧甲基壳聚糖(CMC,浙江澳兴生物科技有限公司,分子量30万,羧化度80%),三聚磷酸钠(TPP),吐温-80,乙酸乙酯为分析纯,甲醇为色谱纯,水为纯净水(娃哈哈集团有限公司)。
1.2 仪器Model J2-21低温高速离心机,LC-2010A高效液相色谱仪,KQ-50E超声清洗仪(昆山市超声仪器有限公司),AL204电子天平(梅特勒-托利多公司),透射电子显微镜(LEOL LEM-1010),Zetasize粒径分析仪(Malvern公司)。
2 方法和结果
2.1 纳米微球制备条件吐温-80与乙醇混匀制成3份混合乳化剂,二者的体积比(Km)分别为1∶5,1∶2和1∶1;以0.5%盐酸为溶剂,配制4.2、6.3和8.4 mg/ml的CMC溶液,以0.5%盐酸为溶剂,配制2.8、3.7、4.7、5.6和6.5 mg/ml TPP溶液。用乳化交联法制备空白纳米微球,取2 ml乙酸乙酯,加入3 ml混合乳化剂,在常温下超声5 min,以30滴/min速度滴入0.5%盐酸,形成O/W微乳液。继续超声30 min,待微乳逐渐变清,滴入一定浓度CMC溶液,再滴入3 ml一定浓度的TPP溶液,继续超声1 h,记录不同配方时体系的相变状态,其中肉眼有乳光的体系为纳米微球混悬液。不同配方时体系的相变状态见表1和表2。选择每个组合中,体系有肉眼乳光时(+)所用的最高TPP溶液浓度,作为以后正交分析时所用TPP溶液的浓度,此时纳米微粒的交联比较充分。

表1 混合乳化剂的体积比_为1∶2和1∶5时反应体系状态

表2 _混合乳化剂的体积比为1∶1反应体系状态_
2.2 含量测定条件的考查
2.2.1 色谱条件[6]色谱柱:TIANHE C18柱(250 mm×4.6 mm,5 μm);流动相:甲醇-水(20∶80);检测波长:290 nm;流速:1.0 ml/min;柱温:40℃;进样20 μl。
2.2.2 溶液液备
2.2.2.1 对照品溶液的制备精密称取醋甲唑胺标准品10 mg,置于50 ml量瓶中,用0.5%盐酸配制成2 μg/ml的溶液,即得储备液。取适量,用0.5%盐酸稀释,配制成浓度为0.4 μg/ml的对照液。
2.2.2.2 供试品混悬液的制备载药纳米微球的制备:用乳化交联法,将一定质量的醋甲唑胺原料药溶于2 ml乙酸乙酯,加入3 ml混合乳化剂,在常温下超声5 min,以30滴/min速度滴入0.5%盐酸,继续超声30 min,待变清时,滴入CMC溶液,再滴入3 ml TPP溶液,继续超声1 h,即得到载药纳米微球混悬液。
2.3.2.3 空白混悬液的制备依“2.2.2.2”项下方法,去除醋甲唑胺对照品,制得空白混悬液。
2.2.3 分离条件考查取对照品溶液、供试品溶液和空白对照溶液,依“2.2.1”项下色谱条件进样,记录色谱图,见图1。空白纳米微球出峰时间为8~13 min,醋甲唑胺出峰时间为15 min左右,空白溶液中成分与醋甲唑胺能较好地分离且空白溶液无干扰,此时的浓度高于正交试验时体系中吐温-80浓度。因此空白纳米微球和吐温-80对醋甲唑胺浓度测定均无较大影响。

图1 对照品(A)供试品(B)空白对照(C)HPLC色谱图
2.2.4 标准曲线的考查精密量取“2.2.2.1”项下储备液适量,分别用0.5%盐酸稀释,配制成浓度为0.1、0.2、0.4、0.6和0.8 μg/ml的系列标准液,按照“2.2.1”项下色谱条件注入液相色谱仪,测定峰面积积分值,以醋甲唑胺浓度(Y)对峰面积积分值(X)进行线性回归,得回归方程Y=50 793 X-220(r2=0.999 9),表明醋甲唑胺在0.1~0.8 μg/ml之间与峰面积呈良好线性相关。
2.2.5 精密度试验取0.4 μg/ml浓度醋甲唑胺标准品溶液,连续进样6次,按照“2.2.1”项下色谱条件注入液相色谱仪测定峰面积,RSD为1.34%,表明重复性较好。
2.2.6 回收率试验取空白纳米微球混悬液配置醋甲唑胺低中高浓度(0.2、0.4和0.6 μg/ml)的标准品溶液,每个浓度平行3份,按照“2.2.1”项下色谱条件注入液相色谱仪,测定峰面积,得平均回收率为97.8%,RSD为1.99%,表明方法准确度较好,见表3。
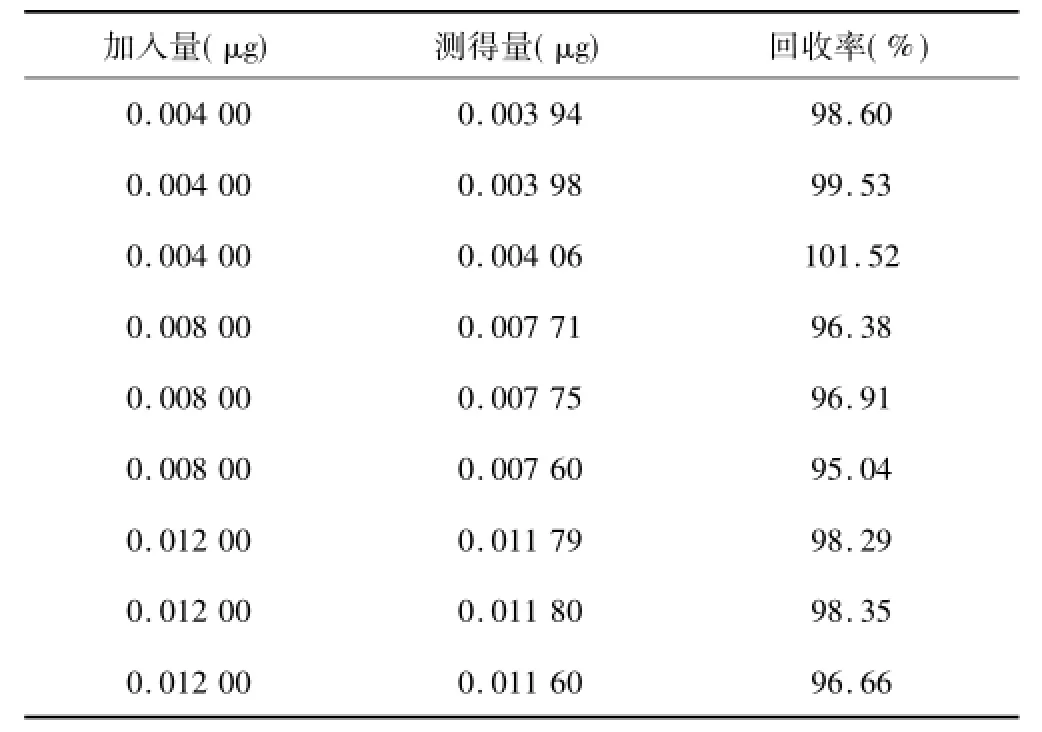
表3 回收率试验测定结果(n=9)
2.3 正交试验选定CMC溶液浓度(A)、混合乳化剂中吐温-80与乙醇的体积比例(B),醋甲唑胺质量(C)和空白因素(D),TPP溶液浓度为该组合下体系为纳米微球悬液时的最高浓度。每个因素有3个水平,按照L9(34)正交设计(见表4),以包封率、纳米微球粒径和多分散系数为评价指标,选出最佳工艺条件。验证试验按候选的工艺条件重复4次,测定包封率。纳米微球混悬液在4℃下16 000 r/min离心,取上清液,定容至25 ml,稀释500~1 500倍,按照正交试验表分别取适量溶液进样,计算上清液中醋甲唑胺的浓度及醋甲唑胺的包封率。包封率=(醋甲唑胺总质量-上清液中醋甲唑胺质量)/醋甲唑胺总质量×100%。用粒径分析仪测量各组纳米微球的粒径范围。结果见表5-8。
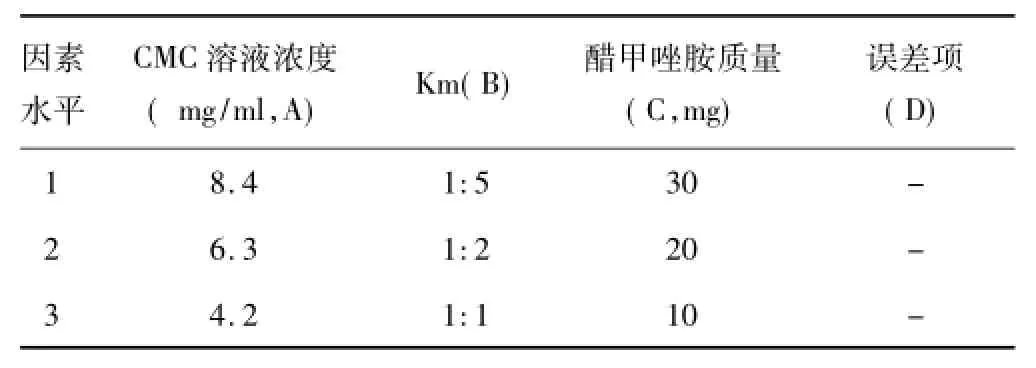
表4 因素水平表

表5 正交试验结果

表6 以纳米微球径为指标的方差分析

表7 以包封率为指标的方差分析

表8 以多分散系数为指标的方差分析
方差分析表明,以纳米微球径为指标,在所选因素水平范围内,各因素作用顺序为A>B>C,因素A对包封率有显著性影响,而因素B和C不具有显著性影响。以包封率为指标,各因素作用顺序为A>C>B,因素A对包封率有显著性影响,而因素B和C不具有显著性影响。以多分散系数为指标,各因素作用顺序为B>A>C,只有因素B对包封率有显著性影响。选择A3为最优项,可以获得粒径较小,且包封率较高的纳米微球,选择含吐温-80量最小的B1为最优项,此时多分散系数更小,纳米微球更均匀,还可以减少吐温-80用量,减少潜在不良反应。验证试验测得A3B1C1、A3B1C2、A3B1C3的平均包封率分别为46.43%、49.36%和48.36%(n=4),选取A3B1C2为最优组合。
2.4 纳米微球形态学观察将最佳工艺条件制备的CMC-醋甲唑胺纳米微球混悬液用醋酸铀负染后,在透射电镜下(270×10 K)观测纳米微球的形态为较规整的球型,粒径在400~600 nm。照片见图2。粒径分析仪测量载药纳米微球的平均粒径386.0nm,多分散系数0.332。

图2 纳米微球的电镜形态
3 讨论
乳化交联法可以用亲水性壳聚糖类载体包载亲脂性药物,如高礼[7]等将普罗布考溶于二氯甲烷中,得到O/W乳剂,在经过壳聚糖与TPP交联得到壳聚糖-普罗布考纳米微球。乳化交联法要求油相易于挥发,且在水中有一定的溶解性,使载体材料易于在水油界面上交联。乙酸乙酯溶解醋甲唑胺较好,且能满足上述要求,选为本实验的油相。实验的O/W乳剂按照汪杨[8]等人的自微乳化方法配置。
本实验中使用4.2 mg/ml CMC制备纳米微球悬液时,CMC/TPP最高为2.5~3∶1,低于使用6.3和8.4 mg/ml CMC时的CMC/TPP比例,而药物包封率也高于后者。可能的原因是使较高浓度的CMC在TPP浓度较低,纳米微球交联尚不完全时就已经趋于形成沉淀。
实验证实通过乳化交联法可以制备羧甲基壳聚糖为载体,携带醋甲唑胺的纳米微球。纳米微球的安全性和局部给药效果需要进一步实验证实。
1Motwani S K,Chopra S,Talegaonkar S,et al.Chitosan-sodium alginate nanoparticles as submicroscopic reservoirs for ocular delivery:Formulation,optimization and in virto characterization[J].Eur J Pharm Biopharm,2008,68(3):513-525
2Amrite A C,Edelhauser H F,Singh E R,et al.Effect of circulation on the disposition and ocular tissue distribution of 20nm nanoparticles after periocular administration[J].MoL Vis,2008,14(29):150-160
3Di Colo G,Zambito Y,Burgalassi S,et al.Effect of chitosan and of N-carboxymethyl chitosan on intraocular penetration of topically applied ofloxacin[J].Int J Oharm,2004,273:37-44
4孙一洲,柳力敏,钟一凡,等.醋甲唑胺与吸收剂对视网膜分支静脉阻塞激光光凝术后黄斑水肿的疗效[J].实用药学与临床,2011,14(6):476-477
5杨飏,高殿文.醋甲唑胺治疗青光眼的临床研究[J].辽宁医学杂志,2005,19(3):156
6陆晓梅,王淼,赵人琤.高效液相法测定兔眼房水中醋甲唑胺的含量.南京医科大学学报(自然科学版),2007,27(05):457-459
7高礼,万锕俊.普罗布考壳聚糖纳米微球子的制备及体外释放[J].中国新药杂志,2009,18(19):1892-1896
8汪杨,吴伟,阙俐.油-吐温-醇-水体系伪三元相图在自微乳化制剂研究中的应用[J].中国医药工业杂志,2005(6):345-348
Otimization on preparation technology of carboxymethyl chitosan-methazolamide nanoparticles by orthogonal design
Zhang Guixian,Chen Bin,Wang Xiaohui,Li Nan,Liu PeiLi,Li Guangyuan,Zhu Junmei
(Tianjin Institute of Medical and Pharmacoutical Sciences,Tianjin 300020)
Objective:To prepare carboxymethyl chitosan(CMC)drug-loaded nanoparticles,with methazolamide as model drug.The drug encapsulation efficiency and morphology should be measured.Methods:Drug-loaded nanoparticles were preparated in microemulsion by emulsion crosslinking method.The design of formulation factors that may affect the drug entrapment efficiency was optimized to select optimal formulation.Results:The concentration of carboxymethyl chitosan solution has a significant effect on the entrapment efficiency,when sodium tripolyphosphate(TPP)solution concentration and weight of methazolamide don’t effect on the entrapment efficiency.Entrapment efficiency of optimization of drug-Loaded nanoparticles was 49.36%.The nanoparticles is regular and baLL-type,with average particLe size in 386.0 nm on electron microscope.Conclusion:Nanoparticles can be formated with hydrophilic carboxymethyl-chitosan coating lipophilic methazolamide by emulsion crosslinking method,and high encapsulation efficiency can be achieved.
carboxymethyl-chitosan,nanoparticles,methazolamide,emulsion crosslinking
TQ460.6
A
1006-5687(2014)02-0010-04
2013-01-29
天津市卫生局科技基金(青年)项目(No.2012KY34)

