SO2在活性炭上的吸附平衡、动力学及热力学研究
李 兵,薛建明,许月阳,王宏亮,马春元,陈建民
(1.国电科学技术研究院(国电环境保护研究院),江苏南京 210031;2.山东大学环境科学与工程学院,山东济南 250100;3.山东大学燃煤污染物减排国家工程实验室,山东济南 250061)
SO2在活性炭上的吸附平衡、动力学及热力学研究
李 兵1,2,薛建明1,许月阳1,王宏亮1,马春元3,陈建民2
(1.国电科学技术研究院(国电环境保护研究院),江苏南京 210031;2.山东大学环境科学与工程学院,山东济南 250100;3.山东大学燃煤污染物减排国家工程实验室,山东济南 250061)
为深入研究SO2在活性炭上的吸附过程,基于固定床反应器研究了某商业活性炭对烟气中SO2的吸附性能,考察了SO2体积分数、吸附温度对活性炭吸附SO2的影响,分析了SO2在活性炭表面的吸附平衡、吸附动力学和热力学特性。结果表明,随着SO2体积分数的增加,SO2初始吸附速率和平衡吸附量增加;随着吸附温度的增加,SO2初始吸附速率和平衡吸附量降低。活性炭对SO2的吸附平衡数据符合Langmuir和Freundlich吸附等温线模型;SO2在活性炭上的动态吸附过程符合Bangham吸附动力学模型。吸附热力学研究表明,吸附过程中焓变为-19.21 kJ/mol,吸附自由能变为-10.17~-9.29 kJ/mol,吸附熵变为-27.69~-27.17 J/(mol·K),该吸附过程是一个自发、放热、熵降低过程,升温不利于SO2在活性炭上的吸附。
SO2;活性炭;吸附平衡;吸附动力学;吸附热力学
燃煤电站锅炉烟气排放出大量SO2,造成酸雨等全球性大气公害,为控制SO2的排放,烟气脱硫技术已在国内外得到广泛应用。在各种烟气脱硫技术中,石灰石-石膏湿法烟气脱硫技术成熟,但存在耗水量大、生成的固体脱硫产物易造成二次污染的缺点;而活性炭(焦)吸附脱硫是一种干法烟气脱硫工艺,既能减排SO2,又能回收硫资源,同时对烟气中的其他污染物(SO3、NOx、二恶英、汞等)也有一定的脱除效果,具有广阔的应用前景[1-8]。
活性炭吸附系统的吸附平衡、吸附动力学及吸附热力学数据是选择合适的吸附剂、设计吸附过程、建立吸附模型、分析吸附系统经济性的基础[9-13]。Karatepe等[9]研究了在SO2+N2体系下,SO2在活性炭上的吸附平衡,符合Freundlich吸附等温线模型,但是活性炭在N2和SO2的混合气体条件下对SO2的吸附机理与活性炭在烟气条件下的脱硫机理不同[1-2]。在N2和SO2的混合气体条件下,活性炭对SO2的吸附以物理吸附为主,而在烟气条件下,由于水蒸气和O2的存在,活性炭不仅作为吸附剂而且作为催化剂,将SO2催化氧化为SO3,然后与H2O结合,生成H2SO4,储存在活性炭的孔隙中。余兰兰[11]考察了烟气中SO2在污泥制备的吸附剂上的吸附平衡及吸附热力学特性;高继贤[12]研究了烟气条件下SO2在ZL50活性炭上的吸附平衡及吸附热力学特性,但文献[11-12]中SO2的平衡吸附量是通过对短时间内的吸附实验数据(文献中实验未能持续到SO2吸附平衡)拟合得到的,缺乏实验依据。因此,需要进一步深入研究。本文基于固定床反应器研究活性炭对烟气中SO2的吸附性能,考察SO2体积分数、吸附温度对活性炭吸附SO2的影响,从吸附平衡、吸附动力学和热力学角度分析SO2在活性炭上的吸附过程,为工业吸附过程的设计提供基础数据。
1 实 验
1.1 实验材料
将某商业颗粒活性炭筛分,选择粒径在1.7~2.0 mm的活性炭,用蒸馏水洗涤,洗去表面杂质,在105℃的恒温干燥箱中干燥24 h,除去活性炭中的水分。活性炭的孔隙结构性质通过N2吸附等温线表征,在Micromeritics ASAP2020仪器上测量N2吸附等温线(-196℃),通过BET方法计算活性炭的比表面积(ABET);通过p/p0=0.98处的吸附量计算总孔容积(V);按照t-plot方法计算活性炭的微孔表面积和微孔容积;平均孔径按照4V/ABET计算。
1.2 SO2动态吸附实验
在恒温固定床反应器上进行活性炭吸附SO2的实验,实验系统如图1所示。反应器由圆柱形玻璃制成,内径15 mm,高500 mm,多孔玻璃板布置在距反应器底部250 mm处用于支撑活性炭;反应器外部为电加热装置,具有程序控温的功能,实现反应温度的精确控制。模拟烟气由高纯N2,高纯O2,SO2,H2O按照一定比例配制,其中N2,O2,SO2/N2(SO2体积分数为5%)由气瓶提供,流量由质量流量计(Sevenstar CS200)精确控制。H2O由N2冲击恒温水浴携带,调整携带H2O的N2流量和恒温水浴的温度,实现所需的H2O浓度。气体在混合器内混合均匀后进入反应器,从混合器到反应器入口管路保温,保证H2O以气体形式存在。将0.5 g干燥后的活性炭置入反应器内进行SO2的吸附实验。模拟烟气中SO2体积分数为0.02%~0.30%,H2O体积分数为8%,O2体积分数为6%,N2为平衡气,反应气体流量为400 mL/ min。反应器出口气体中SO2的体积分数经傅里叶变换红外烟气分析仪(FT-IR,Gasmet Dx4000)在线测量,通过SO2的穿透曲线计算活性炭吸附SO2的量,以每克活性炭吸附的SO2(mg)表示。
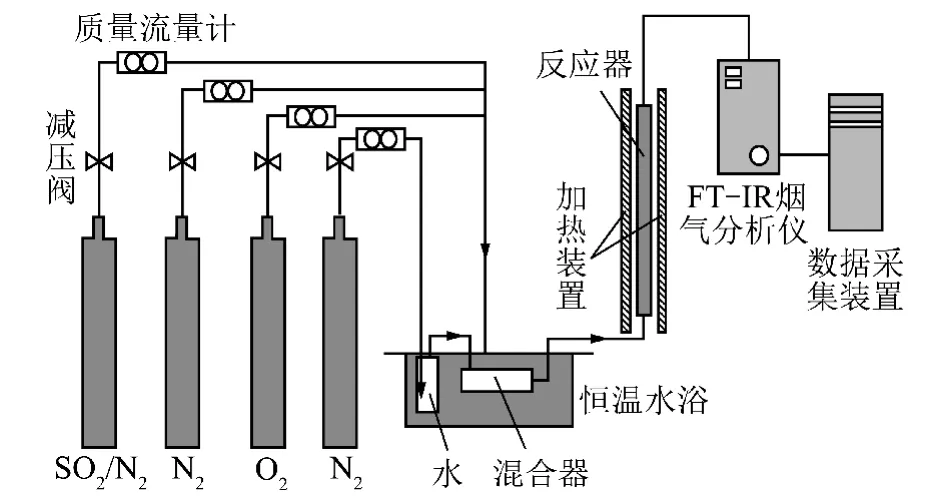
图1 实验系统Fig.1 Schematic diagram of the experimental system
2 结果与讨论
2.1 活性炭的性质表征
由图2可知,按照IUPAC(国际理论与应用化学联合会)的分类,活性炭的N2吸附等温线属于Ⅰ型吸附等温线,呈现微孔吸附特征[14]。N2吸附量在较低相对压力区域急剧增加,然后随着相对压力的升高,吸附量缓慢增加,在较高相对压力区域,吸附量随着相对压力的增加基本不变,吸附等温线呈现水平的趋势;脱附曲线存在明显的滞后环,说明活性炭除了具有微孔,还有一部分中孔。
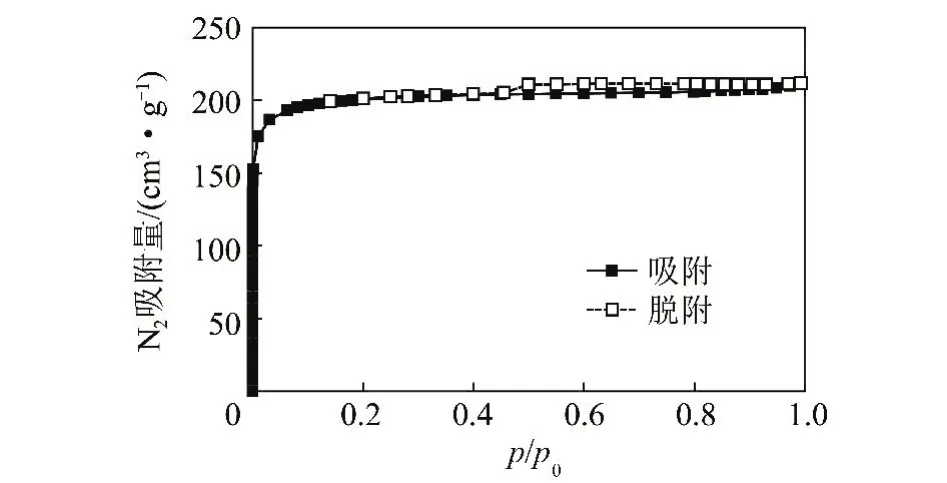
图2 活性炭的N2吸附/脱附等温线Fig.2 N2adsorption/desorption isotherms of activated carbon
活性炭的孔隙结构参数:比表面积为605.008 m2/g,微孔表面积为514.780 m2/g,微孔容积为0.271 cm3/g,总孔容积为0.326 cm3/g,平均孔径为2.154 nm。可见活性炭具有较大的比表面积和发达的微孔结构,微孔容积占总孔容积的比例较大。SO2,O2,H2O分子的动力学直径分别为0.411, 0.346,0.264 nm,均小于活性炭的平均孔径,SO2, O2,H2O分子能够扩散到活性炭的微孔中。
2.2 SO2在活性炭上的吸附动力学
图3为活性炭吸附SO2随时间的变化过程,在吸附的初始阶段,SO2吸附量增加较快,呈现较快的吸附速率;随着吸附的进行,活性炭的吸附速率急剧下降,达到一定的吸附时间后下降幅度开始变缓,SO2吸附量增加缓慢,直至达到SO2吸附平衡。
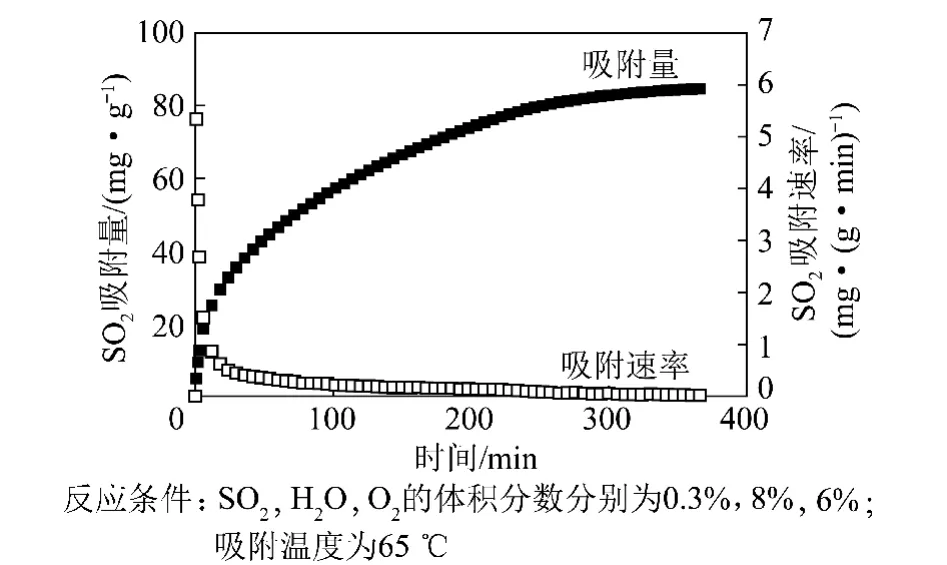
图3 活性炭吸附SO2随吸附时间的变化曲线Fig.3 The change curves of SO2adsorption onactivated carbon with time
SO2在活性炭表面的吸附过程包括气膜扩散、孔内扩散和表面吸附,只有当吸附质分子从气相扩散到活性炭微孔表面时,吸附反应才会发生,吸附速率由其中最慢的一步控制,通常气膜扩散的速率较大,吸附过程不由气膜扩散控制[7]。为了研究活性炭对SO2的吸附动力学特性,确定适合于描述吸附过程的吸附动力学模型,采用粒内扩散模型和Bangham吸附动力学模型对实验数据进行分析。
粒内扩散模型[7,15-17]为
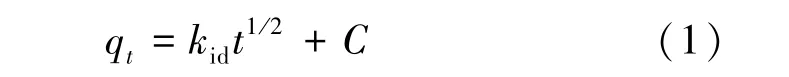
其中,qt为t时刻活性炭对SO2的吸附量,mg/g;kid为粒内扩散速率常数,mg/(g·min1/2);C为常数。如果qt~t1/2呈现线性关联,说明SO2在活性炭上的吸附为粒内扩散过程控制。
图4为qt~t1/2之间的关系,二者在整个吸附过程中不符合直线关联,而是呈现分阶段线性关系,说明在不同的吸附阶段存在不同的反应机制控制吸附过程[16-17]。在初始阶段,快速的吸附速率是由于在活性炭表面附近微孔发生吸附,活性炭表面空的活性位多,SO2首先在活性炭上进行很快的物理吸附,然后发生催化氧化反应;随着反应的进行,一些表面活性位被SO2占据,一些活性位被生成的H2SO4所覆盖,SO2需要扩散到活性炭内部微孔中的活性位上发生吸附,粒内扩散在该阶段起主要作用,因此吸附速率快速下降;达到一定的吸附时间后活性位基本上被占据,部分H2SO4从活性位上脱附而空出活性位继续吸附氧化SO2,该阶段吸附速率与H2SO4的脱附速率有关[8],吸附速率缓慢,逐渐降低直至达到吸附平衡。
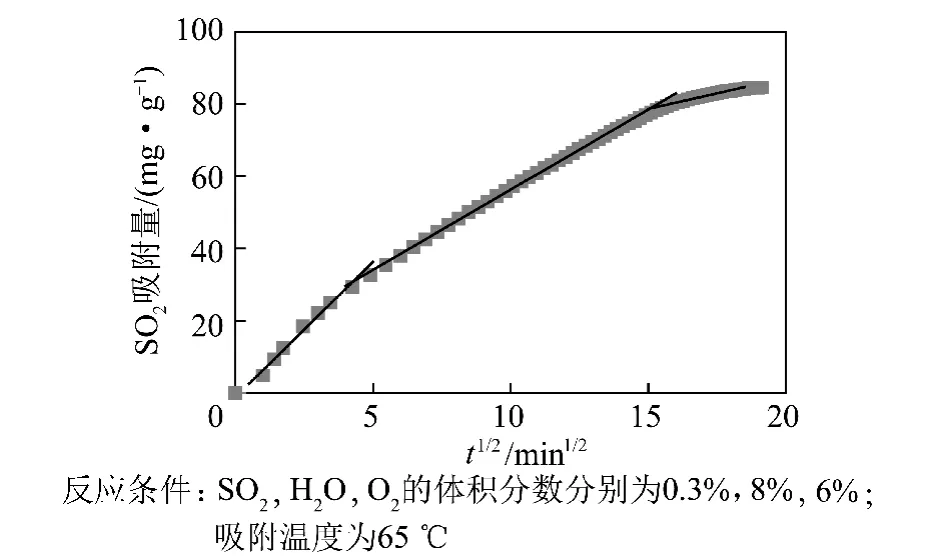
图4 粒内扩散模型Fig.4 Intraparticle diffusion model
Bangham吸附动力学模型[12,18]的表达式为

式中,qe为SO2的平衡吸附量,mg/g;k为常数, min-n;n为常数。
Bangham吸附动力学模型对SO2在活性炭上的吸附随时间变化的拟合曲线如图5所示,表1为拟合的相关参数(包括SO2吸附过程中粒内扩散控制阶段的粒内扩散模型拟合参数)。可以看出,Bangham模型的计算值和实验值吻合良好,相关性系数R2值较高,说明SO2在活性炭上的动态吸附过程可以用Bangham模型较好地描述。
2.3 SO2体积分数、吸附温度对活性炭吸附SO2的影响及吸附等温线分析
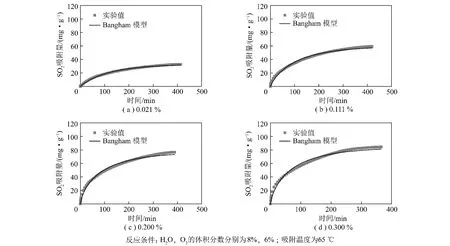
图5 SO2体积分数对活性炭动态吸附SO2的影响Fig.5 Effect of SO2concentration on SO2adsorption on activated carbon
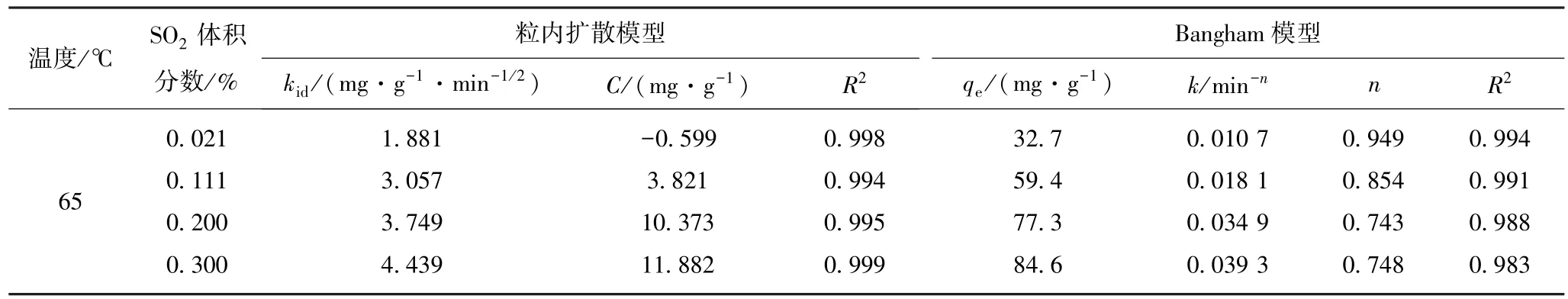
表1 粒内扩散模型和Bangham模型拟合相关参数Table 1 Parameters of intraparticle diffusion model and Bangham model fitting
图5为吸附温度65℃时,SO2体积分数对活性炭吸附SO2的影响。随着SO2体积分数的增加,SO2吸附量逐渐增加,SO2初始吸附速率增加较多,后期趋于相同。当SO2体积分数从0.021%增加到0.300%时,SO2平衡吸附量从32.7 mg/g增加到84.6 mg/g。从表1可知,粒内扩散阶段,粒内扩散速率常数随着SO2体积分数的增加而增加。SO2体积分数增加,增加了气相和活性炭表面SO2的浓度差,增加了吸附的驱动力用来克服从气相到活性炭表面的传质阻力,从而增加了活性炭对SO2的初始吸附速率和平衡吸附量。但SO2平衡吸附量并不随着SO2体积分数的增加而成线性增加,这是由活性炭脱除烟气中SO2的机理决定的:在烟气条件下,由于烟气中水蒸气和O2的存在,活性炭不仅作为吸附剂而且作为催化剂,烟气中的SO2被活性炭吸附并催化氧化为H2SO4,储存在活性炭微孔内。在吸附过程中,活性位不断被占据,没有显著的再生发生[12],同时,活性炭的微孔容积是一定的。
吸附温度是影响活性炭脱硫的重要因素,温度影响到SO2在活性炭表面的吸附和催化氧化,从吸附角度来说,气相中分子在固体表面的吸附是一个瞬间过程,伴随着体系自由能的减少,同时也损失其自由度,导致焓的减少,无论是哪种吸附力,吸附过程总是放热的,因此温度升高对气体吸附不利;从表面催化氧化反应角度来讲,化学反应存在化学键的断裂和生成,需要一定的温度条件。图6为吸附温度对活性炭吸附SO2的影响,随着温度的升高,SO2初始吸附速率及平衡吸附量逐渐降低。活性炭脱除烟气中的SO2首先是一个吸附过程,SO2在活性炭表面进行物理吸附,然后在O2和H2O的作用下被活性炭催化氧化为H2SO4,SO2,O2,H2O在活性炭表面的吸附可能是整个反应过程的控制步骤。温度对物理吸附影响较大,随着温度的升高,降低了SO2的物理吸附,进而影响了SO2在活性炭上的催化氧化,另外,随着温度的升高,水蒸气的吸附量下降非常明显,使生成的H2SO4不能及时从活性位上脱附[19],从而导致SO2初始吸附速率及平衡吸附量降低。
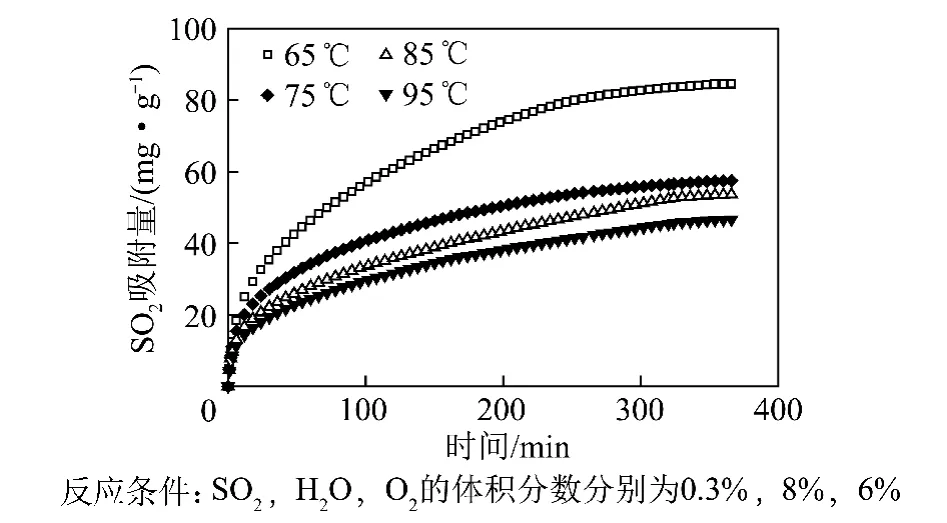
图6 吸附温度对活性炭吸附SO2的影响Fig.6 Effect of temperature on SO2adsorption on activated carbon
气体在活性炭表面的吸附平衡通常用Langmuir吸附等温线模型和Freundlich吸附等温线模型描述。
Langmuir吸附等温线模型假设吸附发生在均匀表面的单分子层定位吸附,忽略被吸附分子之间的横向相互作用,方程[14,20]为
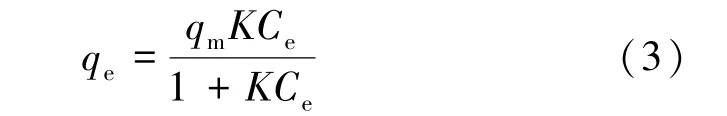
式中,qm为SO2在活性炭上的单分子层最大吸附量,mg/g;K为与吸附剂和吸附质之间的亲和力有关的Langmuir吸附常数,L/mmol;Ce为SO2的吸附平衡浓度,mmol/L。
通过转化,将式(3)线性化为

Freundlich吸附等温线模型假设吸附热在非均匀表面随着表面覆盖度的增大而呈对数规律降低,方程[14,20]为

其中,KF为与温度、吸附剂有关的吸附常数,mg· L1/n/(g·mmol1/n);n′为与温度、吸附强度有关的无因次常数。对式(5)线性化得到

吸附温度分别为65,75,85,95℃时,利用Langmuir和Freundlich吸附等温线模型的线性形式对SO2在活性炭上的吸附平衡数据进行拟合,结果如图7所示,拟合的相关参数见表2。

图7 SO2在活性炭表面的吸附平衡数据拟合Fig.7 Linear fitting of adsorption equilibrium of SO2on activated carbon
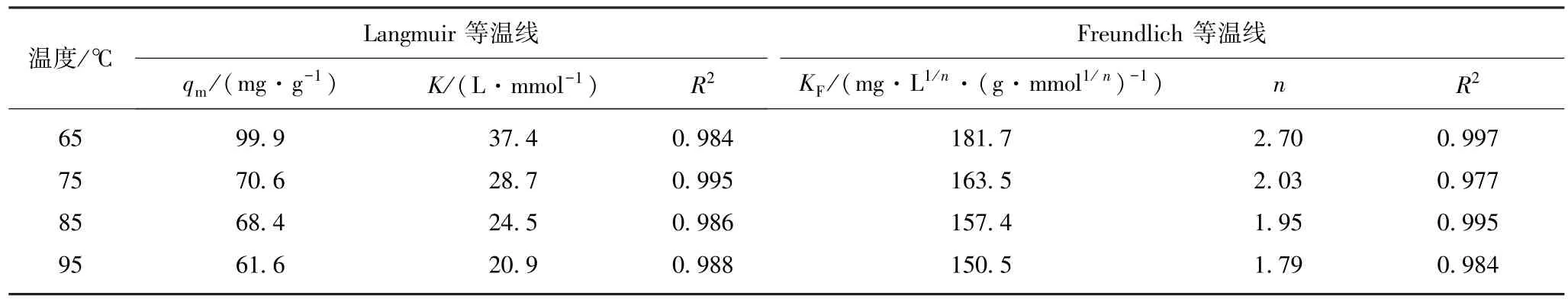
表2 吸附等温线模型拟合的相关参数Table 2 Parameters of linear fitting of adsorption equilibrium
结果表明,Freundlich和Langmuir吸附等温线模型都能很好地描述活性炭对SO2的吸附,qm,K,KF,n随着温度的升高而降低,升温不利于反应的进行。Freundlich模型中的参数n值大于1,说明SO2易于被活性炭吸附。
2.4 吸附热力学
研究吸附热力学可以了解吸附过程的趋势、程度和驱动力,对解释吸附特点、规律以及吸附机理有着重要意义。吸附过程的各热力学参数的变化一般由Gibbs方程和Vant’Hoffs方程计算得到[21-22],即

式中,R为气体常数,取8.314 J/(mol·K);T为热力学温度,K;ΔG为吸附自由能变,kJ/mol;ΔH为吸附焓变,kJ/mol;ΔS为吸附熵变,J/(mol·K);K′为常数。
以ln K对1/T作图,结果如图8所示。活性炭对SO2的吸附热力学参数的计算结果见表3。从表3可以看出,吸附自由能变ΔG为负值,表明活性炭对SO2的吸附是自发过程,且随着温度的升高,ΔG绝对值降低,表明随着温度的升高,吸附过程自发趋势降低,升温不利于吸附的进行;吸附焓变ΔH为负值,说明该吸附过程为放热反应,并且吸附焓变的数值与SO2的汽化潜热相当,说明烟气中SO2在活性炭上的吸附脱除过程中SO2的物理吸附是必须的;吸附熵变ΔS为负值,说明活性炭对SO2的吸附使得吸附质分子的自由度减少,吸附过程熵减少。
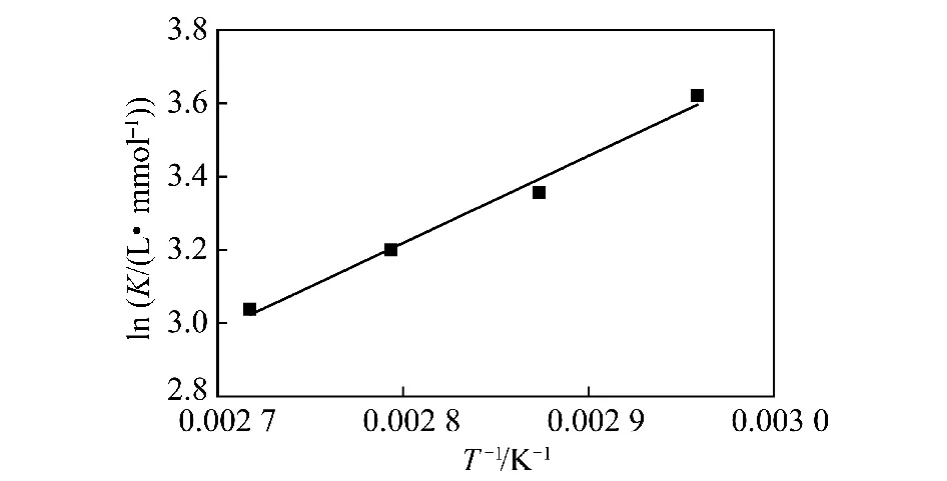
图8 SO2在活性炭上吸附的ln K对1/T的关系Fig.8 The relationship between ln K and 1/T for SO2adsorption on activated carbon
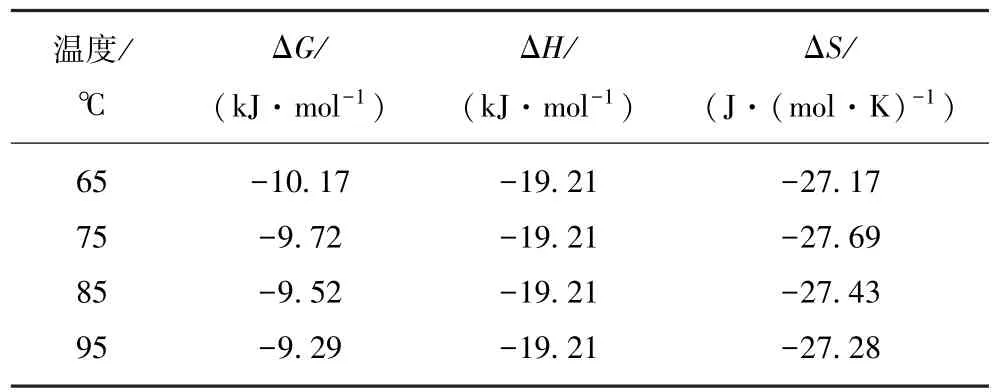
表3 SO2在活性炭上的吸附热力学参数Table 3 Thermodynamic parameters of SO2adsorption on activated carbon
3 结 论
(1)活性炭吸附SO2在初始阶段呈现较快的吸附速率,该阶段SO2吸附速率和表面吸附有关;随着吸附的进行,表面活性位逐渐被占据,SO2需要扩散到活性炭内部微孔中的活性位上发生吸附,活性炭的吸附速率急剧下降,粒内扩散起着主要作用;在接近吸附饱和阶段,SO2吸附量增加缓慢直至吸附平衡,该阶段与H2SO4的脱附有关。SO2在活性炭上的动态吸附过程遵循Bangham吸附动力学模型。
(2)随着SO2体积分数的增加,SO2初始吸附速率和平衡吸附量增加;随着吸附温度的增加,SO2初始吸附速率和平衡吸附量降低。用Langmuir和Freundlich吸附等温线模型拟合吸附数据,发现Langmuir和Freundlich模型能够很好地预测SO2在活性炭表面的吸附平衡。
(3)吸附热力学研究表明,SO2在活性炭上的吸附过程中,焓变为-19.21 kJ/mol,吸附自由能变为-10.17~-9.29 kJ/mol,吸附熵变为-27.69~-27.17 J/(mol·K),该吸附过程是一个自发、放热、熵降低过程,升温不利于SO2的吸附。
[1] Mochida I,Korai Y,Shirahama M,et al.Removal of SOxand NOxover activated carbon fibers[J].Carbon,2000,38(2):227-239.
[2] Jastrzab K.Properties of activated cokes used for flue gas treatment in industrial waste incineration plants[J].Fuel Processing Technology,2012,101:16-22.
[3] 李 兵,蒋海涛,张立强,等.SO2在活性炭表面的吸附平衡和吸附动力学[J].煤炭学报,2012,37(10):1737-1742.
Li Bing,Jiang Haitao,Zhang Liqiang,et al.Adsorption equilibrium and kinetics of SO2on activated carbon[J].Journal of China Coal Society,2012,37(10):1737-1742.
[4] 李兰廷.活性焦干法联合脱硫脱硝的正交实验[J].煤炭学报, 2009,34(10):1400-1404.
Li Lanting.Orthogonal test on combined desulphurization and denitrification by activated char[J].Journal of China Coal Society, 2009,34(10):1400-1404.
[5] 刘少俊,高 翔,曹飞飞.化学性质对活性炭脱硫的影响[J].煤炭学报,2013,38(7):1242-1247.
Liu Shaojun,Gao Xiang,Cao Feifei.Effect of chemical properties on SO2removal by activated carbons[J].Journal of China Coal Society,2013,38(7):1242-1247.
[6] 李兰廷.活性焦脱硫脱硝的机理研究——烟气组成的影响[J].煤炭学报,2010,35(S):185-189.
Li Lanting.Mechanism of removal of SO2and NO on activated coke: Effect of component of flue gas on activated coke[J].Journal of China Coal Society,2010,35(S):185-189.
[7] 尹艳山,张 军,盛昌栋.NO在活性炭表面的吸附平衡和动力学研究[J].中国电机工程学报,2010,30(35):49-54.
Yin Yanshan,Zhang Jun,Sheng Changdong.Adsorption equilibrium and kinetics of NO removal on activated carbons[J].Proceedings of the CSEE,2010,30(35):49-54.
[8] 步学朋,徐振刚,李文华,等.活性焦性质对脱除SO2性能的影响研究[J].煤炭学报,2011,36(5):834-839.
Bu Xuepeng,Xu Zhengang,Li Wenhua,et al.The effects of activated coke properties on SO2removal[J].Journal of China Coal Society,2011,36(5):834-839.
[9] Karatepe N,Orbak I,Yavuz R,et al.Sulfur dioxide adsorption by activated carbons having different textural and chemical properties[J].Fuel,2008,87(15-16):3207-3215.
[10] Plazinski W,Rudzinski W,Plazinska A.Theoretical models of sorption kinetics including a surface reaction mechanism:A review[J].Advances in Colloid and Interface Science,2009,152(1-2):2-13.
[11] 余兰兰.污泥吸附剂的制备及其应用研究[D].南京:南京理工大学,2006.
Yu Lanlan.Study on preparation of adsorbents made from sewage sludges and their application[D].Nanjing:Nanjing University of Science&Technology,2006.
[12] 高继贤.移动床炭法变温吸附烟气净化与硫回收过程研究[D].北京:清华大学,2010.
Gao Jixian.Studies of flue gas purification and sulfur recovery process by carbon moving bed temperature swing adsorption method [D].Beijing:Tsinghua University,2010.
[13] Choi J W,Choi N C,Lee S J,et al.Novel three-stage kinetic model for aqueous benzene adsorption on activated carbon[J].Journal of Colloid and Interface Science,2007,314(2):367-372.
[14] 章燕豪.吸附作用[M].上海:上海科学技术文献出版社,1989.
Zhang Yanhao.Adsorption[M].Shanghai:Shanghai Science and Technology Literature Press,1989.
[15] Rudzinski W,Plazinski W.Kinetics of dyes adsorption at the solidsolution interfaces:A theoretical description based on the two-step kinetic model[J].Environment Science and Technology,2008,42 (7):2470-2475.
[16] Kebbedy L J,Vijaya J J,Sekaran G.Equilibrium,kinetic and thermodynamic studies on the adsorption of m-cresol onto microand mesoporous carbon[J].Journal of Hazardous Materials,2007, 149(1):134-143.
[17] Senthilkumaar S,Varadarajan P R,Porkodi K.Adsorption of methylene blue onto jute fiber carbon:Kinetics and equilibrium studies [J].Journal of Colloid and Interface Science,2005,284(1):78-82.
[18] 刘 义.活性炭法烟气脱硫机理和应用研究[D].西安:西安交通大学,2003.
Liu Yi.Mechanism and application of activated carbon desulfurization from flue gas[D].Xi’an:Xi’an Jiaotong University,2003.
[19] Kisamori S,Kuroda K,Kawano S,et al.Oxidative removal of SO2and recovery of H2SO4over poly(acrylonitrile)-based activated carbon fibers[J].Energy and Fuel,1994,11:1337-1341.
[20] Gokmen V,Serpen A.Equilibrium and kinetic studies on the adsorption of dark colored compounds from apple juice using adsorbent resin[J].Journal of Food Engineering,2002,53(3):221-227.
[21] 李大伟,陈登宇,朱锡锋.稻壳炭基高比表面多孔氧化硅的表征及Cu(Ⅱ)吸附特性[J].化工学报,2011,62(12):3434-3439.
Li Dawei,Chen Dengyu,Zhu Xifeng.Characterization and Cu(Ⅱ) adsorption property of rice-hust-char-based porous silica with large specific surface area[J].Journal of Chemical Industry and Engineering,2011,62(12):3434-3439.
[22] 姚 超,秦泽勇,吴凤芹,等.直接耐酸性枣红在脱硅稻壳活性炭上的吸附热力学与动力学特性[J].化工学报,2011,62(4): 977-985.
Yao Chao,Qin Zeyong,Wu Fengqin,et al.Kinetic and thermodynamic characteristics of direct fast bordeaux adsorption on activated carbon from silicon-freed rice hull[J].Journal of Chemical Industry and Engineering,2011,62(4):977-985.
Equilibrium,kinetics and thermodynamics of SO2adsorption on activated carbon
LI Bing1,2,XUE Jian-ming1,XU Yue-yang1,WANG Hong-liang1,MA Chun-yuan3,CHEN Jian-min2
(1.GuoDian Science and Technology Research Institute(State Power Environmental Protection Research Institute),Nanjing 210031,China;2.School of Environmental Science and Engineering,Shandong University,Jinan 250100,China;3.National Engineering Laboratory for Coal-fired Pollutants Emission Reduction,Shandong University,Jinan 250061,China)
In order to study the process of SO2adsorption on activated carbon,the flue gas SO2adsorption removal by activated carbon was investigated based on a fixed bed reactor.The effects of SO2inlet concentration and adsorption temperature on SO2adsorption were also investigated and the adsorption equilibrium,kinetics and thermodynamics were analyzed.The initial SO2adsorption rate and the amount of SO2adsorbed increase with the SO2inlet concentration increase,and decrease with the adsorption temperature increase.Langmuir and Freundlich adsorption isotherm model presents a better fitted results for SO2adsorption on activated carbon.The Bangham kinetic model can be used to predict the kinetics of SO2adsorption on activated carbon.The thermodynamics results indicate that the adsorption enthalpy is-19.21 kJ/mol,the Gibbs free energy is-10.17--9.29 kJ/mol,and the entropy is-27.69--27.17 J/ (mol·K),therefore,the adsorption is a spontaneous,exothermic,and entropy decreasing process.The SO2adsorption on activated carbon is unfavorable at higher temperature.
SO2;activated carbon;adsorption equilibrium;adsorption kinetics;adsorption thermodynamics
X701.3
A
0253-9993(2014)10-2100-07
2014-03-26 责任编辑:张晓宁
国家高技术研究发展计划(863)资助项目(2013AA065401)
李 兵(1983—),男,山东聊城人,博士后。Tel:025-58625039,E-mail:13869187893@163.com
李 兵,薛建明,许月阳,等.SO2在活性炭上的吸附平衡、动力学及热力学研究[J].煤炭学报,2014,39(10):2100-2106.
10.13225/j.cnki.jccs.2014.0400
Li Bing,Xue Jianming,Xu Yueyang,et al.Equilibrium,kinetics and thermodynamics of SO2adsorption on activated carbon[J].Journal of China Coal Society,2014,39(10):2100-2106.doi:10.13225/j.cnki.jccs.2014.0400

