不锈钢丝刷电极电解还原硝基苯废水
陈凌峰,谭巧巧,朱梅萍,李玉红
(常熟理工学院 化学与材料工程学院,江苏 常熟 215500)
硝基苯(NB)可用于合成染料、医药、农药、橡胶、塑料助剂、洗涤剂等,其本身也可作为炸药、香料及医药产品,是一种重要的化工原料,因而也是一种常见的有机污染物.硝基苯类污染物进入水体后,由于具有极高的化学稳定性,同时因为毒性很大导致微生物难以降解,因此可以长时间保持不变,造成长久的水体污染.因此对硝基苯类废水的降解研究是环境化学领域重要的课题[1-4].
国内外治理硝基苯废水的各种方法都有各自的优缺点,很难有一种方法能经济高效地将其治理达标[5].一种可行的思路是,先采用电化学还原的方法处理硝基苯废水,使其转为化学活性较强的其他化合物如酚类、苯胺类,甚至苯环出现开环,以利于进一步的化学氧化降解;或者首先使硝基苯类化学物质转为毒性较弱的物质,以利于生物降解的开展[6].
电解法水处理技术的优势在于,无需在水处理过程中添加其他化学药品,设备体积小,占地少,操作简便灵活,污泥量少,后处理极为简单,已在很多废水治理中获得成功[7-8].缺点是,需要考虑电极的损失,如经常采用的铁、铝电极[9-10],金属的消耗不仅是成本的重大来源,也可能造成进一步的环境污染.因此出现了一些惰性的贵金属电极如钌、铱、钛等在电解法处理污染废水的应用,但由于价格昂贵,经济上不适用于处理废水,同时由于目前使用较少,微量溶解的这些贵金属元素对环境的影响还不可知.综上可知,寻找一种无毒、便宜、催化活性较好的电极,对于电解法处理污水非常关键.不锈钢丝刷电极在一定程度上具备了上述特点:不锈钢制备过程中加入一些过渡金属元素,可制备成高比表面积的状态,便宜易得、具有较高催化活性,且具有相当大的化学稳定性[11].
本文研究了采用不锈钢丝刷为阴极,催化电解法处理硝基苯废水.考察了不同电压对电解催化还原产物的影响.采用双波长等吸收消除干扰法和萘乙二胺偶氮光度法分别确定不同电解电压时产物的浓度及其随电解时间的变化.并对不同电压下电解处理的效果进行了比较.
1 材料与方法
1.1 实验材料和仪器
不锈钢丝刷购自安徽晋烨线材有限公司,材质为304不锈钢;石墨电极购自上海弘枫实业有限公司,其余药品均为分析纯,所有药品在使用前未做任何处理.
采用浙江余杭市宏泰电子仪器厂的WYJ-303双组直流稳压电源提供电解电压.电解体系的紫外光谱采用北京普析通用仪器有限责任公司TU-1901型双光束紫外可见分光光度计测量;萘乙二胺偶氮光度法测电解体系中硝基苯、苯胺含量使用的是上海精密科学仪器有限公司的721型分光光度计.
1.2 电解过程
在2.5 L大烧杯中加入约含0.24 g硝基苯、10 g Na2SO4的2 L水溶液,放入石墨电极和不锈钢丝刷电极(中心间距约10 cm),分别用铜导线与稳压电源的正极、负极连接.
电解电压为20 V时,每隔5 min取1 mL电解液稀释10倍后测试其紫外光谱(200~400nm),直至紫外光谱不再变化为止.
电解电压为5 V时,在电解的某一时刻(如5 min)取样100 mL、0.5 mL、0.5 mL、1 mL,以备测试.1 mL样品用于稀释10倍后测其紫外光谱.由于取样量较大,会对原始体系产生影响,因此需重新配置电解液,再于另一电解时刻(如10 min)同样取样.如此循环,取样时间间隔逐渐延长,直至测试结果几乎相同为止.
需要说明的是,不锈钢丝刷电极可以重复使用,几乎不影响电解效果.
1.3 紫外分光光度测量(萘乙二胺偶氮光度法)
1.3.1 硝基苯含量的确定
根据文献[12]测试电解液中硝基苯和苯胺含量.先将0.5 mL样品在酸性条件下与亚硝酸盐重氮化,再与盐酸萘乙二胺偶合,生成紫红色染料,根据波长在545 nm处的吸收进行定量,可测得样品中含苯胺的量.然后在Zn粉还原条件下(可将硝基苯还原为苯胺),再依照上述方法,可测得溶液中苯胺和硝基苯的总量.二者的差值即为试样中硝基苯的含量.此方法中认为干扰物(酚类)对两次测试的扰动是相同的,因此在差值计算中抵消.
1.3.2 苯胺含量的确定
为消除酚类对苯胺测定的干扰,需采用蒸馏法.将1.2节所述100 mL试样置于蒸馏烧瓶中,用4%氢氧化钠溶液调节至碱性,加热蒸馏.待蒸出80 mL时,停止加热,稍冷后,往蒸馏烧瓶中加入20 mL水,继续蒸馏到100 mL蒸馏液为止.取0.5 mL蒸馏液,再采用萘乙二胺偶氮光度法测试苯胺含量.
2 结果与讨论
2.1 电压20 V时的电解结果
2.1.1 电解液的紫外光谱
图1所示为20 V电压下电解液稀释10倍后的紫外光谱随时间的变化.从图中可以看出,随着电解时间的逐渐增加吸收峰位置及强度发生变化,从最初的268 nm(硝基苯的特征吸收峰)左右处有一个吸收峰向230 nm和280 nm处两个吸收峰转变(苯胺的特征吸收).可明显看出,在20 V电压下,硝基苯在阴极逐渐被还原为苯胺.

图1 电压为20 V时电解液稀释10倍后的紫外光谱随时间的变化图.箭头所指为随着时间延长吸收峰值变化的方向
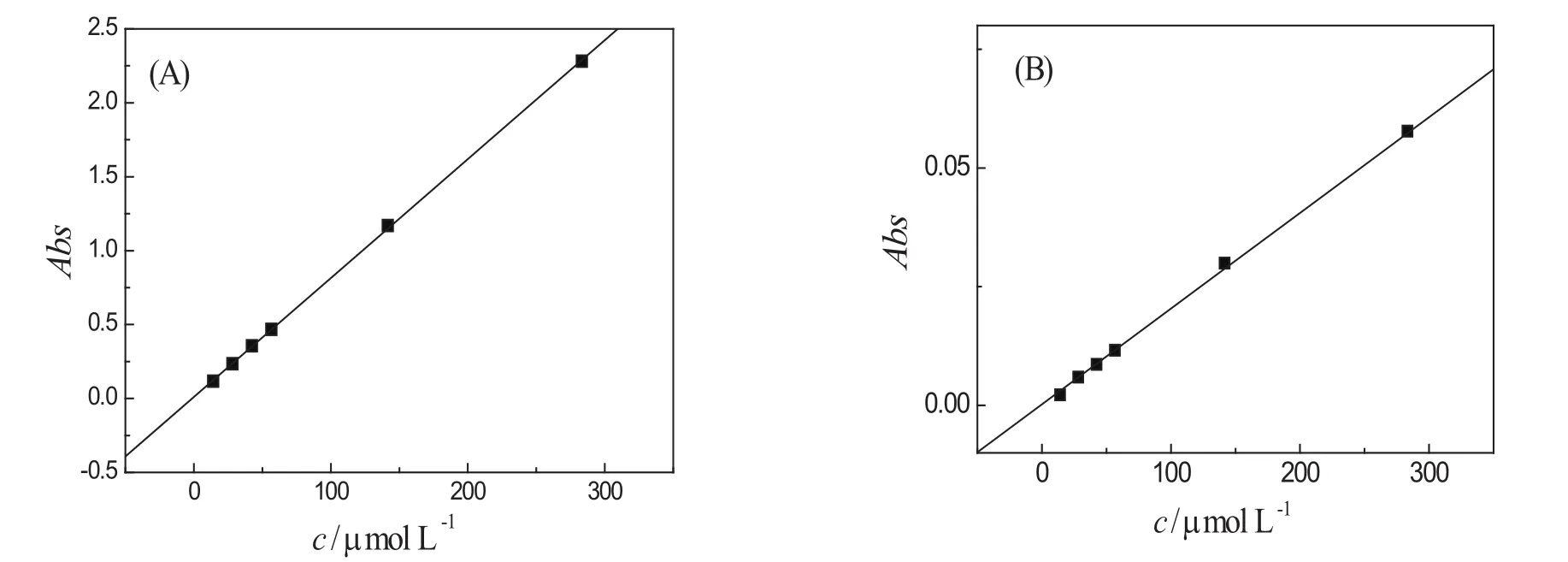
图2 苯胺的吸光度与浓度的关系图
2.1.2 双波长等吸收消除干扰法解谱
为了获得混合体系中硝基苯和苯胺各自的浓度,可应用双波长等吸收消除干扰法[13].苯胺的吸收峰之一处在230 nm处(该处硝基苯吸收相对较弱),工作曲线的测试结果表明,该波长处硝基苯的吸收与302 nm处相同.因此混合体系的230 nm与302 nm处的吸收值的差即可认为是苯胺在该两波长吸收值的差(硝基苯的吸收已完全抵消),再对照相应的回归方程,即可获得苯胺的浓度.图2中给出了230 nm与302 nm处苯胺吸收值的线性回归关系.因此,电解液中苯胺浓度的计算公式为
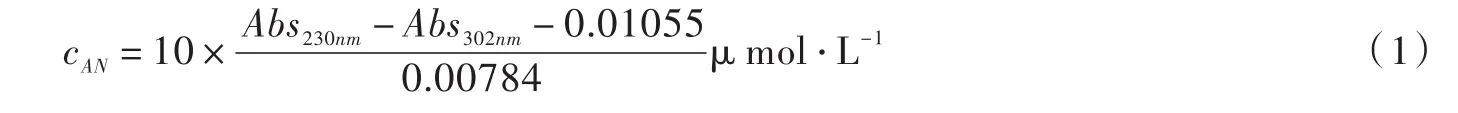
系数10倍是由于紫外光谱是对电解液稀释10倍后进行测量的,用初始硝基苯浓度扣除苯胺浓度,即得电解液中随时间变化的硝基苯浓度.
计算电解液中苯胺及硝基苯浓度所需的吸光度值及计算结果均列于表1中.计算结果同时还表示在图3中.从图3可以看出,在20 V电压下,电解还原大约在70 min达到平衡,约77.1%的硝基苯被还原为苯胺(硝基苯初始浓度为 1023.47 μmol·L-1).
2.2 电压为5 V的电解结果
图4为采用5 V电压电解达90 min时电解液稀释10倍后的紫外光谱.吸收峰位置出现在218 nm、226 nm、230 nm、277 nm、304 nm.230 nm是苯胺的特征吸收,277 nm可以看作是苯胺280 nm和硝基苯268 nm吸收峰叠加的结果.此外218 nm和226 nm峰的出现表明可能产生了马来酸(其特征峰在211 nm)[14]与苯胺特征峰的叠加;304 nm表明电解可能同时产生了对苯二酚(特征峰为290 nm)[15]和对硝基苯酚(在317 nm有特征峰)[16].由此可见,电压降低后体系的组成变得复杂,双波长等吸收消除干扰法不再适合分析电解产物成分.因而采用萘乙二胺偶氮光度法.该方法定量所需的工作曲线见图5,硝基苯和苯胺含量的求解结果表示在表2和图6中.
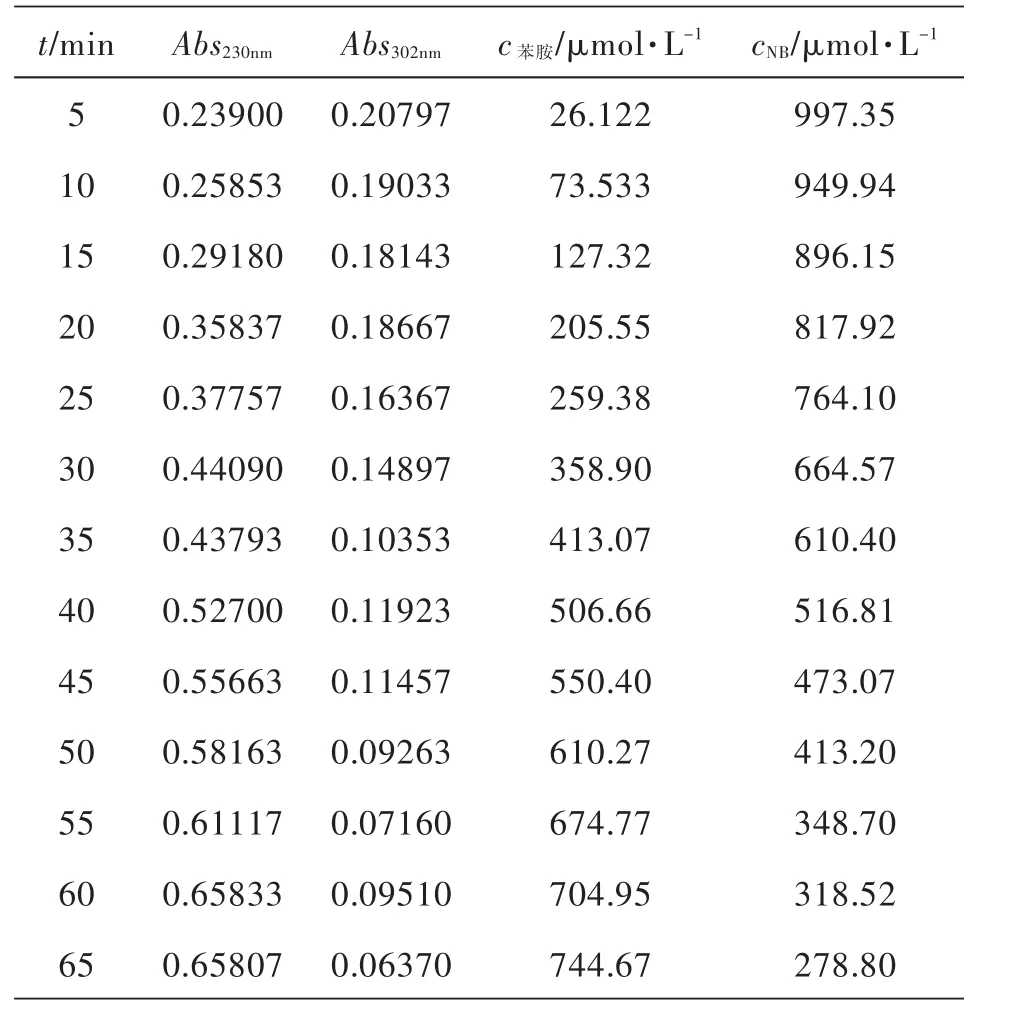
表1 电压20 V时电解硝基苯溶液双波长等吸收消除干扰法解得苯胺、硝基苯浓度
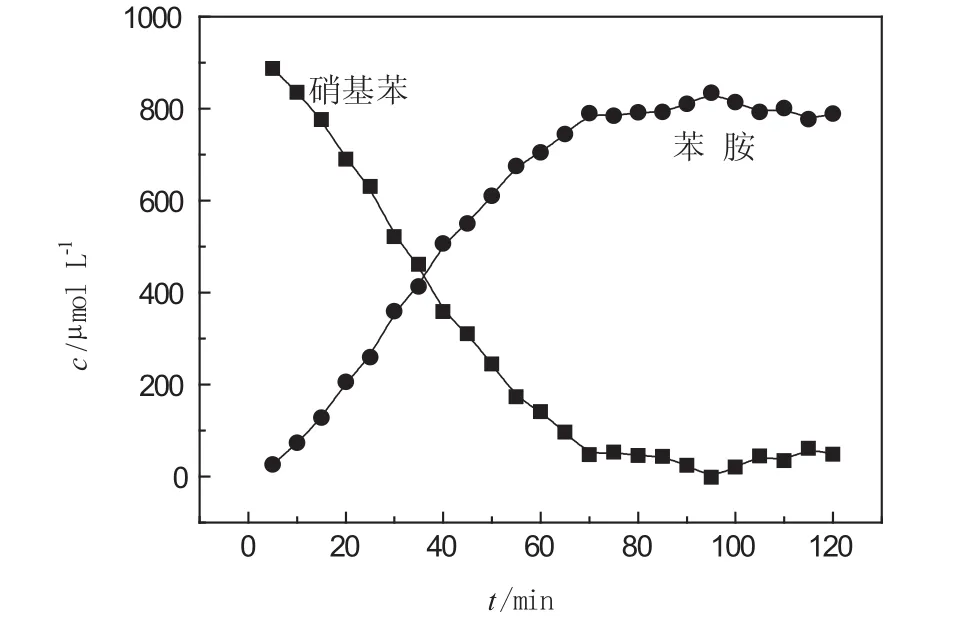
图3 双波长等吸收消除干扰法解谱所得电解液中硝基苯、苯胺浓度与时间的关系图
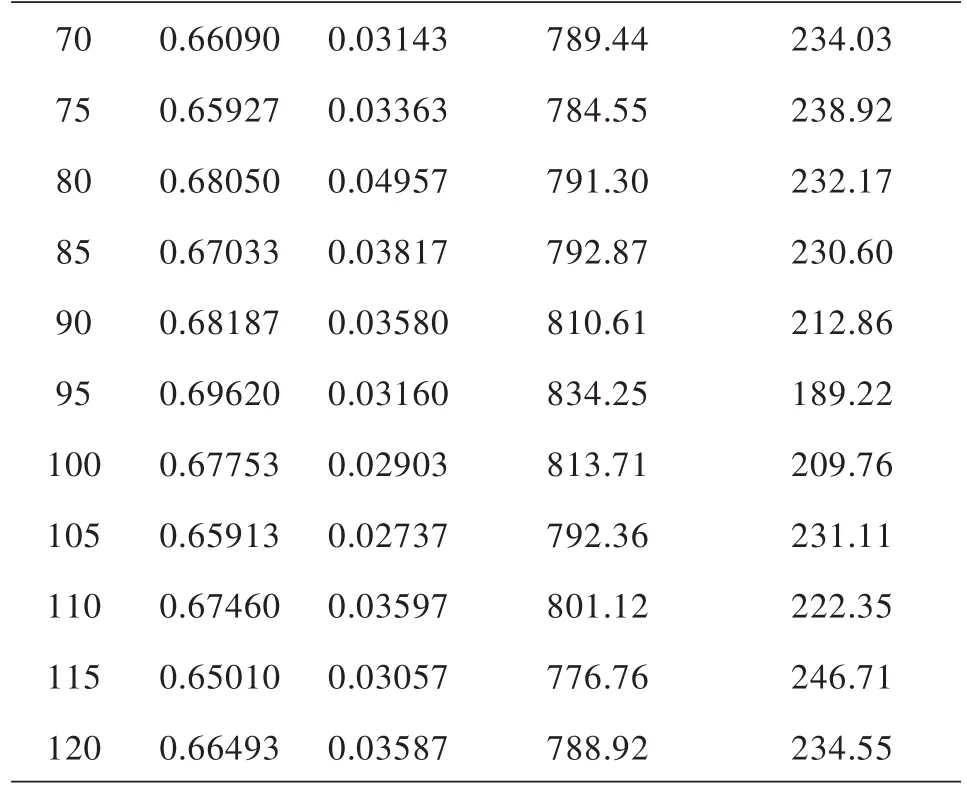
续表1
由图6可看出,5 V电压时大约需要90 min硝基苯转化率达到最大(约98.1%,硝基苯初始浓度为 9 74.74 μmol·L-1).需要注意的是,产物苯胺的浓度虽然也在90 min达到最大值,但其浓度远小于硝基苯浓度下降的值,这也印证了图4的结果,说明硝基苯还被还原为其他物质;此后苯胺的浓度并没有保持不变,而是继续下降,说明苯胺和其他产物之间可能发生了反应.
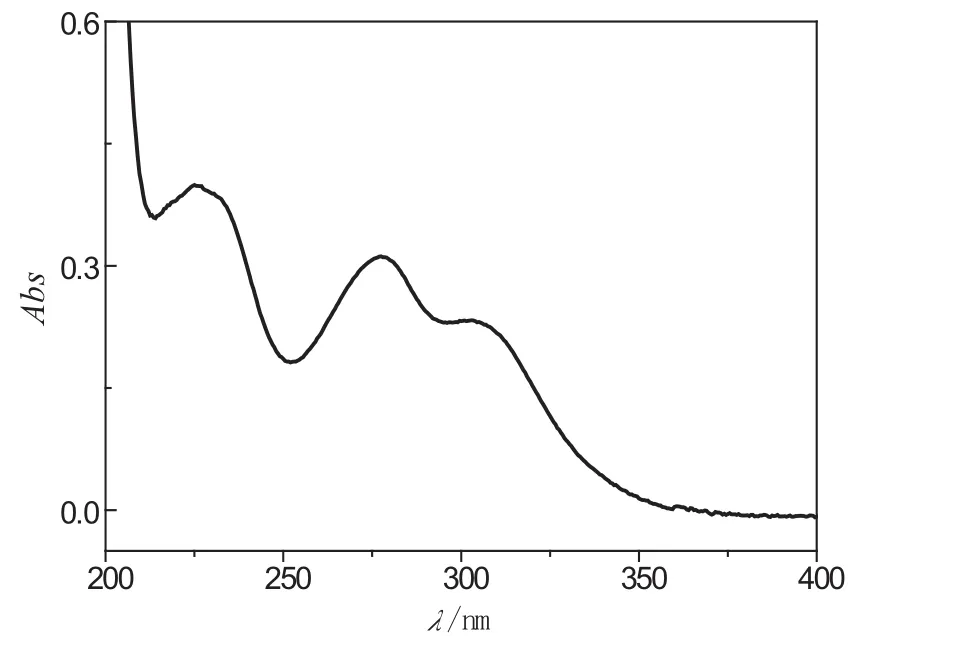
图4 电压为5 V,电解体系90 min时电解液稀释10倍后的紫外光谱
3 结论
本研究讨论了电解电压对应用不锈钢丝刷作为阴极电解还原硝基苯废水结果的影响.20 V电压下,硝基苯被单一地还原为苯胺,约需70 min转化率可达最大值(77.1%);5 V电压下,硝基苯的还原产物除苯胺外,可能还有马来酸、对苯二酚和对硝基苯酚,约需90 min硝基苯转化率可达最大值(98.1%).本研究表明采用不锈钢刷电极可以有效地对高毒性、高稳定性的硝基苯废水进行预处理,以提高其进一步反应、降解的可能性.
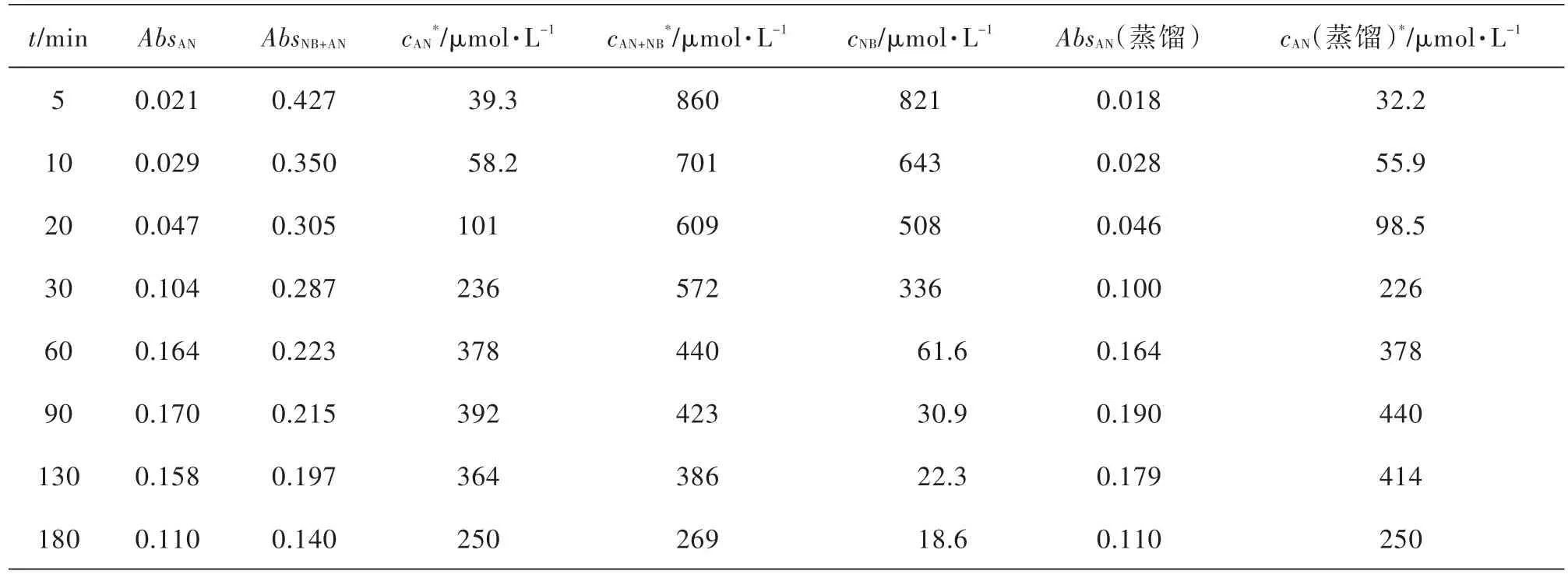
表2 电压为5 V时电解后硝基苯和苯胺含量的确定
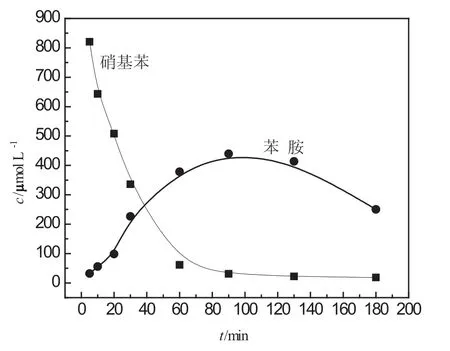
图6 5 V电解体系硝基苯和苯胺含量随时间的变化
[1]于凌,张凤君,王丹瑞,等.纳滤-Fenton试剂联合作用处理硝基苯废水[J].水处理技术,2011,37(3):68-71.
[2]孙猛,赵勇胜,董军,等.地下环境中Fe2+对硝基苯的还原衰减作用模拟研究[J]. 环境科学,2011,32(5):1372-1376.
[3]Casado J,Fornaguera J,Galán M I.Mineralization of Aromatics in Water by Sunlight-Assisted Electro-Fenton Technology in a Pilot Reactor[J].Environ Sci Technol,2005,39(6):1843-1847.
[4]Rodgers J D,Bounce N J.Electrochemical Treatment of 2,4,6-Trinitro⁃toluene and Related Compounds[J].Environ Sci Technol,2001,35(2):406-410.
[5]唐萍,周集体,王竞.硝基苯废水治理的研究进展[J].工业水处理,2003,23(3):16-19.
[6]秦娜娜,查磊,李磊磊,等.外电流直接电解法处理硝基苯废水的研究[J].水处理技术,2010,36(12):117-121.
[7]Zhong S T,Zhao W,Sheng C,et al.Mechanism for Removal of Organic Sulfur from Guiding Subbituminous Coal by Electrolysis[J].Energy Fuels,2011,25(8):3687-3692.
[8]Kishimoto N,Matsuda N.Bromate Ion Removal by Electrochemical Reduction Using an Activated Carbon Felt Electrode[J].Envi⁃ron Sci Technol,2009,43(6):2054-2059.
[9]Can O T,Bayramoglu M,Kobya M.Decolorization of Reactive Dye Solutions by Electrocoagulation Using Aluminum Electrodes[J].Ind Eng Chem Res,2003,42(14):3391-3396.
[10]Caňizares P,Martínez F,Carmona M,et al.Continuous Electrocoagulation of Synthetic Colloid-Polluted Wastes[J].Ind Eng Chem Res,2005,44(22):8171-8177.
[11]Call D F,Merrill M D,Logan B E.High Surface Area Stainless Steel Brushes as Cathodes in Microbial Electrolysis Cells[J].Envi⁃ron Sci Technol,2009,43(6):2179-2183.
[12]魏复盛.水和废水监测分析方法[M].4版.北京:中国环境科学出版社,2002:515-517.
[13]李丽华,张金生,尹学博,等.微波消解-双波长等吸收分光光度法同时测定合金钢中钴和镍[J].冶金分析,2001,21(1):27-29.
[14]高翠英,孟俊亮,李彦威.紫外分光光度法测定马来酸含量[J].太原理工大学学报,2008,39(3):230-240.
[15]牟建.紫外光谱法测定苯酚与苯胺和对苯二酚[J].环境科学与技术,2011,34(6G):249-252.
[16]高丽丽,亚森江·库那洪,魏琳,等.紫外可见光谱谱峰归一校正法检测对硝基苯酚[J].环境科学与技术,2011,34(2):111-114.

