白眉蛇毒血凝酶治疗上消化道出血的系统评价
高红瑾 ,王少明,庄 捷(.福建省立医院药学部,福建 福州 35000;2.福建医科大学省立临床医学院,福建 福州 35000)
上消化道出血(upper gastrointestinal bleeding,UGIB)起病急、进展快,常表现为急性大量出血,危及患者生命,是消化系统常见临床急症,我国报道的病死率为2.5% ~10.0%[1-2]。该病以呕血和黑便为主要症状,常见病因为消化性溃疡、食管胃底静脉曲张、急性胃黏膜病变和胃癌[3]。我国自主研发的白眉蛇毒血凝酶是从长白山白眉蝮蛇蛇毒中提取的含凝血酶和类凝血酶的复合制剂,其止血机制为促使纤维蛋白原降解生成纤维蛋白,后者在血管破损处吸附血小板,形成止血栓[4],其是具有靶向作用的生物制剂,仅在出血部位产生作用,并不使血液处于高凝状态[5]。国内学者已进行不少关于其治疗上消化道出血的疗效观察,但存在单个研究样本量小、随机方法描述不清楚、盲法及统计学处理不明确等不足。本文利用循证医学的基本原理和方法对白眉蛇毒血凝酶治疗上消化道出血进行综合分析,旨在为白眉蛇毒血凝酶治疗上消化道出血的疗效提供循证医学证据。
1 资料与方法
1.1 研究类型
选择随机对照试验(randomized controlled trial,RCT)。
1.2 研究对象
经临床确诊为上消化道出血的患者,患者年龄、性别、发病时间不限。
1.3 干预措施
研究组:采用白眉蛇毒血凝酶联合常规治疗方案。对照组:采用常规治疗方案。其他干预措施在2 组间一致。
1.4 观察指标
(1)24、48、72 h 内止血率;(2)无效率,出血停止时间>72 h 或因出血死亡视为无效;(3)不良反应发生率。
1.5 排除标准
(1)联用其他药物影响治疗因果关系判断者;(2)虽为RCT 但采用自身对照者;(3)重复发表的研究。
1.6 检索策略
通过计算机检索中国知网服务条纹(CNKI)、万方数据知识服务平台(WANFANG DATA)、中国生物医学文献服务系统(SinoMed)、PubMed、OvidSP 等。中文检索词:白眉蛇毒血凝酶、出血;英文检索词:hemocoagulase from agkistrodon halys pallas、hemorrhage、bleeding。检索策略采用全文与摘要相结合的方式,并追溯纳入文献的参考文献,所有检索时限均从数据库建库至2014 年8 月。
1.7 纳入研究质量评价
由研究者将纳入的文献进行整理,按照Cochrane Reviewer's Handbook 随机对照试验的质量标准对文献中所涉及的方法学如随机方法、分配隐藏、盲法及失访/退出4 条内容进行质量评价。若研究满足以上4 条者为A 级;若1 条或1条以上评价标准仅为部分满足者为B 级;若1 条或1 条以上评价标准完全不满足者为C 级。
1.8 统计学方法
所有数据均采用Cochrane 协作网提供的RevMan5.2 软件进行数据统计分析。计数资料采用风险比(risk ratio,RR)或风险差(risk difference,RD)为疗效分析统计量,各效应量均以95%可信区间(95%confidence interval,95%CI)表示。各纳入研究异质性检验采用Cochrane Q 检验,计算I2值。若研究间无统计学异质性(I2≤50%,P≥0.10),选择固定效应模型进行Meta 分析;若存在统计学异质性(I2>50%,P<0.10)则分析异质性产生的原因,当异质性来源不能用临床异质性和方法学异质性解释时采用随机效应模型进行meta 分析。假设检验采用t检验,P<0.05 为差异具有统计学意义,检验水准:α=0.05。异质性检验和统计分析结果均在森林图中列出,采用漏斗图分析可能的发表偏倚。
2 结果
2.1 文献检索结果
初检获得文献161 篇,通过阅读摘要及全文,按照纳入与排除标准剔除149 篇,最终纳入12 篇[6-17]。所有纳入研究均以中文发表,实施地点均在中国;未检索到符合纳入标准的英文研究。
2.2 纳入研究的基本特征
12项研究共纳入1272例患者,其中研究组657 例,对照组615 例。4 项研究的观察对象为多病因(包括消化性溃疡、肝硬化并发食管胃底静脉曲张破裂、胃癌等)上消化道出血患者[6-9],6 项研究的观察对象为消化性溃疡并发出血患者[10-15],1 项研究的观察对象为颅脑损伤并发应激性溃疡出血患者[16],1 项研究的观察对象为食管胃底静脉曲张破裂出血患者[17]。所有研究均对研究组及对照组的治疗方法进行了详细描述,且均有明确的测量指标,见表1。
2.3 纳入研究的方法学质量评价
纳入的12 项研究均提及采用随机方法进行分组,有2 项研究描述了具体随机分组方法,其余均没有具体描述;12 项RCT 中有1 项提及了双盲,其余均未提及盲法;所有RCT 均没有描述具体的分配隐藏情况,见表2。
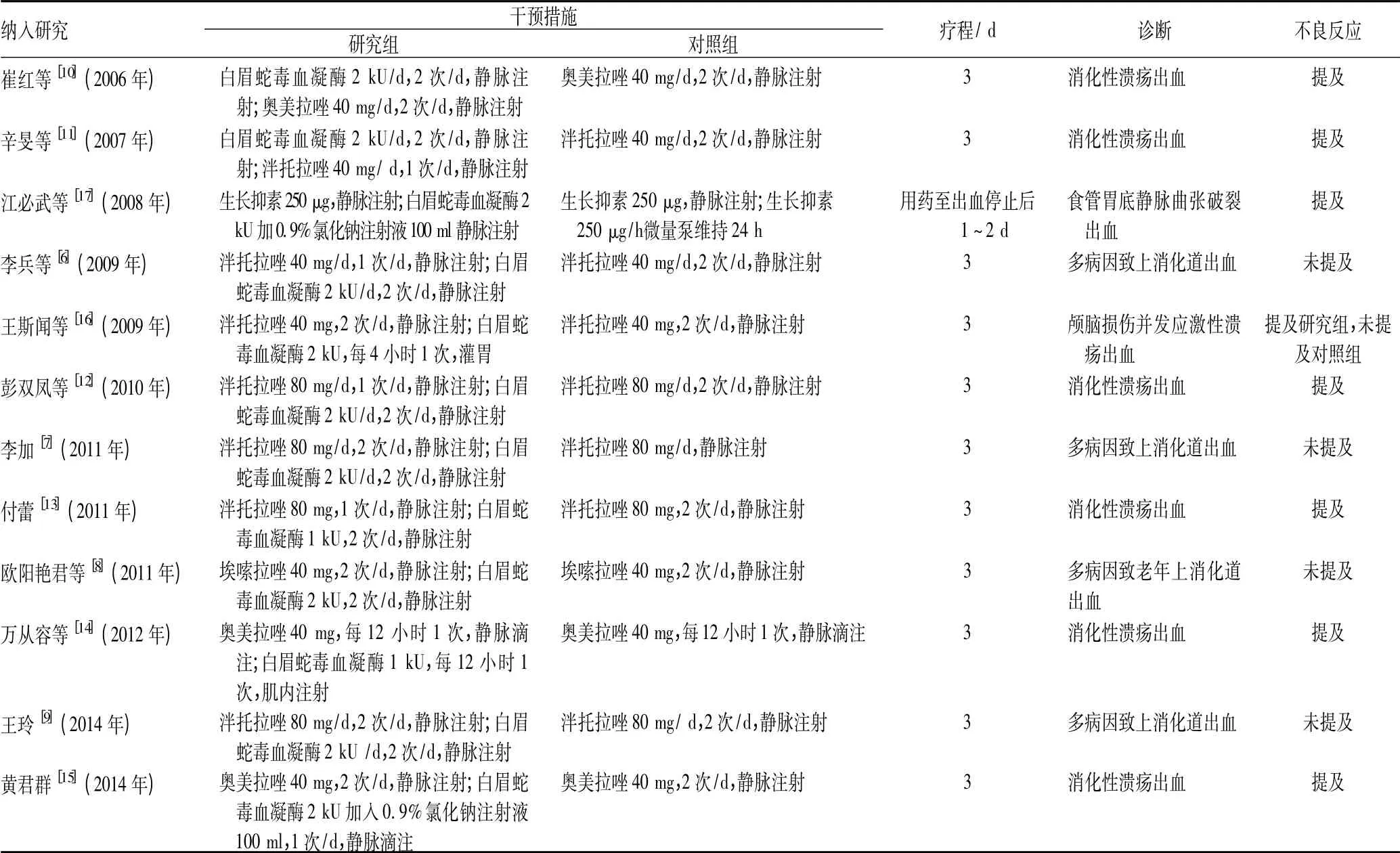
表1 纳入研究基本情况Tab 1 Basic data of the included studies
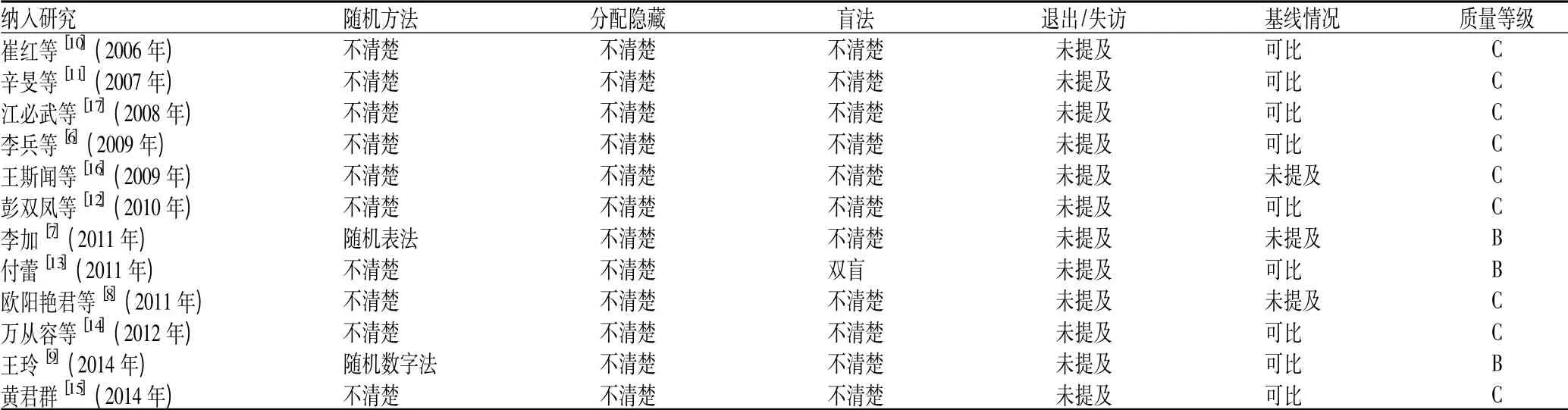
表2 纳入研究的方法学评价Tab 2 Methodological quality assessment of the studies included
2.4 Meta 分析结果
2.4.1 白眉蛇毒血凝酶治疗上消化道出血止血率分析:2 项研究比较了白眉蛇毒血凝酶联合常规治疗与常规治疗24 h 内止血率[15,17],研究间无统计学异质性(I2=0%,P=0.870 0),组间比较差异有统计学意义(RR=1.44,95%CI=1.05 ~1.98,P=0.020 0);7 项研究比较了白眉蛇毒血凝酶联合常规治疗与常规治疗48 h 内止血率[6-12],研究间无统计学异质性(I2=0%,P=0.61),组间比较差异有统计学意义(RR=1.19,95%CI=1.07 ~1.31,P=0.001);3 项研究比较了白眉蛇毒血凝酶联合常规治疗与常规治疗72 h 内止血率[13-14,16],研究间无统计学异质性(I2=9%,P=0.330 0),组间比较差异有统计学意义(RR=1.39,95%CI=1.17 ~1.64,P=0.000 2),见图1。
2.4.2 白眉蛇毒血凝酶治疗上消化道出血无效率分析:12 项研究均比较了白眉蛇毒血凝酶联合常规治疗与常规治疗的无效率[6-17],研究间无统计学异质性(I2=10%,P=0.340 0),研究组治疗上消化道出血无效率明显低于对照组,差异有统计学意义(RR=0.28,95%CI=0.20 ~0.38,P<0.01),见图2。
2.4.3 白眉蛇毒血凝酶治疗上消化道出血的安全性评价:7 项研究观察了研究组和对照组患者的不良反应[10-15,17],其中白眉蛇毒血凝酶组360 例患者,对照组328 例患者。不良反应主要表现为口干、恶心、头晕、皮疹等。研究间无统计学异质性(I2=0%,P=1.000 0),组间比较差异无统计学意义(RD=0.01,95%CI= -0.02 ~0.03,P=0.670 0),表明研究组与对照组的安全性相当,见图3。
2.5 倒漏斗图分析
以止血率结果做倒漏斗图显示不对称分布,提示存在一定的发表偏倚,见图4。
3 讨论
白眉蛇毒血凝酶经十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-polyacrylamide gel electrophoresis,SDS-PAGE)检测含有3 种组分,相对分子质量分别为(54±5)、(34±5)、(15±3)×103,相对百分含量分别为7.0% ~12.0%、76.0% ~82.0%、7.0% ~12.0%,与凝血相关的物质是类凝血酶和类凝血激酶[18]。白眉蛇毒血凝酶中的类凝血酶作用于纤维蛋白原优先释放纤维蛋白肽B,经过一段延滞期后才是纤维蛋白肽A 的释放[19]。在正常血管内,白眉蛇毒血凝酶只发挥类凝血酶样作用而不导致血小板黏附,当血管破损时可发挥类凝血酶样和类凝血激酶样双重作用,不影响血液中凝血酶原数目,且无血栓形成危险[20]。
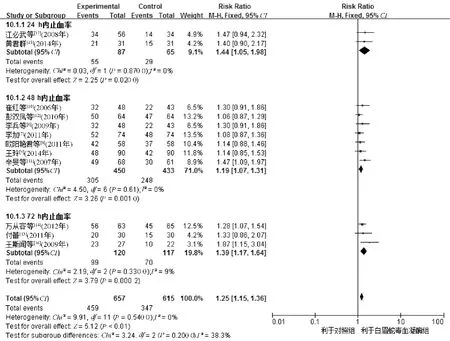
图1 白眉蛇毒血凝酶治疗上消化道出血止血率的Meta 分析Fig 1 Meta-analysis of hemostatic rate in patients with upper gastrointestinal bleeding treated with hemocoagulase from Agkistrodon halys (pallas)
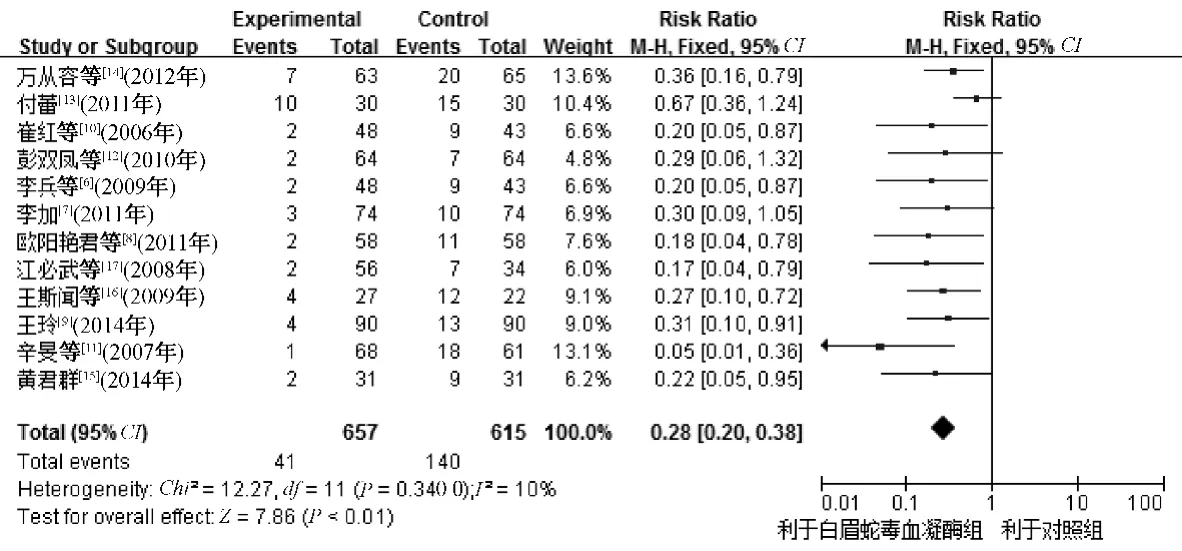
图2 白眉蛇毒血凝酶治疗上消化道出血无效率的Meta 分析Fig 2 Meta-analysis of ineffective rate in patients with upper gastrointestinal bleeding treated with hemocoagulase from Agkistrodon halys (pallas)

图3 白眉蛇毒血凝酶治疗上消化道出血不良反应发生率的Meta 分析Fig 3 Meta-analysis of incidence of adverse drug reactions in patients with upper gastrointestinal bleeding treated with hemocoagulase from Agkistrodon halys (pallas)
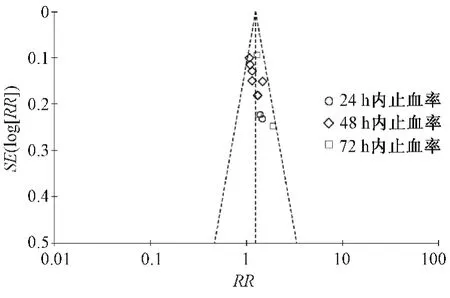
图4 发表偏倚的Meta 分析漏斗图Fig 4 Funnel diagram of meta-analysis of publication bias
本研究的局限性:(1)药物原因,白眉蛇毒血凝酶主要成分为长白山白眉蝮蛇蛇毒中提取而来,主要在国内使用,因此,本研究检索虽不限语种,但检索后纳入文献均为中文,可能因语言偏倚而影响研究结果。(2)纳入研究的RCT 质量不高,存在选择性偏倚、实施偏倚及测量性偏倚的可能性。(3)虽然多数纳入研究进行了基线比较和分析,但存在病情严重程度不一致,使研究中2 组效果的比较差异不能排除是由基线资料不平衡所致。
总之,通过Meta 分析可初步证实,白眉蛇毒血凝酶治疗上消化道出血是安全、有效的,但由于纳入研究的方法质量较低,可能存在发表性偏倚,期待更多高质量的随机双盲对照试验提供高质量的证据。
[1] 许勤,胡乃中,崔小玲.1520 例上消化道出血病因和临床特点分析[J].临床消化病杂志,2011,23(1):12-15.
[2] 闫锁劳.上消化道出血528 例回顾性分析[J]. 基层医学论坛,2011,15(19):618-619.
[3] 索宝军,周丽雅,丁士刚,等. 急性消化道出血的病因及其相关因素分析[J].中华医学杂志,2011,91(25):1757-1761.
[4] 吴广通,张夏华,石玉岚.注射用白眉蛇毒血凝酶止血机制初步研究[J].中国医药导报,2011,8(11):47-49.
[5] 黄俊何.白眉蝮蛇毒血凝酶的药理作用和临床应用[J]. 蛇志,2010,22(1):39-41.
[6] 李兵,林凤.白眉蛇毒血凝酶与泮托拉唑联用在上消化道出血中的应用[J].当代医学,2009,15(9):145.
[7] 李加. 白眉蛇毒血凝酶联合泮托拉唑治疗上消化道出血的临床疗效分析[J].中国医药指南,2011,9(29):277-278.
[8] 欧阳艳君,张艳梅. 注射用白眉蛇毒血凝酶联合埃嗦拉唑治疗老年性上消化道出血疗效观察[J]. 辽宁医学院学报,2011,32(5):403-404.
[9] 王玲.白眉蛇毒血凝酶联合泮托拉唑治疗上消化道出血临床观察[J].实用中医药杂志,2014,30(2):126-127.
[10] 崔红,胡珉.邦亭与洛赛克联用治疗上消化道出血的疗效观察[J].医学理论与实践,2006,19(10):1173-1174.
[11] 辛旻,李莉.注射用白眉蛇毒血凝酶与泮托拉唑联用治疗上消化道出血的疗效观察[J].中国药物与临床,2007,7(9):717-718.
[12] 彭双凤,冯念涛.泮托拉唑与注射用白眉蛇毒血凝酶联用治疗消化性溃疡合并出血的疗效观察[J]. 中国现代药物应用,2010,4(5):59-60.
[13] 付蕾.泮托拉唑联用白眉蛇毒血凝酶治疗消化性溃疡并出血的疗效分析[J].中国医药指南,2011,9(15):116-117.
[14] 万从容,杜安民.国产奥美拉唑与白眉蛇毒血凝酶联合治疗消化性溃疡并出血的临床疗效分析[J].内科,2012,7(5):480-481.
[15] 黄君群.注射用白眉蛇毒血凝酶联合奥美拉唑钠治疗消化性溃疡并发出血的疗效观察[J].临床合理用药杂志,2014,7(15):60-61.
[16] 王斯闻,邹延红,刘丹,等. 胃灌注白眉蛇毒血凝酶治疗颅脑损伤并发应激性溃疡27 例[J]. 医药导报,2009,28(8):1035-1036.
[17] 江必武,吴玉芳,毛德华,等. 白眉蛇毒凝血酶联合生长抑素治疗食管静脉曲张破裂出血的临床观察[J]. 血栓与止血学,2008,14(5):228-229.
[18] 黄仲义.白眉蛇毒血凝酶与血凝酶的对比[J].中国新药与临床杂志,2005,24(7):585-587.
[19] Guan LF,Chi CW,Yuan M. Study on the thrombin-like enzyme preferentially releasing fibrinopeptide B from the snake venom of Agkistrodon halys Pallas[J].Thromb Res,1984,35(3):301-310.
[20] 潘梦垚,王凯英.蛇毒血凝酶研究进展和在临床应用安全性评价[J].生物技术世界,2012(1):4-7.

