基于纤维素的温敏性互穿网络水凝胶的制备与表征
刘晓倩,楚晖娟,魏宏亮,朱 靖,何 娟
(河南工业大学 化学化工学院,河南 郑州 450001)
0 前言
水凝胶是通过物理交联或化学交联形成的亲水的聚合物网络,它能够在水中溶胀而不溶解.由于其特殊的性质,在生物、医学、农业等领域获得了广泛的应用[1].其中,基于纤维素的水凝胶的研究格外引人注目,这是由于纤维素是地球上最丰富、可以再生的天然资源,除具有生物相容性强、可生物降解的优势外,还具备价廉、无毒、无污染等特点.然而,大多数纤维素水凝胶的机械强度较低,功能单一,从而限制了其应用.为了提高水凝胶的机械强度,改善水凝胶的性能,人们常用互穿网络技术(IPN)制备水凝胶[2-3].互穿网络型的水凝胶包含着两个或几个在分子水平上相互交缠的网络,网络之间不存在化学键[4],因此这两种物质均能保持自身原有的特征,水凝胶的性质也可通过控制聚合物的类型及浓度进行调节[5-6].制备IPN 水凝胶主要有同步和顺序两种方法[7].同步法是将所有的反应物全部混匀,要求他们各自的反应互不影响,从而得到相互贯穿的聚合物网络.由于各物质之间的反应没有相互关系,故反应同时进行没有次序之分;顺序法也称分步法,是先在一定条件下制备一种聚合物网络,然后再控制条件形成第二种聚合物网络.本论文采用顺序法形成IPN 水凝胶,依次通过Diels-Alder 反应、光聚合形成两种网络.Diels-Alder 反应是一个可逆的原子经济性反应,具有反应条件温和、不需要催化剂或引发剂、也不需要有机溶剂等优点[8];而光聚合可在室温或生理条件下进行,具有固化速度快,反应可控性强,反应放出的热量少等优点,在制备可注射水凝胶方面有广泛的应用.因此,本论文首先通过Diels-Alder 反应形成纤维素网络,然后通过光聚合引入另一具有温度敏感性的聚(N-异丙基丙烯酰胺)网络,研究了其结构及性能.
1 材料与方法
1.1 原料及仪器
N-异丙基丙烯酰胺、羟丙基甲基纤维素(HPMC)、丁二酸酐:分析纯,阿拉丁试剂有限公司;2,2-二甲氧基-2-苯基苯乙酮:纯度98%,Fluka 公司;顺丁烯二酸酐:分析纯,天津市科密欧化学试剂有限公司;丙氨酸:分析纯,中国惠兴生化试剂有限公司;1,3-二环己基碳二亚胺(DCC)、4-二甲氨基吡啶(DMAP)、糠胺:分析纯,Sigma 公司;其他试剂均为分析纯.N-丙氨酸马来酰亚胺(AMI)及丁二酸糠酰胺(SFA)按照 文献[9]合成,结构式如图1 所示.
光引发剂溶液:将100 mg 的2,2-二甲氧基-2-苯基苯乙酮溶解于1 mL N-乙烯基吡咯烷酮配制得到.
Hitachi S-4300 扫描电镜:日本日立公司;Specode75 型红外光谱仪:日本岛津公司;DHR-1流变仪:美国TA 公司.
1.2 羟丙基甲基纤维素(HPMC)的修饰
参照文献 [9],用AMI 及SFA 修饰羟丙基甲基纤维素得到HPMC-SFA 及HPMC-AMI.其反应过程如图1 所示.

图1 HPMC-AMI 及HPMC-SFA 的合成过程[9]Fig.1 Synthetic route of HPMC-AMI and HPMC-SFA[9]
1.3 互穿网络水凝胶的制备
将N-异丙基丙烯酰胺、HPMC-SFA 及HPMC-AMI按一定的质量比加入到2mL水中,搅拌溶解后,向溶液中加入交联剂聚乙二醇二甲基丙烯酸酯0.0703g,光引发剂溶液0.1mL,混合均匀后将其升温到50℃反应4.5h,发生了基于Diels-Alder反应的凝胶化现象,形成第一网络.
然后将形成的水凝胶置于紫外灯(20 W,365 nm)下照射5min,N-异丙基丙烯酰胺与交联剂发生了光聚合,形成第二网络.将形成的互穿网络水凝胶标记为GelIPN.为了对照,分别制备了只含纤维素网络的水凝胶(记作GelCellulose)及只含聚N-异丙基丙烯酰胺网络的水凝胶(记作GelPNIPAN),投料比见表1.

表1 制备水凝胶时的投料比Table 1 Feeding ratio of raw materials
1.4 水凝胶的表征
1.4.1 扫瞄电镜
将制备好的产品用蒸馏水浸泡,每隔6 h 换水1 次,2 d 后,冷冻干燥48 h,用液氮进行脆断,对样品喷金,用日立公司Hitachi S-4300 扫描电镜观察样品断面的形貌.
1.4.2 红外表征
将干燥后的水凝胶磨成粉末,将样品粉末与干燥的KBr 混合研磨压片,用Specode75 型红外光谱仪在4 000 cm-1到500 cm-1范围内进行红外光谱测定.
1.4.3 溶胀度的测定
取0.3 g 左右的干凝胶称质量(m0),放入一定温度的水中浸泡,每隔一定时间取出,称取水凝胶的质量(m1),按照下列公式计算溶胀度(SR).

1.4.4 流变性的测定
在聚四氟乙烯模具中,制备厚度为1 mm,直径 为 40 mm 的 水 凝 胶,用 Discovery Hybrid Rheometer HR-1(TA Instruments,USA)在温度扫描模式下进行动态流变测试.升温范围25 ℃到60℃,升温速率2 ℃/min.
2 结果与分析
2.1 互穿网络水凝胶的制备过程
为了说明IPN 水凝胶的形成过程,在小瓶a中加入N-异丙基丙烯酰胺、交联剂及光引发剂,在小瓶b 中加入N-异丙基丙烯酰胺、交联剂、HPMC-AMI、HPMC-SFA、光引发剂,在小瓶c 中只加入HPMC-AMI、HPMC-SFA 及光引发剂,加入适量水溶解后,然后让3 个小瓶分别经过加热及光照过程,结果如图2 所示.由图2 可知,在50 ℃下加热4.5 h 后,小瓶b、c 内发生凝胶化,而小瓶a内仍然呈溶液状态,经过光照后,小瓶a 内发生凝胶化.这说明加热不会导致聚(N-异丙基丙烯酰胺)网络的形成,加热只能导致HPMC-SFA 与HPMC-AMI 之间的Diels-Alder 反应,形成纤维素网络.可见,通过Diels-Alder 反应串联光聚合形成互穿网络水凝胶是可行的.

图2 GelPNIPAN(a)、GelIPN(b)、GelCellulose(c)的制备过程Fig.2 Photographs in the process of gel formation:GelPNIPAN(a)、GelIPN(b)、GelCellulose(c)
将GelIPN、GelCellulose与GelPNIPAN冷冻干燥后用液氮脆断,可以防止水凝胶的孔洞结构因失去水分而坍塌破坏,较好地保持了其三维孔洞结构.扫描电镜结果如图3 所示.
由图3 可知,GelPNIPAN结构紧密,孔洞较少;GelCellulose结构疏松,孔洞较大,网状结构不规整.而GelIPN具有排列较整齐的蜂窝状多孔结构,孔洞大小及分布较均匀.由此可知,形成互穿网络后增加了纤维素水凝胶的交联密度及机械强度.
2.2 红外光谱分析
GelPNIPAN(a)、GelIPN(b)、GelCellulose(c)的 红 外 谱图如图4 所示,谱图(a)中3 297 cm-1及3 082 cm-1 分别为N—H 伸缩振动吸收峰和面内弯曲振动倍频峰,1 664 cm-1处附近为酰胺上C=O 伸缩振动吸收峰(酰胺Ⅰ带),1 549 cm-1处附近是由酰胺上N—H 面内弯曲振动及C—N 伸缩振动的组合吸收产生的吸收峰(酰胺Ⅱ带),异丙基上双甲基由于对称振动耦合分裂成的双峰出现在1 367 cm-1、1 388 cm-1.谱图(c)中,3 474 cm-1处强而宽的吸收带是HPMC 上—OH 的伸缩振动引起的,1 057 cm-1为纤维素C—O—C 的特征吸收峰,2 922 cm-1为亚甲基的吸收峰,1 668 cm-1、1 724 cm-1为SFA及AMI 中C=O 的伸缩振动吸收峰,1 457 cm-1、1 374 cm-1、1 297 cm-1、940 cm-1处的吸收峰可分别归属于—CH3的非对称、对称变形振动、面内及面外弯曲振动,由于HPMC 中甲基的含量较少,故而甲基的这些振动较弱.形成互穿网后,由于聚合物链间的相互作用吸收峰的强弱发生改变,但GelIPN同时拥有GelPNIPAN与GelCellulose的特征峰,而没有新的吸收峰出现,故互穿网络水凝胶为物理结合形成.

图3 GelPNIPAN( a)、GelIPN( b)、GelCellulose( c)的SEM 图Fig. 3 SEM images of GelPNIPAN( a)、GelIPN( b)、GelCellulose( c)

图4 GelPNIPAN(a)、GelIPN(b)、GelCellulose(c)的红外谱图Fig.4 FTIR spectra of GelPNIPAN(a)、GelIPN(b)、GelCellulose(c)
2.3 溶胀度的测量
由图5 可知,0~4 h 溶胀速率较快,随着时间的推移,溶胀度的变化逐渐变慢,在8 h 左右趋于平衡.3 种水凝胶在37 ℃下具有较高的溶胀度,其中GelCellulose在水中的溶胀度最大,主要是由于单独的纤维素水凝胶交联密度较低,结构比较疏松,故吸水能力较强,溶胀度较大;GelPNIPAN的交联密度大,结构紧密,孔洞较少,故其溶胀度较小;GelIPN的溶胀度介于纤维素水凝胶和N-异丙基丙烯酰胺水凝胶之间.

图5 GelPNIPAN(a)、GelIPN(b)、GelCellulose(c)的溶胀度随时间的变化曲线Fig.5 The swelling ratio of hydrogels with time GelPNIPAN(a)、GelIPN(b)、GelCellulose(c)
由图6 可知,3 种水凝胶的溶胀度均随温度的升高而下降,其中GelPNIPAN的溶胀度随温度变化最显著,而GelCellulose的溶胀度随温度变化最小.GelCellulose的溶胀度随温度升高而下降应该与HPMC在水中的溶解度随温度的升高而下降有关.文献报道[10],由于疏水作用,随着温度的升高,HPMC 的水溶液会发生凝胶化.而GelPNIPAN的溶胀度随着温度的升高而下降,这是由于在聚(N-异丙基丙烯酰胺)水凝胶中,存在疏水基团(—C(CH3)2)与 亲水 基 团(—CONH—).温度较低时,凝胶中的亲水基团与水形成氢键,大分子链周围的水分子依靠氢键形成有序化程度较高的溶剂化层,使大分子链溶解于水中,而随着温度的升高,分子内与大分子间的疏水作用增强,出现去水合作用使大分子开始收缩,大分子链疏水部分的溶剂化层逐渐被破坏,水分子从溶剂化层排出,从而导致凝胶溶胀度降低,凝胶体积收缩[11].GelIPN综合了GelPNIPAN和GelCellulose的性质,水凝胶的溶胀度及温敏性处于它们的中间,因此可以通过控制互穿网络水凝胶的组成调节其溶胀性能.
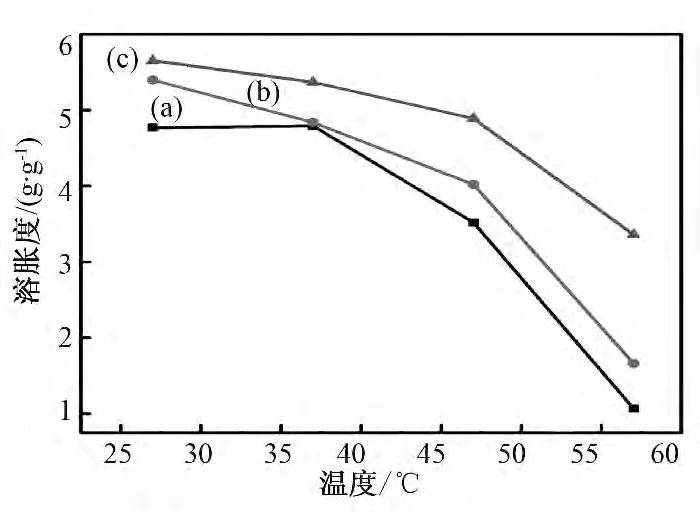
图6 GelPNIPAN(a)、GelIPN(b)、GelCellulose(c)的溶胀度随温度的变化曲线Fig.6 The swelling ratio of the hydrogels with temperature GelPNIPAN(a)、GelIPN(b)、GelCellulose(c)
2.4 流变性能表征
由图7 可知,水凝胶GelPNIPAN、GelCellulose及GelIPN的储能模量(G’)均大于损耗模量(G”),即弹性形变优于黏性形变,表明我们通过光聚合或Diels-Alder 反应合成的水凝胶皆具有较好的网络结构,表现出一定的刚性与机械强度.GelPNIPAN的G’在42 ℃时随温度升高开始明显下降,而其G”在38℃时随温度升高而显著上升,当温度超过36 ℃时,G’、G”随温度的变化而趋于平缓.这与聚(N-异丙基丙烯酰胺)水凝胶的温度敏感性质相一致.温度较低时,聚合物链比较舒展,弹性较好,因而G’较大,G”较小.温度升高后,凝胶体积收缩,链段之间距离变小,弹性变小,因而G’变小,G”变大.GelIPN的G’及G”均随温度的升高而变小,而GelCellulose的G’ 及G”随温度升高没有明显变化.在室温至43℃之间,GelIPN的G’ 处于GelPNIPAN与纤维素水凝胶之 间,而温度高于43 ℃后,GelCellulose的G’ 大 于GelIPN及GelPNIPAN.这表明GelCellulose的模量G’ 及G”随温度基本无变化,而GelIPN的模量G’及G”随温度变化有一定响应性,其响应性应该是由于聚(N-异丙基丙烯酰胺)水凝胶网络的存在.可见,互穿网络水凝胶的性能可以通过调节两个网络的组成来调节.

图7 水凝胶的G’和G”随温度的变化曲线Fig.7 Rheological behavior of hydrogels with temperature
3 结论
本论文通过Diels-Alder 反应串联光聚合,通过两步法合成了具有温敏性的纤维素互穿网络水凝胶.该方法条件温和,在水相中就可进行,是一种具有应用潜力的制备互穿网络水凝胶的方法.制备的互穿网络水凝胶在37 ℃有较高的溶胀度,且其溶胀度随着温度的升高而下降,G’及G”随温度的变化也有所改变.该水凝胶结合了纤维素水凝胶及聚(N-异丙基丙烯酰胺)水凝胶的特点,在生物医学方面具有广泛的应用前景.
[1]Cui L,Jia J,Guo Y,et al.Preparation and characterization of IPN hydrogels composed of chitosan and gelatin cross-linked by genipin[J].Carbohydrate Polymers,2014,99:31-38.
[2]Darnell M C,Sun J Y,Mehta M,et al.Performance and biocompatibility of extremely tough alginate/polyacrylamide hydrogels[J].Biomaterials,2013,34:8042-8048.
[3]Wang J,Li J,Li H,et al.Modulated ion recognition by thermosensitive ion-imprinted hydrogels with IPN structure[J].Materials Letters,2014,131:9-11.
[4]Alzari V,Ruiu A,Nuvoli D,et al.Three component terpolymer and IPN hydrogels with response to stimuli[J].Polymer,2014,55:5305-5313.
[5]Matricardi P,Meo C D,Coviello T,et al.Interpenetrating Polymer Networks polysaccha -ride hydrogels for drug delivery and tissue eng -ineering[J].Advanced Drug Delivery Reviews,2013,65:1172-1187.
[6]Tong X,Yang F.Engineering interpenetrating network hydrogels as biomimetic cell niche with independently tunable biochemical and mechanical properties[J].Biomaterials,2014,35:1807-1815.
[7]Dragan E S.Design and applications of interpenetrating polymer network hydrogels[J].Chemical Engineering Journal,2014:243:572-590.
[8]Wei H L,Yang Z,Chu H J,et al.Facile preparation of poly(N-isopropylacrylamide)-based hydrogels via aqueous Diels-Alder click reaction[J].Polymer,2010,51:1694-1702.
[9]Wang G F,Chu H J,Wei H L,et al.Click synthesis by diels-Alder reaction and characterization of hydroxypropylmethyl cellulose -based hydrogels[J].Chemical Papers,2014,68(10):1390-1399.
[10]Xu X M,Song Y M,Ping Q N,et al.Effect of ionic strength on the temperature -dependent behavior of hydroxypropyl methylcellulose solution and matrix tablet [J].Journal of Applied Polymer Science,2006,102:4066-4074.
[11]王云普,袁昆,裴小维.聚N-异丙基丙烯酰胺/纳米SiO2复合水凝胶的合成及溶胀性能[J].高分子学报,2005(4):584-588.
——2021年山东高考物理卷第2题赏析

