镍钛类水滑石衍生物富氧选择性催化还原NO
袁德玲,唐首锋,*,张庆瑞,李新勇(.燕山大学环境与化学工程学院,河北秦皇岛066004; .大连理工大学环境学院,辽宁大连604)
镍钛类水滑石衍生物富氧选择性催化还原NO
袁德玲1,唐首锋1,*,张庆瑞1,李新勇2
(1.燕山大学环境与化学工程学院,河北秦皇岛066004; 2.大连理工大学环境学院,辽宁大连116024)
摘要:采用制备镍钛类水滑石前驱体的方法制备其衍生物催化剂,用于富氧条件下C3H6选择性催化还原NO反应。结果表明,镍钛类水滑石衍生物催化剂在410℃时对NO的转化率达到67%。该催化剂表现出以锐钛矿为主,含有少量氧化镍和钛酸镍的混合结构。硝酸盐物种是C3H6选择性催化还原NO反应的活性中间体。
关键词:镍钛类水滑石;选择性催化还原;氮氧化物;原位红外;脱硝
0 引言
随着汽车工业和交通运输业的快速发展,我国的机动车保有量迅速增大,在不断消耗能源的同时也造成了环境污染,尤其是机动车尾气排放的氮氧化物引起了一系列严重的环境问题,例如:雾霾、光化学烟雾以及臭氧空洞等,受到了人们的高度重视。贫燃发动机能够显著地减少能源的消耗和污染物的排放,有着广阔的应用前景,但其尾气中大量的氧气会导致传统三效催化剂的催化活性大大降低,尾气中的氮氧化物无法去除[1]。因此,开发能够在富氧条件下有效去除氮氧化物的催化剂具有重要的理论和现实意义。
碳氢化合物选择性催化还原NO被认为是控制机动车尾气排放NO最有效的方法之一[2],且该方法无需外源添加还原剂,具有巨大的应用潜力。对于富氧HC-SCR技术来说,开发高效的催化剂是提高脱硝效率的关键,也是这一技术的研究热点。研究表明: Ni基催化剂对富氧条件下碳氢化合物选择性催化还原NO表现出一定的活性,而且Ni被认为是催化体系中的活性组分[3]。TiO2因其廉价、无毒而被广泛地用作选择性催化还原NO催化剂的载体。结合这两种组分的优点,本文采用合成类水滑石前驱体的方法对复合氧化物进行改性,最终获得镍钛类水滑石衍生物催化剂,以期达到提高催化活性的目的,对其在富氧条件下C3H6选择性催化还原NO的性能进行了研究,并且探讨了催化剂结构与催化性能之间的关系。
1 实验部分
1.1催化剂制备
采用共沉淀法合成镍钛类水滑石前驱体。首先,将Ni(NO3)2·6H2O加入到去离子水中,搅拌溶解;将Ti(SO4)2加入到去离子水中,加热搅拌溶解制备微乳液,控制Ni/Ti的摩尔比为2∶1。将两种待用溶液与尿素溶液混合,搅拌至完全溶解,缓慢加热至90℃持续反应48 h,将所得沉淀物水洗,于70℃干燥24 h后,获得类水滑石前驱体。450℃下煅烧6 h获得镍钛混合氧化物催化剂。
1.2催化剂表征
催化剂的X-射线衍射(XRD)图谱使用LabX-6000型X射线粉末衍射仪(日本岛津公司)测得(CuKα射线,λ= 0.154 06 nm,扫描范围10°~80°,扫描速度5°/min)。催化剂的物理结构使用NOVA 4200e型气体吸附分析仪(美国康塔仪器公司)测定,N2吸附-脱附实验在-198℃(液氮)条件下进行。
X-射线电子能谱(XPS)表征采用Perkin-Elmer PHI 5600 X-射线光电子能谱仪进行。辐照光源采用AlKα,能量为1 486.6 eV,电压15 kV,电流为20 mA。全谱扫描2次(步长0.5 eV),分谱扫描15次(步长0.2 eV)。图谱校正采用C1s1/2=284.6。电子自旋共振(ESR)表征采用德国布鲁克有限公司的EPR/ESR320型电子顺磁共振波谱仪检测。测定参数为:有心磁场为4 100 G,微波频率为9.8 GHz(X带),扫频宽度为8 000,调制带宽为10.25 G,时间常数为40.96 ms,时间为2×103ms。
1.3催化活性测试
催化剂的活性测试在固定床气态反应装置上进行。石英反应管的直径为6 mm,催化剂用量为0.2 g。反应气成分为1 000 ppm NO + 1 000 ppm C3H6+ 10% O2+ He(平衡气)。反应气流量为100 mL/min。尾气中的C3H6组分采用气相色谱(天美7980Ⅱ)进行在线分析,采用6DX-104色谱柱和氢火焰检测器(FID)。NO的测定采用化学传感器多组分气体分析仪Testo 350。
1.4原位红外研究
原位FTIR的实验在VERTEX 70红外光谱仪(布鲁克公司)上进行,取0.02 g样品压成圆片,400℃He气预处理1 h。入口气体的流速为40 mL/min。
2 结果与讨论
2.1催化剂的表征
图1为镍钛类水滑石前驱体及其衍生物催化剂的XRD谱图。煅烧前的催化剂前驱体表现出明显的层状材料特征,即低角度区的衍射峰强且对称,高角度区的峰弱且对称性差。2θ≈11°,24°,34°,37°,47°和61°处的衍射峰被认为是水滑石(003),(006),(101),(012),(015)和(116)晶面的衍射峰。说明本研究合成的催化剂前驱体具有水滑石的结构。煅烧后得到的催化剂层状结构消失,表现出氧化物的结构,2θ≈25.28°、37.80°、48.05°、55.06°、62.69°和68.76°处的衍射峰均对应锐钛矿结构。此外,2θ≈43.36°、63.01°衍射峰对应于钛酸镍,37.24°对应于氧化镍。由XRD的谱图可知镍钛类水滑石衍生物催化剂表现为以锐钛矿为主,同时含有少量的钛酸镍和氧化镍的混合结构。
采用氮气吸附的方法对催化剂的比表面积以及孔径分布进行表征。图2为镍钛类水滑石衍生物催化剂氮气吸附-脱附曲线及孔径分布情况。其吸附曲线为Ⅳ型,回滞环为H2型,说明该催化剂具有复杂的孔结构,孔的形状主要是圆柱形和球形。根据BET公式计算催化剂的比表面积是171 m2/g,BJH公式计算催化剂的平均孔径是3.82 nm。根据XRD的表征结果说明镍钛类水滑石衍生物催化剂的主要晶相为锐钛矿,而商品锐钛矿比表面积为47 m2/g[4],与之相比,本研究中合成的镍钛类水滑石衍生物催化剂具有较大的比表面积,可以提供更多的吸附位点,有利于提高催化反应活性。
采用XPS的手段对NiTi类水滑石衍生物催化剂的表面元素价态进行表征,结果如图3所示。图3(a)为镍钛类水滑石衍生物催化剂的XPS全谱,从图中可以看出所有样品都主要含有Ni、Ti和O元素。图3(b)给出了催化剂中Ni元素2p轨道的结合能图谱,催化剂的Ni2p3/2和Ni2p1/2轨道在856±0.4 eV和853±0.4 eV处出现结合能谱峰,表明镍以正二价形式存在[5]。显然,正二价的镍比正一价的镍和零价的镍具有更高的正电,即更高的受电子性。NO是典型的带有负电的物种,因此,正二价的镍更容易和NO发生化学吸附,有利于催化反应的发生。

图2 镍钛类水滑石衍生物催化剂的N2吸附脱附曲线及孔径分布图谱Fig.2 N2adsorption-desorption isotherms and BJH pore size distribution (inset) of NiTi hydortalcite-derived catalyst
图3(c)给出了O1s轨道的结合能图谱。O1s的结合能谱峰宽且明显不对称,表明催化剂表面存在多个氧物种。其中,530 eV处较为明显的结合能峰是与金属离子相连的晶格氧的特征峰,结合能稍高的峰对应的是表面化学吸附氧、缺陷氧以及低配位的氧物种。说明催化剂中的氧的主要以氧化物中的晶格氧形式存在,并含有少量表面化学吸附氧[5-6]。已有的研究表明,这些表面化学吸附氧物种对催化反应有着积极的贡献[6]。图3(d)中是Ti2p轨道的结合能图谱,Ti2p3/2和Ti2p1/2轨道的分别在大约458±0.4 eV和464±0.4 eV处出现结合能谱峰,说明催化剂中表面的Ti以正四价形式存在[7]。图4为镍钛类水滑石衍生物催化剂的ESR图谱。Ni元素在ESR检测中只有Ni2 +有ESR信号,其他形式的Ni均无信号。图中显示样品中存在正二价的Ni,且并无超精细结构存在,这一结果与XPS表征结果一致。镍钛类水滑石衍生物催化剂表现出了各向同性的ESR相应信号,表明Ni2 +在正八面体结构的中心位置,且正八面体结构晶体结构的周期性良好[8]。ESR表征结果进一步说明正二价的镍位于正八面体结构的中心,且晶体结构良好、分散均匀。分散均匀被普遍认为是有利于催化反应活性的提高。

图3 镍钛类水滑石衍生物催化剂的XPS图谱Fig.3 XPS profile of NiTi hydortalcite-derived catalyst
2.2催化活性评价
图5显示了镍钛类水滑石衍生物催化剂在富氧条件下选择性催化还原NO的催化性能。随着反应温度的升高,NO的转化率先增加后下降,410℃时N2收率达到最大值67%。C3H6的转化率随着反应温度的升高而增加,430℃时完全转化。NO的转化率达到最大值时的410℃对应C3H6的转化率接近100%,由此说明反应温度超过410℃时,NO的转化率的下降是由缺少还原剂引起的。作为一种廉价的混合氧化物催化剂,该催化剂的富氧条件下的催化活性表现出一定的优势[9]。原因可能是催化剂中正二价的镍均匀地分散在正八面体晶格结构的中心,为含氮物种提供了良好的化学吸附位点。此外,表面表化学吸附O物种对催化反应有着积极的贡献,也可能是较高催化活性的原因。为了进一步探讨化学吸附物种的形成及催化机理,采用原位红外的手段对反应过程进行详细的研究。
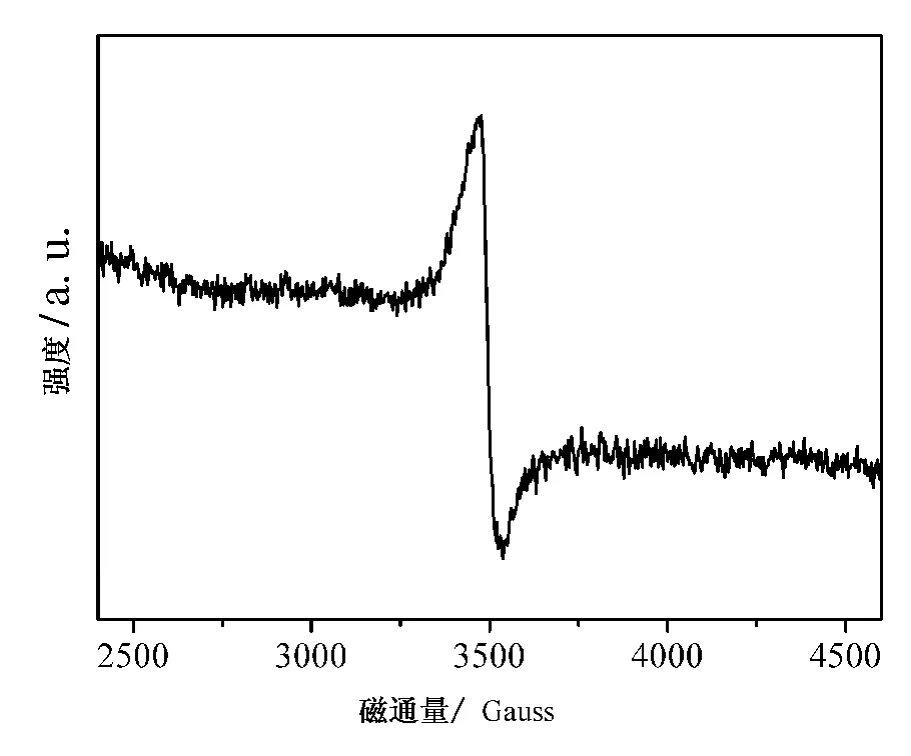
图4 镍钛类水滑石衍生物催化剂的ESR图谱Fig.4 ESR profile of NiTi hydortalcite-derived catalyst
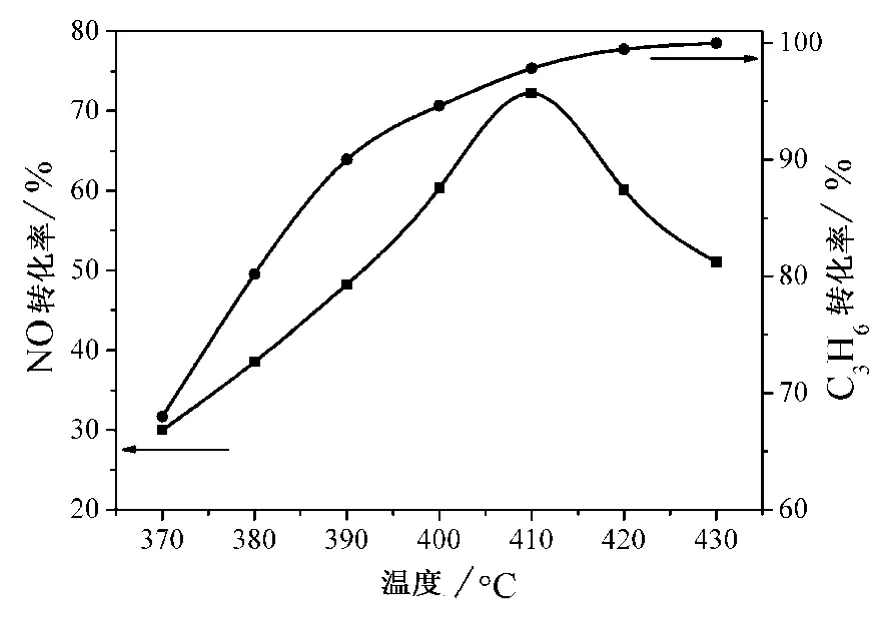
图5 镍钛类水滑石衍生物催化剂上NO转化率和C3H6转化率Fig.5 Catalytic performance of NiTi hydortalcite-derived catalyst as a function of temperature
2.3原位红外研究
原位红外的手段能够研究反应中间体及反应机理,能够在线的给出反应过程中催化剂表面形成的吸附物种的种类及相对含量的变化情况,是目前研究催化反应机理较为先进的手段。图6 (a)给出了镍钛类水滑石衍生物催化剂最佳反应温度条件下共吸附NO和O2的红外图谱,图中1 905 cm-1和1 845 cm-1处的红外谱峰归属为NO的气态吸附(NO-),1 627 cm-1和1 599 cm-1归属于二齿桥式酸盐,1 577 cm-1和1 504 cm-1处的红外谱峰归属于单齿酸盐,1 360~1 390 cm-1处的红外谱峰归属离子态的硝酸盐(NO3-)2[10]。图中单齿硝酸盐随吸附时间的延长逐渐分解,表明单齿硝酸盐在反应条件下不稳定。试验结果表明:随着反应过程中NO和O2通过镍钛类水滑石衍生物催化剂,催化剂表面可能形成的含氮物种为气态吸附NO、二齿桥式酸盐以及不稳定的单齿硝酸盐。
图6(b)给出了镍钛类水滑石衍生物催化剂最佳反应温度条件下吸附C3H6的红外图谱,图中1 660 cm-1处的红外吸收谱峰归属为表面吸附的C3H6,1 577 cm-1处的红外峰归属为乙酸盐,1 440 cm-1处的红外峰归属为碳酸盐,1 370 cm-1和1 328 cm-1处的红外峰归属为甲酸盐[11]。图中1 630~1 450 cm-1范围内出现的较宽红外吸收峰是有机分子上不同形式的振动重叠引起的,说明催化剂表面形成了大量的C3H6不完全氧化产物。试验结果表明:在反应气氛条件下,催化剂表面可能形成了表面吸附的C3H6、乙酸盐、碳酸盐、甲酸盐以及大量的C3H6不完全氧化产物。
为了进一步研究反应条件下中间体的变化情况以及反应机理,图6(c)给出了镍钛类水滑石衍生物催化剂最佳反应温度、反应气氛条件下及关闭反应系统后的红外图谱。在反应气氛条件下检测到气态吸附-NO(1 905 cm-1和1 845 cm-1)、二齿硝酸盐(1 627 cm-1和1 600 cm-1)、单齿硝酸盐(1 577 cm-1和1 504 cm-1)、C3H6(1 664 cm-1)、乙酸盐(1 577 cm-1)、甲酸盐(1 370 cm-1和1 328 cm-1)以及碳酸盐(1 440 cm-1)。该结果说明:在反应过程中,催化剂表面形成了上述含氮物种及C3H6不完全氧化产物。
关闭红外反应池的进气口和出气口后继续反应并采集红外图谱(6(c)Ⅰ和Ⅱ)Ⅰ和Ⅱ为反应气氛30 min后关闭系统继续反应30 min和90 min,能够反应在封闭体系内物种的反应特性。关闭反应系统后,硝酸盐的吸收峰消失,乙酸盐、甲酸盐和碳酸盐的吸收峰强度明显增强。表明硝酸盐和未完全氧化的碳氢化合物发生反应被消耗,因而吸收峰消失,说明硝酸盐是该反应的活性物种。在没有气体吹扫的条件下,红外池中的残留的C3H6在催化剂表面不断发生化学吸附,且没有足够的含氮吸附物种与之反应,导致乙酸盐、甲酸盐和碳酸盐的吸收峰强度明显增强,这一结果说明该催化剂具有非常强的C3H6不完全氧化能力。原位红外的研究结果说明,NO在富氧条件下能够在镍钛类水滑石衍生物催化剂表面生成硝酸盐,这些硝酸盐可以和C3H6的不完全氧化物种发生反应,硝酸盐是C3H6选择性催化还原反应的重要中间体。

图6 镍钛类水滑石衍生物催化剂的原位FTIR图谱Fig.6 In situ FTIR spectra over NiTi hydortalcite-derived catalyst
3 结论
1)本文合成了镍钛类水滑石前驱体,其衍生物催化剂用于富氧条件下C3H6选择性催化还原NO反应表现出了良好的催化活性,410℃时NO的转化率达67%。
2)镍钛类水滑石衍生物催化剂的结构以锐钛矿为主,含有少量氧化镍和钛酸镍的混合结构,镍元素以正二价的形式存在。
3)硝酸盐是C3H6选择性催化还原NO反应的活性中间体,提高反应中硝酸盐的生成量可以提高反应的催化活性。
参考文献
[1]Wu Y,Zhang S J,Li M L,et al.The challenge to NOxemission control for heavy-duty diesel vehicles in China[J].Atmospheric Chemistry And Physics,2012,12(19) : 9365-9379.
[2]Thirupathi B,Smirniotis P G.Nickel-doped Mn/TiO2as an effcient catalyst for the low-temperature SCR of NO with NH3: Catalytic evaluation and characterizations[J].Journal of Catalysis,2012,288∶74-83.
[3]Baran R,Kaminska I I,Srebowata A,et al.Selective hydrodechlorination of 1,2-dichloroethane on NiSiBEA zeolite catalyst: Influence of the preparation procedure on a high dispersion of Ni centers [J].Microporous and Mesoporous Materials,2013,169∶120-127.
[4]邹学军,李新勇.肇启东,等.可见光响应的LaVO4/TiO2纳米管的合成、表征及对气相甲苯的光催化性能[J].高等学校化学学报,2012,33 (5) : 1046-1049.
[5]Guan B,Lin H,Zhu L,et al.Selective catalytic reduction of NOxwith NH3over Mn,Ce substitution Ti0.9V0.1O2-delta nanocomposites catalysts prepared by self-propagating high-temperature synthesis method[J].Journal of Physical Chemistry C,2011,115(26) : 12850-12863.
[6]Chen Z H,Wang F R,Li H,et al.Low-temperature selective catalytic reduction of NOxwith NH3over Fe-Mn mixed-oxide catalysts containing Fe3Mn3O8Phase[J].Industrial&Engineering Chemistry Research,2012,51(1) : 202-212.
[7]Ji L,Sreekanth P M,Smirniotis P G,et al.Manganese oxide/titania materials for removal of NOxand elemental mercury from flue gas[J].Energy&Fuels,2008,22(4) : 2299-2306.
[8]Doretta C,Marcella B,Vincenzo M,et al.Cr and Ni Doping of Li4Ti5O12: Cation Distribution and Functional Properties[J].Journal of Physical Chemistry C,2009,113: (45) 19664-19671.
[9]Klingstedt F,Arve K,Eranen K,et al.Toward improved catalytic low-temperature NOxremoval in diesel-powered vehicles[J].Accounts of Chemical Research,2006,39(4) : 273-282.
[10]Yuan D,Li X,Zhao j,et al.A novel Cu-containing catalyst derived from Ti-embedded hydrotalcite-like compounds for selective catalytic reduction of NO with C3H6under lean-burn conditions [J].Journal of Catalysis,2014,309: 268-279.
[11]Shan W,Liu F,He H,et al.A superior Ce-W-Ti mixed oxide catalyst for the selective catalytic reduction of NOxwith NH3[J].Applied Catalysis B-Environmental,2012,115-116: 100-106.
NiTi hydrotalcite-derived catalyst for selective catalytic reduction of NO under lean-burn conditions
YUAN De-ling1,TANG Shou-feng1,ZHANG Qing-rui1,LI Xin-yong2
(1.School of Environmental and Chemical Engineering,Yanshan University,Qinhuangdao,Hebei 066004,China;
2.School of Environmental Science and Technology,Dalian University of Technolgy,Dalian,Liaoning 116024,China)
Abstract:A derivative catalyst was derived from the NiTi hydrotalcite-like compound,and tested in the selective catalytic reduction of NO by C3H6in the presence of excess O2.The result showed that the NO conversion of NiTi hydrotalcite-derived catalys was achieved 67% at 410℃.A major anatase with less nickel oxide and nickel titanate mixed structure was displayed in this catalyst,and nitrate (NO3(-)) was the reactive intermediate produced during the selective catalytic reduction of NO with C3H6.
Key words:NiTi hydrotalcite-like compound; selective catalytic reduction; nitrogen oxide; In situ FTIR; DeNOx
作者简介:袁德玲(1983-),女,辽宁大连人,博士,主要研究方向为大气污染控制; *通信作者:唐首锋(1983-),男,湖南湘潭人,博士,主要研究方向为环境污染控制,Email: tangshf@ ysu.edu.cn。
基金项目:河北省自然科学基金资助项目(B2012203060,B2015203300) ;秦皇岛科技支撑计划资助项目(201401A048) ;燕山大学博士基金资助项目(B878) ;工业生态与环境工程教育部重点实验室开放基金资助项目(KLIEEE-14-05) ;燕山大学青年教师自主研究计划资助项目(14LGB021)
收稿日期:2014-10-15
文章编号:1007-791X(2015) 01-0078-06
DOI:10.3969/J.ISSN.1007-791X.2015.01.012
文献标识码:A
中图分类号:X511

