自主创设问题情境,构建金属学习策略
黄淑玉
化学学习能力是学生运用科学的学习方法独立获取信息、加工和利用信息、分析和解决化学实际问题的一种个性特征。其实质是知识的结构化、网络化、程序化的知识、技能和方法。
金属的性质是中学化学的主要知识,课标要求通过生活经验了解金属的物理性质,在科学探究过程中认识金属的化学性质,提高学生的科学素养,养成处理信息、理论分析的能力。所以如何进行有效的学习,是所有教师一直探索的问题。毫无疑问,通过学生发现问题,自主创设问题情境进行探究,来构建认知结构,能取得事半功倍的效果。
由于本节教学重点、难点是建构常见金属的化学性质知识网络,培养学生由学会到会学的能力。为突破教学重点、难点,创设高效课堂,用多媒体进行辅助教学,在学习过程中可以采取合作讨论和小组实验的学习方法将自主学习落实到课堂。
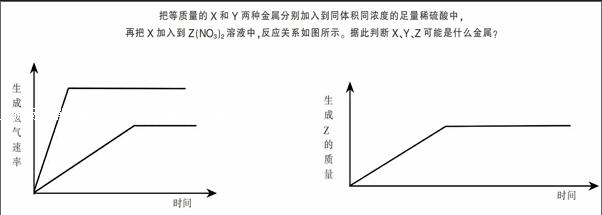
为使学生学有所成,安排学生通过研读教材,查阅报刊书籍,网络等方式对金属进行前置性学习,并在课堂导入时进行交流。经过交流,学生就能知道金属在生活中有广泛的用途,比如,金银可以做装饰品,铁制品可以做炊具,铜可以做导线,所以学生很快自主汇总出金属的物理性质:即良好的金属光泽,导热导电,延展性。同时也会提出以下问题,焰火原料中有金属镁、铜、铝,那是不是铝和铜金属也能与氧气反应呢?由金属镁、铁、铜制作雕像能被酸雨腐蚀,那是不是镁铁铜金属能与酸反应呢?铁真能与硫酸铜反应制取金属铜吗?
针对这些质疑,引领学生采取小组合作方式:分别设计实验进行探究,在探究结论基础上进行拓展引导学生构建完整的知识网络。为保持学生对生活和自然界化学现象的好奇心和探究欲望,在课下延学中让学生利用身边的物质,建立家庭实验室。
具体教学过程如下:
探究1:各小组对打磨好的铝片、铜片进行加热
观察到铝片变暗了,铜表面变黑了。然后根据铁和铜与氧气反应用类比思维指导学生写出铜和铝与氧气反应的方程式。
然后不失时机地提出:“铝制品为什么耐腐蚀”为什么“真金不怕火炼”的问题,引导学生既得出了某些金属能与氧气反应生成氧化物的规律,又学会了用辩证思维看待金属的氧化反应。这样通过学生的积极参与,既练习了学生的语言表达能力,也培养了对知识的归纳能力。
探究2:各小组分别将外观形状相同的镁、铁、铜三种金属丝进行打磨,分别放入等质量、等浓度的稀盐酸中进行实验
学生不仅能观察到镁和铁能与酸反应生成气体,而且还根据了镁与酸反应的速率远远快于铁与酸反应的速率得出了镁比铁活泼的延学思维。然后引领学生通过研读教材写出镁和铁与盐酸反应的方程式。这时组织学生观察FeCL2化学式,强调铁参加置换反应化合价为+2价,所以溶液为浅绿色,然后引领小组讨论:“为什么加铁粉的麦片能补铁” ?让学生夯实基础的同时,也知道化学改善了人类生活,拉近了化学知识与生活的距离。再结合小组实验中,铜不能与酸反应的事实,学生很快归纳概括出:只有某些金属能与稀盐酸反应生成氢气。同时在该实验中学生还学会了用控制变量法进行实验。
探究3:将打磨后的几枚铁钉放入硫酸铜溶液中
十几秒钟后,学生就能观察到奇迹,铁钉表面附着了红色物质。接着可以向学生展示了前一天准备的实验,学生就可以看到了美丽的铜树和浅绿色的溶液,并告诉他们继续你们的实验,美丽的化学也将永远陪伴他们,而后提问生成的红色物质是什么?溶液为什么由蓝色变成了浅绿色时,学生很容易就能分析出红色物质是铜,铁原子变成了亚铁离子。同时也能自豪地写出了铁与硫酸铜反应生成了铜与硫酸亚铁的方程式。接着多媒体展示:“铁桶为什么不能盛波尔多液”?学生就得出铁与硫酸铜这样的盐类物质反应生成铜和亚铁盐的规律。
接着进行以下能力训练,将化学与数学知识融合,学生练习阅读文字、分析图表和对信息进行加工的能力(见下图),构建常见金属铁的知识网络。
为了提升学生素质,在课下延学中让学生利用身边的食醋、铁钉、电池外壳等物质,建立家庭实验室,制取少量氢气,在探究中就能知道金属的防护措施,并提高了节约能源的意识。而且在这逐步进行的探究活动中,学生看到了五彩缤纷的化学物质,认识了丰富多彩的化学变化,理解了化学来源于生活,服务于生活的真谛。
总之本节课用兴趣做教师,用情景点燃思维,用实践来关注学生的成长历程,让学生在质疑中发现知识,在探究中体验快乐,永远对生活和自然界化学现象保持好奇心和探究欲望,就能逐步养成会学化学的能力。
(责编 田彩霞)
——以硫酸铜饱和溶液析出晶体的计算为例

