镍磷纳米化学复合镀中纳米二氧化钛的分散性研究
陈尔跃*,杨晓超,徐娟,郭祥峰
(齐齐哈尔大学,黑龙江 齐齐哈尔 161006)
镍磷纳米化学复合镀中纳米二氧化钛的分散性研究
陈尔跃*,杨晓超,徐娟,郭祥峰
(齐齐哈尔大学,黑龙江 齐齐哈尔 161006)
利用X射线光电子能谱仪(XPS)分析了不同纳米TiO2含量的Ni-P化学镀液所制备的Ni-P-TiO2复合镀层中纳米TiO2的含量及其分布状况,在以乳酸为配位剂、聚乙烯吡咯烷酮(PVP)为表面活性剂的Ni-P-TiO2化学复合镀液中,采用红外-可见-紫外分光光度法研究了不同用量的乳酸和PVP以及镀液pH对纳米TiO2分散性的影响,获得了最佳的分散条件:纳米TiO2加入量3.0 ~4.0 g/L,PVP 0.2 g/L,乳酸4.5 mL/L,pH 5.0 ~ 5.5。
镍-磷合金;纳米二氧化钛;化学复合镀;乳酸;聚乙烯吡咯烷酮;分散性;稳定性
First-author’s address:Qiqihar University, Qiqihar 161006, China
纳米复合镀一般是在原有镀液的基础上通过添加纳米粒子,使纳米粒子与沉积金属单质或者合金共同在基体表面沉积形成纳米复合镀层。纳米复合镀层不仅可以提升镀层的耐磨、耐蚀等性能,且由于纳米粒子本身具有一定的特殊性质如光催化、杀菌等,因此纳米复合镀层通常也兼具纳米粒子的性质。纳米TiO2是纳米复合镀常用的添加粒子,具有化学稳定性好、耐腐蚀、对人体无毒无害等优点。纳米TiO2粒子在复合镀液中极易发生团聚,这不仅影响纳米TiO2本身的性能,而且对镀层性能(如耐蚀性、硬度等)造成一定的影响[1-4]。曲彦平等[5]研究发现,通过在镀液内添加阴离子和非离子表面活性剂,纳米粒子在镀液内分散均匀、镀层硬度、耐磨性等表现优异。
本文在Ni-P镀液配方[6]的基础上进行改进,以聚乙烯吡咯烷酮(PVP)作为表面活性剂、乳酸为配位剂,并添加纳米TiO2形成复合镀液,利用分光光度法结合实际上镀操作,研究了TiO2、PVP和乳酸的用量及镀液pH对Ni-P-TiO2镀液稳定性的影响。
1 实验
1. 1 试剂与仪器
(1) 试剂:Na3PO4·12H2O、NaH2PO2·H2O、NiSO4·6H2O、乳酸、无水乙酸钠、聚乙烯吡咯烷酮,分析纯,天津市凯通化学试剂有限公司;纳米TiO2粉末,粒径5 nm,江苏优锆纳米材料有限公司。
(2) 仪器:JJ-1电动搅拌器(金坛市城东新瑞仪器厂)、pHS-25型精密酸度计(成都广谱科学仪器有限公司)、Lambda750近红外-可见-紫外分光光度计(美国PerkinElmer公司)、ESCALAB 250Xi型X射线光电子能谱仪(美国Thermo Scientific公司)。
1. 2 化学复合镀液的配制与复合镀液吸光光谱测试
将26 g/L NaH2PO2·H2O、27 g/L NiSO4·6H2O、1 ~ 5 mL乳酸、12 g/L无水乙酸钠、0.1 ~ 2.0 g/L PVP配制成主盐浓度为0.12 mol/L的浓溶液A;纳米TiO2用一定量去离子水分散10 h使其充分润湿,配制成纳米粒子浓度为0.37 mol/L浓悬浊液B。在转速70 r/min搅拌下,将B缓慢加入A后,定容制成化学复合镀液,利用NaOH或者H2SO4溶液调节pH为5,然后将化学复合镀液稀释25倍,用近红外-可见-紫外分光光度计测试其190 ~1 000 nm内的吸光度,以确定最佳测试波长。
纳米化学复合镀基本流程:除油→清洗→酸洗→清洗→上镀。
除油:首先用乙醇擦拭基材(铜片,尺寸为1 cm × 1 cm)表面,再利用碱性除油剂(NaOH 5 g/L,无水Na2CO320 g/L,Na3PO420 g/L,OP-10 1 g/L)除油,温度70 °C,时间20 min。
酸洗:分别用8%(质量分数,下同)稀硫酸与5%稀硝酸浸泡5 min。上镀:pH 5,温度 85 °C,机械搅拌,上镀时间30 min。
1. 3 性能测试
(1) 通过分光光度法表征纳米TiO2的分散性和镀液稳定性。将一定波长的入射光照射在复合镀液上,通过红外-可见-紫外分光光度计测定吸光度,可根据吸光度的大小来判断纳米粒子在复合镀液中的分散效果[7]。吸光度的大小可以通过式(1)来表示:式中,A表示吸光度;k表示吸光系数,L/(mol·cm);n表示单位体积的粒子数,mol/L。由式(1)可以看出,吸光度的大小与悬浮在复合镀液中纳米粒子个数成正比。复合镀液的吸光度越高,则代表着纳米粒子在复合镀液中的分散效果越好。

在最佳测试波长下,将含有不同浓度的纳米TiO2、PVP和乳酸以及不同pH的化学复合镀液静置,每隔30 min取上层液稀释25倍,利用红外-可见-紫外分光光度计测试吸光度。
(2) 用ESCALAB 250Xi型X射线光电子能谱仪(XPS)对镀件进行Ti元素扫描。
2 结果与讨论
2. 1 最佳测试波长
利用红外-可见-紫外分光光度计测定添加3 g/L纳米TiO2后的Ni-P-TiO2纳米化学复合镀液与Ni-P化学镀液的吸光度,测试结果如图1所示。由图1可知,Ni-P化学镀液在400 nm处有最大吸收峰;曲线B为Ni-P-TiO2化学复合镀液在280 nm与400 nm处有最大吸收峰。因此可以判定,400 nm为Ni-P化学镀液的最大吸收波长,280 nm为纳米TiO2的最大吸收波长。分光光度法测定纳米粒子在镀液中分散性是将可被TiO2吸收波长的入射光照射在化学复合镀液,当光线进入镀液时一部分光被TiO2纳米粒子阻挡,而没有被阻挡的光则会透过镀液进入检测器内而显示出吸光度。当纳米复合镀液中悬浮的纳米粒子越多,表明其在镀液中的分散性越好,透光率越小,吸光度也就会越大;另一方面,镀液本身对纳米粒子的吸光影响越少,越能真实反映出纳米粒子在镀液内的分散情况[8]。如图1所示,在波长为450 nm时,化学镀液的吸光度接近于零,而添加纳米TiO2后的化学复合镀液在此处有较强的吸收,因此450 nm为最佳测试波长。
2. 2 纳米TiO2加入量对镀液分散性和稳定性的影响
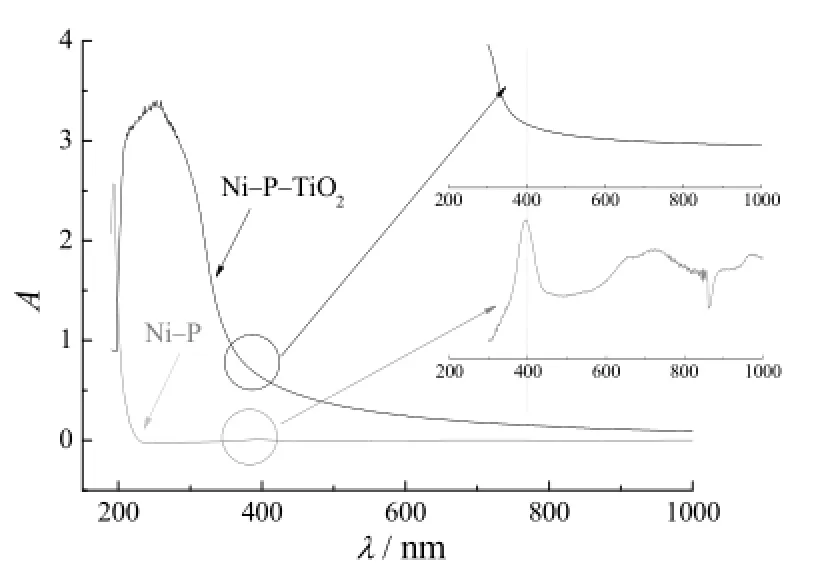
图1 Ni-P化学镀液与Ni-P-TiO2纳米化学复合镀液的吸光度曲线Figure 1 Absorbance curves for Ni-P electrolessplating bath andNi-P-TiO2electroless nanocomposite plating bath
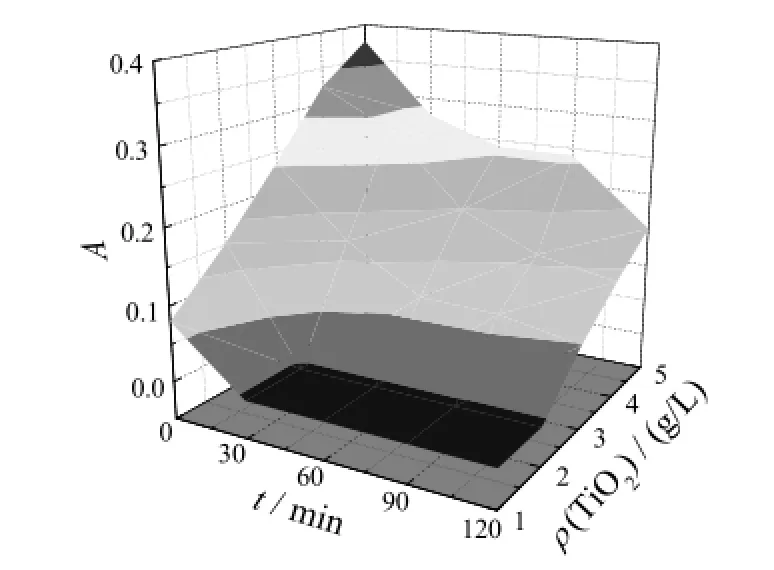
图2 纳米TiO2含量和镀液静置时间对吸光度的影响Figure 2 Effect of content of nano-TiO2and standing time of the bath on absorbance编者注:图2原为彩色,请见C1页。
图2描述的是纳米TiO2不同加入量和不同静置时间对镀液上层液吸光度的影响。沉降时间为0 min时,随着纳米粒子加入量增大,吸光度增大。这是因为在单位体积溶液内纳米粒子含量增加,悬浮在溶液中的纳米粒子也会随着增大。镀液静置时间在0 ~ 40 min时所有测试液的吸光度均发生下降,而纳米粒子添加量在1.0 ~2.5 g/L的测试液的吸光度接近于零。这是因为纳米粒子含量过低,粒子表面吸附的电荷过多,容易发生团聚。镀液静置时间在40 ~ 60 min时,纳米TiO2添加量在2.0 ~ 3.0 g/L与4.0 ~ 5.0 g/L的测试液的吸光度均在下降,而添加量在3.0 ~ 4.0 g/L的测试液的吸光度基本保持不变。这是因为镀液中的纳米粒子含量过多,部分粒子在没有外力的干扰下团聚在一起,受到重力的影响迅速沉降下来。镀液静置时间在60 ~ 120 min时,纳米粒子添加量在2.0 ~ 4.0 g/L的测试液的吸光度基本保持不变[9]。因此,纳米粒子添加量在2.0 ~ 4.0 g/L时,镀液的稳定性最好。
XPS不仅可以获得元素种类以及价态等信息,而且可以针对某一元素或者某一元素的价态进行扫描以获得其二维分布图。通过利用XPS元素分布成像功能对纳米TiO2加入量为1.0、2.0、3.0、4.0和5.0 g/L时所制备的镀件表面进行分析,结果如图3所示。图中白色像素点表示的是纳米TiO2在500 μm × 500 μm的镀层中的分布情况。可见,纳米TiO2加入量在1.0 g/L和2.0 g/L时,白色像素点分布不均匀,局部过于集中,即镀件表面的纳米粒子分布不太均匀,局部纳米粒子含量过高。纳米TiO2加入量在3.0 g/L和4.0 g/L时白色像素点分布均匀,证明镀件表面的纳米粒子分布均匀。镀液中纳米TiO2加入量对镀层中Ti原子分数的影响见图4。由图4可见,此时镀层中TiO2的含量基本一致。纳米TiO2加入量在5.0 g/L时,白点分布均匀,但是局部过于集中,证明镀件表面的纳米TiO2分布均匀,但局部含量过高。适宜的纳米TiO2加入量为3.0 ~ 4.0 g/L。

图3 不同TiO2含量的镀液制备的Ni-P-TiO2镀层中TiO2的分布Figure 3 Distribution of TiO2in the Ni-P-TiO2deposits prepared from the bath with different contents of TiO2
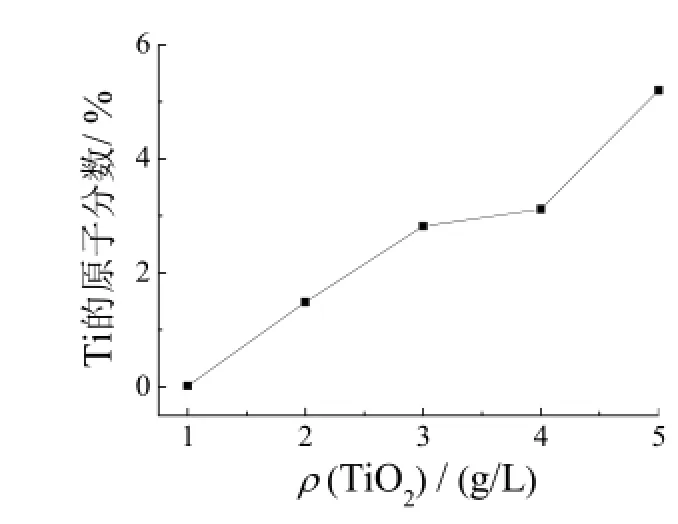
图4 纳米TiO2添加量对复合镀层中TiO2含量的影响Figure 4 Effect of dosage of nano-TiO2in electrolyte on content of TiO2in the composite deposit
2. 3 聚乙烯吡咯烷酮对纳米TiO2的分散性和镀液稳定性的影响
PVP是一种性能优异的表面活性剂。在化学复合镀液内加入表面活性剂不仅起到减少孔隙率的作用[10],而且对纳米粒子也具有分散作用。图5描述的是在纳米TiO2含量为3.0 g/L的镀液中加入不同含量的PVP,在不同静置时间时对镀液上层液吸光度的影响。静置时间为0 min时,将不同浓度的PVP加入化学复合镀液中,随着PVP加入量的增加,吸光度逐渐增大。镀液静置时间0 ~ 30 min时,不同PVP添加量的所有待测液的吸光度均随着静置时间的延长而下降。静置时间在30 ~ 80 min时,PVP添加量在0.0 ~ 0.2 g/L与0.4 ~ 1.0 g/L时,测试液的吸光度基本接近于零;而PVP添加量在0.2 ~ 0.4 g/L时,测试液的吸光度基本保持不变,静置80 min后吸光度才开始下降。这是因为少量PVP在纳米TiO2颗粒表面时,PVP的环形结构起到了空间位阻的作用,并与PVP上负电性的酰胺基团相结合,可以抑制粒子的相互靠近。但是大量的PVP则会导致PVP中长的碳氢链之间相互缔合形成胶团,从而产生团聚,大大降低了纳米粒子在化学复合镀液中的分散性能[11],导致镀液不稳定。因此,PVP的加入量控制在0.2 g/L为宜。
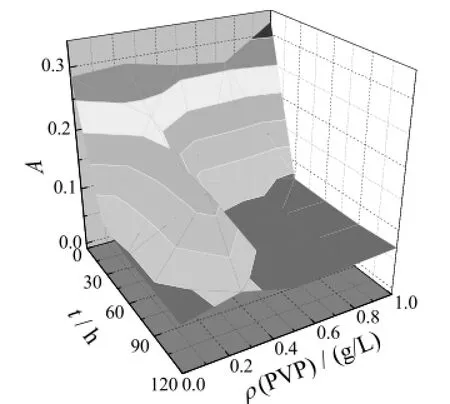
图5 PVP的用量和镀液静置时间对吸光度的影响Figure 5 Effect of dosage of PVP and standing time of the bath on absorbance编者注:图5原为彩色,请见C1页。
2. 4 pH对纳米粒子分散性的影响
研究了纳米TiO2添加量为3.0 g/L、PVP的加入量为0.2 g/L时,镀液的pH对镀液稳定性的影响,结果见图6。如图6所示,纳米复合镀液的吸光度随pH的增大而增大,即随着pH的增大,纳米TiO2在溶液中的分散性越来越好。这是因为纳米TiO2分散在水溶液中时,当溶液的pH较小时,纳米粒子表面的羟基吸附了溶液中的H+,纳米粒子表面带正电荷;当溶液pH较高时,纳米粒子表面失去了H+而吸附了OH-,带负电。因此,随着溶液pH增大,溶液中带负电的纳米TiO2增多[12],静电斥力增强,继而提高了纳米粒子在溶液中的分散性[13]。在上镀过程中发现,pH >5.5时,所得镀层表面粗糙、有颗粒感,因此pH在5.0 ~ 5.5为最佳。
2. 5 乳酸含量对纳米TiO2分散性的影响

图6 pH对镀液稳定性的影响Figure 6 Effect of pH value on stability of the bath

图7 乳酸加入量对镀液吸光度的影响Figure 7 Effect of lactic acid dosage on absorbance of the bath
乳酸含量对纳米TiO2分散性的影响见图7。如图7所示,当乳酸加入量在4.5 mL/L时,镀液吸光度最大,纳米TiO2粒子在镀液中的分散性为最佳;随着乳酸加入量的增加,吸光度逐渐降低,纳米TiO2粒子在镀液中的分散性逐渐变差。这是因为乳酸在溶液中一部分发生电离,生成乳酸根和质子H+,纳米TiO2粒子吸收乳酸根,由于乳酸根带负电,纳米TiO2表面也带负电,纳米粒子表面的电荷密度增加,粒子之间排斥力增大,纳米粒子在镀液的分散性增强。但是当乳酸浓度进一步增大时,粒子之间的静电排斥力将有所减少。这是因为随着乳酸浓度增加,溶液中反粒子浓度也会相应增加,使扩散层的厚度变薄,分散系的稳定性会减弱,继而纳米粒子在镀液中的分散性降低[14]。
3 结论
通过分光光度法和沉降法研究了不同条件下纳米TiO2在Ni-P-TiO2化学复合镀液中的分散性和镀液稳定性,确定了Ni-P-TiO2化学复合镀液最佳条件:纳米TiO2加入量3.0 ~ 4.0 g/L,表面活性剂PVP加入量0.2 g/L,pH 5.0 ~5.5,乳酸加入量4.5 mL/L。XPS元素成像表明,纳米TiO2在最佳条件下制备的Ni-P-TiO2镀层中分布均匀。
[1] 郭鹤桐, 张三元. 复合电镀技术[M]. 北京: 化学工业出版社, 2007: 9-10.
[2] 张凤桥, 季孟波, 李兰兰, 等. 纳米粒子复合镀的研究现状[J]. 电镀与精饰, 2005, 27 (6): 18-23, 35.
[3] 黄新民, 张胡海, 刘岩, 等. 化学复合镀Ni-P-TiO2纳米颗粒涂层功能特性[J]. 应用化学, 2006, 23 (3): 264-267.
[4] 张乃军, 周苏闽. Ni-P/纳米TiO2复合镀层的抗菌性能研究[J]. 淮阴工学院学报, 2006, 15 (5): 75-78.
[5] 曲彦平, 李德高, 宋影伟, 等. Ni-P-TiO2(纳米)化学复合镀层中纳米粉分散机理的研究[J]. 表面技术, 2004, 33 (3): 9-10, 66.
[6] 武晓威, 冯玉杰, 韦韩, 等. Ni-P化学镀制备钡铁氧体基红外-微波一体化隐身材料[J]. 无机材料学报, 2009, 24 (1): 97-102.
[7] 李秀艳, 杨贤锋, 吴明娒. 不同介质中水热合成纳米TiO2粉体及其光催化性能研究[J]. 无机材料学报, 2008, 23 (6): 1253-1258.
[8] 孙秀果, 魏雨, 贾振斌. 纳米二氧化钛粉体在水中的分散行为[J]. 电子元件与材料, 2003, 22 (5): 11-13.
[9] 梁宇, 谢广文. 化学复合镀Ni-P-纳米TiO2涂层的研究进展[J]. 腐蚀科学与防护技术, 2005, 17 (增刊): 469-470.
[10] 陈金媛, 李娜, 方金凤. 表面活性剂对纳米TiO2在水中分散与沉降性能的影响[J]. 浙江工业大学学报, 2012, 40 (6): 595-598.
[11] 吴雪兰. 纳米SiO2浆料的分散稳定性能及其对半导体硅片的电化学作用研究[D]. 长沙: 中南大学, 2005: 26-27.
[12] 周海鸥. 聚乳酸/二氧化硅有机无机杂化材料的制备和表征[D]. 合肥: 合肥工业大学, 2004: 21.
[13] 李东光. 化学镀液配方与制备200例[M]. 北京: 化学工业出版社, 2012: 44.
[14] 莫松平, 陈颖, 李兴, 等. 表面活性剂对二氧化钛纳米流体分散性的影响[J]. 材料导报, 2013, 27 (12): 43-46.
[ 编辑:韦凤仙 ]
Study on dispersity of nano-titania during electroless nickel-phosphorus nanocomposite plating
/ CHEN Er-yue*,YANG Xiao-chao, XU Juan, GUO Xiang-feng
The content and distribution of nano-TiO2in Ni-P-TiO2composite deposit prepared from Ni-P electroless plating bath with different contents of nano-TiO2were analyzed by X-ray photoelectron spectroscopy (XPS). The effects of the dosages of lactic acid (as a complexant) and polyvinylpyrrolidone (PVP, as a surfactant) and bath’s pH on dispersity of nano-TiO2in the Ni-P-TiO2composite plating bath were studied by infrared-visible-ultraviolet spectrophotometry. The optimal dispersion conditions were obtained as follows: nano-TiO23.0-4.0 g/L, PVP 0.2 g/L, lactic acid 4.5 mL/L, and pH 5.0-5.5.
nickel-phosphorus alloy; nano-titania; electroless composite plating; lactic acid; polyvinyl pyrrolidone; dispersity; stability
TQ153.2
A
1004 - 227X (2015) 16 - 0898 - 05
2015-03-13
2015-06-02
黑龙江省高校科研创新团队项目(2012TD012)。
陈尔跃(1959-),男,黑龙江人,博士,副教授,研究方向为物理化学。
作者联系方式:(E-mail) eryue_59@163.com。

