RP-HPLC法同时测定西洋参含片中4种成分
闫玉梅,赵梅梅,王笑笑,方佳成,廖 莎,王世祥,郑晓晖,2*
(1.西北大学生命科学学院,西安 710069;2.深圳清华大学研究院,深圳 518057)
RP-HPLC法同时测定西洋参含片中4种成分
闫玉梅1,赵梅梅1,王笑笑1,方佳成1,廖莎1,王世祥1,郑晓晖1,2*
(1.西北大学生命科学学院,西安710069;2.深圳清华大学研究院,深圳518057)
摘要:目的建立同时测定西洋参含片中人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1及拟人参皂苷 F11含量的RP-HPLC方法。方法色谱柱为Agilent TC-C18(250 mm × 4.6 mm,5 μm);流动相为0.5 mL·L-1磷酸溶液(A)-乙腈(B),梯度洗脱;流速:1.0 mL·min-1;检测波长:203 nm;柱温:30 ℃。 结果人参皂苷Rg1和人参皂苷Re及人参皂苷Rb1在2.5 ~ 500 μg·mL-1、拟人参皂苷F11在5.0 ~ 1 000 μg·mL-1范围内线性关系良好(r ≥ 0.999 4);平均加样回收率均大于95.0%。结论该方法简便、准确,重复性好,可作为西洋参含片的质量控制方法。
关键词:西洋参;人参皂苷Rg1;人参皂苷 Re;人参皂苷Rb1;拟人参皂F11
西洋参为五加科植物西洋参PanaxquinquefoliusL. 的干燥根,原产于美国、加拿大,我国西洋参均为人工栽培,集中分布在吉林、辽宁、北京、陕西和山东等地。西洋参味苦,性凉,入心、肺、肾经,功能以补益为主,可滋阴降火、益气生津[1-2]。西洋参既是名贵上品中药,又是高级滋补佳品。西洋参中的主要活性成分是皂苷类成分,其中拟人参皂苷 F11是特有成分[3-6]。据报道[7-11]西洋参具有促进人体新陈代谢,抗缺氧、抗疲劳、抗衰老,维护人体心、肺、肝、肾等多方面的生理保健功能。经常服用西洋参,可强身健体,延年益寿。近年来,西洋参含片作为保健食品已经被广泛使用,但对其质量控制缺乏监测。本文建立了一种同时测定西洋参含片中上述4种皂苷含量的高效液相色谱法[12],该方法快速、准确、重复性好,为西洋参制剂的质量控制提供依据。
1仪器与试药
1.1仪器Agilent 1100系列高效液相色谱系统(包括四元泵,DAD检测器,Agilent Chemstation工作站,美国Agilent公司);Sartorius BP221S 万分之一电子天平;NF6000-2减压旋转蒸发仪(上海申生科技有限公司);KQ5200DE 型数控超声波清洗仪(江苏省昆山市超声仪器有限公司);VORTEX QILINBETER-6快速混匀器;CJB-A油浴仪;TGL-16G高速离心机(上海安宁科学仪器公司)。
1.2试药市售西洋参含片(含糖)Ⅰ(规格为900 mg/片×12片/盒×6盒);市售西洋参含片(无糖)Ⅱ(规格为700mg/片×20片/盒×10盒);市售西洋参无糖含片Ⅲ(规格为1 000 mg/片×12片/盒×10盒);市售无糖西洋参含片Ⅳ(规格为700 mg/片×16片/盒×10盒);人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和拟人参皂苷F11对照品(中国药品生物制品检定所,批号分别为:110703-201128,110754-201123,110704-201223,110841-200505);乙腈为色谱纯(美国Fisher公司);甲醇、正丁醇、磷酸为分析纯;水为超纯水。
2方法与结果
2.1对照品溶液的制备分别精密称取人参皂苷 Rg1、人参皂苷Re、人参皂苷Rb1和拟人参皂苷 F115.0 mg,置于5.0 mL棕色量瓶中,用甲醇溶解并定容至刻度,制备成质量浓度为1.0 mg·mL-1的对照品溶液。
2.2供试品溶液的制备精密称取供试品粉末0.25 g,置于具塞锥形瓶中,精密加入水饱和的正丁醇12.5 mL,称定质量,置于油浴(135 ℃)中加热回流提取1.5 h,放冷,再称定质量,用水饱和的正丁醇补足减失的质量,摇匀,过滤。将滤液减压旋转蒸发挥干溶剂,残渣加入体积分数为50%的甲醇5 mL使其溶解,摇匀,过滤,9 000 r·min-1离心10 min,取上清液,过0.45 μm有机滤膜,4 ℃冷藏备用。
2.3色谱条件及系统适用性色谱柱:Agilent TC-C18(250 mm×4.6 mm,5 μm);流动相:A相为0.5 mL·L-1的磷酸溶液,B相为乙腈,梯度洗脱,洗脱程序:0~10 min,20%~22% B;10~30 min,22% B;30~65 min,22%~55% B;检测波长:203 nm;流速:1.0 mL·min-1;柱温:30 ℃;进样量:50.0 μL。在上述色谱条件下,样品中人参皂苷 Rg1、人参皂苷Re、人参皂苷Rb1和拟人参皂苷 F11与其他组分均达到了基线分离(R≥1.5)。见图1。

图1高效液相色谱图
A.混合对照品;B.市售西洋参含片(含糖)Ⅰ供试品;C.市售西洋参含片(无糖)Ⅱ供试品;D.市售西洋参无糖含片Ⅲ供试品;
E.市售无糖西洋参含片Ⅳ供试品;F.阴性对照品1.人参皂苷 Rg1;2.人参皂苷 Re;3.人参皂苷 Rb1;4.拟人参皂苷 F11
Fig.1HPLC chromatograms of different samples
A. mixed reference substances; B. marketedPanaxquinquefolius Tablets (with sugar) Ⅰ sample; C. marketedPanaxquinquefolius Tablet (without sugar) Ⅱ sample; D. marketedPanaxquinquefolius Tablets (without sugar) Ⅲ sample; E. marketedPanaxquinquefolius Tablets (without sugar) Ⅳ sample;1.ginsenoside Rg1;2.ginsenoside Re;3.ginsenoside Rb1;4.pseuoginsenoside F11
2.4方法学考察
2.4.1线性关系考察精密吸取2.1 项下各对照品溶液,用甲醇配制成系列质量浓度混合对照品溶液(人参皂苷 Rg1、人参皂苷Re、人参皂苷Rb1分别为2.5,12.5,25.0,50.0,125.0,250.0和500.0 μg·mL-1;拟人参皂苷 F11为5.0,25.0,50.0,125.0,250.0,500.0和1 000.0 μg·mL-1)按照拟定色谱条件进样分析。以对照品溶液质量浓度(X,μg·mL-1)对峰面积(Y)进行线性回归,结果如表1所示,说明4种组分在拟定的色谱条件下,具有较好的线性关系以及检测灵敏度。
2.4.2精密度实验精密吸取混合对照品溶液50.0 μL(含人参皂苷 Rg1、人参皂苷Re和人参皂苷Rb1均为50 μg·mL-1,拟人参皂苷 F11为125 μg·mL-1)重复进样6次,按照峰面积值计算,其相对标准偏差RSD值分别为1.0%,0.7%,0.9%和0.8%。结果表明,仪器精密度良好。
表14种成分的线性关系
Tab.1 The linear relationship of the four components

成分回归方程线性范围/μg·mL-1r人参皂苷Rg1Y=11.668X-50.3042.5~500.00.9994人参皂苷ReY=15.244X-2.89562.5~500.00.9996人参皂苷Rb1Y=9.0484X+19.0432.5~500.00.9999拟人参皂苷F11Y=3.2659X+8.09495.0~1000.00.9995
2.4.3重复性实验取西洋参制剂(市售无糖西洋参含片Ⅳ)6份,分别按照2.2 项下方法制备供试品溶液,并进行测定。人参皂苷 Rg1、人参皂苷Re、人参皂苷Rb1和拟人参皂苷 F11峰面积的 RSD值分别为2.3%,2.4%,2.0%和2.3%。结果表明,样品重复性良好。
2.4.4稳定性实验在相同色谱条件下,精密吸取供试品溶液50.0 μL(市售无糖西洋参含片Ⅳ)考察其在0,2,4,6,8,10和12 h内的稳定性。人参皂苷 Rg1、人参皂苷Re、人参皂苷Rb1和拟人参皂苷 F11峰面积的 RSD值分别为2.2%,2.5%,0.9%和1.9%。结果表明,供试品溶液在12 h内测定结果稳定。
2.4.5加样回收率实验精密称取已知含量的西洋参制剂(市售无糖西洋参含片IV)约0.25 g,平行6份,精密称定。分别加入4种对照品溶液适量(含人参皂苷Rg10.16 mg、人参皂苷Re 0.32 mg、人参皂苷Rb12.50 mg和拟人参皂苷F110.52 mg),按照2.2 项下制备方法制备供试品溶液,在拟定色谱条件下进样分析,并记录峰面积,回收率实验结果见表2。人参皂苷 Rg1、人参皂苷Re、人参皂苷Rb1和拟人参皂苷 F11平均回收率分别为98.5%(RSD=1.8%),98.0%(RSD=0.9%),99.5%(RSD=0.6%),98.0%(RSD=1.2%)。人参皂苷 Rg1、人参皂苷Re、人参皂苷Rb1和拟人参皂苷 F11的平均回收率均大于95.0%。结果表明,该方法回收率良好。
表2回收率实验结果
Tab.2 Results of the recovery test

序号加入量/mg测得量/mg回收率/%人参皂苷Rg1人参皂苷Re人参皂苷Rb1拟人参皂苷F11人参皂苷Rg1人参皂苷Re人参皂苷Rb1拟人参皂苷F11人参皂苷Rg1人参皂苷Re人参皂苷Rb1拟人参皂苷F1110.160.322.500.520.320.655.021.0698.8898.0699.6898.1820.160.322.500.520.330.665.041.0695.7497.2799.1597.8030.160.322.500.520.320.655.001.0498.5498.21100.08100.2840.160.322.500.520.320.654.991.0799.6599.06100.2197.5850.160.322.500.520.320.645.031.06100.8899.1599.4198.0360.160.322.500.520.330.665.071.0897.3596.7298.5596.60
2.5样品测定按照2.2项下方法制备供试品溶液,以拟定色谱条件进样50.0 μL,每批样品平行测定3次,记录峰面积,按照标准曲线法计算人参皂苷 Rg1、人参皂苷Re、人参皂苷Rb1和拟人参皂苷 F11的含量。测定结果见表3。
表3样品测定结果
Tab.3 Sample determination results
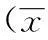
±s, n=3)
3讨论
3.1色谱条件的选择
3.1.1流动相的选择对甲醇-水、乙腈-水和乙腈-0.5 mL·L-1磷酸溶液等多种不同比例流动相进行比较,发现选择乙腈-0.5 mL·L-1磷酸溶液梯度洗脱时分离效果最好。样品2 h图谱显示65 min后无特征峰出现。故选择本系统为流动相。
3.1.2检测波长的选择结合人参皂苷的吸收特征,在203 nm波长下,以乙腈-0.5 mL·L-1磷酸溶液为流动相,C18反相色谱进行初试,再采用二极管阵列检测器(DAD)检测,全波长扫描分析,发现检测波长为203 nm时,各供试液所出的色谱峰较多,并且各色谱峰能够较好地分离,最终确定检测波长为203 nm。
3.1.3测定成分参考《中国药典》2010年版一部西洋参项下,对人参皂苷 Rg1、人参皂苷Re、人参皂苷Rb1含量的规定,为了更好的控制西洋参含片的质量,本实验选择对其主要有效成分人参皂苷 Rg1、人参皂苷Re、人参皂苷Rb1及特征性成分拟人参皂苷 F11的含量进行测定,结果表明,该方法对人参皂苷 Rg1、人参皂苷Re、人参皂苷Rb1和拟人参皂苷 F11的测定简便易行,可以作为西洋参含片质量控制的参考方法。
3.2提取方法[13]本实验所用提取条件在参考《中国药典》的基础上,经过多次优化而确定。分别以水饱和的正丁醇、体积分数为50%,70%和100%的甲醇将0.25 g样品溶于圆底烧瓶中,加热回流1.5 h,结果表明,水饱和的正丁醇提取的4种成分的含量最高。同时对提取时间进行了考察,分别回流提取1.0,1.5和2.0 h,结果表明,2.0与1.5 h提取结果基本一致,最终以水饱和的正丁醇加热回流提取1.5 h为最佳提取方法。
4结论
从结果可知,西洋参含片中人参皂苷 Rg1、人参皂苷Re、人参皂苷Rb1与特征性成分拟人参皂苷F11的含量存在一定差异。西洋参制剂中的4种皂苷总含量范围在0.54%~1.40%,其中人参皂苷Rg1在0.02%~0.07%范围内,人参皂苷 Re在0.012%~0.13%范围内,人参皂苷 Rb1在0.37%~1%范围内,拟人参皂苷 F11在0.08%~0.30%范围内。比较发现所测西洋参制剂中人参皂苷 Rb1含量较高,拟人参皂苷 F11次之。比较市售4个厂家生产的西洋参含片中4种指标成分的含量,发现存在一定差别,其中市售无糖西洋参含片IV中4种指标成分的含量最高,其次是市售无糖西洋参含片II含量较高。
本实验采用HPLC法同时测定西洋参含片中人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和拟人参皂苷F11的含量,节省了分析时间,减少了溶剂的使用量和样品的进样量,同时该方法精密度、稳定性和回收率良好,可用于西洋参制剂的鉴别和质量控制。
参考文献:
[1]国家药典委员会.中国药典2010年版[S].一部.北京:中国医药科技出版社,2010:122-123.
[2]李岚,陈华.HPLC法测定不同产地西洋参中人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1含量[J].中国医药导报,2011,8(20):103-104.
[3]Dou D Q,Hou W B,Chen Y J. Studies on the characteristic constituents of Chinese ginseng and American ginseng[J]. Planta Med,1998,64(6):585-586.
[4]Tanaka O,Kasai R,Morita T. Chemistry of ginseng and related plants: recent advances[J]. Abst Chin Med,1986,1(1):130-152.
[5]刘利亚,王娅芳,张卫国,等.西洋参类保健食品中总皂苷与人参皂苷Re、Rb1等功效成分含量相关性研究[J].中国食品卫生杂志,2010,22(4) :315-318.
[6]陈双厚.西洋参化学成分及药理作用研究概况[J].西北药学杂志,1990,5(4):43-45.
[7]李冀,柴剑波,赵伟国.西洋参抗疲劳作用及对迟发型超敏反应单核吞噬细胞功能影响的实验研究[J].中华中医药学刊,2007,25(10):2002-2004.
[8]张崇禧,郑友兰,李向高,等.国产西洋参芦头中皂甙的分离鉴定[J].中成药,1994,16(2):37-38.
[9]李向高,马英春,王秀全,等.西洋参的研究[M].北京:中国科学技术出版社,2001:06.
[10]金庆武.西洋参在保健食品中的应用[J].中国自然医学杂志,2002,4(2):101-103.
[11]王筠默.西洋参药理作用研究的最新进展[J].人参研究,2001,13(4):2-5.
[12]陈键.HPLC法测定含化上清片中白花前胡甲素和白花前胡乙素的含量[J].西北药学杂志,2015,30(3):251-252.
[13]韩丹丹,吴文夫,魏建华,等.HPLC测定不同提取方法对西洋参单体皂苷含量的影响[J].人参研究,2013,25(2):25-27.
Simultaneous determination of four components inPanaxquinquefoliusL. Tablets by RP-HPLC
YAN Yumei1,ZHAO Meimei1,WANG Xiaoxiao1,FANG Jiacheng1,LIAO Sha1, WANG Shixiang1,ZHENG Xiaohui1,2*(1. College of Life Sciences,Northwest University,Xi′an 710069,China;2. Research Institute of Tsinghua University in Shenzhen,Shen-zhen 518057,China)
Abstract:ObjectiveTo establish an RP-HPLC method for simultaneous determination of four components in Panax quinquefolius L. Tablets ,including gensenoside Rg1, gensenoside Re,gensenoside Rb1and pseuoginsenoside F11. MethodsThe analysis was performed on an Agilent TC-C18column (250 mm×4.6 mm,5 μm) with 0.5 mL·L-1phosphoric acid-acetonitrile with step gradient elution. The flow rate was 1.0 mL·min-1with detection wavelength of 203 nm. The column temperature was kept at 30 ℃. ResultsThe ginsenoside Rg1,ginsenoside Re,ginsenoside Rb1and pseuoginsenoside F11showed good linear relationship in the ranges of 2.5-500.0,2.5-500.0,2.5-500.0 and 5.0-1 000.0 μg·mL-1,respectively. All of the average recovery rates were more than 95.0%. ConclusionThis method is simple,accurate,reliable and reproducible. It can be used for the quality control of Panax quinquefolius L. Tablets.
Key words:Panax quinquefolius L.;gensenoside Rg1;gensenoside Re;gensenoside Rb1;pseuoginsenoside F11
收稿日期:(2015-07-17)
通信作者:*郑晓晖,男,教授
作者简介:闫玉梅,女,在读硕士研究生
基金项目:国家自然科学 (编号:81303185);陕西省重点科技创新团队计划(编号:2013KCT-24);高等学校博士学科点专项科研基金项目(编号:20136101120030)
中图分类号:R927.2
文献标志码:A
文章编号:1004-2407(2016)01-0005-04
doi:10.3969/j.issn.1004-2407.2016.01.002

