ZnS/Ni2P复合物的合成、表征及光催化性能
刘淑玲,马兰兵,王正奇,仝建波
ZnS/Ni2P复合物的合成、表征及光催化性能
刘淑玲1, 2,马兰兵1, 2,王正奇1, 2,仝建波1, 2
(1. 陕西科技大学教育部轻化工助剂化学与技术重点实验室,西安 710021;2. 陕西科技大学化学与化工学院,西安 710021)
以ZnS微球作为前驱体,乙酸镍为镍源,白磷为磷源,采用水热法制备ZnS/Ni2P复合物。通过XRD,FE-SEM和TEM表征得知,ZnS/Ni2P复合物由立方相的ZnS微球和复合于微球表面的六方相Ni2P颗粒组成,且ZnS微球由ZnS纳米颗粒组成。光催化降解染料实验测试结果显示,ZnS/Ni2P复合物与单一的ZnS相比,催化性能得到显著改善。同时,探究了不同的ZnS与Ni2P质量比对复合物性能的影响,结果表明Ni2P与ZnS的相对复合比例太大或太小都会对复合物性能的提升产生不良影响,最佳ZnS:Ni2P的质量比为4:1。
ZnS/Ni2P;复合材料;水热法;光催化降解;ZnS颗粒
近年来,由纺织、造纸和其它一些产业产生的有机污染废水已经导致了严峻的生态及环境问题[1]。为了减轻废弃的染料对水体和自然环境造成的严重污染,多种相关技术诸如细菌清除染料、纳米材料吸附染料等得到了显著的发展。其中,光催化方法由于具有高效率以及适用性强等优势[2],在有机废水处理方面展现出了巨大的潜力和应用优势。而纳米光催化剂作为其中的佼佼者,迅速被人们所发现、接受并逐渐得到发展[3]。自1972年FUJISHIMA和HONGDA[4]在《Nature》发表TiO2电极上光解水以来,人们开始对纳米半导体的光催化行为进行研究。目前,半导体纳米材料作为纳米光催化剂已经成为光催化研究的热点,获得研究者的广泛青睐与深入研究[5]。硫化锌(ZnS)作为一种II-VI族化合物直接带隙半导体材料,禁带宽度为3.6~3.8 eV,是一种应用广泛的半导体光学和光电材料[6−7],可以应用在荧光材料、光激发二极管、太阳能电池、传感器等众多光学和电学领域[8−10]。另外,由于ZnS具有丰富的光生电子−空穴对,因此它在光催化领域也有着不俗的表现,特别是在光催化降解染料方面有着很大的优势[11−13]。然而,由于ZnS光生电子−空穴对分离效率低,ZnS难以取得满意的光催化反应效率。另一方面,II-VI半导体如CdS,ZnS等在使用过程中存在光腐蚀现象,不但影响了它们的实际应用,还可能对环境产生危害。基于对材料性能要求的提高及应用范围拓展的需求,提升ZnS材料的光催化性能十分必要。化学修饰(化学改性)是一种非常有效的提升光催化剂活性方法,包括掺杂贵金属、非金属;复合窄带隙半导体,例如Fe2O3,WO3,Bi2O3,Ni2P等;引入碳质材料,如石墨烯[14−15]。同半导体复合可以大幅促进光生电子−空穴对的产生和分离,从而可以极大地提高光催化剂的活性[16−17]。因此将半导体材料与ZnS复合制得光催化性能增强的复合物也成为可能。过渡金属磷化物由于其独特的物理和化学特性,使其在磁学、电学、数据存储、催化等领域有着广泛的应用[18−19],特别是在加氢脱硫[20]、脱氮方面[21]和光催化降解[22−23]领域。磷化镍(Ni2P, Eg=1.0 eV[24])作为过渡金属磷化物的一员,在抗腐蚀、抗氧化、防水材料[25]及催化剂等方面均表现出一定的应用价值。特别是在光催化领域,Ni2P有着良好的应用价值。如NI等[26]利用水热法制得了具有较好的光催化降解能力的Ni2P纳米材料。GAO等[27]报道了一种高效的Ni2P/CdS催化剂,在光照射下它可以迅速地将硝基芳烃降解还原。所以将Ni2P与ZnS复合是提高ZnS材料光催化活性的有效方法。制备Ni2P的方法有很多种,如:程序升温还原法、低温等离子体还原法、水热/溶剂热法等[28−30]。其中,水热法由于操作简单,易于调控等特点受到人们的广泛关注,已经合成了各种形貌和尺寸的磷化镍纳/微米材料,如LI等[31]在低温下通过水热法合成出了空心球状Ni2P,LIU等[32]和WANG等[33]利用水热法控制合成出了纳米尺寸的磷化镍。本研究采用水热法,以已制备的ZnS作为前驱体,乙酸镍作为镍源,白磷作为磷源制备ZnS/Ni2P复合物。利用XRD,FE-SEM和TEM对ZnS和ZnS/Ni2P复合物的物相和形貌进行分析。同时,以有机污染物吡咯红B为降解目标,对ZnS和ZnS/Ni2P复合物的光催化性能作比较。同时对不同ZnS:Ni2P复合比例的复合物性能进行讨论,研究ZnS/Ni2P复合物在降解过程中的光催化机理。
1 实验
1.1 ZnS微球的制备
在磁力搅拌下,将0.2795 g(1 mmol)二水合乙酸锌溶于盛有15 mL蒸馏水的锥形瓶中,待其溶解完全,接着向体系中滴加0.45 mL冰醋酸,搅拌20 min后,再向溶液中加入0.1142 g(1.5 mmol)硫脲,继续搅拌至溶液呈无色透明状后将其转移进20 mL聚四氟乙烯做内衬的不锈钢反应釜中,封釜,并将其置于恒温干燥箱中在170 ℃下反应8 h。反应结束后,待反应釜自然冷却至室温,离心分离得白色沉淀,分别用乙醇和蒸馏水洗涤产物数次,最后将产物置于真空干燥箱中于60 ℃干燥6 h。收集产物,待进一步表征和实验所用。所用的所有原料均为分析纯并均未经进一步纯化处理,水为二次蒸馏水。
1.2 ZnS/Ni2P复合物的制备
准确称量上述步骤所制备的ZnS微球0.0194 g(0.2 mmol),将其加入到盛有18 mL蒸馏水的锥形瓶中,超声20 min使ZnS分散均匀,然后置于磁力搅拌器上,称取0.0124 g(0.05 mmol)乙酸镍加入到体系中,继续搅拌20 min使乙酸镍溶解完全,紧接着向溶液中加入0.1 g十六烷基三甲基溴化铵(CTAB),继续搅拌20 min,之后再加入0.1 mL氨水,待体系混合均匀。最后,将所得的混合溶液转移进容积为23 mL的内衬为聚四氟乙烯的不锈钢反应釜中,并称取0.0248 g(0.2 mmol)白磷加入反应釜中,封釜,于180 ℃反应12 h。反应结束后,待反应体系自然冷却至室温,经离心得到黑色沉淀,分别用乙醇、苯和蒸馏水洗涤产物数次,然后将产物置于60 ℃的真空干燥箱中干燥 24 h。收集产物,待进行表征和后续实验所用。
对不同ZnS:Ni2P复合比例(质量比)对吡咯红B溶液降解的影响实验,制备时只更改乙酸镍的加入量来合成不同复合比例ZnS/Ni2P。
1.3 产物表征及性能测试
用型号为Rigaku D/Max-3c的X线衍射仪(XRD)分析产物的结构与物相,采用的靶材为Cu K(= 0.15418 nm)。用型号为Hitachi S−4800的场发射扫描电子显微镜(FE−SEM)进行产物的形貌分析。利用FEI公司生产的Tecnai G2 F20型透射电子显微镜(TEM)对产物的形貌进行分析,其加速电压为200 kV。
于容量瓶中配制浓度为1.0×10−5mol/L的吡咯红B溶液并将其作为目标降解物,在40 W的紫外灯照射下,进行光催化降解实验。分别称取之前制备的ZnS微球和ZnS/Ni2P复合物各50 mg,置于暗处并超声20 min,使所加入的催化剂能够很好的分散于50 mL配制好的吡咯红B溶液中。对所得的混合物分别进行暗处理,即在暗处于磁力搅拌器上搅拌20 min,从而使其达到吸附−脱附平衡。暗处理后对混合物进行第一次取样,之后每隔15 min光照后,对混合物取样一次。最后,对所取的样进行离心并倒出上层清液,利用紫外可见分光光度计对其进行检测。
2 结果与讨论
2.1 结构与组分分析
图1所示为ZnS微球和ZnS/Ni2P复合物的物相分析结果。由图可知,曲线A的主要特征衍射峰均可以指标化为立方相结构的ZnS(JCPDS NO. 65-0309,晶胞参数=5.400 Å),且在2角28.61°,47.59°,56.47°处的特征衍射峰分别对应ZnS结构的(111),(220)和(311)晶面。衍射峰峰形尖锐,说明产物的结晶度较高;没有其它相或杂质的衍射峰出现,说明产物的纯度高。从曲线B看出,除立方相结构ZnS的特征衍射峰以外,还可以观察到其它的2角在40.76°,44.65°和54.16°处的特征衍射峰,它们可以分别指标化为六方相Ni2P的(111),(021)和(300)晶面,与JCPDS卡片报道值相一致(JCPDS NO. 65-3544,=5.862 Å,=3.372 Å)。
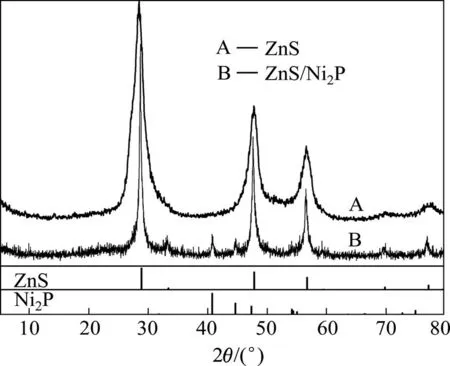
图1 ZnS和ZnS/Ni2P复合物的XRD图谱
2.2 形貌和尺寸分析
图2所示为ZnS微球及ZnS/Ni2P复合物的SEM照片。由图2(a)可知,制备的ZnS样品由大量单分散的尺寸较均一的微球组成,微球平均直径约3 µm。图2(b)所示为单个ZnS微球的SEM照片,可以看出ZnS微球的表面由细小的颗粒组成,可以推测整个ZnS微球由ZnS纳米颗粒堆积而成,且其表面较光滑。由图2(c)可知,ZnS/Ni2P复合物也展现了尺寸较均一的微球形貌,但其表面变得相对粗糙。这种特征从图2(d)中可以更加清楚地看到,即ZnS微球表面包裹着Ni2P粒子,这也进一步证实了由XRD测试得出的结论。但是,获得的ZnS/Ni2P复合物中的Ni2P粒子形貌相对不规整。
图3所示为ZnS微球及ZnS/Ni2P复合物的TEM照片。从图3(a)看出,ZnS微球的表面相对平整、光滑,微球直径约为3 µm。ZnS/Ni2P复合物微球的表面变得相对粗糙,说明Ni2P纳米颗粒沉积在ZnS微球的表面。
2.3 ZnS和ZnS/Ni2P复合物的光催化活性
图4(a)~(c)所示为室温下紫外灯照射90 min后,加入不同催化剂的吡罗红B溶液的紫外可见吸收谱图,其中图4(a)为未加任何催化剂的紫外可见吸收谱图;图4(b)和(c)分别为加入ZnS微球和加入ZnS/Ni2P复合微球的紫外可见吸收谱图。由图4(a)~(c)可以看出,随紫外光照射时间延长,最大吸收波长在525 nm处的吡咯红B溶液吸收峰的强度逐渐减弱;且在紫外光照射90 min后,加入不同催化剂的吡咯红B溶液吸收峰的强度减弱程度不同。显然,未加催化剂时,吡咯红B几乎不发生降解,这为探讨催化剂对吡咯红B分子降解的贡献中消除了其自身的影响。在有催化剂存在时,吡咯红B溶液的降解较无催化剂时好。此外,ZnS/Ni2P复合物较单纯的ZnS展现出更强的降解能力。图4(d)为相对应的降解率曲线图,图中轴0−t/0代表降解率,其中0为经暗处理后吡罗红B溶液达到吸附脱附平衡时的初始浓度;t为光照时间为t时溶液的浓度。曲线A,B和C分别代表未加催化剂、加入ZnS和加入ZnS/Ni2P复合物的降解率曲线。由图可以更加直观的观察到,未加催化剂时,吡罗红B溶液几乎没有降解。而当加入ZnS/Ni2P复合物后,吡罗红B溶液的降解率达到了72%,高于加入ZnS后吡罗红B溶液的降解率62%。ZnS/Ni2P复合物增强的光催化活性可以归因于壳层磷化镍颗粒的修饰。一般而言,在紫外光的照射下,ZnS激发产生的空穴和电子大部分会迅速重新结合,从而降低了ZnS的光催化活性。另外ZnS本身存在的光腐蚀现象,也会破坏ZnS,造成ZnS损失。然而对于ZnS/Ni2P复合物,由于Ni2P的带隙较窄,在紫外光的照射下,由ZnS光激发产生的电子(e−)和空穴(h+)会在电势能的驱动下迁移到Ni2P价带和导带。因此,ZnS的光生电子和空穴可得到有效地分离,从而降低了它们重新结合的机会,使其光催化降解效率得到显著提升[34]。另外,将Ni2P同ZnS复合,虽然不能完全将ZnS的光腐蚀现象消除,但可在很大程度上缓解,从而减少ZnS的损失,促进其光催化反应效率[27]。

图2 ZnS微球和ZnS/Ni2P复合物的SEM图片

图3 ZnS微球和ZnS/Ni2P复合物的透射电镜图
复合物中不同组分的相对浓度会对其性能产生影响。所以,分别对不同ZnS:Ni2P复合比例对吡咯红B溶液降解的影响进行研究。图5所示为吡咯红B溶液在不同ZnS:Ni2P复合比例下的降解率曲线图。图中曲线a,b和c分别代表ZnS:Ni2P为2:1,8:1和4:1时的降解率曲线。可明显看出,当Ni2P浓度相对较高时(如曲线a),ZnS/Ni2P复合物对吡咯红B 90 min的降解率约为23%,低于实验中采取的ZnS:Ni2P为4:1时的降解率72%,其原因可能是当Ni2P含量相对较高时,高浓度的Ni2P会覆盖ZnS/Ni2P复合物界面间的活性位点,使得ZnS不能够有效地参与到光催化反应中,进而影响光催化活性。而当Ni2P含量相对较低时(如曲线b),ZnS/Ni2P复合物的降解率达到61%,同样低于72%,可能的原因是低浓度的Ni2P只能够使少量ZnS的光生电子和空穴转移到Ni2P的导带和价带上,使得ZnS的光催化效率不能够得到显著提升,故Ni2P的相对含量少会导致ZnS/Ni2P复合物的光催化活性较低。所以,最佳的ZnS:Ni2P复合配比为4:1。

图4 加入不同催化剂时吡咯红B的紫外可见吸收谱图及降解率曲线

图5 吡咯红B在不同ZnS/Ni2P比例的降解率曲线
3 结论
1) 通过水热合成法制备出ZnS/Ni2P复合物。该复合物由立方相的ZnS微球和复合于微球表面的六方相Ni2P颗粒组成。与单一ZnS相比,ZnS/Ni2P复合物的催化性能明显提高。
2) 不同的ZnS:Ni2P复合比例对复合物性能有较明显的影响,Ni2P与ZnS的相对浓度太大或太小都不利于复合物光催化性能的改善。
[1] SHARMA M, JAIN T, SNGH S, et al. Photocatalytic degradation of organic dyes under UV-visible light using capped ZnS nanoparticles[J]. Solar Energy, 2012, 86(1): 626−633.
[2] FAN Y Z, DENG M H, CHEN G P, et al. Effect of calcination on the photocatalytic performance of CdS under visible light irradiation[J]. Journal of Alloys and Compounds, 2011, 509(5): 1477−1481.
[3] RAJABI H R, FARSI M. Effect of transition metal ion doping on the photocatalytic activity of ZnS quantum dots: Synthesis, characterization, and application for dye decolorization[J]. Journal of Molecular Catalysis A: Chemical, 2015, 399: 53−61.
[4] FUJISHIMA A, HONDA K. TiO2photoelectrochemistry and photocatalysis[J]. Nature, 1972, 238(5358): 37−38.
[5] LIU M, PIAO L Y, LU W M, et al. Anatase TiO2single crystals with exposed {001} and {110} facets: Facile synthesis and enhanced photocatalysis[J]. Chemical Communications, 2010, 46(10): 1664−1666.
[6] LlIDDELL C M, SUMMERS C J. Monodispersed ZnS dimmers, trimers, and tetramers for lowers symmetry photonic crystal lattices[J]. Advanced Materials, 2003, 15(20): 1715−1719.
[7] PI Z B, SU X L, YANG C, et al. Chemical vapor deposition synthesis and photoluminescence properties of ZnS hollow microspheres[J]. Materials Research Bulletin, 2008, 43(8): 1966−1970.
[8] 邓意达, 贺跃辉, 唐建成, 等. ZnS光电材料制备技术的研究进展[J]. 粉末冶金材料科学与工程, 2002, 7(1): 31−37. DENG Yida, HE Yuehui, TANG Jiancheng, et al. Progress in investigation and preparation methods of ZnS photoelectric materials[J]. Materials Science and Engineering of Powder Metallurgy, 2002, 7(1): 31−37.
[9] ERKAYA Y, NMINIBAPIEL D, ARYAL K, et al. ZnS films deposited by ALD for solar cell applications[J]. ECS Transactions, 2013, 50(51): 45−48.
[10] PRAKASAM B A, LAHTINEN M, PEURONEN A, et al. Phase selective synthesis of ZnS nanoparticles from structurally new dithiocarbamate precursor[J]. Materials Letters, 2015, 144: 19−21.
[11] LI Y, HE X Y, CAO M H, et al. Micro-emulsion-assisted synthesis of ZnS nanospheres and their photocatalytic activity[J]. Materials Research Bulletin, 2008, 43(11): 3100−3110.
[12] LI X Y, HU C G, LIU H, et al. ZnS nanoparticles self-assembled from ultrafine particles and their highly photocatalytic activity[J]. Physica E, 2011, 43(5): 1071−1075.
[13] 汤化伟, 李珍. 硫化锌微米球的水热合成和光催化性能[J]. 人工晶体学报, 2012, 41(1): 125−129. TANG Huawei, LI Zhen. Hydrothermal Synthesis and Photocatalytic Properties of Zinc Sulfide Microsphere[J]. Journal of Synthetic Crystals, 2012, 41(1): 125−129.
[14] 周志超, 段学臣, 朱奕漪, 等. 溶胶凝胶法制备掺杂纳米TiO2粉末及其光催化性能[J]. 粉末冶金材料科学与工程, 2013, 18(3): 434−440. ZHOU Zhihao, DUAN Xuechen, ZHU Yiyi, et al. Doped nano titania powder prepared by sol-gel technique and its photocatalytic activity[J]. Materials Science and Engineering of Powder Metallurgy, 2013, 18(3): 434−440.
[15] MONDAL C, SINGH A, SAHOO R, et al. Preformed ZnS nanoflower prompted evolution of CuS/ZnS p-n heterojunctions for exceptional visible-light driven photocatalytic activity[J]. New Journal of Chemistry, 2015, 39(7): 261−267.
[16] ANUGA D, SUBHENDU K P, SUBHADRA C. Synthesis and optical and electrical properties of CdS/ZnS Core/Shell Nanorods[J]. Journal of Physical Chemistry C, 2007, 111(46): 17260−17264.
[17] ZHANG J T, TANG Y, WENG L, et al. Versatile strategy for precisely tailored Core@Shell Nanostructures with single shell layer accuracy: The case of metallic shell[J]. Nano Letters, 2009, 9(12): 4061−4065.
[18] ZHENG X F, YUAN S L, TIAN Z M, et al. Nickel/nickel phosphide pore-shell structured Nanoparticles: Synthesis, chemical, and magnetic architecture[J]. Chem Mater, 2009, 21(20): 4839−4845.
[19] CUI Y H, XUE Z M, FU Z W, et al. Nanocrystalline CoP thin film as a new anode material for lithium ion battery[J]. Journal of Alloys and Compounds, 2013, 555: 283−290.
[20] 宋华, 王紫东, 代敏, 等. Ni2P催化剂的低温还原法合成及其HDS性能[J]. 燃料化学学报, 2014, 42(6): 733−737. SONG Hua, WANG Zidong, DAI Min, et al. Preparation of Ni2P catalyst at low reduction temperature and its HDS performance[J]. Journal of Fuel Chemistry and Technology, 2014, 42(6): 733−737.
[21] 李景锋, 李学辉, 柴永明, 等. 磷化镍的制备、表征及其催化性能研究进展[J]. 化工进展, 2013, 32(11): 2621−2630. LI Jingfeng, LI Xuehui, CHAI Yongming, et al. Progress in the fabrication, characterization and catalytic reactivity of nickel phosphide[J]. Chemical Industry and Engineering Progress, 2013, 32(11): 2621−2630.
[22] OYAMA S T. Novel catalysts for advanced hydroprocessing: Transition metal phosphides[J]. Journal of Catalysis, 2003, 216(1/2): 343−352.
[23] LIU S L, LI S, LI M M, et al. Synthesis of tin phosphides (Sn4P3) and their high photocatalytic activities[J]. New Journal of Chemistry, 2013, 37(3): 827−833.
[24] PANNEERSELVAM A, MALIK M A, AFZAAL M, et al. The chemical vapor deposition of nickel phosphide or selenide thin films from a single precursor[J]. Journal of the American Chemical Society, 2008, 130(8): 2420−2421.
[25] MOTOJIMA S, HAGURI K, TAKAHASHI Y, et al. Chemical vapor deposition of nickel phosphide Ni2P[J]. Journal of the Less Common Metals, 1979, 64(1): 101−106.
[26] NI Y, JIN L, HONG J. Phase-controllable synthesis of nanosized nickel phosphides and comparison of photocatalytic degradation ability[J]. Nanoscale, 2011, 3(1): 196−200.
[27] GAO W Z, XU Y, CHEN Y, et al. Highly efficient and selective photocatalytic reduction of nitroarenes using the Ni2P/CdS catalyst under visible-light irradiation[J]. Chemical Communications, 2015, 51(67): 13217−13220.
[28] DENG Y, ZHOU Y, YAO Y, et al. Facile synthesis of nanosized nickel phosphides with controllable phase and morphology[J]. New Journal of Chemistry, 2013, 37(12): 4083−4088.
[29] WANG R, SMITH K J. The effect of preparation conditions on the properties of high-surface area Ni2P catalysts[J]. Applied Catalysis A: General, 2010, 380(1): 149−164.
[30] GUAN J, WANG Y, QIN M, et al. Synthesis of transition-metal phosphides from oxidic precursors by reduction in hydrogen plasma[J]. Journal of Solid State Chemistry, 2009, 182(6): 1550−1555.
[31] LI J, NI Y, LIAO K, et al. Hydrothermal synthesis of Ni12P5hollow microspheres, characterization and photocatalytic degradation property[J]. Journal of Colloid and Interface Science, 2009, 332(1): 231−236.
[32] LIU Z, HUANG X, ZHU Z, et al. A simple mild hydrothermal route for the synthesis of nickel phosphide powders[J]. Ceramics International, 2010, 36(3): 1155−1158.
[33] WANG B, HUANG X, ZHU Z, et al. Hydrothermal synthesis method of nickel phosphide nanoparticles[J]. Applied Nanoscience, 2012, 2(4): 423−427.
[34] RAJESHWAR K, DE TACCONI N R, CHENTHAMARAKSHAN C R. Semiconductor-based composite materials: preparation, properties, and performance[J]. Chemistry of Materials, 2001, 13(9): 2765−2782.
(编辑 高海燕)
Synthesis, characterization and photocatalytic properties of ZnS/Ni2P composites
LIU Shuling1, 2, MA Lanbing1, 2, WANG Zhengqi1, 2, TONG Jianbo1, 2
(1. Key Laboratory of Auxiliary Chemistry and Technology for Chemical Industry, Ministry of Education, Shanxi University of Science and Technology, Xi’an 710021, China;2. College of Chemistry and Chemical Industry, Shanxi University of Science and Technology, Xi’an 710021, China)
ZnS/Ni2P composites were synthesized via the hydrothermal route using ZnS as raw materials, nickel acetate as nickel source and white phosphorus as phosphorus source. After being characterized by using XRD, FE-SEM and TEM, the corresponding results show that the composites are composed of the cubic ZnS microspheres which are made up of ZnS particles, and hexagonal Ni2P particles which are attached to the surfaces of ZnS microspheres. Furthermore, photocatalytic degradation experiments were carried out, and the results indicate that the ZnS/Ni2P composites show superior photocatalytic activity compared to the pure ZnS microspheres. Also, the photodegradation experiments for pyronine B with various mass ratios of ZnS:Ni2P were implemented. It can be found that very large or very small ratios of ZnS:Ni2P will have a negative influence on the photocatalytic activity. The optimal mass ration of ZnS:Ni2P is 4:1.
ZnS/Ni2P; composites material; hydrothermal method; photocatalytic degradation; ZnS particle
O614
A
1673−0224(2016)04−555−07
国家自然科学基金资助项目(21301113);陕西省自然科学基金(2015JM2059);陕西省教育厅重点科研计划项目(15JS011)
2015−09−09;
2015−10−13
刘淑玲,副教授,博士。电话:15829706348; E-mail: shulingliu@aliyun.com

