钒电池电解液中氯离子测定方法研究
常 芳, 曹 沾, 刘效疆, 李晓兵, 陈 伟
(中国工程物理研究院电子工程研究所,四川绵阳621900)
钒电池电解液中氯离子测定方法研究
常 芳, 曹 沾, 刘效疆, 李晓兵, 陈 伟
(中国工程物理研究院电子工程研究所,四川绵阳621900)
使用氧化还原电极与复合银电极相结合的方法测定钒电解液中氯离子含量。研究表明,三、四价钒离子不会干扰钒电解液中氯离子的测定,利用钒电解液自身的氧化还原特性将钒电解液中影响测定的二、五价钒离子转化成三、四价钒离子,从而测定各种价态钒溶液中的氯离子浓度。浓度≤2.0mol/L,取样体积0.5~2 mL的钒电解液中钒离子浓度不影响测定。回收率为98.83%~101.40%,测量标准偏差,表明该方法简便、快速、准确,适合大批量钒电解液的现场充放电过程中氯离子含量数据监控。
钒电解液;氯离子;含量测定;电位滴定法
全钒氧化还原液流电池(钒电池)作为一种新型能量存储系统,具有可快速和大容量充放电、功率和容量可调等特性,是解决风能、太阳能存储的理想储能电源[1]。电解液是钒电池能量存储与转换的核心[2]。尽管国内外钒电池的研究已进入实用化阶段,但是由于钒电池充电后,在较高温度下,正极电解液中容易析出五氧化二钒沉淀;较低温度下,负极电解液容易析出二价钒沉淀,使钒电池的使用温度受限于10~40℃[3-4]。2011年,美国学者研究发现,用盐酸和硫酸混合水溶液作为钒电池支持电解液系统,使钒电解液中的氯离子浓度在2~6mol/L之间,形成硫、盐混合电解液支持体系,可使钒电解液的温度稳定范围扩宽到-5~50℃,拓展了钒电池的使用范围。
为了控制钒电解液配制过程氯离子含量(盐酸易挥发)及随时掌握加入电堆运行过程中电解液中氯离子浓度的变化趋势,需要及时跟踪检测电解液中氯离子的含量。目前测定Cl-含量的主要方法有沉淀滴定法[5]、分光光度法、离子色谱法、电位滴定法及温度滴定法等[6]。由于各种价态的钒离子都有非常鲜艳的特征颜色,并且钒电解液中氯离子含量很高(≥3mol/L),所以光度法、离子色谱法都不适合钒电解液中氯离子测定。钒电解液中含有V2+、V3+、V4+、V5+四种离子,V2+、V3+具有还原性,V5+具有强烈的氧化性,氧化还原电位滴定法并不适合钒电解液中氯离子的测定,温度滴定法操作繁琐。沉淀滴定法中与氯离子形成沉淀的汞和铬酸银等滴定剂对环境和人体都有毒害,尽可能不用。本文将DSC140-SC氧化还原复合电极和DM141-SC银复合电极结合使用,在电位滴定仪上测定钒电解液中氯离子含量,并对测定条件进行了研究,建立了钒电解液中氯离子含量的测定方法,该方法的建立对控制钒电解液中氯离子的含量,研究钒电池充放电过程中支持电解液盐酸在电堆中的存在情况都有非常重要的意义。
1 实验
1.1 仪器和试剂
仪器:T50自动电位滴定仪;DSC141-SC银复合电极;DSC140-SC氧化还原复合电极。试剂:0.1mol/L硝酸银标准溶液,称取17.5 g硝酸银溶于1 000 mL水中,摇匀,保存于棕色瓶中,用基准氯化钠标定;0.5mol/L盐酸标准溶液,量取45 mL分析纯盐酸加入1 000 mL水中,用基准碳酸钠标定盐酸浓度;≥1.5mol/L二价或三价钒电解液,VOSO4硫酸溶液在小电解槽中充电后形成的负极电解液;≥1.5mol/L五价钒电解液,VOSO4硫酸溶液在小电解槽中充电后形成的正极电解液,若非特别说明,实验用水均为去离子水。
1.2 实验方法
1.2.1 负极钒电解液
准确吸取1.0~2.0 mL钒电解液加入T50测量杯,加去离子水至50 mL,将测量杯安装在T50电位滴定仪上,插入DSC140-SC氧化还原复合电极,若含有二价钒离子,开启搅拌,从测量杯盖开口处逐滴加入不含氯离子的五价钒电解液,依据溶液的颜色及电极显示的电位数值,当钒离子全部被氧化为三价或四价钒离子时,换用DSC141-SC银复合电极,用标准硝酸银溶液滴定至滴定图形上出现滴定突跃,记录出现电位滴定突变点时对应的标准硝酸银溶液体积;若只含有三价钒离子,直接插入DSC141-SC银复合电极,用标准硝酸银溶液滴定至滴定图形上出现滴定突跃,记录滴定用标准硝酸银体积按式(1)计算钒电解液中氯离子浓度:

1.2.2 正极钒电解液
准确吸取1.0~2.0 mL钒电解液加入T50测量杯,加离子水至50 mL,加入1 mL稀硫酸溶液,用离子水稀释至50 mL,将测量杯安装在T50电位滴定仪上,若只有四价钒离子,直接插入DSC141-SC银复合电极,用标准硝酸银溶液滴定至滴定图形上出现滴定突跃,记录滴定用标准硝酸银体积;若含有五价钒离子,先插入DSC140-SC氧化还原复合电极,开启搅拌,从测量杯盖开口处逐滴加入不含氯离子的二价或三价钒电解液,依据溶液的颜色及电极显示的电位数值,当五离子全部被还原为四价钒离子时,换用DSC141-SC银复合电极,用标准硝酸银溶液滴定至滴定图形上出现滴定突跃,记录出现电位滴定突变点时对应的标准硝酸银溶液体积,按式(2)计算钒电解液中氯离子浓度。
记录出现电位滴定突变点时对应的标准硝酸银溶液体积;若含有五价钒离子,则按式(2)计算钒电解液中氯离子浓度:

2 结果与讨论
2.1 钒离子价态的影响
2.1.1 三、四价钒的影响
分别取含氯离子的三、四价钒电解液,加水稀释至50 mL,直接用硝酸银标准溶液滴定,随着滴定剂的加入,溶液中出现大量白色沉淀,滴定图形如图1、图2所示,含氯离子的三、四价钒电解液中,用硝酸银测定只有唯一一个AgCl沉淀终点。另取不含氯离子的三、四价钒电解液,用硝酸银标准溶液滴定,四价钒电解液中未发现任何沉淀,三价钒电解液中会出现轻微浑浊现象,但一旦滴加几滴氯离子,溶液中马上出现AgCl沉淀,未有银镜反应发生。说明氯离子存在时,硝酸银优先与氯离子反应。在1.0 mL三、四价钒电解液中加入已知浓度的稀盐酸,用浓度为0.102 2mol/L标准硝酸银直接测定,测定的氯离子加标回收率见表1。
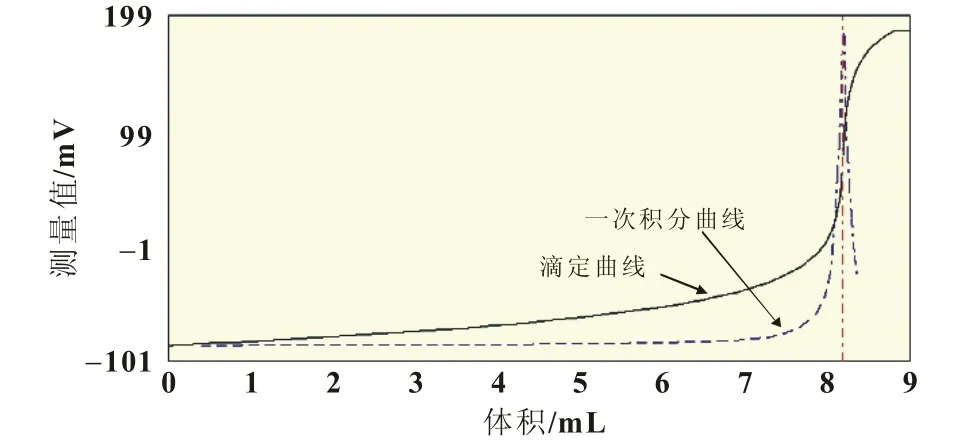
图1 含氯离子三价钒电解液滴定曲线

图2 含氯离子四价钒电解液滴定曲线
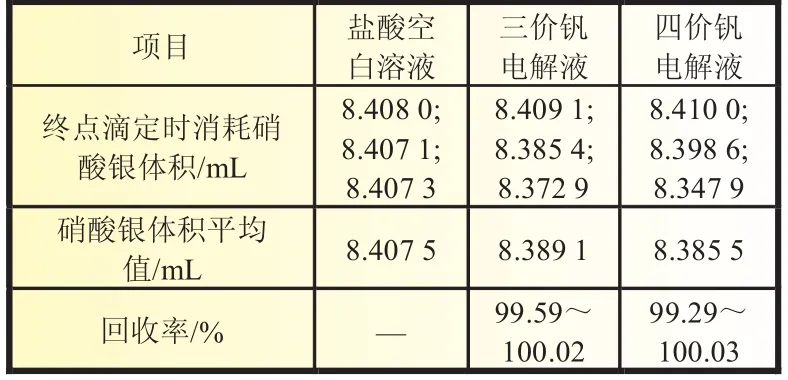
表1 三、四价钒电解液中氯离子加标回收率
由表1可知,加入盐酸后,三、四价钒电解液中氯离子回收率在99.29%~100.03%之间,三次测量的重现性较好,三、四价钒离子不会对测定造成干扰,可以直接用硝酸银溶液测定三、四价钒电解液中氯离子含量。
2.1.2 二价钒离子的影响
取含氯离子的二价钒电解液,加水稀释至50 mL,直接用硝酸银标准溶液滴定,随着滴定剂的加入,溶液中出现大量沉淀,银复合电极测得的滴定图形如图3所示。
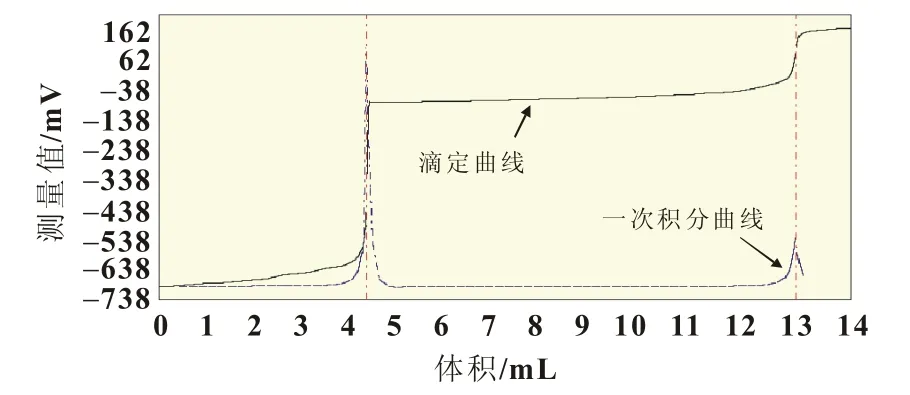
图3 含氯离子二价钒电解液滴定曲线
由图3可知,用硝酸银滴定含氯离子的二价钒电解液,滴定图上出现两个体积不同的电位突跃,表明滴定过程发生了两次氧化还原反应。取不含氯离子的二价钒电解液及稀盐酸溶液,分别用硝酸银直接滴定,滴定图形如图4、图5所示。
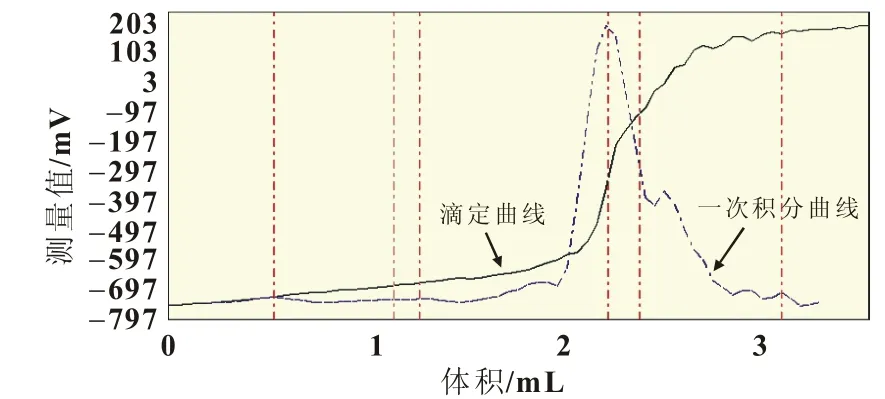
图4 不含氯离子的二价钒电解液滴定曲线
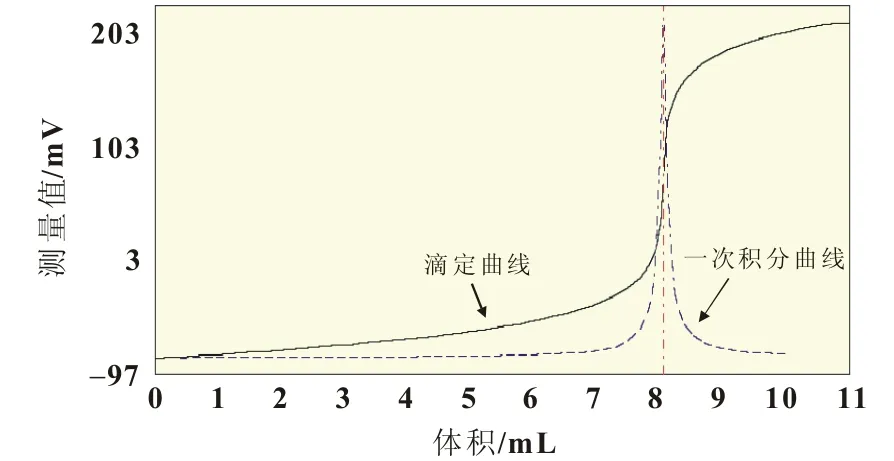
图5 硝酸银滴定盐酸溶液滴定曲线
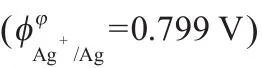
2.1.3 五价钒离子的影响
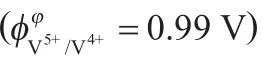
2.2 钒离子浓度的影响
测定二价钒电解液和五价钒电解液中的氯离子含量时,利用不同价态钒离子具有的氧化还原性能,分别加入不含氯离子的正、负极钒电解液,将强还原性的二价钒离子和强氧化性的五价钒离子氧化还原成三、四价钒离子后,再用硝酸银标准溶液测定钒电解液中的氯离子含量。为研究加入的钒离子浓度对氯离子测定的影响,取不同体积不含氯离子的三、四钒电解液,加入浓度为0.119 7mol/L的盐酸溶液10 mL,用浓度为0.102 2mol/L标准硝酸银按实验方法测定,实验结果见表2。

表2 不同体积的钒电解液中氯离子加标回收率
由表2可知,待测钒电解液取样体积为0.5~2.0 mL时,氯离子回收率几乎不受取样钒电解液体积的影响,钒电解液取样体积为5 mL时,氯离子回收率小于98.00%,因为氯化银沉淀颗粒具有很强的吸附性,随着钒电解液取样体积变大,待测溶液中钒离子浓度相应升高,大量的钒离子就会吸附在氯化银沉淀表面,影响银电极对沉淀终点的判断。目前使用的钒电解液浓度为1.0~2.0mol/L,为避免大量的钒离子干扰测定及节省标准溶液,测试过程中,钒电解液体积取样量1.0~2.0 mL即可。
2.3 pH值的影响
溶液中3.0≤pH≤7.0,四种价态的钒离子都可能与碱反应形成不同的沉淀,影响银电极对AgCl沉淀的判断,同时pH值过大,Ag+与OH-会生成AgOH沉淀,随即又析出黑色Ag2O沉淀,即:

AgOH见光进一步分解为:
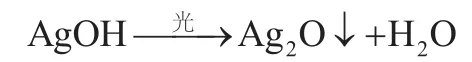
钒电解液酸度在2.0~4.0mol/L,取1.0 mL钒电解液稀释至50 mL时,测量杯中H+含量为0.08~0.16mol/L,测量体系pH<2.0,所以测量过程无需再调溶液酸碱度。
2.4 钒电解液中Cl-测量结果及回收率
取不同充放电状态含氯离子的钒电解液,按实验方法测定5次平行测定值的标准偏差及加入浓度为0.119 7mol/L的盐酸溶液20 mL,用浓度为0.102 2mol/L标准硝酸银测定的回收率见表3,含氯离子的不同价态钒电解液中,五次测量标准偏差小于0.030 1mol/L,加入盐酸后的氯离子回收率98.83%~101.40%。

表3 钒电解液中Cl-测量结果及回收率
3 结论
将DSC140-SC氧化还原复合电极和DM141-SC银复合电极结合使用,在电位滴定仪上测定钒电解液中氯离子含量,三、四价钒既不与电极发生反应,也不影响滴定过程,可以直接测定。利用不同价态的钒电解液自身的氧化还原特性,将能与Ag电极发生氧化反应的五价钒离子、与Ag+发生还原反应的二价钒离子转化为可直接测定的三、四价钒离子后再测量,减少了其他实验试剂进入测量体系可能带来的误差。浓度≤2.0mol/L,取样体积0.5~2 mL的钒电解液中钒离子浓度不影响氯离子含量测定。用银电极法测定氯离子含量很高的钒电解液,具有操作简单、实验时间短、易于掌握等优点,适合大批量的钒电解液的现场充放电过程氯离子含量监控。该方法准确性好、精密度高,回收率为98.83%~101.40%,<0.030 1mol/L。
[1]CHANG F,HU C W,LIU X J,et al.Coulter dispersant as positive electrolyte additive for the vanadium redox flow battery[J]. Electrochim Acta,2012,60:334-338.
[2]JOERISSEN L,GARCHE J,FABJAN C.Possible use of vanadium redox-flow batteries for energy storage in small grids and stand-alone photovoltaic systems[J].J Power Sources,2004,127: 98.
[3]ZHAO P,ZHANG H M,ZHOU H,et al.Characteristics and performance of 10 kW class all-vanadium redox-flow battery stack[J]. J Power Sources,2006,162:1416.
[4]RAHMAN F,SKYLLAS-KAZACOS M.Vanadium redox battery: positive half-cell electrolyte studies[J].J Power Sources,2009,189:1212.
[5]化学工业部化学试剂标准化技术归口单位,化学工业部化学试剂质量监测中心.化学试剂标准大全[M].北京:化学工业出版社,1995:62-63.
[6]中科院青海盐湖所分析室.卤水和盐的分析方法[M].2版.北京:科学出版社,1993:61-64.
[7]KAUSAR N,HOWE R,SKYLLAS-KAZACOS M,et al.Raman spectroscopy studies of concentrated vanadium redox battery positive electrolytes[J].J Appl Electrochem,2001,31:1327-1332.
Study on determination of chloride ions in electrolyte of vanadium redox batteries
The content of chloride ions in vanadium electrolyte was determined by combination of redox electrode and composite sliver electrode.The results indicate V3+and V4+neither react with electrode nor influence the process of titration.According to the self redox property of vanadium with different valences,V5+and V2+could be transformed into V3+and V4+byreacting with Ag and Ag+respecttively.Therefore,transforming V5+and V2+into V3+and V4+before determination could reduce the error caused by other reagents. The determination of chloride ions would not be influenced when the concentration of vanadium ions was less than 2.0mol/L and sample volume was 0.5-2 mL.The recovery of the sample is 98.83%-101.40%,and RSDs is less than 0.030 1mol/L.The results show that this method is fast,accurate and has good precious and accuracy,and can be successfully applied to on-line determining the content of chloride ions in large quantities of vanadium electrolyte.
vanadium electrolyte;chloride ion;content determination;potentiomereic titration
TM 912.9
A
1002-087 X(2016)04-0803-04

2015-09-05
常芳(1974—),女,甘肃省人,高级工程师,主要研究方向为钒电池及电源材料。

