湿法消解
—氢化物原子荧光光谱法同时测定土壤中砷和硒
陈磊磊 , 余长合 , 袁锡泰
(河南省地质矿产勘查开发局 第一地质环境调查院 , 河南 郑州 450045)
湿法消解
—氢化物原子荧光光谱法同时测定土壤中砷和硒
陈磊磊 , 余长合 , 袁锡泰
(河南省地质矿产勘查开发局 第一地质环境调查院 , 河南 郑州450045)
摘要:建立(HNO3-HClO4-HCl)混合酸湿法消解—氢化物原子荧光光谱法同时测定土壤样品中砷和硒的方法。实验优化了消解条件及仪器测定条件,并对4种土壤成分分析标准物质进行准确度和加标回收试验。结果显示,砷和硒的检出限分别为3.3、1.3 μg/kg,加标回收率分别为94.6%~105%、91%~109%,该方法可用于大批量土壤样品中砷和硒的同时测定。
关键词:土壤 ; 砷 ; 硒 ; 湿法消解 ; 原子荧光光谱法
0前言
砷在土壤中的累积,不仅影响动植物的生长发育,危害土壤微生物的种类和数量,而且还可以通过食物链进入人体,对人类的生命健康造成威胁[1]。人体蓄积过量的硒会中毒[2]。人体主要从食物中获得硒营养,植物中的硒主要来源于土壤[3]。因此,准确分析监测土壤中砷、硒的含量对人体健康和环境保护有至关重要的作用。
目前,土壤中砷、硒含量的测定方法很多,但同时测定这两种元素的方法主要包括氢化物发生—原子荧光光谱法(HG-AFS)、电感耦合等离子体发射光谱法(ICP)和电感耦合等离子质谱法(ICP-MS)三种[4-6]。其中,ICP和ICP-MS两种技术均因仪器造价高,对实验室条件和专业技术人员要求较高而未能在基层检测机构得到广泛应用[7]。HG-AFS技术具有分析灵敏度高、干扰少、线性范围宽、可多元素同时分析、操作相对简单等优点,是一种优良的痕量分析技术。因此,采用HG-AFS技术测定环境样品中的砷、硒成为国内众多分析测试实验室的常规测试技术[8-10]。
本文以HNO3-HClO4-HCl混合酸为消解液体系对土壤进行湿法消解,采用HG-AFS技术进行分析检测,旨在建立一种快速、准确且能同时测定土壤中砷、硒含量的方法。
1实验部分
1.1仪器与试剂
AFS-3100双道原子荧光光度计,北京海光仪器有限公司。砷、硒原子荧光空心阴极灯,北京有色金属研究总院。
砷标准储备液(100 μg/mL):称取0.132 0 g经过105 ℃干燥2 h的As2O3置于50 mL烧杯中,加入10 mL NaOH(40 g/L)溶液使之溶解,加入5 mL盐酸,转入至1 000 mL容量瓶中,用高纯水洗涤烧杯并定容至刻度,摇匀备用。
硒标准储备液(100 μg/mL):称取0.100 0 g硒粉(光谱纯)置于50 mL烧杯中,溶于少量硝酸中,加入2 mL高氯酸,置沸水浴中加热3~4 h,冷却后再加入8.4 mL盐酸,再置于沸水浴中2 min,冷却后转移至1 000 mL容量瓶中,并用高纯水定容,摇匀后备用。
土壤成分分析标准物质:GBW07402(GSS-2),GBW07403(GSS-3),GBW07404(GSS-4),GBW07407(GSS-7),地球物理化学勘查研究所。
(1+1)(体积比)浓盐酸+水溶液,(1+1)(体积比)硝酸—高氯酸混合液;10%硫脲—10%抗坏血酸混合液:10.0 g硫脲加热溶解于少量高纯水中,再加入10.0 g抗坏血酸,搅拌溶解,冷却转移至100 mL容量瓶中,定容,摇匀备用。
载流:5%(体积比)盐酸溶液
硼氢化钾溶液(20 g/L):氢氧化钾5.0 g,硼氢化钾20.0 g,溶于1 000 mL水中,现配现用。
实验所用试剂均为优级纯,所用玻璃器皿均在(1+1)硝酸浸泡24 h后冲洗干净,备用。
实验用水为高纯水,电阻率达到18.20 MΩ·cm,北京普析通用仪器有限公司。
1.2土壤样品前处理
将新鲜土样置于50 ℃恒温干燥箱中8 h烘干,冷却后,采用四分法分别量取适量样品后,粉碎,通过0.149 mm孔径筛,混匀后用塑料袋盛装,密封并保存。
称取风干、过筛的土壤样品0.1~0.5 g(精确至0.000 1 g),置于50 mL溶样杯中,加入(1+1)硝酸—高氯酸混合液10~15 mL,盖上小表面皿,静置过夜。然后置于160 ℃自动控温电热板上消化至无色(土样成灰白色),继续消化至冒白烟后,取下稍冷,加入适量(1+1)盐酸溶液,置于沸水浴中加热一定时间,取下冷却至室温。
将玻璃小漏斗插于50 mL容量瓶中,用慢速定量滤纸将消解液过滤,用高纯水洗涤,将洗涤液一并转移至容量瓶中,定容、摇匀、待测。以相同操作步骤制备2~3个全程序空白样品。
1.3标准曲线绘制及土壤样品的测定
对砷、硒标准储备液进行逐级稀释,分别稀释至1.0、0.1 μg/mL,作为标准使用液。分别吸取砷标准使用液0、0.1、0.2、0.5、0.8、1.0 mL,硒标准使用液0、0.2、0.5、1.0、2.0、3.0 mL置于10 mL比色管中,用高纯水定容至刻度。加入2.0 mL(1+1)浓盐酸+水溶液,适量10%硫脲—10%抗坏血酸混合液,摇匀,室温静置30 min后进行测定。砷、硒标准系列的浓度如表1所示。

表1 砷、硒标准系列浓度
分取10 mL土壤消解液及空白溶液,置于10 mL比色管中,加入2.0 mL(1+1)浓盐酸+水溶液,适量10%硫脲—10%抗坏血酸混合液,摇匀,室温静置30 min后进行测定。
1.4仪器工作条件
经优化实验选择的砷、硒仪器分析参数如表2所示。
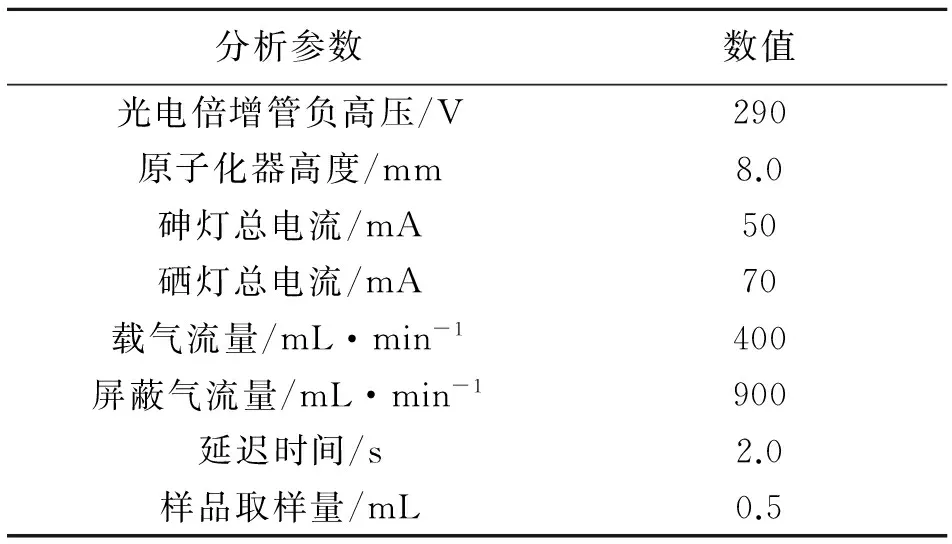
表2 砷、硒仪器分析参数
2结果与讨论
2.1(1+1)硝酸—高氯酸混合酸体积的选择
准确称取0.5 g(精确到0.000 1 g)GBW07407(GSS-7)土壤标样三组置于50 mL溶样杯中,加入溶样杯消解液的体积分别选择5、10、15 mL,进行消解。每组土壤样品均进行三次平行消解。测定同标准曲线的测定方法,每组土壤样品均测定三次,最终结果取3个平行样的平均值。砷、硒测定值随加入(1+1)硝酸—高氯酸体积的变化,如表3所示。
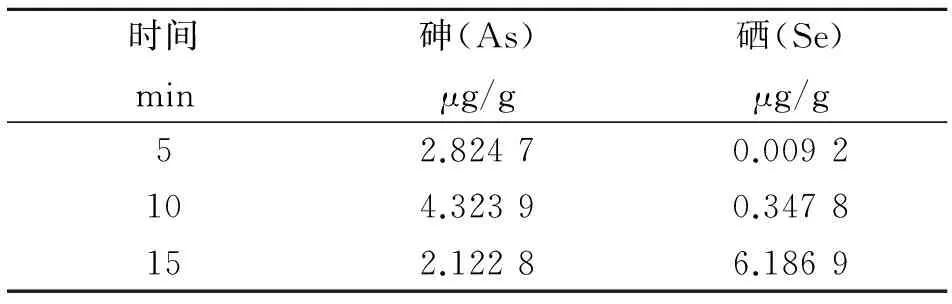
表3 (1+1)硝酸—高氯酸混合酸体积对As、Se测定值的影响
由表3可知,随着(1+1)硝酸—高氯酸体积的增加,砷元素测定浓度呈现先增加后明显降低的趋势,硒含量却呈现了先缓增后骤增的现象,加入体积为10 mL时,砷、硒测定结果分别为4.323 9 μg/g和0.347 8 μg/g,标准值为4.8 μg/g±1.3 μg/g和0.32 μg/g±0.05 μg/g,在标准误差允许范围内。实验选择10 mL(1+1)硝酸—高氯酸作为加入消解液体积。
2.2(1+1)浓盐酸+水体积的选择
土壤样品经过混合酸消解后,需要加入盐酸将Se6+还原化成Se4+,此过程需在沸水浴中进行[11]。实验准确称取0.500 0 g GBW07407(GSS-7)土壤标样三组,消解冷却后,(1+1)浓盐酸+水的体积选择5、10、15 mL分别加入到3个平行溶样杯中,置于沸水浴中继续反应一段时间。冷却后,过滤,洗涤并定容,进行测定。砷、硒测定值随加入(1+1)浓盐酸+水体积的变化,如表4所示。
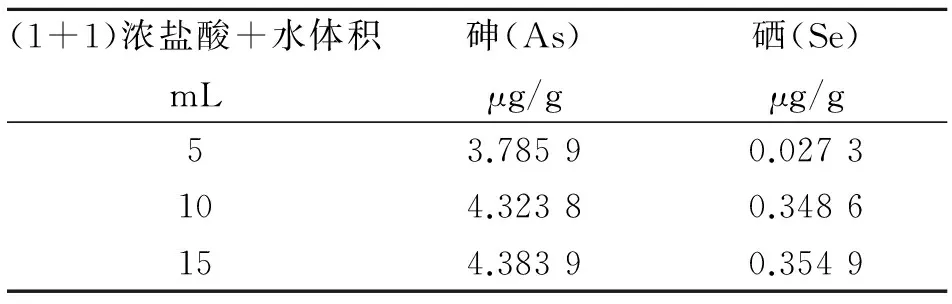
表4 (1+1)盐酸体积对As、Se测定值的影响
由表4可知,(1+1)浓盐酸+水体积的变化对砷和硒两种元素测定结果的影响基本相同。随着(1+1)浓盐酸+水加入体积的增加,砷和硒的测定值均呈现了逐渐增大而后基本稳定不变的状态。加入10 mL时,砷和硒两种元素的测定值分别为4.323 8 μg/g和0.348 6 μg/g,测定值在标准值的误差允许范围内。因此,实验选择加入10 mL(1+1)浓盐酸+水。
2.3沸水浴中反应时间选择
消解液中加入(1+1)浓盐酸+水,并置于沸水浴可将溶液中Se6+还原化成Se4+。实验准确称取0.500 0 g GBW07407(GSS-7)土壤标样三组,消解,冷却,然后置于沸水浴中继续反应,反应时间选择0、5、10、15、20 min。冷却后,过滤,洗涤并定容,进行测定。砷、硒测定值随沸水浴中反应时间不同的变化,如表5所示。
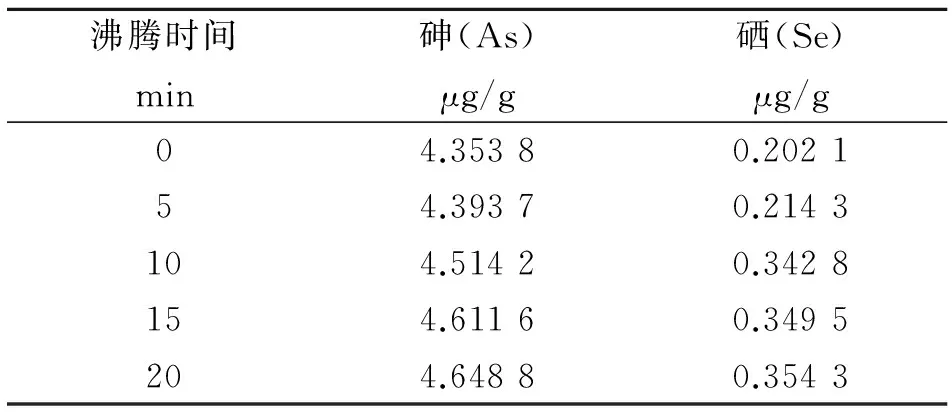
表5 沸水浴中反应时间对As、Se测定值的影响
由表5可知,沸水浴中的时间会明显影响到土壤中硒含量的测定,也会对砷的测定值产生一定的影响。随着沸水浴中反应时间的增加,消解液中的砷、硒测定值均呈现先升高后趋于稳定的状态。置于沸水浴的时间>15 min时,砷、硒测定值基本不随时间而发生变化;沸水浴中反应时间为15 min时,砷、硒含量的测定值分别为4.611 6、0.349 5 μg/g,在标准值的允许误差范围内。因此,实验选择消解液在沸水浴中反应时间为15 min。
2.410%硫脲—10%抗坏血酸混合液体积选择
样品测定过程中加入硫脲—抗坏血酸混合液,可以将标样中的As5+转化成As3+,对硒含量测定的影响还不明确[13]。实验准确称取0.500 0 g GBW07407(GSS-7)土壤样品3个分别置于50 mL溶样杯中,均加入10 mL(1+1)硝酸—高氯酸混合酸后,置于160 ℃自动控温电热板上消解。取下冷却后,加入10 mL(1+1)盐酸置于沸水浴中继续反应15 min。冷却后过滤,将滤液转移至50 mL容量瓶中,并洗涤定容,进行测定。
每个消解液中取10 mL分别置于4个50 mL容量瓶中,均加入2 mL(1+1)浓盐酸+水,每个消解液分别置于4个容量瓶中,加入1、2、3、4 mL10%硫脲—10%抗坏血酸混合液,用纯水定容至标线,混匀,室温静置30 min后测定。消解液中砷、硒测定值随着加入硫脲—抗坏血酸混合液体积变化而呈现的变化,如表6所示。

表6 10%硫脲—10%抗坏血酸混合液对As、Se测定值的影响
由表6可知,硫脲—抗坏血酸混合液的加入量对硒的测定结果影响基本可以忽略,砷的测定值却发生明显的变化。随着混合酸体积的增加,砷的测定值逐渐升高而后趋于恒定,在10%硫脲—10%抗坏血酸混合液加入体积为3 mL时,消解液中砷的测定值为4.732 9 μg/g,硒的测定值也基本上稳定在0.361 4 μg/g,均在标准值误差允许范围内。因此,本实验选择加入硫脲—抗坏血酸体积为3 mL。
2.5标准曲线及检出限
在优化的消解条件及测量条件下,根据仪器设定的检出限测定程序,对空白溶液进行11次平行测定,并继续测定标准系列。结果显示砷、硒分别在0~100 μg/L和0~10 μg/L范围内具有良好的线性关系。按土壤取样量0.500 0 g,最后定容至50 mL,计算砷、硒的检出限。其线性方程、相关系数及检出限见表7。
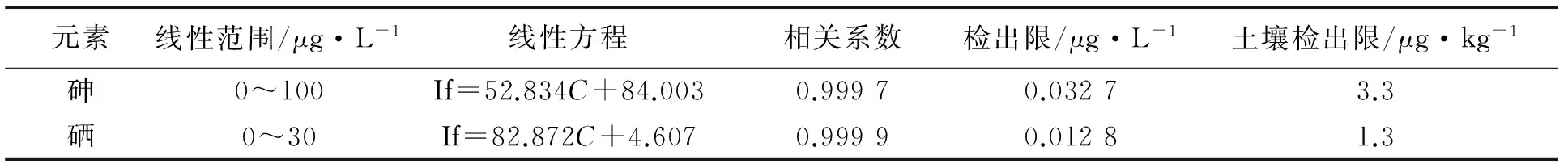
表7 砷、硒线性方程、相关系数及检出限
2.6标准样品分析及加标回收实验
对GBW07402(GSS-2),GBW07403(GSS-3),GBW07404(GSS-4),GBW07407(GSS-7)4个土壤标准样品进行消解并平行测定6次,同时加入砷、硒标准溶液测定其加标回收率。结果如表8所示。
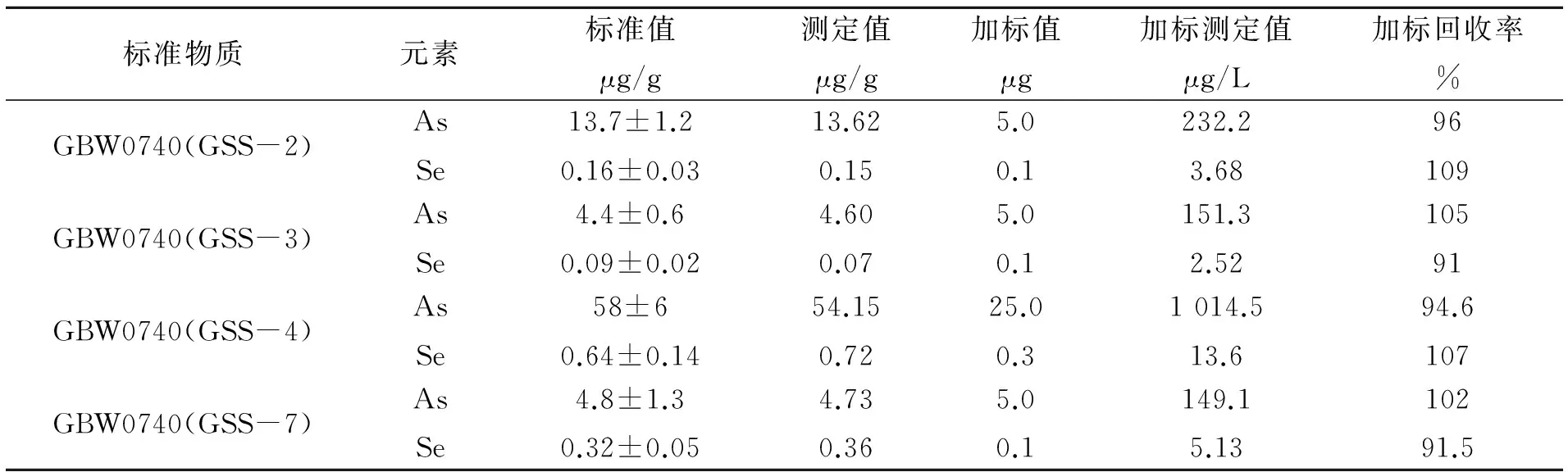
表8 土壤标准物质分析结果及加标回收试验
由表8可知,在优化的条件下标准物质的测定值均在标准值的误差范围内,砷、硒的加标回收率分别为94.6%~105%、91%~109%。由此可见,该方法准确度高,可以满足土壤中砷和硒的同时测定。
3结论
采用HNO3-HClO4-HCl混合酸为消解液体系对土壤进行湿法消解,氢化物原子荧光光谱法(HG-AFS)同时测定砷和硒的含量。在优化的消解条件和测量条件下,该方法具有良好的线性及较低的检出限,准确度高、稳定性好、干扰少、操作相对简单,可广泛应用于一般检测实验室大批量土壤样品中砷和硒的同时检测。
参考文献:
[1]张立萍.砷污染土壤的稳定化修复研究[D].华中科技大学,2013.
[2]唐兴敏,陈萍.微波消解—原子荧光光谱法测定植物样中砷汞硒[J].资源环境与工程,2013,27(2):222-225.
[3]王兆双.土壤有效硒提取方法比较及其生物有效性研究[D].华中农业大学,2014.
[4]秦海波,朱建明,李社红,等.高压密闭罐溶样—氢化物原子荧光法测定环境样品中的砷[J].矿物学报,2010,30(3): 398-401.
[5]朱建明,李璐,秦海波,等.高压密闭罐溶样—氢化物原子荧光法测定环境样品中的硒[J].矿物学报,2008, 28: 187-190.
[6]贺与平,李维平,何素芳,等.氢化物发生原子荧光光谱法测定螺旋藻中无机硒和有机硒[J].光谱实验室,2009, 26(6): 1404-1408.
[7]祖文川,武彦文,孙畅,等.微波消解—双道原子荧光光谱法同时测定茶叶中砷和硒[J].现代科学仪器,2010,3(6): 53-55.
[8]于兆水,陈海杰,张勤.氢化物发生—原子荧光光谱法对环境水样中砷(Ⅲ)与砷(Ⅴ)的直接测定[J].分析测试学报,2009,28(2): 216-219.
[9]秦海波,朱建明,李社红,等. 高压密闭罐溶样—氢化物原子荧光法测定环境样品中的砷[J].矿物学报,2010, 30(3): 398-402.
[10]凤海元,时晓露,黄勤.微波消解—氢化物发生原子荧光光谱法测定茶园土壤中的砷[J].岩矿测试,2013, 32(1): 53-57.
[11]陶秋丽,韩张雄,熊英,等.微波消解—氢化物发生原子荧光光谱法测定粉煤灰中的硒[J].岩矿测试,2013,32(3): 445-448.
[12]杨力,徐晓宇,戴晖.氢化物原子荧光法测定废水中砷和硒[J].广东化工,2010,37(12): 135-136.

收稿日期:2016-03-26
作者简介:陈磊磊(1986-),女,助理工程师,从事环境样品分析检测的研究,电话:18339991032。
中图分类号:O657.34
文献标识码:B
文章编号:1003-3467(2016)06-0050-04

