NaCl对齿肋赤藓叶肉细胞超微结构的影响
刘卫国,丁俊祥, 邹 杰, 林 喆,唐立松
1 新疆大学资源与环境科学学院, 绿洲生态重点实验室, 乌鲁木齐 830046 2 中国科学院新疆生态与地理研究所, 荒漠与绿洲生态国家重点实验室, 乌鲁木齐 830011 3 中国科学院大学, 北京 100049 4 中国科学院阜康荒漠生态系统研究站, 阜康 831505
NaCl对齿肋赤藓叶肉细胞超微结构的影响
刘卫国1,*,丁俊祥1,2,3,4, 邹杰1, 林喆1,唐立松2,4
1 新疆大学资源与环境科学学院, 绿洲生态重点实验室, 乌鲁木齐830046 2 中国科学院新疆生态与地理研究所, 荒漠与绿洲生态国家重点实验室, 乌鲁木齐830011 3 中国科学院大学, 北京100049 4 中国科学院阜康荒漠生态系统研究站, 阜康831505
摘要:齿肋赤藓(Syntrichia caninervis)是古尔班通古特沙漠苔藓结皮层中的优势物种,对荒漠生态系统的稳定性及功能多样性具有十分重要的意义。利用透射电镜技术对不同浓度NaCl胁迫下齿肋赤藓叶肉细胞超微结构进行了观察。结果表明:齿肋赤藓叶肉细胞在未胁迫(0 mmol/L)处理下排列疏松,各种细胞结构完整,叶绿体基质排列均匀且叶绿体内含少量淀粉粒和脂质球。在轻度盐NaCl胁迫(100 mmol/L)下,齿肋赤藓叶肉细胞结构依然保持完整,叶绿体基质均匀,叶肉细胞超微结构仅有较小变化。在中度盐NaCl胁迫(200、300 mmol/L)下,齿肋赤藓叶肉细胞发生质壁分离,出现晶体结构,且中央大液泡发生破裂;叶绿体由梭形变成椭球形或圆球状,出现空泡化并伴随有轻微的解体;叶绿体类囊体肿胀,脂质球数量增加。在高度NaCl胁迫(400、500 mmol/L)下,齿肋赤藓细胞的质壁分离加剧,叶肉细胞出现大量泡状结构和膜片层,叶肉细胞死亡;叶绿体片层结构消失,空泡化加重,脂质球数量增加且体积变大,叶绿体内外膜消失,叶绿体大部分解体,在叶肉细胞中几乎看不到叶绿体的存在。上述结果表明,叶绿体膜结构的损伤与盐胁迫下叶肉细胞死亡有密切关系。
关键词:齿肋赤藓;NaCl胁迫;叶肉细胞;超微结构
生物结皮是由隐花植物如蓝藻、荒漠藻、地衣、苔藓类和土壤微生物与表层土壤颗粒胶结而形成的十分复杂的复合体,是干旱、半干旱地区生态系统的重要组成部分。在维管束植物分布稀疏的干旱区,生物结皮是地表主要的生物覆盖层,在土壤稳定性、固氮、土壤肥力以及水分循环等方面起着重要作用[1]。在干旱区生态系统中,盐分同水分一样对生物的生长、发育、分布以及生理生态过程等都具有重要的影响[2]。生物结皮对盐分具有一定的忍耐特性。耐盐性是一种综合性状表现,不同种类生物结皮由于耐盐方式和机理的不同,其组织或细胞内的生理生化变化也不同[2- 3]。
苔藓植物具有很强的耐旱能力,因此以往的研究多集中于探讨其耐旱特性和机理,如苔藓植物在抗旱过程中的形态变异[4- 5]、生理生化机制[6- 7]、繁殖方式[8- 9]等。在荒漠地表,高蒸发量和有限的降水是造成苔藓生物结皮遭受盐胁迫的重要原因,研究区地表土壤的高盐度是影响该苔藓生存的重要环境因子之一。同水分胁迫一样,盐胁迫也是干旱区植物经常遭受的胁迫形式。有关植物细胞超微结构响应和适应盐胁迫的研究已有很多,如韦存虚、徐威等[10,11]研究了NaCl胁迫对白三叶叶片超微结构的影响,Shu等[12]观察了盐胁迫对黄瓜的超微结构的影响,Elkahoui等[13]分析了长春花细胞在生理和超微结构方面对盐胁迫的响应,Queirós、Gao等[14- 15]研究了NaCl对马铃薯的超微结构及生理特性的影响。然而,目前从细胞超微结构探讨盐分胁迫对苔藓生物结皮影响的研究仍不多见。
细胞超微结构(细胞器)是植物一系列生理活动异常的细胞学基础。有研究表明,经一段时间盐处理后,植物叶肉细胞内出现空腔、淀粉粒,类囊体与叶绿体膜扭曲[11],叶绿体变形或外膜逐渐断裂解体、核膜模糊,线粒体损伤,内外膜界限不清[13-20],表皮和皮层细胞中液泡数量增加等一系列不同程度的歧变[11,20]。那么,在不同浓度盐胁迫下苔藓生物结皮叶肉细胞超微结构将会发生什么样的变化?为此,本研究选取藓类结皮层中的优势物种——齿肋赤藓(Syntrichiacaninervis)为实验材料。通过电镜照射成像,从亚细胞水平观察齿肋赤藓在不同NaCl浓度(0、100、200、300、400、500 mmol/L)处理下细胞超微结构的变化,以期探究齿肋赤藓生物结皮叶肉细胞可能的盐分积累位点,从而为苔藓生物结皮在盐分胁迫下出现的生理变化和耐盐性提供初步的实验依据, 也为今后对该苔藓生物结皮进行更多的应用研究和开发提供一些基础性的资料。
1材料与方法
1.1供试材料
2014年 5月于古尔班通古特沙漠南缘腹地,选取未受任何干扰、生长良好且长势一致的齿肋赤藓生物结皮作为实验对象。采用水湿法取回后立即进行消毒处理,然后置于培养箱(温度为(20±0.5) ℃)培养1周。从中挑选高约0.6—0.8 cm的齿肋赤藓生物结皮,使之以单株形式存在。每25株整合为1个样本置于培养皿,根据当地齿肋赤藓生物结皮生长特性,选用浓度为0、100、200、300、400、500 mmol/L NaCl溶液进行处理,每组处理5次重复。每次定时处理前,先将样本移入已消毒的新培养皿中,然后进行盐溶液处理。同时,仔细观察样本的长势及变化情况,待培养至第7天时,在每个盐分处理下选取3—5株长势一致样本用于电镜样品的制备。
1.2样品制备与观察
将齿肋赤藓生物结皮植株下半部切除,保留顶部1—2 mm2立刻投入4%戊二醛溶液中固定,随后用磷酸缓冲液(pH为7.2的PBS)洗涤,再以1%的锇酸固定1.5h,分别用浓度梯度为30%、50%、70%、80%、90%、95%、100%的乙醇逐级脱水。随后,用比值为1∶1和4∶1的丙酮和酒精依次浸泡半个小时,纯丙酮浸泡过渡,并用比值为1∶1的环氧树脂和丙酮浸泡1h,比值为4∶1的环氧树脂与丙酮浸泡3h,纯环氧树脂浸泡12h后用Epon- 812渗透包埋。在恒温恒湿箱中按等梯度温度加温至60 ℃,然后放置12个h。借助LKB型超薄切片机切片,切片经醋酸铀-柠檬酸铅双重染色,随后采用EM- 1200EX透射电子显微镜观察照相。
2实验结果
2.1齿肋赤藓超微结构变化
2.1.1齿肋赤藓叶肉细胞壁变化
齿肋赤藓生物结皮的叶肉细胞壁在小于100 mmol/L NaCl胁迫下结构完整饱满,相邻细胞壁间界限分明,细胞壁与原生质清晰可见。在100 mmol/L NaCl胁迫下,细胞壁出现轻微的质壁分离现象(图1-A)。在200 mmol/L NaCl胁迫下,细胞壁结构完整,表面现凹凸不平现象;由于细胞外Na+含量增多,细胞失水,而出现明显的质壁分离现象,但细胞壁间界限仍较分明,细胞壁与原生质体间界限依旧清晰可见。细胞壁完整,细胞膜清晰可见,箭头所指方向为发生质壁分离的现象(图1-B);出现明显质壁分离现象,如箭头所指方向(图2-S)。在300 mmol/L NaCl胁迫下,细胞壁结构完整,内侧出现轻微模糊现象,质壁分离现象已加剧,细胞壁间界限出现模糊,细胞壁与原生质体的界限同样清晰可见(图1-C, 图2-T)。在400 mmol/LNaCl胁迫下,细胞壁结构仍完整,内侧模糊现象稍有加重,质壁分离现象进一步加剧,相邻细胞壁间界限模糊不分明,但细胞壁与原生质体间界限仍清晰可辨(图1-D, 图2-W)。当浓度为500 mmol/L NaCl胁迫时,细胞壁结构仍完整,在与0—100 mmol/L NaCl浓度时相比,细胞壁轮廓已不饱满,内侧模糊,细胞壁间的界限不清晰。这都表征,齿肋赤藓生物结皮在高浓度盐胁迫下出现严重的质壁分离现象,细胞质遭到严重损害,细胞壁与原生质体间的界限部分模糊不清(图1-E,图2-Y)。
2.1.2齿肋赤藓叶肉细胞叶绿体变化
在0—100 mmol/L NaCl处理下,齿肋赤藓叶肉细胞的叶绿体呈梭型,结构规则完整,轮廓清晰,具双层被膜,分布在细胞边缘;类囊体腔小且扁平,基粒间有基质片层相连,基粒片层与基质片层结构完整、层次清晰、排列紧密、排列方向与叶绿体长轴基本平行,基质均匀,发育良好,并在叶绿体中发现淀粉粒,细胞质和叶绿体中发现少量的圆形颗粒物(图3-F, G)。当胁迫浓度为200 mmol/L NaCl时,叶绿体双层膜开始有轻微的损坏,叶绿体中的基质片层结构开始出现模糊、松散、排列紊乱;同时,基粒片层和基质片层减少,且表现一定的扭曲,基质片层结构也开始模糊,开始出现类囊体空泡化,叶绿体内已有较多的圆形颗粒物(图3-H)。浓度增加到300 mmol/L NaCl时,部分叶绿体双层膜有被破坏现象,且基粒片层和基质片层结构模糊不清,只见一些松散的基粒片层结构,叶绿体开始膨胀,内部出现空洞,空泡化程度达到20%—30%,叶绿体向细胞质中间分布,其内部积累较多的圆形颗粒 (图3-I, J)。当浓度达到400 mmol/L NaCl时,叶绿体被膜破坏严重,并出现断裂和解体,片层有一定扭曲,基质片层结构开始模糊,排列紊乱,叶绿体膨胀严重,空泡化程度高达40%—60%,积累了大量的圆形颗粒(图3-K, L)。在500 mmol/L NaCl胁迫下,叶绿体膜完全破裂,叶绿体内含物质外溢,类囊体、基粒和基质片层结构完全消失,大量的圆形颗粒出现(图3-M)。
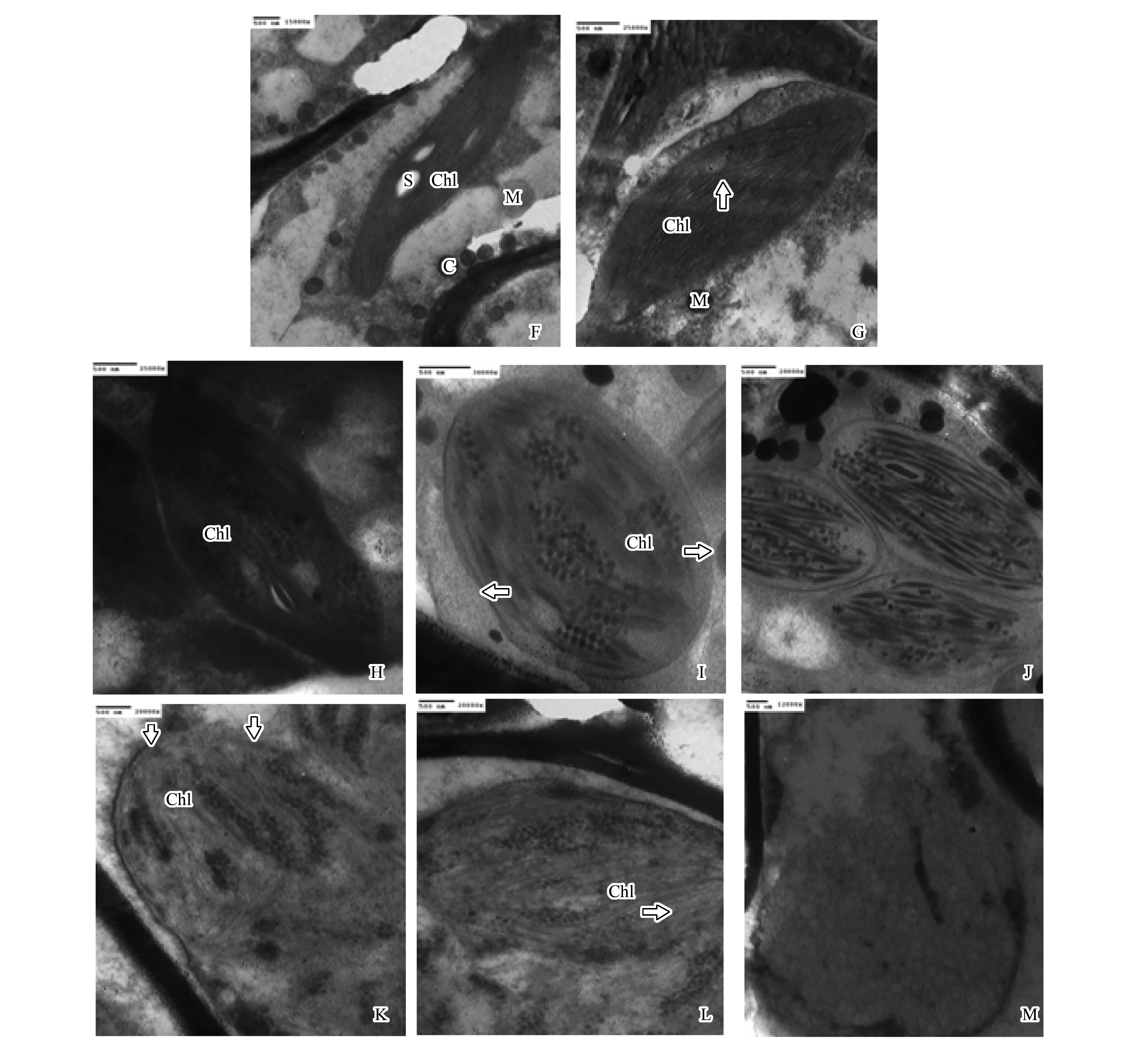
图3 不同盐浓度下苔藓叶肉细胞叶绿体超微结构变化Fig.3 The ultrastructural changes of chloroplast in Moss biologic crust under different concentrations of NaCl
2.1.3齿肋赤藓叶肉细胞核的变化
在0—100 mmol/L NaCl处理下,齿肋赤藓叶肉细胞核为圆形,核膜清晰可见,核仁位于细胞核中央(图2-N, Q)。伴随浓度增加为200 mmol/L NaCl时,细胞核膜开始蜷曲变形、凹凸不平、呈椭圆形、核仁已遭到破坏,并向细胞外侧移动,出现染色质外溢、核质减少等现象(图2-R)。在300 mmol/L NaCl胁迫下,细胞核膜边缘模糊,核仁移至细胞核边缘,核仁模糊甚至消失,核质严重外溢(图2-T),且细胞质中有圆形颗粒沉淀(图2-U);当浓度增加到 400 mmol/LNaCl时,出现严重质壁分离现象(图2-W);此时,部分细胞膜出现解体,如箭头所指(图2-X);在 500 mmol/LNaCl浓度时,齿肋赤藓叶肉细胞核已经萎缩、破裂解体(图2-Y)。总体,随着NaCl浓度的增加,细胞核由清晰可见的椭圆形逐渐变化为核膜边缘模糊,核仁移至细胞核边缘,核仁模糊甚至消失,核质严重外溢,最终细胞核破裂解体。
3讨论与结论
在低盐处理(小于100 mmol/L NaCl)下,齿肋赤藓叶肉细胞超微结构基本不受影响,这表明齿肋赤藓具有一定的耐盐性,能够在一定程度盐渍化土壤环境中生长。在中(200—300 mmol/L NaCl)、高(400—500 mmol/L NaCl)浓度的盐胁迫下,齿肋赤藓叶肉细胞均受到不同程度的胁迫伤害,尤以叶绿体和细胞核的表现最为突出。叶肉细胞中的叶绿体是感受盐胁迫最敏感细胞器。本研究中,在轻度盐分胁迫下,齿肋赤藓叶绿体能够维持其结构和膜的完整性;而随着盐分浓度增加,叶绿体开始出现不同程度的破坏,如叶绿体发生形变、膜结构出现断裂和解体、类囊体与基粒和基质片层发生变形等。这些结构的变化是细胞衰老、病变或严重胁迫情况下表现的普遍现象[21- 24]。此外,随着NaCl浓度的增加,齿肋赤藓叶绿体内出现大量的脂质球。脂质球的增加利于提高细胞质浓度、降低渗透势,确保水分和无机盐类营养的吸收,故脂质球的增多现象是齿肋赤藓耐盐性增强的标志之一,这在其它植物耐盐特性的研究中也得到了证实[25- 28]。据此本研究推测,齿肋赤藓生物结皮通过在细胞体内积累大量脂质球等能量物质来抵制胁迫伤害,而在环境适宜的条件下,齿肋赤藓又能将这些能量物质重新加以利用。这也许是苔藓、藻类和地衣生物结皮应对环境胁迫的重要保护机制之一。另外,当叶绿体内、外膜被破坏,其功能将完全尚失,而在内、外膜保持完整时,盐胁迫解除后,叶绿体仍能恢复其光合作用。叶绿体的完整与否决定了光合作用的进行,因此,保持其结构的完整性在植物生长中是必要的[16-18, 29]。本实验中,齿肋赤藓叶绿体膜在低于200 mmol/L NaCl浓度下有轻微的损坏,在更高浓度NaCl处理下叶绿体内、外膜才出现降解消失,这体现了齿肋赤藓在结构和功能特性方面对盐渍生境的适应。
本研究中,齿肋赤藓叶肉细胞在高浓度NaCl处理(300—500 mmol/L)下出现严重的质壁分离现象(图1-E,图2-Y)。在大于300 mmol/L NaCl处理下,细胞质遭到严重损害,细胞壁与原生质体的界限部分模糊不清;细胞核由清晰可见的椭圆形逐渐变化为核膜边缘模糊,并逐渐萎缩、破裂解体;核仁移至细胞核边缘,逐渐模糊甚至消失,核质严重外溢,出现细胞核破裂解体现象。这些变化将造成细胞膜系统不可逆的损伤,致使细胞正常的物质代谢、能量转换和信息传递无法顺利完成,导致细胞新陈代谢过程中断,使齿肋赤藓叶肉细胞生命活动趋于停止。因此,本研究认为可以通过观测盐胁迫条件下植物细胞的超微结构来筛选本土耐盐性苔藓类生物结皮。
叶肉细胞器对盐胁迫的敏感性和耐受性存在明显差异。本研究中,叶绿体对盐分胁迫最为敏感,其次是液泡和细胞核,细胞壁和内膜系统则对盐胁迫表现不敏感,对盐胁迫的耐受能力相对较强。较厚的细胞壁作为屏障,可限制Na和Cl进入原生质体中,从而保护细胞免遭金属离子的毒性[30- 33]。在低浓度NaCl(小于200 mmol/L)处理下,齿勒赤藓的叶肉细胞结构仍保持完整性。这表明特定的细胞结构支持是保证齿肋赤藓生物结皮稳定生长在高温、干旱、强辐射和盐碱性生境中的前提。另外,齿肋赤藓生物结皮能够适应小于200 mmol/L NaCl的盐分环境,而当NaCl浓度超过200 mmol/L时,齿肋赤藓叶肉细胞的细胞核和叶绿体表现出明显的毒害特征;同时,叶肉细胞的膜系统也会受到一定程度的伤害,当NaCl高于400 mmol/L时,叶肉细胞会因无法恢复活性而降解消失,使齿肋赤藓叶肉细胞失活,最终可能导致苔藓生物结皮死亡。在今后研究中,应以细胞超微观结构研究为基础,深入探究其它类生物结皮可适应的临界盐度及相应的生理生化调节机制。
参考文献(References):
[1]Li X R, Zhang Y M, Zhao Y G. A study of biological soil crusts: recent development, trend and prospect. Advances in Earth Science, 2009, 24(1): 11- 24.
[2]Belnap J. The potential roles of biological soil crusts in dryland hydrologic cycles. Hydrological Processes, 2006, 20(15): 3159- 3178.
[3]Zhang Y M, Chen J, Wang L, Wang X Q, Gu Z H. The spatial distribution patterns of biological soil crusts in the Gurbantunggut Desert, Northern Xinjiang, China. Journal of Arid Environments, 2007, 68(4): 599- 610.
[4]陶冶, 张元明. 叶片毛尖对齿肋赤藓结皮凝结水形成及蒸发的影响. 生态学报, 2012, 32(1): 7- 16.
[5]张元明. 荒漠地表生物土壤结皮的微结构及其早期发育特征. 科学通报, 2005, 50(1): 42- 47.
[6]Khandelwal A, Cho S H, Marella H, Sakata Y, Perroud P F, Pan A, Quatrano R S. Role of ABA and ABI3 in desiccation tolerance. Science, 2010, 327(5965): 546- 546.
[7]Cabot C, Sibole J V, Barceló J, Poschenrieder C. Lessons from crop plants struggling with salinity. Plant Science, 2014, 226: 2- 13.
[8]Benassi M, Stark L R, Brinda J C, McLetchie D N, Bonine M, Mishler B D. Plant size, sex expression and sexual reproduction along an elevation gradient in a desert moss. The Bryologist, 2011, 114(2): 277- 288.
[9]Herrnstadt I, Kidron G J. Reproductive strategies ofBryumdunensein three microhabitats in the Negev Desert. The Bryologist, 2005, 108(1): 101- 109.
[10]徐威, 王瑜, 袁庆华, 王志英, 姜毅. NaCl 胁迫对白三叶叶片超微结构的影响. 中国草地学报, 2013, (6): 104- 108.
[11]韦存虚, 王建军, 王建波, 周卫东, 孙国荣, 梁建生. Na2CO3胁迫对星星草叶肉细胞超微结构的影响. 生态学报, 2006, 26(1): 108- 114.
[12]Shu S, Yuan L Y, Guo S R., Sun J, Yuan Y H. Effects of exogenous spermine on chlorophyll fluorescence antioxidant system and ultrastructure of chloroplasts inCucumissativusL. under salt stress. Plant Physiology Biochemistry, 2013, 63: 209- 216.
[13]Elkahoui S, Barhoumi Z, Djébali N, Djébali W, Chaïbi W, Limam F, Smaoui A. Physiological and ultrastructural responses ofCatharanthusroseuscell suspension to salt stress. Russian Journal of Plant Physiology, 2013, 60(2): 244- 249.
[14]Gao H J, Yang H Y, Bai J P, Liang X Y, Lou Y, Zhang J L, Wang D, Zhang J L, Niu S Q, Chen Y L. Ultrastructural and physiological responses of potato (SolanumtuberosumL.) plantlets to gradient saline stress. Frontiers in Plant Science, 2015, 5: 787- 800.
[15]Queirós F, Rodrigues J A, Almeida D P F, Fidalgo F. Differential responses of the antioxidant defence system and ultrastructure in a salt-adapted potato cell line. Plant Physiology and Biochemistry, 2011, 49(12): 1410- 1419.
[16]Maathuis F J M. Sodium in plants: perception, signalling, and regulation of sodium fluxes. Journal of Experimental Botany, 2014, 65(3): 849- 858.
[17]Cabot C, Sibole J V, Barceló J, Poschenrieder C. Lessons from crop plant struggling with salinity. Plant Science, 2014, 226: 2- 13.
[18]Zhang X K, Lu G Y, Long W H, Zou X L, Li F, Nishio T. Recent progress in drought and salt tolerance studies in Brassica crops. Breeding Science, 2014, 64(1): 60- 73.
[19]饶本强, 张列宇, 吴沛沛, 李敦海, 刘永定. 集球藻对盐胁迫的生理适应及细胞结构变化. 水生生物学报, 2012, 36(2): 329- 338.
[20]魏美丽, 张元明. 生物结皮中齿肋赤藓叶片细胞显微与亚显微结构特征. 中国沙漠, 2009, 29(3): 493- 498.
[21]Wittenbach V A, Ackerson R C, Ciaquiata R T, Hebert R R. Changes in photosynthesis, ribulose bisphosphate carboxylase, proteolytic activity, and ultrastructure of soybean leaves during senescence. Crop Science, 1980, 20(2): 225- 231.
[22]Crawford S A, Wildens S. Ultrastructural aspects of damage to leaves ofEucalyptuscamaldulensisby the psyllidCardiaspinaretator. Micron, 1996, 27(5): 359- 366.
[23]Cheeseman J M. Mechanisms of salinity tolerance in plants. Plant Physiology, 1988, 87(3): 547- 550.
[24]Asada K. The water-water cycle in chloroplasts: scavenging of active oxygens and dissipation of excess photons. Annual Review of Plant Biology, 1999, 50(1): 601- 639.
[25]贾恢光, 赵曼容. 典型盐地植物叶绿体超微结构的研究. 西北植物学报, 1990, 10(1): 70- 72.
[26]郑文菊, 王勋陵, 沈禹颖. 几种盐地生植物同化器官的超微结构研究. 电子显微学报, 1999, 18(5): 507- 512.
[27]孟凡娟, 庞洪影, 王建中, 李淑艳, 王彦杰. NaCl和Na2SO4胁迫下两种刺槐叶肉细胞叶绿体超微结构. 生态学报, 2011, 31(3): 734- 741.
[28]苏芳莉, 李海福, 陈曦, 陈佳琦, 王铁良. 盐胁迫对芦苇细胞超微结构的影响. 西北植物学报, 2011, 31(11): 2216- 2221.
[29]Bennici A, Tani C. Ultrastructural characteristics of callus cells ofNicotianatabacumL. var. BELW3 grown in presence of NaCl. Caryologia, 2012, 65(1): 72- 81.
[30]Roy S J, Negrão S, Tester M. Salt resistant crop plants. Current Opinion in Biotechnology, 2014, 26: 115- 124.
[31]Nounjan N, Nghia P T, Theerakulpisut P. Exogenous proline and trehalose promote recovery of rice seedlings from salt-stress and differentially modulate antioxidant enzymes and expression of related genes. Journal of Plant Physiology, 2012, 169(6): 596- 604.
[32]Mishra P, Bhoomika K, Dubey R. Differential responses of antioxidative defense system to prolonged salinity stress in salt-tolerant and salt-sensitive Indica rice (OryzasativaL.) seedlings. Protoplasma, 2011, 250(1): 3- 19.
基金项目:国家自然科学基金项目(31260112)
收稿日期:2014- 10- 12; 网络出版日期:2015- 10- 10
*通讯作者
Corresponding author.E-mail: wgliuxj@126.com
DOI:10.5846/stxb201410122011
Ultrastructural responses ofSyntrichiacaninervisto a gradient of NaCl stress
LIU Weiguo1,*, DING Junxiang1,2,3,4, ZOU Jie1, LIN Zhe1, TANG Lisong2,4
1KeyLaboratoryofOasisEcology,CollegeofResourcesandEnvironmentScience,XinjiangUniversity,Urumqi830046,China2StateKeyLaboratoryofDesertandOasisEcology,XinjiangInstituteofEcologyandGeography,ChineseAcademyofSciences,Urumqi830011,China3UniversityofChineseAcademyofSciences,Beijing100049,China4FukangStationofDesertEcology,ChineseAcademyofSciences,Fukang831505,China
Abstract:Salinity is a major abiotic stress in arid and semiarid areas that has major effects on plant growth, thereby significantly reducing productivity. Biological soil crusts stabilize soil surfaces and aid in the establishment of vascular plants. These crusts have evolved salt resistance mechanisms and unique structures for survival under salinity stress and thus are an integral part of the soil system in arid regions worldwide. However, the effects of salinity on the ultrastructure of biological crusts have not been well investigated. Syntrichia caninervis Mitt is the dominant species in moss crusts of the Gurbantunggut Desert of northwestern China. In this study, S. caninervis was cultured in a concentration gradient of NaCl solution (0, 100, 200, 300, 400, 500 mmol/L) for 7 days. Using transmission electron microscopy, we observed changes in S. caninervis leaf cellular ultrastructure in response to salt stress. Comparisons of changes in cell wells, chloroplasts, and nuclei under the NaCl concentrations showed that under normal conditions (0 mmol/L NaCl), mesophyll cells were arranged loosely, organelles were morphologically integrated, and starch grains and electron-dense globules (plastoglobuli) were present in chloroplasts. No changes in ultrastructure were observed under mild NaCl stress (0—100 mmol/L); the cell structure was intact, and there were no changes in the structure of stroma or mitochondria. Under moderate NaCl stress (200—300 mmol/L), large changes in S. caninervis mesophyll cell structure were found, including swelling of the chloroplast thylakoid membranes, disorganization of grana, and plasmolysis. In addition, there was a marked increase in the number of plastoglobuli, the large central vacuole was ruptured, and chloroplasts showed disintegration. Overall, the ultrastructures of cell nuclei and vacuoles were slightly degraded. Under severe NaCl stress (400—500 mmol/L), the chloroplast membranes and lamellar structures were disorganized and contained a mass of plastoglobuli, and mesophyll cells were degraded and contained many vesicular multicycle-like membrane structures. Cells of the crust moss appeared to have serious plasmolysis as evidenced by the complete collapse of chloroplasts. These results indicate that injury to the membrane structure of various organelles, especially chloroplasts, is associated with the eventual death of mesophyll cells. Therefore, a better understanding of salinity-induced structural variability in Syntrichia caninervis should facilitate the identification of salt-tolerance mechanisms.
Key Words:Syntrichia caninervis; NaCL stress; mesophyll cells; ultrastructure
刘卫国,丁俊祥, 邹杰, 林喆,唐立松.NaCl对齿肋赤藓叶肉细胞超微结构的影响.生态学报,2016,36(12):3556- 3563.
Liu W G, Ding J X, Zou J, Lin Z, Tang L S.Ultrastructural responses ofSyntrichiacaninervisto a gradient of NaCl stress.Acta Ecologica Sinica,2016,36(12):3556- 3563.

