长春西汀固体分散体的制备及热力学
吕春杨,李金宇,荆恒攀(.浙江工业大学药学院,浙江 杭州 3004;.沈阳药科大学药学院,辽宁 沈阳 006)
医药化工
长春西汀固体分散体的制备及热力学
吕春杨1,李金宇2,荆恒攀1
(1.浙江工业大学药学院,浙江杭州310014;2.沈阳药科大学药学院,辽宁沈阳110016)
目的:制备能够提高长春西汀(vinpocetine,VIN)分散状态和溶出速度的固体分散体(solid dispersion,SD),研究VIN在PVPK30中分散的热力学过程。方法:应用溶剂法制备长春西汀固体分散体,并采用差示扫描量热(DSC)分析及X射线衍射分析(X-RD),研究长春西汀在载体中的存在状态。采用溶出度法,考察不同比例的长春西汀、聚乙烯吡咯烷酮及柠檬酸制备的固体分散体对其体外溶出速度的影响,应用溶解度法测定VIN在PVPK30中分散过程的热力学参数。结果:DSC分析及X-RD分析结果表明长春西汀在载体PVPK30中以无定型形态存在。体外溶出结果表明长春西汀与聚乙烯吡咯烷酮比例为1:8和1:7之间时,长春西汀体外溶出速度最快,且两种比例无显著性差异。酸化剂的加入对长春西汀的溶出有一定促进作用,在试验范围内,VIN-PVPK30-SD表观稳定常数(Kc)随温度升高而减小,分散过程的△rH=-5.01 kJ/mol,△rS=-0.01 kJ/mol,△rG<0。结论:加入酸化剂制备的VIN-PVP-CA-SD(1∶7∶0.5)可显著提高长春西汀的溶出速度,并提高了固体分散体的稳定性,VIN在PVPK30中的分散过程是放热过程且主要驱动力为焓驱动。
长春西汀;酸化剂;固体分散体;溶出度;表观稳定常数;热力学参数
长春西汀(Vinpocetine,VIN)是长春花中提取的吲哚生物碱长春胺(Vincamine)的衍生物。能改善脑梗塞后遗症、脑出血后遗症、脑动脉硬化症等诱发的各种症状,是一种有效的抗心脑血管药物。长春西汀极低的溶解度和较强的首过效应导致其极低的口服生物利用度,因而极大地限制该药在临床中的应用。聂淑芳等[1]用羟丙基-β-环糊精包合技术提高VIN在水中的溶解度溶出速度;庄春阳等[2]用纳米脂质载体技术提高VIN的溶解度和口服生物利用度。固体分散体(SD)是使药物在固体载体中处于高度分散状态,从而加快药物的溶出速率,提高药物的溶解度和生物利用度的一种分散系统[3-5]。
本实验采用固体分散技术,以聚乙烯吡咯烷酮(PVPK30)为载体,柠檬酸(CA)为酸化剂,来制备长春西汀固体分散体 (VIN-PVP-SD、VIN-PVPCA-SD)。长春西汀为吲哚类生物碱,具有弱碱性,在处方中加入一定的有机酸能增加其溶解度与溶出速度[6]。考察载体用量和酸化剂用量对长春西汀固体分散体溶出度的影响,考察酸化剂的加入对长春西汀固体分散体稳定性影响,并研究长春西汀在载体PVPK30中的分散热力学。为长春西汀固体分散体的制备和进一步开发高生物利用度的长春西汀新剂型提供参考。
1 试药与仪器
1.1试药
长春西汀(VIN,东北制药总厂,纯度99.0%);聚维酮(PVPK30,BASF);柠檬酸(CA,天津博迪化工股份有限公司);十二烷基硫酸钠(SDS,天津博迪化工股份有限公司);无水乙醇(分析纯,山东禹王化学试剂厂);其余均为分析纯。
1.2仪器
Spectrum-754PC型紫外分光光度计(上海光谱仪器有限公司);XS105DU型电子分析天平(Mettler Toledo);ZRCD6-B智能溶出仪 (上海黄海药检仪器厂);TA-60型DSC差示热分析仪(日本岛津);DX-2700型粉末X衍射分析仪(丹东奥龙集团)。
2 方法
2.1制备方法
2.1.1固体分散体的制备
采用溶剂法制备长春西汀。按比例称取VIN、PVPK30和柠檬酸(CA)适量,分别加入适量无水乙醇,超声溶解后混匀。用旋转蒸发法快速挥去乙醇至粘稠状态,然后置于40℃电热恒温真空干燥箱中,干燥12 h,取出粉碎过80目筛,置干燥器中保存备用。
2.1.2物理混合物(PM)制备
按比例精密称取VIN及PVPK30、CA(均过80目筛),等量递加法混合均匀,置干燥器中备用。2.2体外释放度的考察
2.2.1检测波长的确定精密称定干燥的VIN 10 mg于100 mL容量瓶中,加无水乙醇稀释定容,即得100 μg·mL-1的VIN标准溶液。精密量取此标准溶液5 mL,置于10 mL容量瓶中,加乙醇稀释定容,即得50 μg·mL-1的VIN溶液。重复上述步骤,配制得相同浓度的PVPK30,CA,SDS溶液。在200~400 nm范围内扫描,结果表明:VIN在波长272 nm处有最大吸收,其他辅料无干扰。
2.2.2标准曲线
精密移取 0.3 mL、0.5 mL、1.0 mL、1.5 mL、2.0 mL、2.5 mL、30 mL的VIN标准溶液,分别置于10 mL容量瓶中,用溶出介质稀释定容,得质量浓度(ρ)为3 μg·mL-1、5 μg·mL-1、10 μg·mL-1、15 μg·mL-1、20 μg·mL-1、25 μg·mL-1、30 μg·mL-1的VIN溶液。分别在272 nm波长下,以乙醇为空白,测定各溶液的吸光度(A),以A为纵坐标,ρ为横坐标,作线性回归,得回归方程为A= 0.0302ρ+0.0225,r=0.9995。表明VIN质量浓度在3~30 μg·mL-1范围内与吸光度呈良好的线性关系。
2.2.3体外释放度的测定
按 《中国药典》2010版二部释放度测定法第二法,以500 mL 0.5%(W/V)SDS溶液为溶出介质,转速50 r/min,温度(37±0.5)℃。精密称取相当于VIN 10 mg的不同比例的VIN-SD、PM和VIN原料药,加入到溶出杯中,分别于5 min、10 min、15 min、20 min、25 min、30 min、35 min、40 min、45 min、50 min、60 min取样5 mL(即时补充5 mL溶出介质),经0.45 μm微孔滤膜过滤,取续滤液在272 nm波长下测定吸光度。根据各个时间点的吸光度,代入标准曲线计算药物浓度,换算药物累积释放度(Q),并绘制释放度曲线。
2.2.4固体分散体稳定性的考察
将自制的VIN-PVP-SD(1:7)和VIN-PVPCA-SD(1∶7∶0.5)放置于40℃、75%RH的环境下,分别在0、1、2、3个月时,分别考察药物的溶出稳定性。
2.3理化性质考察
2.3.1差示扫描量热法(DSC)分析
工作条件:以空铝坩埚为参照,取新铝坩埚放入样品。扫描速率为10℃/min,扫描范围为30℃~230℃,氮气流保护,每次测样3~5 mg。
2.3.2X射线衍射(X-RD)分析
测定条件:铜靶,电压35 kV,管电流20 mA,扫描角度 (2θ)3°~50°,扫描速度2°/min,步长0.03°。
2.4 VIN在PVPK30中分散作用的热力学
在20 mL浓度分别为0mmol·L-1,0.1mmol·L-1,0.2 mmol·L-1,0.3 mmol·L-1,0.4 mmol·L-1,0.5 mmol·L-1的PVPK30溶液中加入过量的长春西汀原料药。置于恒温水浴振荡器中分别于25℃,37℃,50℃下振荡72 h。经0.45 μm微孔滤膜过滤,取续滤液在272 nm波长下测定吸光度,并绘制溶解度曲线。根据溶解度曲线按下式计算VIN-PVPK30表观稳定常数Kc(Kc=斜率/[截距(1-斜率)])[7]。再根据方程:lnKc=-△rH/RT+△rS/R,以lnKc对1/T进行线性回归,即可求得反应的焓变△rH、熵变△rS值。最后根据△rG=△rH-T△rS,求得分散过程的自由能△rG。
3 结果
3.1体外释放度测定
比较不同载体比例的长春西汀固体分散体和PM(1∶7∶0.5)及VIN原料药的药物溶出特性,体外释放曲线见图1。体外释放度结果通过Weibull分布模型[8-9]拟合,计算溶出参数 T50(药物释放50%所需时间),Td(药物释放63.2%所需时间)并进行方差分析,见表2。

Fig.1 Dissolution profiles of VIN from PM and several SDs

Tab.1 In vitro dissolution parameters in solution of vinpocetine solid dispersion prepared by different various weight ratios of PVPK30(n=5)
3.2差示扫描量热法分析
通过DSC仪测定VIN原料药、PVPK30、VIN和PVPK30物理混合物、VIN-PVP-SD的DSC曲线。测定结果如图3,VIN在152℃附近有一个尖锐的吸热峰,VIN-PVPK30(1:7)物理混合物在对应的峰位处也出现相应的吸热峰。而VIN-PVPK30(1∶7)固体分散体在152℃附近的吸热峰消失。表明VIN在载体PVPK30中以非晶体状态存在。

Fig.2 DSC profiles of VIN-PVP-SD
3.3X-射线衍射分析
通过XRD仪测定VIN原料药、PVPK30、VINPVP-PM、VIN-PVP-SD的XRD曲线,X射线衍射结果见图4。结果表明:VIN在11°~15°之间有多个强的结晶吸收峰,PVP在扫描范围内无明显的强吸收峰;物理混合物中VIN的各个特征峰均明显存在,而在VIN-PVP-SD的衍射谱线中VIN的衍射峰消失,表明VIN在载体PVPK30中VIN以非晶体形态分散,进一步验证了DSC分析的推断。

Fig.3 The X-ray powder diffractograms of VIN-PVP-SD
3.4酸化剂的加入对长春西汀溶出特性的影响
比较加入不同比例酸化剂CA和不加CA的长春西汀固体分散体的药物的溶出参数。溶出曲线见图2,溶出的weibull分布参数见表2,结果表明酸化剂的加入对药物的溶出有一定促进作用。
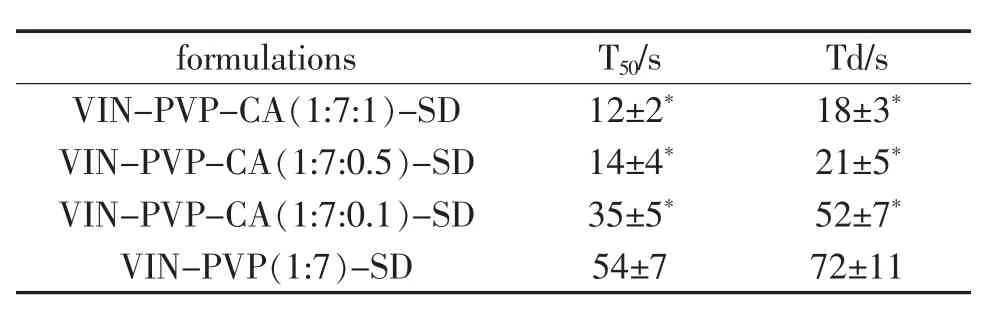
Tab.2 In vitro dissolution parameters in solution of vinpocetine solid dispersion prepared by different various weight ratios of CA(n=5)
3.5稳定性研究结果
比较两种处方的长春西汀固体分散体放置在75%RH、40℃的环境中3个月,定期观察各处方的外观并测定其药物百分含量和溶出特性,结果见表3。结果表明:VIN-PVP-SD随着保存时间的增加,制剂粉末逐渐发黄,药物含量下降,溶出速度也明显减慢。而VIN-PVP-CA-SD在稳定性研究期间,外观未发生明显的变化,药物含量和溶出速度也没有显著性变化。

Fig.4 Drug release profiles from several SDs with CA
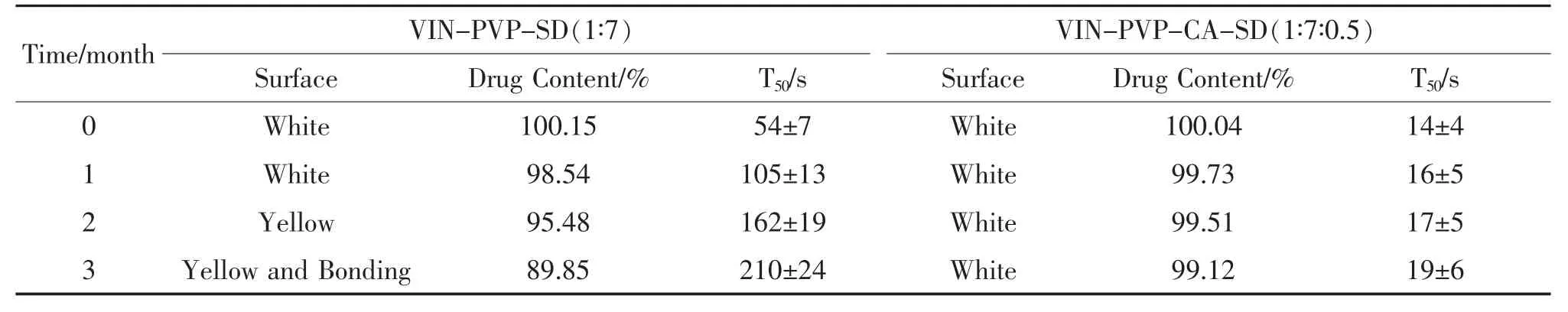
Tab.3 Stability of VIN-SD
3.6VIN在PVPK30溶液中分散作用的热力学

Fig.5 Solubility diagrams for VIN in water with PVPK30at different temperatures
VIN在不同温度下不同浓度PVPK30水溶液中的表观溶解度曲线见图5,热力学参数见表4。由图5可见,在试验范围内,随着PVPK30浓度的增加,长春西汀的溶解度呈线性增大;由表4可知:(1)长春西汀在 PVPK30溶液中的分散过程的△rH<0,△rS<0,该分散过程为放热、熵减反应,此熵变小于0的结果与由DSC判断的结果是一致的,即药物与载体间形成混乱度减小的低共熔物。(2)温度在25℃~50℃时,△rG<0,且随着温度的升高,△rG的负值减小,说明该反应为自发进行,且温度升高将不利于VIN在PVPK30溶液中的溶解分散。综上所述,VIN在PVPK30溶液中分散较容易,且在较低的温度下,VIN在溶液中的分散程度会更好,即长春西汀固体分散体在试验范围内的较低温度下,会有更快的溶出速度,更易形成稳定的VIN溶液。

Tab.4 Thermodynamic parameters of VIN-PVPK30solid dispersion
4 讨论
本实验中,药物和载体比例为1:3(w/w)时,药物在20 min时仍未完全溶解,相对其他比例的固体分散体溶解速度也较低,结果表明:不同载体比例的长春西汀固体分散体中药物释放速率,均高于物理混合物组和原料药组。且随着载体PVPK30比例的增加,VIN-PVP-SD中药物的释放速率也相应提高。药物载体比例为1∶7,1∶8的VIN-PVP-SD间,药物释放速率无显著性差异,但与其他各组药物释放速率存在显著性差异。表明制备的长春西汀固体分散体均可在体外显著提高VIN的溶出速率和程度,而在载体比例达到一定程度时,固体分散体中VIN的释放速率不再显著提高,表明比例达到1∶7及以上时,药物全部以非晶态形式高度分散,DSC和X-RD分析表明固体分散体中药物以非晶体形态高度分散在PVPK30中。
有文献[10-12]报道,固体分散体存在严重的老化现象,导致药物溶出度下降,影响了固体分散体的工业化生产和上市。在本实验中,制备的VIN-PVP-SD也同样存在一定程度的老化现象,而发现在加入酸化剂后,不仅进一步提高了固体分散体中长春西汀的溶出速度,固体分散体的稳定性也显著提高。
在本实验的热力学研究中,△rS<0,表明该分散过程为焓驱动,△rG<0,且随着温度的升高,△rG的负值减小,说明该反应为自发进行,且温度升高将不利于该分散反应。此研究对分散过程中的条件,如分散温度等参数的确定有一定的参考价值。本研究仅对长春西汀固体分散体粉末进行了研究,下一步工作还将对长春西汀固体分散体粉末进行制剂研究和体内药动学进行研究,为进一步开发高生物利用度的长春西汀新剂型提供参考。
[1]Nie S F,Fan X W,Peng Y,et al.In vitro and in vivo studies on the complexes of vinpocetine with hydroxypropyl-beta-cyclodextrin[J].Archives of Pharmacal Research,2007,30(8):991-1001.
[2]Zhuang C Y,Li N,Wang M,et al.Preparation and characterization of vinpocetine loaded nanostructured lipid carriers(NLC)for improved oral bioavailability[J].International Journal of Pharmaceutics,2010,394:179-185.
[3]刘娱姗,高署,柯学,等.难溶性药物固体分散体研究新进展[J].药学进展,2013,37(4):166-173.
[4]Dong W K,Min S K,Abid M Y,et al.Comparison of a solid SMEDDS and solid dispersion for enhancedstability and bioavailability of clopidogrel napadisilate[J].Carbohydrate Polymers,2014,114:365-374.
[5]李建伟,海丽娜,申爱卓,等.瑞格列奈固体分散体的制备及体外溶出[J].沈阳药科大学学报.2014,31(8):606-610.
[6]宁美英,周越,姚丽萍,等.柠檬酸对长春西汀控释片制备及体外释放度的影响研究.2010施慧达杯第十届全国青年药学工作者最新科研成果交流会论文集.2010:61-66.
[7]王静,石晓伟,杨彩琴,等.双苯氟嗪-聚乙二醇固体分散体的制备及热力学[J].中国医院药学杂志,2013,33(11): 861-864.
[8]Vasiliki P,Kosmas K,Marilena V,et al.On the use of the Weibull function for the discernment of drug release mechanisms[J].International Journal of Pharmaceutics. 2006,309:44-50.
[9]彭永富,董慧.药物溶出度Weibull分布的计算机求解[J].中国药学杂志,1996,31(10):606-608.
[10]姚情,唐星.热熔挤出技术制备硝苯地平固体分散体的研究[J].中国药剂学杂志:网络版,2014,06:177-184.
[11]王彦竹,赵勤富,孙清,等.两种介孔二氧化硅载体用于改善西洛他唑溶出度的比较[J].沈阳药科大学学报,2014,31(1):1-8.
[12]郑杨,张志丽,王立红,等.非诺贝特固体分散体制备工艺研究及比较[J].中国药剂学杂志:网络版,2012,10 (2):26-34.
Preparation and Thermodynamics of Solid Dispersion of Vinpocetine
LV Chun-yang1,LI Jin-yu2,JING Heng-pan1
(1.College of Pharmacy,Zhejiang University of Technology,Hangzhou,Zhejiang 310014,China;
2.School of Pharmacy,Shenyang Pharmaceutical University,Shenyang,Liaonin 110016,China)
Objective:To prepare a solid dipersion(SD)of Vinpocetine(VIN),which can enhance the state of dispersion and the rate of dissolution of VIN,and investigate the thermodynamics of VIN in PVPK30.Method:The co-precipitation was used to prepare the VIN-SDs.The dissolution characteristics in vitro of VIN-SD prepared with different ratio of PVPK30and citric acid(CA)were studied.Differential scanning calorimetry(DSC)and powder X-ray diffraction(X-RD)analysis was utilized to test the physicochemical characteristics of VIN-SDs.The solubility and thermodynamic parameters of VIN in PVPK30were determined by solubility techniques.Result:Powder X-ray diffraction and differential scanning calorimetry analysis confirmed that drugs were in the amorphous state in the carrier.When the ratio between VIN and PVP were 1∶7 and 1∶8,the speed of dissolution of VIN-SDs was the best,and had no significant difference.And the dissolution of VIN-SD was improved by adding the acidulant.The apparent stability constant(Kc)was decreased as the temperature increased.In the reaction,△rH=-212.87 kJ/mol,△rS=-0.57 kJ/mol,△rG<0.Conclution:The dissolution rate of VIN was significantly enhanced by the VIN-PVP-CA-SD(1∶7∶0.5)prepared with acidulant,and the stability of the SD(1:7:0.5)was improved.Thermodynamic studies indicated that VIN dispersing into PVPK30is drived by the enthalpy.
Vinpocetine;acidulant;solid dispersion;dissolution rate;apparent stability constant;thermodynamic parameter
医药化工
1006-4184(2016)4-0014-05
2015-05-14
吕春杨(1991-),男,浙江东阳人,硕士研究生,主要从事药物制剂学研究。E-mail:lvchunyang1117@163.com。

