含氮中孔碳负载的Au-Pd双金属催化剂在甲酸分解制氢中的催化性能
陈 旸,高凌峰,邱 镇,余正发,刘清港,王新葵
(大连理工大学化学学院,辽宁 大连 116024)
催化剂制备与研究
含氮中孔碳负载的Au-Pd双金属催化剂在甲酸分解制氢中的催化性能
陈旸,高凌峰,邱镇,余正发,刘清港,王新葵*
(大连理工大学化学学院,辽宁 大连 116024)
以SBA-15作为硬模板剂,吡咯作为碳源和氮源,制得的含氮中孔碳作为载体,采用吸附还原法分别制备了单Pd和Au-Pd双金属催化剂,并考察其在甲酸分解制氢反应中的催化性能。结果发现,Au-Pd/N-C比Au-Pd/C催化剂具有更高的甲酸分解活性,这可能是因为N的亲核作用促进了甲酸中H质子的脱除。由于Au-Pd之间的强相互作用,使Au的加入显著提高了Pd/N-C催化剂甲酸分解活性及其抗CO中毒能力,在50 ℃条件下,分解1 mol·L-1的甲酸初始转换频率 (TOF) 达到2 221 h-1。
催化化学;甲酸分解;掺氮碳材料;Au-Pd双金属催化剂;中孔碳
随着对能源需求的增长以及不可再生能源储量减少,氢气作为一种洁净能源,受到关注[1]。但由于氢气在储存和运输时存在较大的风险,极大地限制了其在工业中的应用。因此,实现有效控制氢气的储存及其释放已成为氢能源利用(尤其是氢燃料电池)方面的关键技术。相较于甲醇、水合肼和氨硼烷等储氢介质,甲酸是生物质加工过程中的主要产品,由于能量密度高、无毒性和在室温下非常稳定,是一种安全、方便的氢气储存材料[2]。用于甲酸制氢反应的催化剂可分为均相催化剂和多相催化剂,均相催化剂主要是一些金属有机配合物,比如钌、铱和铁的络合物[3-6],均相催化剂在甲酸分解反应中表现出优异的催化活性和稳定性,但存在不易分离、使用有机试剂过多和制备过程复杂等不足,阻碍了此类催化剂的大规模应用;多相催化剂具有制备方法简单、易控制和易分离的优势,但仍然面临着进一步降低反应温度和提高催化剂稳定性的挑战。
催化甲酸分解的多相催化剂大多是Pd基催化剂,但甲酸脱水产生的CO很容易将Pd金属毒化,降低了催化活性和稳定性。为解决这一问题,向Pd金属中掺杂Au或B元素,通过调变Pd的表面电子结构,可以提高其抗CO中毒能力[7-9]。另外,多相催化剂催化甲酸分解时,甲酸首先要脱除H质子生成HCOO-,随后伴随着HCOO-中β-H的解离产生CO2和H2。所以通常需要额外添加甲酸盐或碱提高体系中的HCOO-浓度,以促进催化剂的分解效率。将金属纳米粒子负载于含氮载体上,利用纳米粒子界面处N元素形成的微碱性环境,可促进甲酸中H质子的脱除,大大提高催化剂活性。Koh K等[10]和Martis M等[11]分别将金属Pd负载于氨基修饰的SBA-15 和MIL-125载体上,制备的催化剂表现出较高的催化活性,常温条件下,催化甲酸分解的初始转换频率分别为293 h-1和214 h-1。但由于载体在甲酸体系的不稳定性,催化剂的稳定性有待于进一步提高。
本文利用吡咯作为碳源和氮源,通过热解法制备含氮中孔碳材料,考察其负载Pd及Au-Pd后制备的催化剂在甲酸分解制氢反应中的催化性能,为高效分解甲酸多相催化剂的制备提供基础数据。
1 实验部分
1.1原料与试剂
吡咯,分析纯,上海科丰化学试剂有限公司;HAuCl4、PdCl2、甲酸(98%),分析纯,国药集团化学试剂有限公司。
1.2催化剂制备
含氮碳材料(N-C)制备:参考文献[12]的方法,以SBA-15作为模板剂,吡咯同时作为碳源和氮源,合成制备含氮中孔碳材料。0.4 g无水FeCl3分散到20 mL无水乙醇中,常温密封搅拌1 h,加入2 g的SBA-15,继续密封搅拌2 h,(80~100) ℃干燥过夜,120 ℃真空干燥3 h。将处理后的固体和吡咯液体一起放入真空干燥箱,120 ℃真空干燥24 h,使吡咯充分挥发并吸附到SBA-15孔道中,并在FeCl3的作用下氧化聚合成聚吡咯,700 ℃惰性气氛焙烧3 h。 焙烧后样品用20%的HF搅拌处理24 h,使其中的SBA-15模板剂充分溶解,经洗涤干燥后得到N-C材料。
中孔碳的制备:取1.2 g蔗糖溶解于5 g蒸馏水和0.14 g硫酸中,加入1 g的SBA-15。所得悬浮液经超声分散均匀并充分浸渍后,160 ℃保持6 h,使蔗糖完全碳化。为使孔道内完全填充, 再使用含有0.8 g蔗糖、5 g蒸馏水和0.1 g硫酸的溶液浸渍, 同样160 ℃保持6 h碳化处理。将得到的黑色粉末用20%的HF搅拌处理24 h,使其中的SBA-15模板剂充分溶解,经洗涤干燥后得到中孔碳材料。
采用吸附还原法制备Pd/N-C催化剂:准确称取N-C载体0.15 g,分散到20 mL去离子水中,超声分散,加入0.01 g·mL-1的PdCl2溶液1.25 mL,30 ℃水浴中搅拌吸附过夜,采用1 mol·mL-1的NaOH调节溶液pH=9~10,然后加入现配的0.1 mol·mL-1的NaBH4溶液10 mL,30 ℃水浴继续搅拌还原1 h。还原结束后,抽滤,去离子水洗涤,移至真空干燥箱真空120 ℃干燥过夜,即得到负载Pd质量分数为5%的Pd/N-C催化剂。
Au-Pd/N-C和中孔碳负载的Au-Pd/C催化剂采用相同方法制备,金属前驱体为0.34 mL的HAuCl4溶液(0.01 g·mL-1)和1.0 mL的PdCl2溶液(0.01 g·mL-1),Au理论负载质量分数为1%,Pd理论负载质量分数为4%。
1.3催化剂活性评价
甲酸分解反应:10 mL试管中放置20 mg催化剂,加入1 mol·L-1的甲酸2.5 mL,迅速将0.1 g的甲酸钾加入试管,将试管固定至50 ℃水浴锅中,并通过橡皮塞和导气管连接到气体检测装置,通过测量排出水的体积测定甲酸分解反应产生的气体体积。
循环催化性能测试:反应后催化剂过滤洗涤,烘箱80 ℃干燥2 h,继续进行甲酸分解反应,其他步骤不变。
1.4催化剂表征
XRD表征在X′Pert-Pro Super X射线衍射仪上进行,CuKα,工作电压40 kV,工作电流100 mA,扫描范围10°~70°,扫描速率5°·min-1。
N2吸附-脱附等温曲线采用美国康塔公司的Autosorb-iQ型全自动比表面和孔径分布分析仪在77 K下测得,测试前样品在373 K真空条件下脱气8 h,BET方法计算比表面积,BJH模型计算孔体积和孔径尺寸分布。
TEM照片采用FEI Tecnai G2F30 透射电子显微镜,加速电压120 kV;STEM-EDX照片采用配备能谱分析的FEI Tecnai G2 F30 S-Twin透射电子显微镜,工作电压300 kV。
XPS测试在美国Thermo Fisher Scientific公司ESCALAB250型X射线光电子能谱仪上进行,分析室基压为2×10-8Pa,工作压力为1×10-6Pa。
2 结果与讨论
2.1XRD
图1是制备的不同催化剂的XRD图。由图1可以看出,Pd/N-C的XRD图中没有出现任何明显金属Pd衍射峰,表明Pd粒子在载体表面上均匀分散,且粒径较小。而Au-Pd/N-C和Au-Pd/C催化剂在38.5°、44.5°和64.7°处均出现较明显的Au特征衍射峰,表明Au粒子在碳表面的粒径较大。Au在Au-Pd/N-C中可能主要是对Pd起分散作用以及与Pd相互作用修饰Pd的表面电子特性,而不是作为催化活性位点。

图 1 Pd/N-C、Au-Pd/N-C和Au-Pd/C催化剂的XRD图Figure 1 XRD patterns of Pd/N-C,Au-Pd/N-C and Au-Pd/C catalysts(A).Pd/N-C;(B).Au-Pd/N-C;(C).Au-Pd/C
2.2N2-物理吸附
图2为中孔碳与含N-C材料的N2物理吸附等温曲线。由图2计算出中孔碳比表面积和平均孔径分别为770 m2·g-1和38 nm,N-C材料比表面积和平均孔径分别为618 m2·g-1和48 nm,两种材料均存在滞后环,表明制备的碳载体均为介孔材料。

图 2 中孔碳与含N-C材料的N2-物理吸附等温曲线Figure 2 N2-physisorption isotherms of mesoporous carbon and N-doped carbon
2.3TEM
图3 为不同催化剂的TEM照片。由图3可以看出,以N-C为载体时,质量分数5%的Pd在载体表面均匀分布,平均粒径1.7 nm。而Au-Pd催化剂上,双金属纳米粒子发生部分团聚,出现大颗粒的纳米粒子。当Au-Pd的双金属纳米粒子负载到活性碳载体上时,团聚现象更加严重,与XRD的结果一致。

图 3 Pd/N-C、Au-Pd/N-C和Au-Pd/C催化剂的TEM照片Figure 3 TEM images of Pd/N-C,Au-Pd/N-C and Au-Pd/C catalysts(A).Pd/N-C;(B).Au-Pd/N-C;(C).Au-Pd/C
2.4XPS
图4为不同催化剂Pd3d的XPS谱图。由图4可以看出,Au-Pd双金属催化剂中Pd03d的结合能与单金属Pd相比,明显向低结合能处位移,表明制备的双金属纳米粒子中Au和Pd之间存在很强的相互作用,使Pd原子的表面结构发生明显变化。
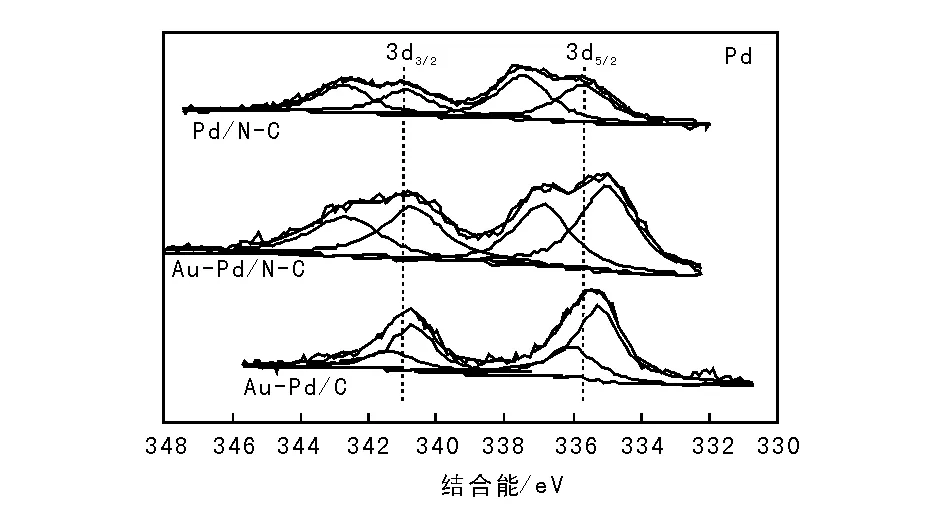
图 4 Pd/N-C、Au-Pd/N-C和Au-Pd/C催化剂sPd3d的XPS谱图Figure 4 XPS spectra of Pd 3d for Pd/N-C,Au-Pd/N-C and Au-Pd/C catalysts
2.5催化剂对甲酸催化分解性能研究
不同催化剂在甲酸分解反应中的催化性能如图5所示。由图5可见,Pd/N-C催化剂虽然表现出一定的初始催化活性,但是在反应10 min后逐渐失活。为了验证Pd/N-C的失活是否由甲酸脱水生成的CO毒化作用所致,向体系通入30 min的O2,然后迅速置换继续反应,发现Pd/N-C又具备了分解甲酸的能力。这是因为通入的O2在Pd的催化作用下消除了Pd表面吸附的CO,使被毒化的Pd活性位重新释放出来,从而可以继续催化甲酸的分解反应。Au-Pd/N-C催化剂上反应25 min后,即实现甲酸的完全分解,而且过程中没有表现出明显的失活现象,初始TOF值达2 221 h-1。可见,Au的引入虽然使得粒子的粒径有所增大,但是由于Au-Pd间强的相互作用,使Pd原子的表面性质发生改变,从而提高其抗CO毒化的能力及分解甲酸的活性。Au-Pd/C催化剂的甲酸分解活性明显低于Au-Pd/N-C催化剂,可能是由于N-C中氮元素的存在一方面可以促进甲酸中氢质子的脱除,另一方面也可以通过静电作用吸附金属粒子,提高金属与载体间的相互作用强度及分散度,从而提高了Au-Pd/N-C催化剂的甲酸分解活性和稳定性。

图 5 Pd/N-C、Au-Pd/N-C和Au-Pd/C催化剂在甲酸分解反应中的催化性能Figure 5 Catalytic performance of Pd/N-C,Au-Pd/N-C and Au-Pd/C catalysts for the decomposition of formic acid
在甲酸分解反应体系中,如何提高和改善催化剂的抗失活和循环使用能力是研究和设计甲酸分解催化剂的关键。图6为Au-Pd/N-C催化1 mol甲酸分解的稳定性实验。从图6可以看出,在连续4次的循环催化反应中,第2次以后的反应速率与第1次相比,有小幅度提高,并且在循环使用中保持不失活。Au-Pd/N-C第2次催化甲酸分解的速率略高于第1次的速率,可能是因为甲酸具有较高的还原性,而且分解过程产生的H2会进一步将部分PdO还原成金属Pd,提高了催化活性位的数量,从而提高了循环催化效率。

图 6 Au-Pd/N-C 催化剂的稳定性实验Figure 6 Stability tests of Au-Pd/N-C catalyst
3 结 论
(1) 以SBA-15作为硬模板剂,吡咯作为碳源和氮源,制备了一种含氮中孔碳材料,以此为载体,采用吸附还原法成功制备了Pd单金属和Au-Pd双金属催化剂,并考察了其在甲酸分解反应中的催化性能。
(2) Au-Pd/N-C催化剂表现出良好的催化甲酸分解活性和稳定性,在反应温度50 ℃条件下,分解1mol ·L-1的甲酸溶液的初始TOF值达到了2 221 h-1,可能因为N作为亲核试剂可以促进甲酸中H质子的脱除。
[1]Wang Y,Sun L,Luo L,et al.The study of portable direct-flame solid oxide fuel cell(DF-SOFC) stack with butane fuel[J].Journal of Fuel Chemistry and Technology,2014,42(9):1135-1139.
[2]Enthaler S,von Langermann J,Schmidt T.Carbon dioxide and formic acid-the couple for environmental-friendly hydrogen storage?[J].Energy & Environmental Science,2010,3(9):1207-1217.
[3]Loges B,Boddien A,Junge H,et al.Controlled generation of hydrogen from formic acid amine adducts at room temperature and application in H2/O2fuel cells[J].Angewandte Chemie International Edition,2008,47(21):3962-3965.
[4]Fellay C,Dyson P J,Laurenczy G.A viable hydrogen-storage system based on selective formic acid decomposition with a ruthenium catalyst[J].Angewandte Chemie,2008,120(21):4030-4032.
[5]Fukuzumi S,Kobayashi T,Suenobu T.Unusually large tunneling effect on highly efficient generation of hydrogen and hydrogen isotopes in pH-selective decomposition of formic acid catalyzed by a heterodinuclear iridium-ruthenium complex in water[J].Journal of the American Chemical Society,2010,132(5):1496-1497.
[6]Boddien A,Mellmann D,Gärtner F,et al.Efficient dehydrogenation of formic acid using an iron catalyst[J].Science,2011,333(6050):1733-1736.
[7]Gu X,Lu Z H,Jiang H L,et al.Synergistic catalysis of metal-organic framework-immobilized Au-Pd nanoparticles in dehydrogenation of formic acid for chemical hydrogen storage[J].Journal of the American Chemical Society,2011,133(31):11822-11825.
[8]Zhou X,Huang Y,Xing W,et al.High-quality hydrogen from the catalyzed decomposition of formic acid by Pd-Au/C and Pd-Ag/C[J].Chemical Communications,2008,(30):3540-3542.
[9]Jiang K,Xu K,Zou S,et al.B-Doped Pd catalyst:boostingroom-temperature hydrogen production from formic acid-formate solutions[J].Journal of the American Chemical Society, 2014,136(13):4861-4864.
[10]Koh K,Seo J E,Lee J H,et al.Ultrasmall palladium nanoparticles supported on amine-functionalized SBA-15 efficiently catalyze hydrogen evolution from formic acid[J].Journal of Materials Chemistry A,2014,2(48):20444-20449.
[11]Martis M,Mori K,Fujiwara K,et al.Amine-functionalized MIL-125 with imbedded palladium nanoparticles as an efficient catalyst for dehydrogenation of formic acid at ambient temperature[J].The Journal of Physical Chemistry C,2013,117(44):22805-22810.
[12]Fulvio P F,Jaroniec M,Liang C,et al.Polypyrrole-based nitrogen-doped carbon replicas of SBA-15 and SBA-16 containing magnetic nanoparticles[J].The Journal of Physical Chemistry C,2008,112(34):13126-13133.
Catalytic performance of Au-Pd supported N-doped mesoporous carbon catalyst for decomposition of formic acid to hydrogen
ChenYang,GaoLingfeng,QiuZhen,YuZhengfa,LiuQinggang,WangXinkui*
(School of Chemistry,Dalian University of Technology,Dalian 116024,Liaoning,China)
The N-doped mesoporous carbon support was prepared by using SBA-15 as the template and pyrrole as N and C source.Pd and Au-Pd bimetallic catalysts were prepared by depositing Pd and Au-Pd on the as-prepared support respectively via adsorption and reduction method in sequence.Their catalytic performance for hydrogen production from decomposition of formic acid was investigated.The results demonstrated that Au-Pd/N-C catalyst possessed better activity of formic acid decomposition than Au-Pd/C catalyst because the nucleophilic N atom probably promoted the removal of the proton from HCOOH.Because of the strong interaction between Au and Pd nanoparticles,the addition of gold to Pd/N-C catalyst could obviously improve the catalytic activity and anti-CO poisoning ability.The initial turnover frequency(TOF) of Au-Pd/N-C reached 2 221 h-1in 1 mol·L-1HCOOH solution at temperature 50 ℃.
catalytic chemistry;formic acid decomposition;N doped carbon;Au-Pd;mesoporous carbon;bimetallic catalyst
doi:10.3969/j.issn.1008-1143.2016.07.005
O643.36;TQ426.82Document code: AArticle ID: 1008-1143(2016)07-0027-05
2016-04-15
国家自然科学基金(21176037)资助项目;大连理工大学基本科研业务费(DUT15LK29)资助项目
陈旸,1996年生,男,安徽省马鞍山市人,本科在读,研究方向为多相催化。
10.3969/j.issn.1008-1143.2016.07.005
O643.36;TQ426.82
A
1008-1143(2016)07-0027-05
通讯联系人:王新葵, 1977年生,女,山东省平度市人,博士,副教授,硕士研究生导师,研究方向为多相催化。

