柱前衍生-高效液相色谱法测定蔬菜中甲醛含量
邓立刚,李增梅,谷晓红,赵善仓,苑学霞,王 磊,张树秋
(山东省农业科学院农业质量标准与检测技术研究所,山东省食品质量与安全检测技术重点实验室,农业部农产品质量安全风险评估实验室,山东济南 250100)
甲醛为较高毒性的物质,在我国有毒化学品优先控制名单上居第二位[1,2]。现已发布的《食品安全国家标准 食品添加剂使用标准》(GB 2760-2014)没有将甲醛列为食品添加剂,因此不能用于食品和农产品中。目前国家标准、行业标准及相关文献均未发现蔬菜中甲醛含量测定的分析方法。因此,为完善蔬菜质量监测手段,确保农产品安全,建立蔬菜中甲醛含量测定的方法势在必行。
目前,甲醛的分析方法主要有分光光度法、色谱法等[3 - 8]。分光光度法尽管设备价廉、操作简单,但因易受样品中基质干扰,易造成假阳性。高效液相色谱法具有灵敏高、准确度好,分析时间短的优点[9,10],但蔬菜样品多富含色素且基质复杂,不利于色谱分离和色谱柱的保护。本方法以蔬菜为主要研究对象,以蔬菜中游离态的甲醛为目标化合物,通过实验条件优化,建立了蔬菜中甲醛含量的高效液相色谱(HPLC)测定方法。该方法简单、精密度和准确度良好,适用于蔬菜中甲醛含量的检测。
1 实验部分
1.1 仪器与试剂
Waters E2695高效液相色谱仪(美国,Waters公司),配二极管阵列检测器(DDA)和Empower 3工作站;Mili-Q Advantage A10超纯水系统(美国,Milipore公司);KQ-500E超声波(昆山市超生仪器有限公司);Laborata 4000旋转蒸发仪(德国,Heidolph公司);MS3涡旋振荡器(德国,IKA公司)。
甲醛标准储备液(100 μg/mL,环境保护部标准样品研究所);乙腈、二氯甲烷(色谱纯,美国Fisher公司);邻苯二甲酸氢钾(优级纯,国药集团化学试剂有限公司);2,4-二硝基苯肼(DNPH)(纯度≥99.0%,德国Sigma公司)。0.01 mol/L邻苯二甲酸氢钾溶液:称取2.04 g邻苯二甲酸氢钾,用水溶解并定容至1 000 mL;0.4 g/L DNPH衍生液:称取2,4-二硝基苯肼0.040 g,加入乙腈溶解,并定容至100 mL。实验用水为超纯水。
1.2 样品处理
1.2.1样品提取称取约5 g试样(精确至0.01 g),置于50 mL容量瓶中,加入40 mL超纯水,超声提取30 min后取出,冷却,加超纯水至刻度,摇匀,用滤纸过滤,弃去初滤液,取续滤液备用。
1.2.2衍生移取5 mL滤液置于50 mL具塞离心管中,依次加入10 mL邻苯二甲酸氢钾溶液和5 mL DNPH衍生液,涡旋振荡混匀,50 ℃±5 ℃恒温培养箱反应60 min,取出冷却至室温。
1.2.3萃取净化将衍生反应液转移至150 mL分液漏斗中,加入20 mL二氯甲烷,振荡萃取,静置分层后收集下层有机相,再加入15 mL二氯甲烷,重复提取2次,合并有机相于150 mL圆底烧瓶中,40 ℃旋转蒸发至约2 mL,转移至5 mL容量瓶中,用少量乙腈洗涤圆底烧瓶,合并到5 mL容量瓶中并定容,混匀后过0.22 μm有机相微孔滤膜,滤液供HPLC测定。
1.3 色谱质谱条件
色谱柱:Waters Sunfire C18色谱柱(250×4.6 mm,5 μm);流动相:乙腈-水(1∶1,V/V);流速:1.0 mL/min;检测波长:355 nm;进样量:10 μL;柱温:40 ℃。
2 结果与讨论
2.1 色谱条件的确定
2.1.1检测波长的确定甲醛在酸性环境条件下能够与2,4-二硝基苯肼衍生生成2,4-二硝基苯腙,使用二极管阵列检测器对2,4-二硝基苯腙进行了200~500 nm波长区间的扫描,该化合物在355 nm处有最大吸收。因此实验选择355 nm为检测波长。
2.1.2流动相条件的选择衍生物2,4-二硝基苯腙为非极性化合物,由于甲醇和水比例接近1∶1时,混合溶液粘度大,色谱柱柱压高,为降低柱压,延长色谱柱使用寿命,故选择乙腈和水作为流动相。探讨了流动相的比例对分离度的影响,乙腈和水体积比例分别选用了60∶40、50∶50、45∶55。实验表明,乙腈和水的比例为50∶50,甲醛衍生物峰分离度最好,见图1。
2.2 2,4-二硝基苯肼(DNPH)衍生液浓度的确定
取100 μg/mL的甲醛标准溶液100 μL,依次加入4.9 mL水和10 mL 0.01 mol/L邻苯二甲酸氢钾溶液,再分别加入0.04~2.0 mg/mL DNPH衍生液各5 mL,同时做空白对照,衍生温度和时间分别为50 ℃、60 min,上机测定。结果表明,当DNPH衍生液浓度为0.2~2.0 mg/mL时,甲醛衍生物的峰面积趋于稳定且达到峰值,见图2-a。结合样品间差异及降低2,4-二硝基苯肼对色谱柱的污染等方面的综合考虑,确定衍生液DNPH浓度为0.4 mg/mL。
2.3 衍生pH 条件的确定
使用稀HCl和NaOH溶液调节0.01 mol/L邻苯二甲酸氢钾溶液的pH值分别为2、3、4、5、6、7,各取10 mL,依次加入100 μL 100 μg/mL甲醛标准溶液、4.9 mL水和5 mL 0.4 mg/mL DNPH衍生液,同时做空白对照,衍生温度和时间分别为50 ℃、60 min,上机测定。结果表明,当0.01 mol/L邻苯二甲酸氢钾溶液的pH范围为2~5时,甲醛衍生物峰面积趋于稳定,且在pH=4~5间峰值最高,见图2-b。新配制的0.01 mol/L邻苯二甲酸氢钾溶液的pH在4.3~5.0范围内,符合甲醛衍生所需的pH环境。
2.4 衍生温度的探讨
取100 μg/mL甲醛标准溶液100 μL,依次加入4.9 mL水、10 mL 0.01mol/L邻苯二甲酸氢钾溶液和5 mL 0.4 mg/mL DNPH衍生液,衍生温度分别设为30 ℃、40 ℃、50 ℃、60 ℃、70 ℃,衍生时间均为60 min,上机测定。结果见图2-c,当衍生温度为50 ℃时,甲醛衍生物峰面积为最高值。因此,确定该实验衍生温度为50 ℃。
2.5 衍生时间的确定
取100 μg/mL甲醛标准溶液100 μL,依次加入4.9 mL水、10 mL 0.01 mol/L邻苯二甲酸氢钾溶液和5 mL 0.4 mg/mL DNPH衍生液,衍生温度50 ℃,衍生时间分别为10、20、30、40、50、60、70、80、90 min,反应液过0.22 μm微孔滤膜,上机测定。见图2-d,当衍生时间为50~90 min时,甲醛衍生物峰面积趋于稳定。考虑到衍生物生成量的稳定性,本方法选择的实验衍生时间为60 min。
2.6 线性方程
分别移取0、5 μL、10 μL、25 μL、50 μL、100 μL甲醛标准储备液(相当于0、0.5 μg、1.0 μg、2.5 μg、5.0 μg、10.0 μg)各置于50 mL具塞离心管中,加入5 mL水,其它步骤同1.2,得到甲醛的浓度分别为0、0.1、0.2 、0.5 、1.0、2.0 mg/L系列标准工作溶液。分别注入高效液相色谱仪中,以测定相应的峰面积(Y)为纵坐标,以标准工作液浓度(X)为横坐标绘制标准曲线。在0~2 μg/mL浓度范围内获得的标准曲线为:Y=355787X+33060,相关系数r为0.9989,线性关系良好。
2.7 方法的回收率、精密度和灵敏度
方法的准确度和精密度通过回收率试验进行考察。在白菜、芹菜、山药、洋葱、韭菜、青椒中分别添加甲醛标准溶液,添加量分别为2.0、5.0、10.0 mg/kg,每个浓度做5个平行。实验结果见表1。添加平均回收率在78.1%~114.2%之间,相对标准偏差(RSD)为0.8%~9.5%。以信噪比(S/N)≥3计算检出限,该方法的检出限为 1 mg/kg,方法的线性范围为1.0~20.0 mg/kg。
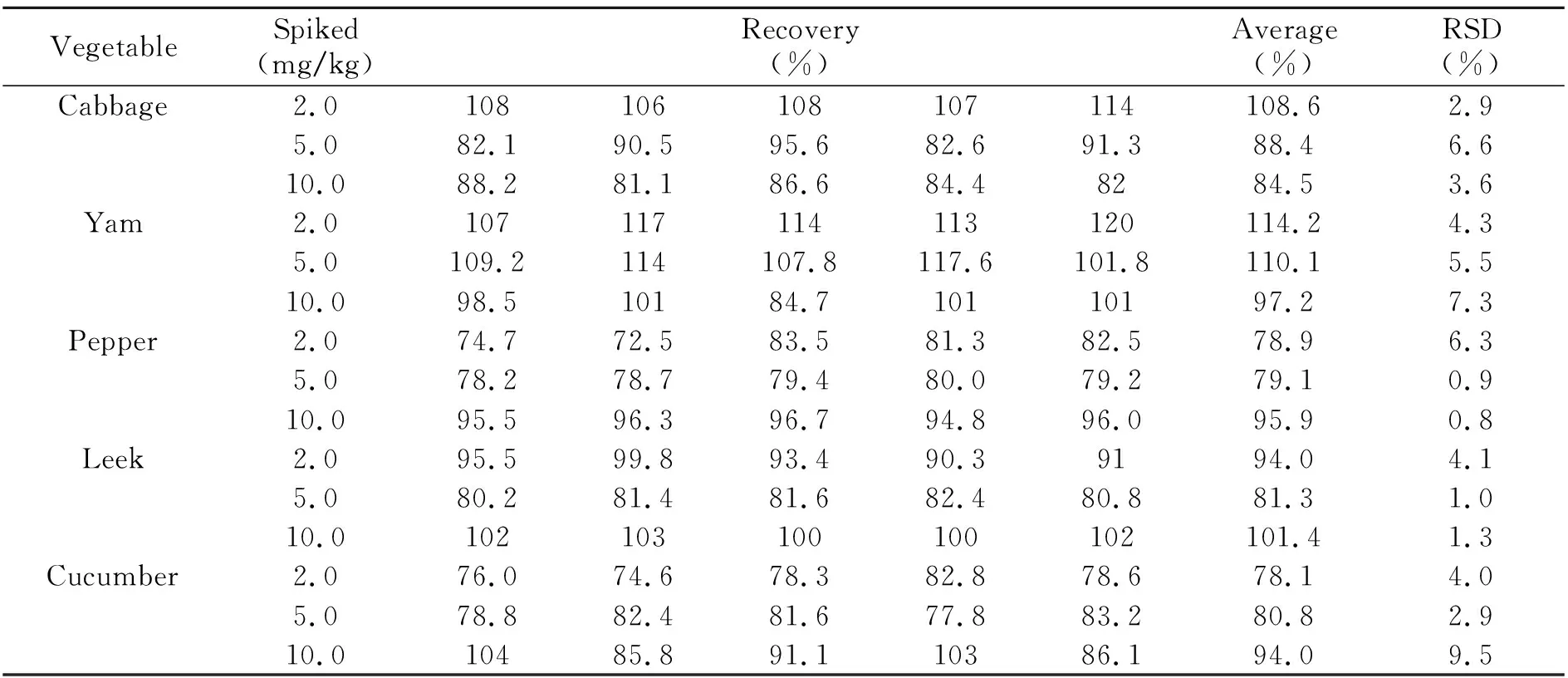
表1 不同蔬菜中甲醛添加回收率(n=5)
2.8 实际样品的测定
按照本方法对10份白菜样品、5份香菇样品进行测定,10份白菜均未检出甲醛,而3份鲜香菇均检出,含量平均为30.5 mg/kg,这与文献报道[11]基本一致,甲醛来源于其自身生理代谢。
3 结论
本文以水为提取剂,以2,4-二硝基苯肼为衍生剂,采用二氯甲烷萃取净化、浓缩,建立了高效液相色谱法测定蔬菜中的甲醛的分析方法。该方法简单、准确、易操作,适用于蔬菜中甲醛含量的测定。

