过氧化环己酮储存过程中热失控危险性研究
臧 娜
(武警学院 消防工程系,河北 廊坊 065000)
过氧化环己酮储存过程中热失控危险性研究
臧娜
(武警学院 消防工程系,河北 廊坊065000)
研究了过氧化环己酮及其与溶液混合后的热分解动力学及实际包装条件下的自加速分解温度(SADT),利用差示扫描量热仪测试了过氧化环己酮及其与溶液混合后的热分解特征,得到不同升温速率下热流随时间的变化曲线,使用Friedman等转化率法对试验数据进行处理,得到了过氧化环己酮的分解反应活化能等动力学参数,并用绝热加速量热仪试验数据对动力学参数求解进行验证。推算了实际条件下达到最大温升速率时间为24 h的初始温度,基于可靠的动力学参数和有限元分析法计算了三种样品的SADT。结果表明过氧化环己酮热分解活化能随反应进程变化而变化,TMRad为24 h时的初始温度分别为53、71、66 ℃,实际包装条件下的SADT为37、61、56 ℃。
过氧化环己酮;热失控;反应动力学;TD24;自加速分解温度
0 引言
过氧化环己酮(Cyclohexanone Peroxide,简称CYHPO),是一种工业上应用比较广泛的有机过氧化物,主要用作橡胶、塑料合成中的交联剂和引发剂。有机过氧化物性质不稳定,在常温或高温下容易放热分解。当受热、与杂质接触、摩擦或撞击时会引起热分解,其安全生产、存储、运输时的条件较严格[1-2]。由于过氧化环己酮的不稳定性,其日常运输和储存过程中,需要采用惰性溶剂保护。一旦处理不当,极易引发火灾爆炸事故。2012年6月19日,北京某研究所,由于过氧化环己酮储存过程中发生热失控,导致火灾爆炸事故,直接经济损失达1 000万元。本文研究目的在于对过氧化环己酮及其溶剂的热危险性进行研究,以避免在运输和储存过程中类似事故的发生。
有机过氧化物属于自反应性化学物质,自加速分解温度(SADT)和绝热条件下达到最大温升速率的时间(TMRad)是评价热失控危险的两个重要参数。其中,国际上对于SADT的求解采用了不同的动力学分析方法[3-11]。然而,对于CYHPO及其溶液的SADT还没有进行系统的研究。因此,本文尝试采用差示扫描量热仪(DSC)对CYHPO及其溶液进行热分析试验,利用等转化率Friedman微分法对热分析数据进行处理,研究反应的动力学参数。另外应用绝热加速量热仪(ARC)对动力学参数的求解进行验证。结合以上两种热分析试验方法,数值计算SADT和TMRad。
1 试验
1.1试验样品
邻苯二甲酸二辛酯(Dioctyl Phthalate,简称DOP)液封过氧化环己酮,分析纯,上海阿拉丁生化科技股份有限公司生产;邻苯二甲酸二丁酯(Dibutyl Phthalate,简称DBP),分析纯,国药化学试剂有限公司生产。在测试前,过氧化环己酮试剂先用乙醇和水分别进行洗涤并抽滤,直到得到接近干燥的白色粉末。处理过的样品可直接用于测试。三种测试样品的含量见表1。
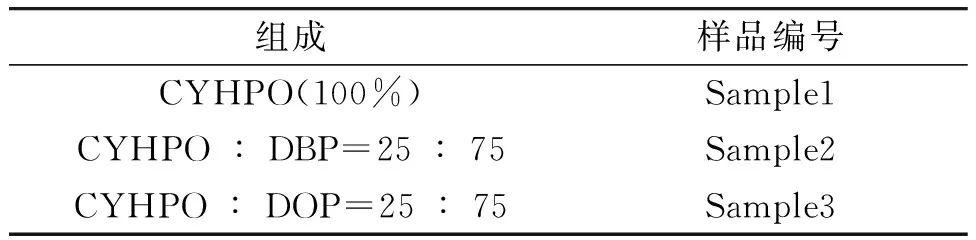
表1 试验样品成分
1.2试验仪器及试验条件
本文采用的DSC由瑞士METTLER-TOLEDO公司制造。升温速率(β)为1、2、4、10 ℃·min-1,试验温度范围为30~300 ℃,样品量为2~5 mg,坩埚采用带镀金垫片的高压坩埚,最高耐压为15 MPa,试验采用氮气气氛保护,流速为200 mL·min-1。
试验采用的ARC为英国THT公司生产的esARC,每次ARC试验时,样品质量为0.5~2.2 g,样品球质量为6.138 g,样品球材质为哈氏合金。测试起始温度50 ℃,终止温度250 ℃,加热梯度5 ℃,检测灵敏度0.02 ℃·min-1,等待时间15 min。
2 试验结果与讨论
2.1DSC试验结果分析
图1为三种样品的DSC测试曲线,其分解放热起始温度(T0)、峰温(Tp)、放热量(△Hd)等数据如表2所示。

图1 三种样品在4 ℃·min-1下的DSC曲线
由图1中曲线可以看出,物质在升温初期(70~80 ℃)存在一个因相变引起的吸热峰,到120 ℃后出现分解放热峰。样品2和样品3的放热分解温度范围和样品1基本一致,这说明溶剂的加入并没有影响试验室规模下样品1的分解过程。

表2 三种样品不同温升速率下热分解特性参数
2.2动力学参数的确定
为准确描述三种样品的反应动力学参数,使用基于Friedman等转化率微分法[12-13]模型的AKTS软件对样品在多重扫描速率下发生热分解的热力学数据进行分析,三种样品热分解动力学参数活化能Eα与反应进程之间的关系见图2。可见,在反应初始和反应终止阶段活化能随反应进程的变化较不稳定,基于这种原因,接下来的分析主要集中在反应进程范围为0.1~0.9之间。

图2 三种样品活化能与反应进程之间的关系
从图2可以看出三种样品的活化能与反应进程之间的趋势并不一样。对于样品1,反应开始时活化能为85 kJ·mol-1,随后活化能逐渐增加,直至达到118 kJ·mol-1,到反应进程0.9,活化能值基本变化不大。对于样品2和样品3,活化能与反应进程的关系相似,样品2反应开始时活化能为230 kJ·mol-1,随后降低到120 kJ·mol-1;样品3反应开始时活化能为230 kJ·mol-1,随后降低到100 kJ·mol-1。当反应进程为0.9时,样品2和样品3的活化能分别降低到110 kJ·mol-1和60 kJ·mol-1。图2证明了溶剂的加入并没有改变样品1的热分解反应机理,且活化能的微小变化并不能认为样品1的分解反应是单一反应,此时的活化能是多个竞争反应和平行反应的综合表征。
2.3动力学参数的验证
为验证上述动力学参数求解方法的有效性,采用ARC试验数据进一步进行分析。表3给出了绝热试验条件及试验结果。对于ARC试验,一旦升温速率超过100 ℃·min-1,由于仪器自身的限制,无法获取更高的温升速率,所以试验仪器记录的数据仅作为动力学参数的验证,这样的数据以“*”标注。
对于DSC试验与绝热条件下ARC试验,不同之处在于与外界的热交换机理不同[14-15]。对于绝热条件,反应过程中的热量完全用于加热试验样品和样品球,反应速率等参数不但取决于反应动力学,还取决于热惰性因子。基于反应动力学和热平衡条件可以模拟出反应速率。
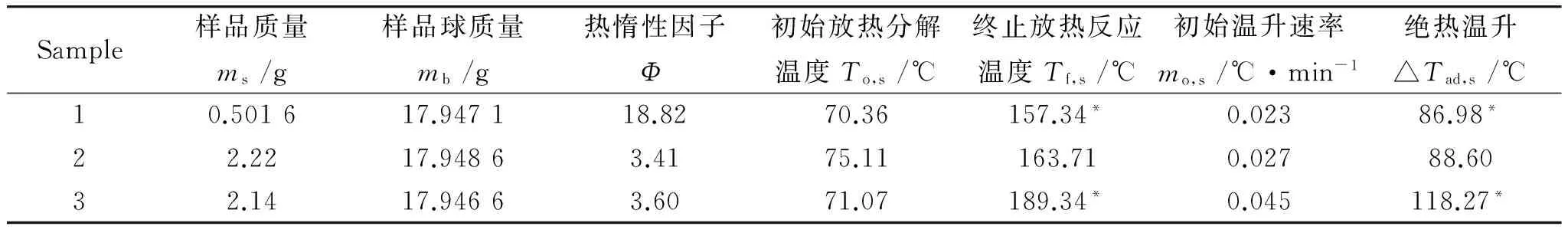
表3 ARC试验条件及测试结果
绝热条件下反应进程的模拟对于储存环节的安全性分析至关重要。在储存过程中,反应物质温度的异常升高往往会导致火灾爆炸事故的发生。图3给出了绝热条件下三种样品在加热-等待-搜寻模式下的试验曲线。从放热反应的过程中可以得出三种样品的TMRad分别为5.01 h、4.54 h和2.6 h。三种样品绝热条件下的试验曲线与基于DSC试验数据的模拟曲线具有较好的一致性。从上述分析可以得出,基于Friedman等转化率求得的反应活化能与反应进程之间的关系曲线可以用于模拟绝热条件下热分解反应过程,进而可以得出三种样品绝热条件下达到最大反应速率时间为24 h所对应的温度(TD24)分别为53、71、66 ℃。
3 自加速分解温度的确定
3.1计算原理
AKTS高等动力学分析软件结合热动力学计算的数据,使用有限元分析的方法扩展了计算方法的应用范围,可以分析非绝热条件下的热行为特征。通过这种方法可以预示在任何环境温度条件下储存过程的热积累和反应进程,可用于评价储存过程中在24 h内的安全性,模拟计算SADT。
反应体系的热安全分析可以建立在体系热平衡基础上,为了分析体系的热平衡,把样品分成若干个紧密相连的小立方体单元,采用自适应网格,热平衡关系如图4所示。
当热量传到周围环境时,体系内的温度分布取决于体系内的产热速率、比热容以及向边界层传递热量的导热速率。根据傅里叶热传导定律,可以得到公式(1)。
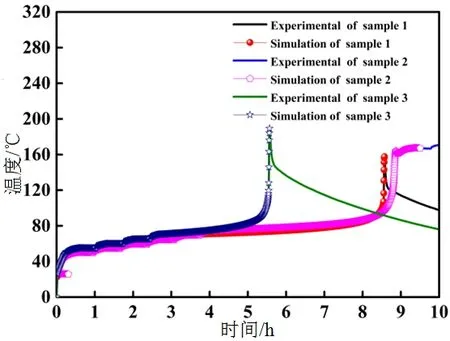
图3 绝热条件下达到最大温升速率时间试验曲线与模拟曲线的对比
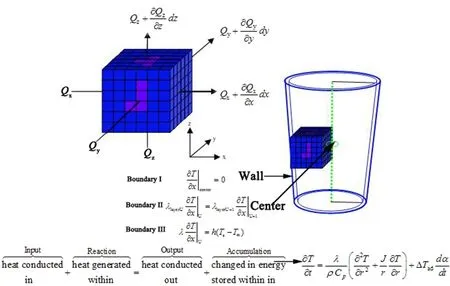
图4 体系热平衡图
(1)
式中,λ为导热系数;ρ为密度;Cp为比热容;T为温度;qr为反应单位体积内放出的热量。通常在柱面坐标内进行研究,经过一系列简化及处理后有:
(2)

3.2计算结果
SADT是评价自反应物质以包件形式储存和运输过程中稳定性的重要参数,指恒温环境中包件内物质在7 d或更短时间内其内部温度超过环境温度6 ℃时的最低环境温度[16-17]。如图5~图7所示,三种样品在钢制容器中储存,SADT值分别为37、61、56 ℃。模拟得出的SADT值与联合国试验值基本一致[18]。上述数值计算结果表明在储存CYHPO过程中应保证温度低于37 ℃。如果温度超过SADT,系统将达到不稳定状态,可能发生火灾爆炸事故。对于样品2和样品3,保证溶剂不挥发的情况下,CYHPO溶液储存比纯CYHPO(样品1)更稳定。
4 结论
4.1从固态反应出发,利用基于Friedman等转化率微分法的AKTS软件对CYHPO及其溶液在多重扫描速率下发生热分解的热力学数据进行分析,得出动力学参数Eα在整个反应进程中并不是常数,CYHPO的热分解是一个复杂的固态反应。
4.2可靠的动力学参数是模拟绝热条件下样品热分解特性的基础,三种样品在绝热条件下达到最大温升速率时间为24 h对应的温度分别为53、71、66 ℃,一旦初始温度超过上述临界温度,三种样品将会发生火灾爆炸事故。
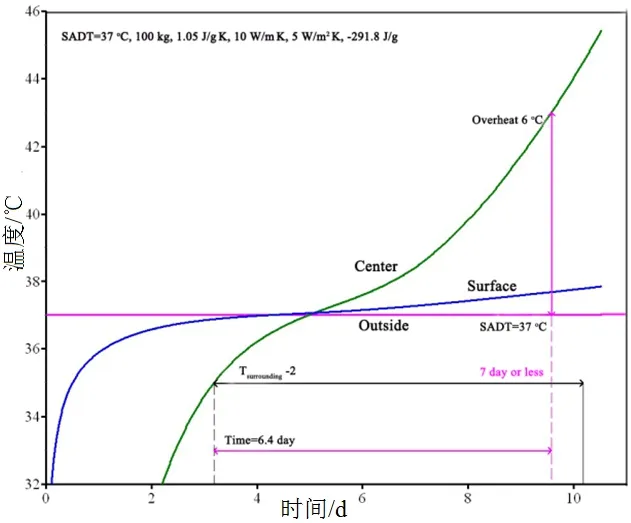
图5 Sample1的SADT计算值
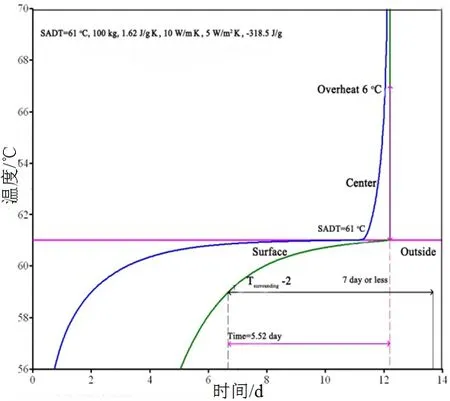
图6 Sample2的SADT计算值
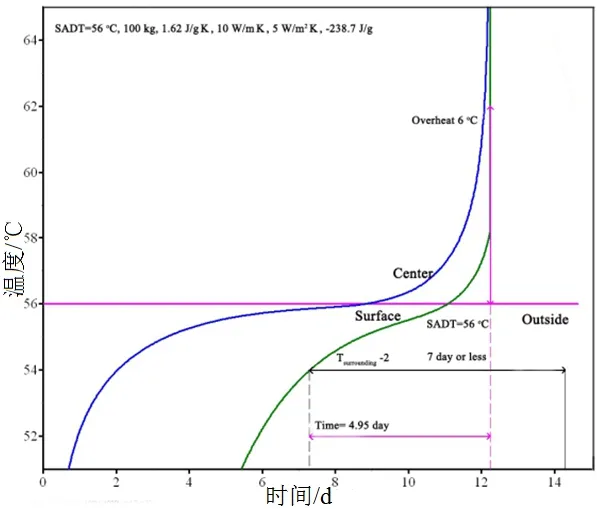
图7 Sample3的SADT计算值
4.3使用有限元分析方法推算出真实包装条件下三种样品的SADT分别为37、61、56 ℃,与联合国试验提供的数值基本吻合,对于避免CYHPO的储存过程发生火灾爆炸事故具有一定的指导意义。
[1] Code for the Storage of Organic Peroxide Formulations:NFPA 432[S].Quincy,MA,USA:National Fire Protection Association,2008.
[2] 朱鹏,刘惠平,周波,等.过氧化环己酮的热稳定性研究[J].上海应用技术学院学报(自然科学版),2011,11(4):330-335.
[3] LIN C P,TSENG J M,CHANG Y M,et al.Modeling Liquid Thermal Explosion Reactor Containing Tert-butyl Peroxybenzoate[J].Journal of Thermal Analysis and Calorimetry,2010,102:587-595.
[4] LIN C P,TSENG J M.Green Thermal Analysis for Predicting Thermal Hazard of Storage and Transportation Safety for Tert-butyl Peroxybenzoate[J].Journal of Loss Prevention in the Process Industries,2012,25:1-7.
[5] MALOW M,MICHAEL-SCHULZ H,WEHRSTEDT K D.Evaluative Comparison of Two Methods for SADT Determination:UN H.1 and H.4[C].In 2009 Mary Kay O’Connor Process Safety Center International Symposium,Texas,USA,2009.
[6] MALOW M,WEHRSTEDT K D.Prediction of the Self-accelerating Decomposition Temperature(SADT) for Liquid Organic Peroxides from Differential Scanning Calorimetry(DSC) Measurements[J].Journal of Hazardous Materials,2005,A120:21-24.
[7] SUN J H,LI Y F,HASEGAWA K.A Study of Self-accelerating Decomposition Temperature(SADT) Using Reaction Calorimetry[J].Journal of Loss Prevention in the Process Industries,2001,14:331-336.
[8] WHITMORE M W,WILBERFORCE J K.Use of the Accelerating Rate Calorimeter and the Thermal Activity Monitor to Estimate Stability Temperatures[J].Journal of Loss Prevention in the Process Industries,1993,6:95-101.
[9] WILBERFORCE J K.The Use of the Accelerating Rate Calorimeter to Determine the SADT of Organic Peroxides[R].Texas,USA:Columbia Scientific Corp,1981.
[10] YANG D,KOSEKI H,HASEGAWA K.Predicting the Self-accelerating Decomposition Temperature(SADT) of Organic Peroxides Based on Non-isothermal Decomposition Behavior[J].Journal of Loss Prevention in the Process Industries,2003,16:411-416.
[11] YU Y H,HASEGAWA K.Derivation of the Self-accelerating Decomposition Temperature for Self-reactive Substances Using Isothermal Calorimetry[J].Journal of Hazardous Materials,1996,45:193-205.
[12] AKTS-Thermokinetics and AKTS-Thermal Safety Software,AKTS AG,Advanced Kinetics and Technology Solutions[EB/OL].http://www.akts.com,2015.
[13] RODUIT B,FOLLY P,BERGER B.Evaluating and SADT by Advanced Kinetics-based Simulation Approach[J].Journal of Thermal Analysis and Calorimetry,2008,93:153-161.
[14] RODUIT B,DERMAUT W,LUNGHI A.Advanced Kinetics-based Simulation of Time to Maximum Rate under Adiabatic Conditions[J].Journal of Thermal Analysis and Calorimetry,2008,93:163-173.
[15] RODUIT B,DERMAUT W,LUNGHI A.Advanced Kinetics Tools for the Evaluation of Decomposition Reactions[J].Journal of Thermal Analysis and Calorimetry,2005,80:229-236.
[16] Recommendations on the Transport of Dangerous Goods,Manual of Tests and Criteria[M].5th ed.ST/SG/AC.10/11/Rev.5.United Nations:New York and Geneva,2009.
[17] Globally Harmonized System of Classification and Labeling of Chemicals(GHS)[M].United Nations:New York and Geneva,2003.
[18] ACROS COM.Part of Thermo Fisher Science[EB/OL].(2008-09-21).http://www.acros.be/(21.09.08).
(责任编辑、校对马龙)
Thermal Runaway Analysis of Cyclohexanone Peroxide during Storage Process
ZANG Na
(DepartmentofFireEngineering,TheArmedPoliceAcademy,Langfang,HebeiProvince065000,China)
Thermal stability properties of cyclohexanone peroxide and SADT(self-accelerating decomposition temperature) in the real package were studied. The curves of thermal decomposition heat flow at the different heating rate were obtained by the DSC. The applied method is based on a differential isoconversional approach and involves the combination of DSC and adiabatic measurement by accelerating rate calorimeter(ARC) for kinetic analysis and prediction. The reliable kinetic parameters and finite element analysis for heat balance were analyzed and used for a simulation of the adiabatic behavior: time to maximum rate under adiabatic conditions (TMRad) and SADT. The results show the activation energy varies dependent on reaction progress, and the initial temperature corresponding adiabatic induction times TMRadequal to 24 for these samples were 53,71 and 66 ℃, respectively. Meanwhile, the SADT for real package of three samples were 37,61 and 56 ℃.
CYHPO; thermal runaway; reaction kinetics; TD24; self-accelerating decomposition temperature
2016-01-30
河北省青年科学基金(E2016507003);河北省高等学校科学技术研究指导项目(ZC2016093)
臧娜(1982—),女,吉林通化人,讲师。
X937
A
1008-2077(2016)04-0018-05

