分散液液微萃取/气相色谱-串联质谱法测定地表水中苯并三唑类紫外线过滤剂
王金成,张海军,陈吉平
(中国科学院大连化学物理研究所,辽宁 大连 116023)
分散液液微萃取/气相色谱-串联质谱法测定地表水中苯并三唑类紫外线过滤剂
王金成*,张海军,陈吉平*
(中国科学院大连化学物理研究所,辽宁大连116023)
建立了地表水中6种苯并三唑类紫外线过滤剂:2-(2-羟基-5-甲基苯基)苯并三唑(UV-P)、2-(5-叔丁基-2-羟苯基)苯并三唑(UV-PS)、2-(5-氯-2-苯并三唑)-6-叔丁基对甲酚(UV-326)、2-(3,5-二叔丁基-2-羟苯基)-5-氯苯并三唑(UV-327)、2-(3,5-二叔戊基-2-羟基苯基)苯并三唑(UV-328)及2-(2-羟基-5-叔辛基苯基)苯并三唑(UV-329)的分散液液微萃取/气相色谱-串联质谱分析方法。以50 μL氯仿为萃取溶剂,600 μL乙醇为分散溶剂,样品pH值为3.0。目标化合物经Rtx®-5MS色谱柱结合程序升温分离后,用多重反应监测模式进行质谱分析,外标法定量。结果表明,6种化合物的基质加标回收率为83.5%~104.5%,相对标准偏差为5.1%~10.1%,方法的检出限为0.002~0.03 μg/L,定量下限为0.008~0.1 μg/L。
苯并三唑类紫外线过滤剂;分散液液微萃取(DLLME);气相色谱-串联质谱(GC-MS/MS);水
有机紫外线过滤剂对280~400 nm范围内的紫外线具有强烈的吸收作用,因此常被添加到个人护理品及工业产品中以防止或降低紫外线照射带来的损害[1-2]。其中,苯并三唑类紫外线过滤剂(BUVSs)是世界上消费量最大的一类紫外线吸收型光稳定剂[3]。 随着苯并三唑类紫外线过滤剂的大量生产和使用,其对环境的污染也日益引起人们关注。有关这类化合物对人类和野生动物的毒性研究报道非常少,但已有文献报道2-(2-羟基-5-甲基苯基)苯并三唑(UV-P)对皮肤有过敏作用[4],也有研究证明苯并三唑类紫外线过滤剂能导致细菌突变以及对植物有毒性作用[5]。UV-320因具有生物累积作用及对哺乳动物的肝脏和其它组织具有毒性作用,自2007年起在日本禁止生产、使用和进口[6]。而2-(3,5-二叔丁基-2-羟苯基)-5-氯苯并三唑(UV-327)由于具有和UV-320类似的生物累积作用,已被日本政府列为Ⅰ类化学污染物检测对象[7]。近年来在日本东南海岸的贻贝、海洋哺乳动物的脂肪及海洋食物链顶端鲨鱼和鸟类的肝脏中检测到2-(5-氯-2-苯并三唑)-6-叔丁基对甲酚(UV-326)、 UV-327和2-(3,5-二叔戊基-2-羟基苯基)苯并三唑(UV-328)[8-9]。
苯并三唑类紫外线过滤剂属亲脂类化合物,在水中的浓度非常低,因此测定前需对样品进行富集浓缩。目前测定环境水样中苯并三唑类紫外线过滤剂的方法有搅拌棒吸附萃取/气相色谱-质谱法[10]、顶空固相微萃取/气相色谱-串联质谱法[11]、搅拌棒吸附萃取/超高效液相色谱-串联质谱法[12]和在线固相萃取/超高效液相色谱-串联质谱法[13]等。分散液液微萃取(DLLME)是2006年由Rezaee和Assadi[14]等提出的一种集采样、富集、分离于一体的样品前处理技术。DLLME方法以操作简单、快速、分析成本低等优点已成功应用于环境中多种污染物的分离分析[15-19]。本文尝试采用分散液液微萃取结合气相色谱-串联质谱联用技术建立了地表水中苯并三唑类紫外线过滤剂的分析方法。
1 实验部分
1.1仪器与试剂
Trace GC Ultra气相色谱仪、TSQ Quantum XLS三重四极杆串联质谱仪(美国Thermo Fisher公司);飞鸽牌TDL-4013离心机(上海安亭科学仪器厂);Vortex Genie 2涡旋振荡器(美国Scientific Industries);氯仿、氯苯、四氯化碳(分析纯,天津科密欧化学试剂有限公司);甲醇、乙腈(LC-MS级,美国 Honeywell公司);乙醇(色谱纯,天津科密欧化学试剂有限公司);实验用水为经Milli-Q净化系统制备的去离子水。2-(2-羟基-5-甲基苯基)苯并三唑(UV-P)、2-(5-叔丁基-2-羟苯基)苯并三唑(UV-PS)、2-(5-氯-2-苯并三唑)-6-叔丁基对甲酚(UV-326)、2-(3,5-二叔丁基-2-羟苯基)-5-氯苯并三唑(UV-327)、2-(3,5-二叔戊基-2-羟基苯基)苯并三唑(UV-328)、2-(2-羟基-5-叔辛基苯基)苯并三唑(UV-329)购于日本东京化成工业株式会社,纯度均大于98%。
1.2色谱-质谱条件
色谱条件:Rtx®-5MS色谱柱(30 m×0.25 mm×0.25 μm,美国 Restek 公司);载气:氦气(纯度99.999%);恒流模式,流速:1.0 mL/min;进样口温度:260 ℃;程序升温:初始70 ℃,保持1 min,以20 ℃/min升至200 ℃,再以3 ℃/min升至280 ℃,保持 6 min;进样方式:不分流进样;进样量:1 μL。

表1 目标化合物的质谱分析参数Table 1 GC-MS/MS parameters for target compounds
*quantitative ion
质谱条件:离子源温度:200 ℃;电子轰击电离(EI)模式,轰击能量:70 eV;以多重反应监测(SRM)模式分析。定量、定性离子对、碰撞能见表1。
1.3分散液液微萃取
精密量取5.0 mL水样 于10 mL 具塞玻璃离心管中,加入0.4 g NaCl,振荡使其溶解;将50 μL氯仿溶于600 μL乙醇,然后用1 mL注射器迅速注入水样中,涡旋振荡2 min后以4 000 r/min离心 5 min,移取底部氯仿1 μL,供气相色谱-串联质谱测定。
1.4标准溶液制备
准确称取6种目标化合物各10 mg以甲醇溶解,并定容于100 mL 容量瓶中,得100 μg/mL的苯并三唑类紫外线过滤剂混标储备液。准确移取0.50 mL 该储备液于100 mL容量瓶中,用甲醇定容,得500 ng/mL混标溶液。将此混标溶液用水稀释成0.01,0.10,1.00,10.00,50.00 ng/mL 系列标准溶液,准确移取5.0 mL,按“1.3”方法进行萃取,用于标准曲线的测定。
2 结果与讨论
2.1仪器条件的优化
为使目标化合物在较短时间内获得最佳分离效果,尝试了不同的程序升温条件,结果发现采用“1.2”色谱条件可使目标化合物获得良好的分离。质谱条件是选择丰度最大的碎片离子作为目标化合物的母离子,然后通过改变不同碰撞电压(10,20,30,40,50 V)进行子离子扫描,初步确定碰撞电压为20 V,再进一步详细优化碰撞电压(15,16,17,18,19,20,21,22,23,24,25 V),以确定最佳碰撞电压及定量定性子离子,质谱分析参数见表1。
2.2萃取条件的优化
以5.00 mL 1.00 ng/mL 的6种目标化合物混标溶液为工作液,以目标化合物的峰面积为萃取效率指标,对萃取条件进行优化。
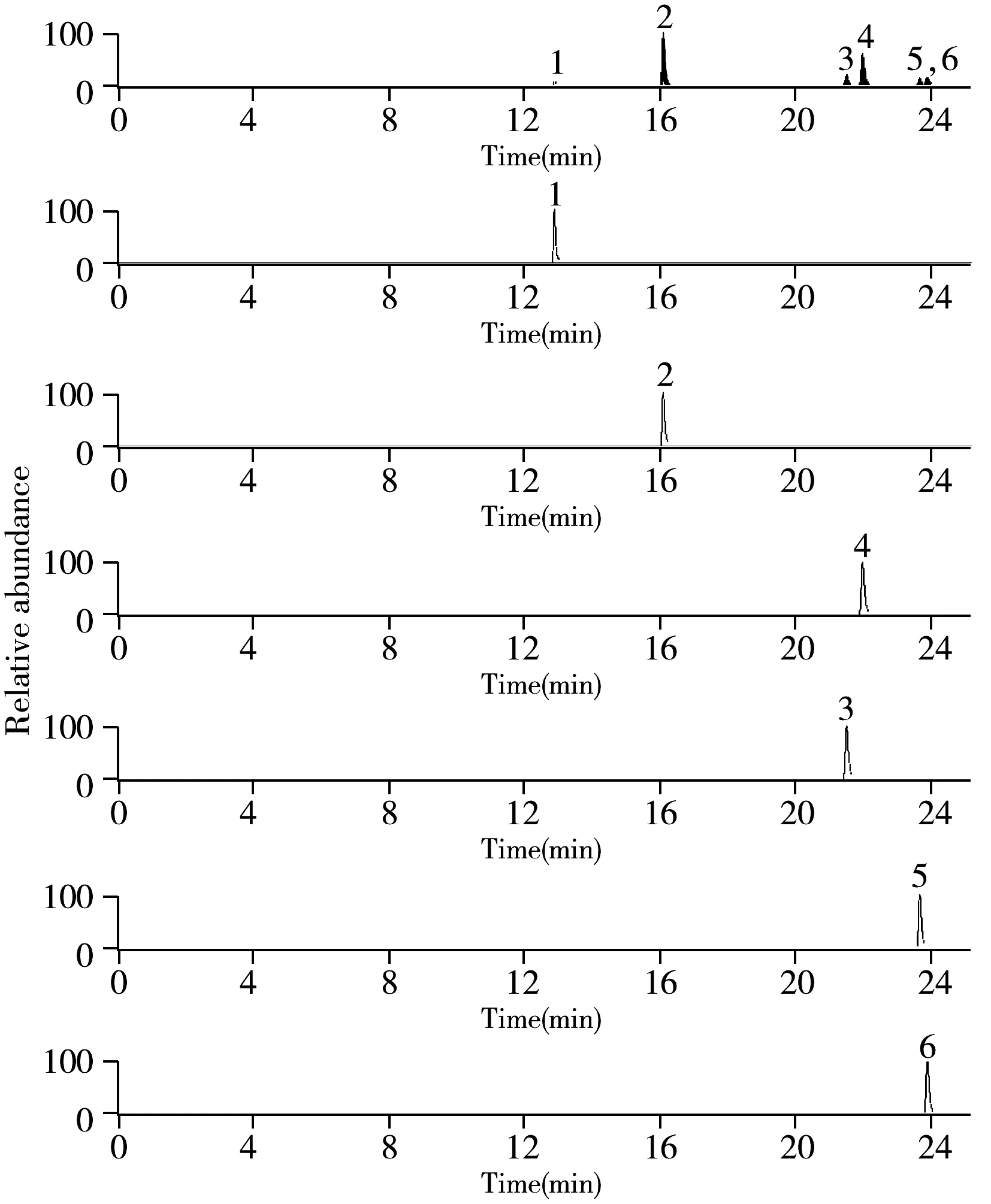
图1 SRM模式下6种目标化合物的选择离子流色谱图Fig.1 SRM chromatograms of 6 target compounds1.UV-P;2.UV-PS;3.UV-326;4.UV-329;5.UV-328;6.UV-327
2.2.1萃取剂的选择及用量分散液液微萃取的萃取溶剂应具有密度比水大,难溶于水,易溶于分散溶剂,对目标化合物有良好的萃取容量等特性。实验考察了氯苯、氯仿和四氯化碳3种溶剂的萃取效率,结果表明氯仿的萃取效率最大,因此选择氯仿为萃取溶剂。
考察了氯仿用量对萃取效率的影响,结果显示萃取效率随氯仿用量的增加而增大,氯仿用量为50 μL时萃取效率达最大值,此后随氯仿用量的增大,萃取效率开始下降。虽然增加萃取溶剂的用量可使更多的目标化合物被萃取出,但同时目标化合物在萃取相中的浓度开始下降,进而导致检测信号的下降。因此实验选择氯仿的最佳用量为50 μL。
2.2.2分散剂的选择和用量分散剂必须与水相和有机相(萃取溶剂)均能互溶,以增加萃取溶剂与水相的接触面积,从而增大萃取效率。实验考察了甲醇、乙醇及乙腈为分散溶剂时对萃取效率的影响,结果表明乙腈为分散剂时的萃取效率最低,而以甲醇和乙醇为分散剂时目标化合物的萃取效率差别不大,由于乙醇的毒性相对较低,因此实验选择乙醇为分散剂,并进一步考察了乙醇用量对萃取效率的影响。结果显示,随着乙醇体积(300~500 μL)的增加,萃取效率变化不大;当乙醇用量大于500 μL时,萃取效率显著增大,乙醇用量大于600 μL后萃取效率基本保持恒定。因此实验选择乙醇用量为600 μL。
2.2.3pH值对萃取效率的影响目标化合物在水相中的形态对萃取效率也有影响,分子形态有利于萃取到有机相,而离子形态则会降低萃取效率。苯并三唑类紫外线过滤剂的分子中含有酚羟基,一定条件下会解离,因此分别考察了pH 3.0,6.0,9.0时的萃取效率。结果表明pH 3.0时的萃取效率最高,pH 9.0时的萃取效率最低,因此选择样品的最佳pH值为3.0。这是由于苯并三唑类紫外线过滤剂在酸性条件下主要以分子形态存在,有利于萃取;而在碱性条件下酚羟基发生解离,使得萃取效率下降。
在上述优化萃取条件下,SRM模式下苯并三唑类紫外线过滤剂的选择离子流色谱图见图1。
2.3线性范围、回收率、精密度、检出限及定量下限
在优化萃取条件下,对5 mL 6种目标化合物系列混标溶液进行液液微萃取,并采用GC-MS/MS测定,得相应的线性回归方程、相关系数及线性范围(表2);并以目标化合物3倍信噪比(S/N=3)时的标准溶液浓度为方法的检出限(LOD),S/N=10时的标准溶液浓度为定量下限(LOQ);以空白海水为基质添加两个浓度水平的混标溶液进行回收率测定,每个浓度平行测定3次,结果见表2。实验结果表明,6种化合物的线性范围为0.01~10 μg/L(UV-PS,UV-329);0.1~10 μg/L(UV-P,UV-326, UV-327,UV-328);线性相关系数均大于0.99;基质加标回收率为83.5%~104.5%,相对标准偏差(RSD)为5.1%~10.1%;方法的LOD为0.002~0.03 μg/L,LOQ为0.008~0.1 μg/L。
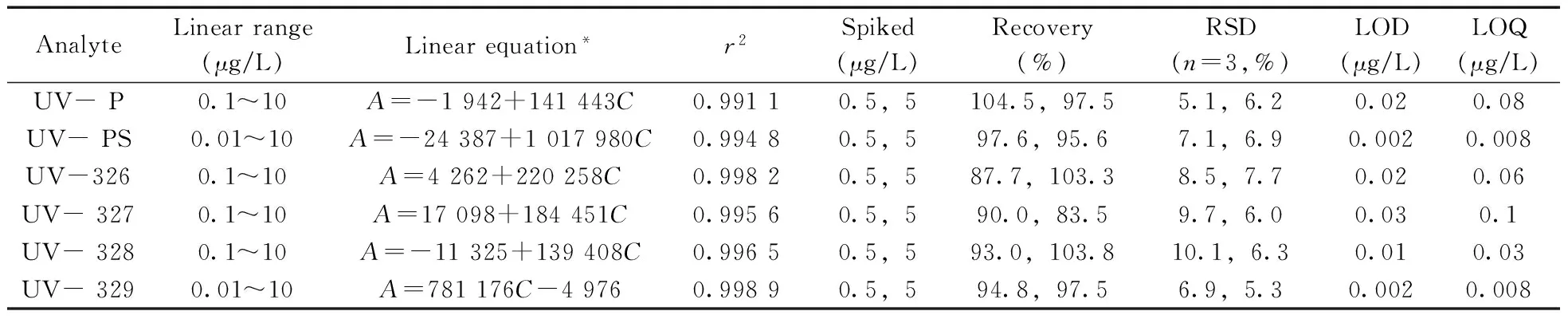
表2 目标化合物的线性范围、相关系数、回收率、精密度、检出限及定量下限Table 2 Linear ranges,correlation coefficients(r2),recoveries,precisions,limits of detection(LOD) and limits of quantitation(LOQ) of six target compounds
*A:peak area;C:concentration of analyte(μg/L)
2.4实际样品的测定
采用本文建立的分析方法对实验室自来水、大连西山水库及星海湾海水进行了测定。样品采于2015年5月10日,测定前于冰箱中4 ℃避光保存。西山水库及实验室自来水中未检测到6种目标化合物;星海湾海水中检出UV-PS(0.08 μg/L)。
3 结 论
本文建立了分散液液微萃取结合气相色谱-串联质谱技术测定水中6种苯并三唑类紫外线过滤剂(UV-P,UV-PS,UV-326,UV-327,UV-328及UV-329)的分析方法。该方法简便、快速、环境友好、灵敏度高,可用于水中苯并三唑类紫外线过滤剂的分析检测。
[1]Crawford J C.Prog.Polym.Sci.,1999,24:7-43.
[2]Himmelsbach M,Buchberger W.Polym.Degrad.Stab.,2009,94:1213-1219.
[3]Sui Z D,Li J,Xia F.PlasticsAdditives(隋昭德,李杰,夏飞.塑料助剂),2011,4 :50-55.
[4]Niklasson B,Björkner B.ContactDermatitis,1989,21:330-334.
[5]Farré M L,Pérez S,Kantiani L,Barcelo D.TrendsAnal.Chem.,2008,27:991-1007.
[6]Ema M,Fukunishi K,Hirose A,Hirata-Koizumi M,Matsumoto M,Kamata E.DrugChem.Toxicol.,2008,31:399-412.
[7]Kim J W,Isobe T,Malarvannan G,Sudaryanto A,Chang K H,Prudente M,Tanabe S.Sci.TotalEnviron.,2012,424:174-181.
[8]Nakata H,Murata S,Filatreau J.Environ.Sci.Technol.,2009,43:6920-6926.
[9]Nakata H,Shinohara R I,Murata S,Watanabe M.J.Environ.Monit.,2010,12:2088-2092.
[10]Carpinteiro I,Ramil M,Rodríguez I,Nogueira J M F.J.Sep.Sci.,2012,35:459-467.
[11]Carpinteiro I,Abuín B,Rodríguez I,Cela R,Ramil M.Anal.Bioanal.Chem.,2010,397:829-839.
[12]Montesdeoca-Esponda S,Toro-Moreno A,Sosa-Ferrera Z,Santana-Rodríguez J J.J.Sep.Sci.,2013,36:2168-2175.
[13]Montesdeoca-Esponda S,Sosa-Ferrera Z,Santana-Rodríguez J J.Anal.Bioanal.Chem.,2012,403:867-876.
[14]Rezaee M,Assadi Y,Hosseini M R M,Aghaee E,Ahmadia F,Berijani S.J.Chromatogr.A,2006,1116:1-9.
[16]Farajzadeh M A,Khoshmaram L.J.Chromatogr.A,2015,1379:24-33.
[17]Pirsaheb M,Fattahi N,Shamsipur M,Khodadadi T.J.Sep.Sci.,2013,36:684-689.
[18]Guo Y Y,Ding Y,Hu X Y,Wang J.J.Instrum.Anal.(郭亚芸,丁燕,胡效亚,王建.分析测试学报),2015,34(9):1040-1044.
[19]Xu L Z,Li X Y,Xian Y P,He M H,Fang J,Huang J F,Guo X D.J.Instrum.Anal.(许丽珠,李秀英,冼燕萍,何敏恒,方军,黄金凤,郭新东.分析测试学报),2015,34(8):923-927.
Determination of Benzotriazole UV Stabilizers in Water Samples by Dispersive Liquid-Liquid Microextraction Combined with Gas Chromatography-Tandem Mass Spectrometry
WANG Jin-cheng*,ZHANG Hai-jun,CHEN Ji-ping*
(Dalian Institute of Chemical Physics,The Chinese Academy of Sciences,Dalian116023,China)
A novel dispersive liquid-liquid microextraction method was developed for the determination of six kinds of benzotriazole UV stabilizers:UV-P,UV-PS,UV-326,UV-327,UV-328 and UV-329 in water samples by gas chromatography with tandem mass spectrometry(GC-MS/MS).The optimal liquid-liquid microextraction experiment conditions were as follows:50 μL chloroform as extractant solvent,600 μL ethanol as dispersive solvent,pH value of sample:3.0.The target compounds were separated on a Rtx®-5MS column(30 m×0.25 mm×0.25 μm) and subsequently determined by triple quadruple mass spectrometry in multiple reaction monitoring mode.Quantitative determination was achieved by the external standard method.The average recoveries of target compounds were in the range of 83.5%-104.5%,with relative standard deviations(RSD,n=5) of 5.1%-10.1%.The method detection limits(LOD) for the six target compounds were in the range of 0.002-0.03 μg/L and the quantitation limits(LOQ) were 0.008-0.1 μg/L.
benzotriazole UV stabilizers;dispersive liquid-liquid microextraction(DLLME);gas chromatography-tandem mass spectrometry(GC-MS/MS);water
2016-02-23;
2016-04-29
国家重点基础研究发展计划(973计划项目)(2009CB421602)
王金成,博士,副研究员,研究方向:绿色样品前处理技术,Tel:0411-84379972,E-mail:wangjincheng@dicp.ac.cn
陈吉平,研究员,研究方向:分离材料、复杂样品分离分析,Tel:0411-84379562,E-mail:chenjp@dicp.ac.cn
10.3969/j.issn.1004-4957.2016.09.018
O657.63;TQ314.2452
A
1004-4957(2016)09-1172-04

