β-烟碱标准样品研制
王 尉,林 楠,周明强,乐胜锋,杜 宁,张经华
(1.北京市理化分析测试中心,北京 100089;2.全国标准样品技术委员会天然产物标准样品专业工作组,北京 100094;3.有机材料检测技术与质量评价北京市重点实验室,北京 100094)
β-烟碱标准样品研制
王尉1,3,林楠1,3,周明强1,3,乐胜锋1,3,杜宁1,2,3,张经华1,2*
(1.北京市理化分析测试中心,北京 100089;2.全国标准样品技术委员会天然产物标准样品专业工作组,北京 100094;3.有机材料检测技术与质量评价北京市重点实验室,北京100094)
依据GB/T 15000 标准样品工作导则,开展了β-烟碱国家标准样品研制工作。采用溶剂提取、萃取、柱色谱、水蒸汽蒸馏等方法制备β-烟碱样品,通过UV,IR,MS 和NMR 等方法对β-烟碱样品进行结构鉴定,并进行均匀性、稳定性检验。采用8 家实验室进行联合定值,对定值结果进行数据分析。β-烟碱标准样品的均匀性和稳定性良好,定值结果为99.12%,置信度95%的扩展不确定度为0.64%。所制得的β-烟碱样品满足标准样品工作导则的要求,可用于有关烟草产品中β-烟碱的检测,以及相关产品的质量控制。
β-烟碱;烟草;标准样品;均匀性;稳定性;定值
烟草中约含有50 种生物碱,存在于60 多个不同品种的烟草中[1],如烟碱、新烟碱、新烟草碱、降烟等[2-3]。其中烟碱又称尼古丁,作为烟草中一种特有的生物碱成分,其含量约占烟草生物碱总量的95%,占烟草干重的0.5%~6.0%,是评价烟叶品质的主要指标,也是衡量香烟吃味的主要指标[4]。烟碱在自然界中有3种异构体,分别为α-烟碱、β-烟碱和γ-烟碱,烟草中主要为β型[5]。
β-烟碱具有十分广泛的用途,该系列的农药属植物杀虫剂,是生产绿色食品的高效杀虫剂和生物性农药[6-8]。它还广泛应用于医药工业,是研制治疗心血管[9]和脑部疾病[10]药物的原料,并具有抗疲劳[11]、抗感染[12]等生理功效。高纯度的β-烟碱作为烟草行业的添加剂,能提高香烟品质,制作卷烟代用品[13-14]。
市场上的烟草相关产品种类繁多,其中β-烟碱含量的检测需要其标准样品作为对照,且在烟草的相关研发中也需标准样品作为研究对象。但目前国内尚无β-烟碱标准样品,因此迫切需要开展该标准样品的研制工作。本文依据GB/T 15000 标准样品工作导则,对制备得到的高纯度β-烟碱进行了纯度分析、结构确认、稳定性检验、均匀性检验、定值工作,最终申报获批成为国家标准样品。
1 实验部分
1.1仪器与试剂
LC-20A高效液相色谱系统(日本岛津公司),配SPD-M20A检测器;GCMS 2010气相色谱质谱仪(日本岛津公司);LC/MSD Trap液相色谱质谱仪(美国安捷伦公司);UV-2550紫外可见分光光度计(日本岛津公司);Spectrum400傅立叶变换红外-近红外光谱仪(美国珀金埃尔默公司);AVANCE 600超导脉冲傅立叶变换核磁共振波谱仪(德国Bruker公司)。
盐酸、甲醇、乙酸、氨水、氯仿、无水硫酸钠(北京化工厂);乙腈、乙酸铵(美国Fisher Scientific公司);实验用水为超纯水。烟叶B2F(河北中烟工业有限责任公司)。
1.2实验方法
1.2.1β-烟碱样品的制备及分装将烟叶粉碎至40目,用盐酸水溶液(pH 3.0)超声提取3次,料液比为1∶10,每次15 min,合并滤液,减压浓缩;再用氨水调至pH>10.0,以氯仿萃取3次,合并有机相,用盐酸水溶液(pH 3.0)反萃取3次,合并水相上732型强酸性阳离子交换树脂,氨水洗脱;然后进行水蒸汽常压蒸馏,盐酸水溶液回收,回收样品用氨水调至pH>10.0,氯仿萃取,去除氯仿后,用无水硫酸钠脱水,最终制得β-烟碱样品。
在相对独立和洁净空间,将β-烟碱样品采用1 mL棕色安瓿瓶进行充氮分装。以每瓶200 mg分装,用十万分之一天平称量,共100瓶样品,记为1~100号。分装好的样品瓶置于4 ℃冰箱中长期保存。
1.2.2纯度分析配制浓度为0.5 mg/mL的β-烟碱样品溶液,采用高效液相色谱(HPLC)、气相色谱-质谱联用(GC-MS)、峰面积归一法等方法对β-烟碱进行纯度分析。
首先,采用HPLC等度和梯度两种洗脱方式,并采用HILIC,C18,氨基柱等不同色谱柱,以及全波长检测对β-烟碱进行纯度分析。HPLC分析条件为:流速:1.0 mL/min;柱温:30 ℃;检测波长260 nm;进样量5 μL。
GC-MS分析条件:DB-5ms色谱柱(30 m×0.25 mm×0.25 μm);流速1.2 mL/min;进样口温度:300 ℃;进样方式:分流 50∶1;升温程序:40 ℃保持3 min,以35 ℃/min升至180 ℃,再以8 ℃/min升至300 ℃,保持8 min;进样量:1 μL。
β-烟碱纯度的测定:依据《YC/T 247-2008 烟草及烟草制品 烟碱纯度的测定 硅钨酸重量法》[15]对β-烟碱进行纯度测定。平行取样5份,经硅钨酸沉淀、过滤、称重,以β-烟碱的质量分数计算其纯度值。
1.2.3结构鉴定UV分析条件:甲醇为溶剂,扫描范围200~400 nm;IR分析条件:KBr压片法,扫描范围650~4 000 cm-1。MS分析条件:电喷雾离子源,采用正离子模式,喷雾器压力50 psi,脱溶剂气为氮气,温度350 ℃,流量10 L/min。NMR分析条件:溶剂为氘代氯仿(CDCl3),采集1H NMR和13C NMR谱图。
1.2.4均匀性、稳定性、定值研究依据GB/T 15000.3—2008《标准样品工作导则(3)标准样品:定值的一般原则和统计方法》[16]开展均匀性、稳定性、定值研究工作。
均匀性:通过随机顺序重复测量的方法,并采用单因素多水平试验方差分析法进行纯度均匀性检验。
稳定性:对β-烟碱样品进行4 ℃,12个月的长期稳定性研究。分别于不同时间取样检测,采用直线作为经验模型,观察斜率值是否有显著变化,预测β-烟碱的稳定性变化。
定值:采用8家实验室HPLC峰面积归一法对β-烟碱进行联合定值。HPLC分析条件同“1.2.2 ”HILIC色谱柱等度洗脱条件。分别随机取3个样品进行检测,每一样品平行测试2次,对各实验室的6个数据进行统计,计算β-烟碱标准样品的标准值和不确定度。
2 结果与讨论
2.1样品制备
目前,对于β-烟碱的常用提取方法有水蒸气蒸馏法、溶剂萃取法、酸/碱浸提法、离子交换树脂法以及超临界CO2流体萃取法等[17-19]。但上述方法得到的β-烟碱纯度不高。本文通过优化组合提取纯化方法,快捷、高效地从烟草中提取分离得到纯度大于99%的β-烟碱,为标准样品的研制提供了重要参考。
2.1.1样品提取由于β-烟碱在烟叶中主要以有机酸盐的形式存在,所以提取溶剂和pH值对提取率有重要影响,酸/碱浸提法是最常用的方法。本文利用盐酸将水提液的pH值调至3.0,即可对有机酸盐型和游离型β-烟碱进行全部的提取。与碱性条件下甲醇提取的方法相比,该方法具有成本低、绿色环保的特点。同时采用超声辅助提取,大大提高了提取效率。
2.1.2β-烟碱的分离纯化利用β-烟碱在碱性水相中呈游离态,易被有机溶剂萃取的特性,采用氯仿萃取可有效地去除提取溶液中单宁、蛋白质、果胶以及大部分有机酸成分;同时,在酸性条件下β-烟碱易被水相反萃取,因此经3次萃取-反萃取可得到含量为45%左右的盐酸盐型β-烟碱的粗提品。为进一步提高样品纯度,利用盐酸盐型β-烟碱带正电的性质,采用732型强酸性阳离子交换树脂进行吸附,氨水洗脱后,可有效去除样品中的色素,富集生物碱类成分。通过水蒸汽常压蒸馏将低沸点游离型的β-烟碱挥发,并用盐酸水溶液回收,去除高沸点成分,可得到纯度大于99%的盐酸盐型β-烟碱。
在生物碱类成分的分离纯化中,所得样品的形式(盐或游离型)备受关注。为了得到游离型β-烟碱,采用氨水调节pH值,将盐酸盐型β-烟碱样品转化成游离型,并用氯仿萃取富集。通过低温旋转蒸发去除氯仿,无水硫酸钠脱水后,可制得淡黄色透明油状的β-烟碱样品。
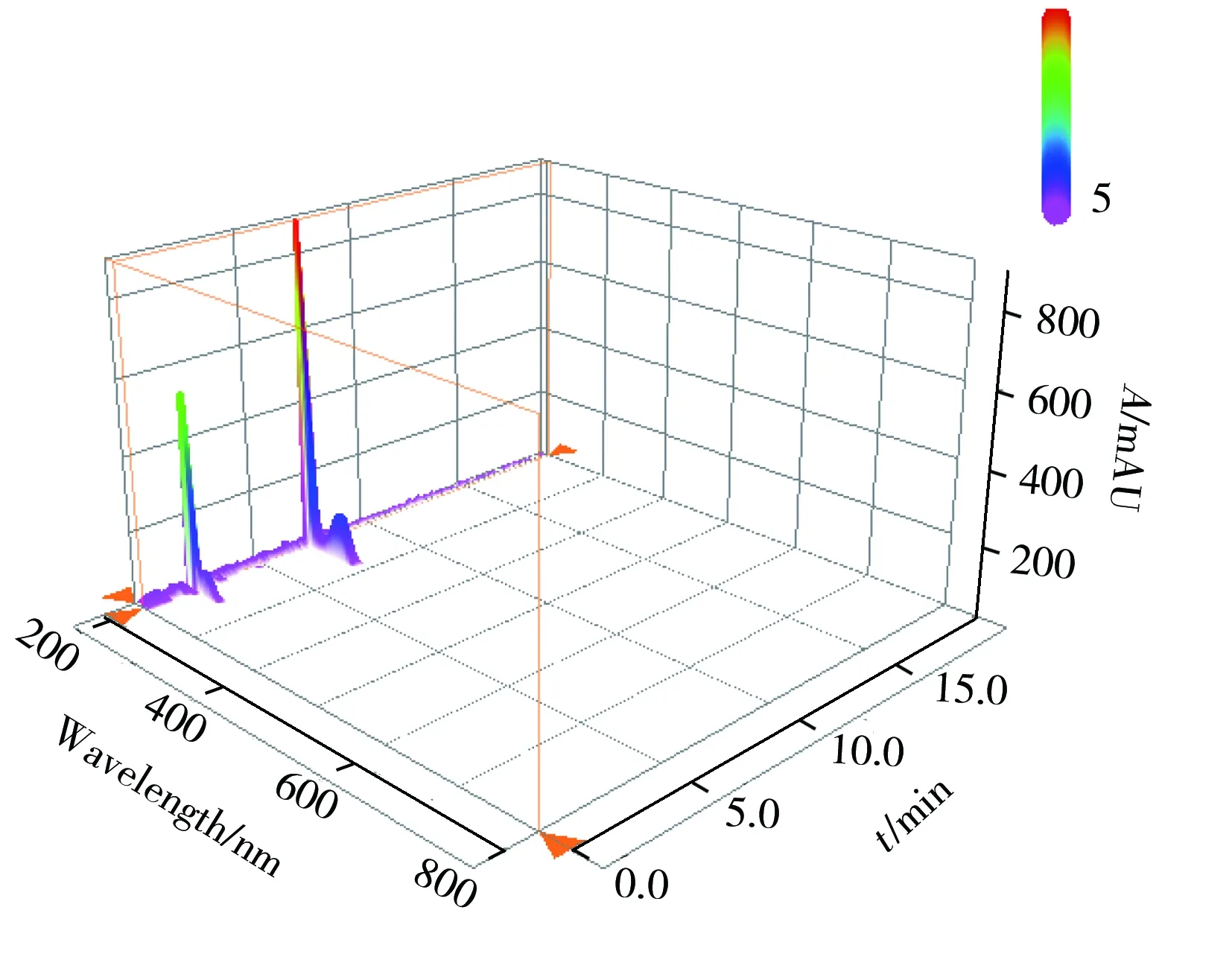
图1 β-烟碱的三维色谱图Fig.1 3D chromatogram of nicotine
2.2纯度分析
2.2.1高效液相色谱法等度和梯度洗脱均使用Waters Atlantis HILIC(150 mm×4.6 mm,5 μm)色谱柱,流动相A为乙腈,B为10 mmol/L乙酸铵(含2%冰醋酸);其中等度洗脱条件为:0~20 min,72%A;梯度洗脱条件为:0~40 min,90%~60%A。不同色谱柱对β-烟碱进行纯度分析的条件分别为:DIKMA Diamonsil(250 mm × 4.6 mm,5 μm)C18色谱柱,流动相A为甲醇,B为0.002 5%三乙胺,0~40 min,50%A;Shodeks NH2-40 E(250 mm×4.6 mm,5 μm)氨基柱,流动相A为乙腈,B为0.5%磷酸,0~20 min,70%A。通过以上色谱方法相结合的方式进行纯度分析,所得β-烟碱的纯度结果具有较好的一致性。
另外,标准样品纯度分析常用的方法是面积归一化法,但由于化合物种类不同,其紫外特征吸收波长也不同,单一的检测波长往往会忽略杂质的存在,因此采用等度洗脱的条件,配备二极管阵列检测器,采集了β-烟碱的三维色谱图(图1),除溶剂峰外,其他波长下无明显杂质峰出现。
2.2.2气相色谱-质谱联用法对于标准样品中的杂质可能存在紫外检测器无响应的情况,利用β-烟碱的挥发性质,采用GC-MS法对该样品的纯度进一步确定,GC-MS总离子图中未发现明显杂质峰,测得β-烟碱的纯度为99.09%。
2.2.3硅钨酸重量法利用硅钨酸与β-烟碱反应生成不溶性烟碱硅钨酸盐的特点,直接称重即可准确计算β-烟碱的纯度。通过5次纯度测定,得到β-烟碱的平均纯度为99.01%。
实验结果表明,硅钨酸重量法和气相色谱-质谱联用方法的测定结果基本一致,证明本文所研制的β-烟碱具有较好的纯度,适用于烟草及相关领域的化学分析和质量控制。
2.3结构确认


表1 β-烟碱的1H 和13C NMR测试结果Table 1 Results of 1H and 13C NMR spectrograms
2.4均匀性检验
采用随机顺序重复测量的方法,根据随机数表,分别抽取10个样品进行均匀性检验。按“1.2.2”纯度分析方法,每个样品平行检测3次,以峰面积百分比读取样品的纯度值。检测数据进行方差分析,以F值检验,确定了β-烟碱样品的均匀性良好。检验结果见表2~3。
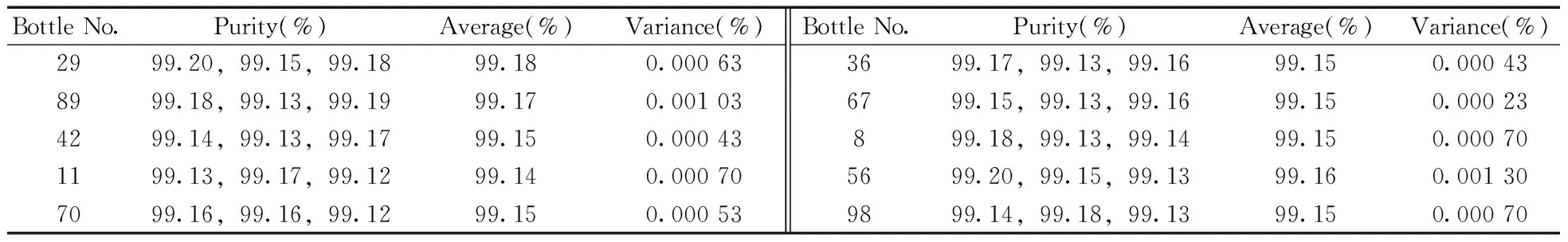
表2 均匀性检验结果Table 2 Results of homogeneity

表3 均匀性检验方差分析结果Table 3 Results of variance analysis for the homogeneity
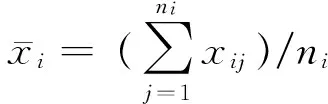
瓶间标准偏差是瓶间方差的平方根:Sbb=SA=1.36×10-4,均匀性检验引入的不确定度u均=Sbb=1.36×10-4。
2.5稳定性检验
按“1.2.2”纯度分析方法,分别于0,3,6,9,12月检测β-烟碱样品,每个样品平行检测3次,以峰面积百分比读取样品的纯度值。稳定性检验结果见表4。
采用直线作为经验模型,观察斜率值是否有显著变化,以此对标准样品的稳定性变化进行预测。

表4 稳定性检验结果Table 4 Results of stability
斜率可用下式计算:
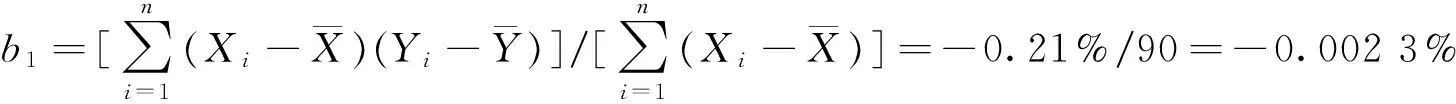
取其平方根s=0.031 6%,与斜率相关的不确定度用公式计算:
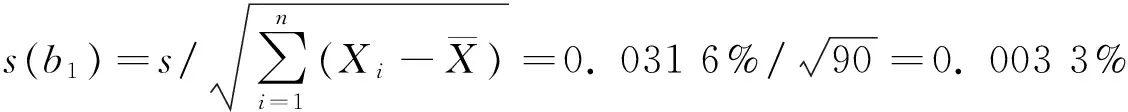
自由度为n-2和p=0.95(95%置信水平)的分布t因子为3.128,由于|b1| 2.6定值结果 对联合定值的8家实验室所采集的测定结果,采用Grubbs检验法进行检验,未发现异常值。经过数据统计,计算得出β-烟碱标准样品的标准值和不确定度。定值结果见表5~6。 表6 定值方差分析结果Table 6 Results of variance analysis for the certification 制备所得标准样品定值结果的不确定度组成如下:均匀性检验引入的不确定度,稳定性检验引入的不确定度以及多个实验室定值引入的不确定度。 在置信概率为95%时,k=2,则扩展不确定度UCRM=2uCRM=0.32%×2=0.64%。 针对我国尚无β-烟碱国家标准样品的现状,开展了该标准样品的研制工作,成功建立了β-烟碱样品的制备方法。并依据GB/T 15000标准样品工作导则,对制得的β-烟碱样品进行均匀性检验、稳定性检验及定值研究,最终申报获批成为国家标准样品。 β-烟碱标准样品的标准值为99.12%,扩展不确定度(95%置信区间)为0.64%。该标准样品符合GB/T 15000标准样品工作导则要求,填补了国内该领域研究的空白,不仅满足烟草及相关产品分析检测、质量控制工作的需求,也为检测结果的准确性、可比性以及溯源性提供了技术支撑。 [1]Rao G H,Zhao M M,Lin W F,Yang X Q.Resour.Sci.(饶国华,赵谋明,林伟锋,杨晓泉.资源科学),2005,27(5):120-127. [2]Dong E H,Tan H,Bao N,Yuan X,Ma K,He J L.GuangzhouChem.Ind.(董二慧,谭红,包娜,袁鑫,马凯,何锦林.广州化工),2012,40(15):33-35. [3]Shi J L,Pang T,Li Y,Song Z B,Gao Y L,Wang B W,Song C M.J.Instrum.Anal.(师君丽,逢涛,李勇,宋中邦,高玉龙,王丙武,宋春满.分析测试学报),2014,33(3):334-338. [4]Xue X P,Chen Y,Wang M S,Pan W J,Li J X.J.AnhuiAgric.Sci.(薛小平,陈懿,王茂胜,潘文杰,李继新.安徽农业科学),2008,36(10):4121-4123. [5]Ma J B.GuangdongChem.Ind.(马俊勃.广东化工),2011,38(10):33-35. [6]Zeng X,Ni J P,Ma Y F,Shi J J,Yan L,Ni L B.Mod.Agrochem.(曾霞,倪珏萍,马亚芳,施娟娟,严柳,倪龙博.现代农药),2013,12(6):1-5. [7]Lü C J,Zhong B Z,Qian J,Gou Z H,Qin W Q.J.Biosaf.(吕朝军,钟宝珠,钱军,苟志辉,覃伟权.生物安全学报),2013,22(3):201-205. [8]Liu J N,Huang H P,Hua J Z,Zhang Y Y,Yao L Y.GuizhouAgric.Sci.(刘佳妮,黄鹤平,华金珠,张瑜瑜,姚丽媛.贵州农业科学),2015,43(3):78-81. [9]Jia B,Xu H P,Zhang R X,Li G R,Liu Y,Fu L.Chin.J.Crit.CareMed.(贾宝,徐宏平,张瑞星,李国荣,刘艳,付莉.中国急救医学),2013,33(2):168-170. [10]Zhang Z N,Zhang G Z.ActaTabacariaSin.(张真娜,张桂治.中国烟草学报),2013,19(6):114-119. [11]Hou X D,Lin X Y,Zhang H B,Du Y M,Jiang Y.Chin.TobaccoSci.(侯小东,蔺新英,张怀宝,杜咏梅,姜迎.中国烟草科学),2014,35(6):90-92. [12]Li K,Wu C T.Chin.J.Exp.Surg.(李锟,吴承堂.中华实验外科杂志),2015,32(4):743-744. [13]Zheng K L,Yu D M.J.ChongqingUniv.(郑奎玲,余丹梅.重庆大学学报),2004,27(3):61-64. [14]Chu Z B,Shui H F,Chen J M.Appl.Chem.Ind.(储志兵,水恒福,陈建民.应用化工),2007,36(1):102-104. [15]YC/T 247-2008.Tobacco and Tobacco Products-Determination of Nicotine Purity-Gravimetric Method Using Tungstosilicic Acid.Tobacco Industry Standards of the People′s Republic of China(烟草及烟草制品 烟碱纯度的测定 硅钨酸重量法.中华人民共和国烟草行业标准). [16]GB/T 15000.3-2008.Directives for the Work of Reference Materials Reference(3)-Materials-General and Statistical Principles for Certification.National Standards(3)-of the People's Republic of China(标准样品工作导则:(3)标准样品:定值的一般原则和统计方法.中华人民共和国国家标准). [17]Yang Y K,Li X M,Zhou J,Xu L L,Yang T.TobaccoSci.Technol.(杨叶昆,李雪梅,周瑾,徐兰兰,杨涛.烟草科技),2006,1:38-40. [18]Liu B F,Xiang X K.FineChem.(刘本发,向兴凯.精细化工),1998,1:55-57. [19]Xu X M,Gao K D,Huang Q L.Chem.Adhes.(徐晓沐,高科达,黄伣丽.化学与黏合),2006,1:50-53. [20]Jeffrey I S,Jaya F,John B,Bruce E W.J.Agric.FoodChem.,1999,47(12):5133-5145. Development of Nicotine Certified Reference Material WANG Wei1,3,LIN Nan1,3,ZHOU Ming-qiang1,3,LE Sheng-feng1,3,DU Ning1,2,3,ZHANG Jing-hua1,2* (1.Beijing Centre for Physical and Chemical Analysis,Beijing100089,China;2.Specialistic Group on Natural Product of National Technical Committee on Reference Materials,Beijing100094,China;3.Beijing Key Laboralory of Detection Technology & Quality Evaluation of Organic Material,Beijing100094,China) According to the directives for the work of reference materials GB/T 15000,nicotine certified reference material was prepared.Nicotine was prepared by extraction,column chromatography and steam distillation.Its chemical structure was identified by UV,IR,MS and NMR method.Its homogeneity and stability were systematically checked.A cooperative certification was conducted by 8 laboratories,and the results of certification for nicotine were analyzed.The homogeneity and stability of the nicotine reference material were good,and the certified value was 99.12% with expanded uncertainty of 0.64% in confidence coefficient of 95%.The reference material of nicotine conforms to directives for the work of reference materials,and it could be used for method validation and quality control of regarding products. nicotine;tobacco;certified reference material;homogeneity;stability;certification 2016-03-28; 2016-04-09 国家质检总局公益性行业科研发展专项(201210209) 张经华,博士,研究员,研究方向:天然产物分离纯化,Tel:010-58717639,E-mail:wangwei_1217@126.com 分析测试技术与标准化 10.3969/j.issn.1004-4957.2016.09.025 O657.63;O629.3 A 1004-4957(2016)09-1203-06
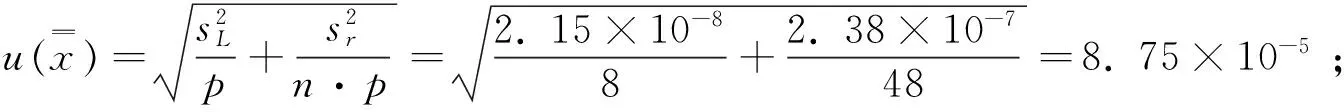
3 结 论

