乙醇法提取植物纤维剩余物中木质素的表征
徐 蕾 孟永斌 张子东 路 祺 刘 英 孟庆焕 聂思铭 祖元刚*
(1.东北林业大学生物资源生态利用国家地方联合工程实验室,哈尔滨 150040; 2.东北林业大学森林植物生态学教育部重点实验室,哈尔滨 150040)
* 通信作者:E-mail:zuyuangangnefu@126.com
乙醇法提取植物纤维剩余物中木质素的表征
徐 蕾1,2孟永斌1,2张子东1,2路 祺1,2刘 英1,2孟庆焕1,2聂思铭1,2祖元刚1,2*
(1.东北林业大学生物资源生态利用国家地方联合工程实验室,哈尔滨 150040;2.东北林业大学森林植物生态学教育部重点实验室,哈尔滨 150040)
以刺五加根茎剩余物为原料,分别以乙醇和碱为溶剂,分离提取得到乙醇法木质素和碱法木质素,两种木质素的酚羟基、羧基、总羟基和羰基活性官能团含量,为实现有机法木质素的高附加值资源化应用提供理论和实验依据。
木质素;碱法木质素;乙醇;官能团
木质素广泛存在于草本植物和木本植物中[1],是自然界中仅次于纤维素的自然储备量第二大天然高分子材料[2],是一类聚芳基化合物,具有复杂的空间网状结构[3],广泛的应用在医药业、工业、农业等[4~6],木质素分子中含有多种活性官能团,包括大量酚羟基和醛基,其化学结构是以苯丙烷类结构单元组成[2]。在碱性条件下[7],木质素可以作为酚类原料与醛反应,在酸性条件下[8],木质素可以作为醛原料与酚反应。此外,将具有酚类结构的木质素加入酚醛树脂生产中,不仅可以降低石化产品酚醛树脂的成本,还可以进一步改善酚醛树脂热压温度高、时间长等缺点。
用有机溶剂替代传统的硫酸盐碱液,提取得到的有机木质素性质更接近天然木质素,保留更多的活性基团,更适于作为化学添加剂,应用于树脂等工业生产中[9]。由于有机溶剂法提取分离木质素,整个生产工艺过程无污染、低能耗、溶剂可回收利用,可得到木质素和纤维素两种产物。因此,该法具有良好的发展前景[10]。
本文将采用乙醇作为木质素提溶液,从刺五加根茎剩余物中分离提取乙醇法木质素,与碱法木质素相比较分析了木质素的酚羟基、羧基、总羟基和羰基等活性官能团含量和组成成分,为实现有机法木质素的高附加值资源化应用提供理论和实验依据。
1 材料与方法
1.1 材料与仪器
刺五加药材购于黑龙江省哈尔滨市三棵树药材市场,经鉴定为刺五加的干燥根茎,该原料经粉碎成小块状,并采用一定浓度的乙醇,提取药物活性成分后得到的剩余物,即为得本实验所使用原料。
乙醇(AR,含量≥99.5%)产地:天津科密欧化学试剂有限公司;冰乙酸(AR,含量≥99.5%)产地:天津市化学试剂六厂;
实验装置:不锈钢高温高压反应釜(3L),产地:大连通产高压釜容器制造有限公司,型号为T25-FYX,最高工作压力:20 MPa,最高工作温度:380℃。
1.2 实验方法
乙醇法[11]木质素制备:刺五加根茎剩余物为原料,使用不锈钢高温高压反应釜,反应温度180℃,反应时间80 min,料液比1∶20,乙醇浓度80%条件下蒸煮,待反应终止,过滤得到有机木质素黑液,加入三倍体积水沉淀得到乙醇法木质素,经40℃真空干燥得到乙醇法木质素粉末。
碱法木质素制备:刺五加根茎剩余物为原料,使用不锈钢高温高压反应釜,在碱量20%(以NaoH计),硫化度25%(占绝干),液比1∶4.5 kg·L-1,蒸煮最高温度165℃,保温时间60 min条件下蒸煮,待反应终止,过滤得到黑液,经过盐酸酸析得到酸析沉淀木质素,用蒸馏水洗至中性,经40℃真空干燥得到碱法木质素粉末。
1.2.1 元素分析
意大利Euro公司的EA3000型元素分析仪测定C、H、N、S元素,测定条件如下:氧化炉温为1120℃,检测器为热导检测器(TCD),柱温为115℃。其中载气为氦气,流速为20 mL·min-1,氧气注入量为20 mL。
1.2.2 分子量测定
木质素分子量测定采用凝胶色谱(GPC)法,仪器为JASCO BORWIN GPC系统,Shodex KF 802.5和803双柱串连。木质素样品先乙酰化处理,然后用四氢呋喃溶解。流动相为四氢呋喃,流速为1.0 mL·min-1,紫外检测器检测波长为280 nm,柱温25℃,进样量为20 μL。
1.2.3 红外光谱分析
应用美国尼高力公司的MAGNA-IR560傅立叶红外光谱仪进行红外光谱分析,将高沸醇法木质素乙酞化,方法同上。取2 mg试样与加200 mg KBr制成薄片,频率范围5 000~400 cm-1,分辨率为2 cm-1,溴化钾作参考物。
1.2.4 TG和DSC分析
木质素热分析采用美国热学分析仪公司的DSC 204差热分析仪(DSC)和美国Perkin Elmer公司热重分析(TG)测试条件:空气气氛,样品质量5 mg左右,以5℃/min的加热速率从50℃加热到500℃。
1.2.5 木质素化学结构的测定
1.2.5.1 总羟基含量的测定
称取木质素40 mg于10 mL磨口试管中,将0.5~0.6 g乙酰化试剂加入该试管中后将其密封,在50℃条件下,反应时间:24 h,然后加入5 mL丙酮,用二氧六环与水的混合溶液(体积为4∶1)洗入25 mL容量瓶中,并定容。然后从容量瓶(25 mL)中取出5 mL溶液,用浓度为0.1N NaOH标准溶液电位滴定到终点,同时做空白对照实验。

(1)
式中:b0为空白样品消耗浓度为0.1N氢氧化钠标准溶液的体积(mL);b为样品消耗浓度为0.1N氢氧化钠标准溶液的体积(mL);f为0.1N氢氧化钠标准溶液校正因子;1.7为1 mL 0.1N氢氧化钠标准溶液对应羟基含量;A为木质素绝干质量(mg)。
1.2.5.2 酚羟基含量的测定
准确称取5~15 mg木质素试样,溶于10 mL水—二氧六环溶液(体积比为1∶9)中,分别取出2 mL溶液,分别移入到两个容量瓶(50 mL)中,其中一个容量瓶用0.2 mol·L-1氢氧化钠溶液稀释并定容,而另一个容量瓶用缓冲溶液(pH=6)稀释并定容,然后将容量瓶摇匀,取出一定溶液移入石英比色皿(1 cm)中,用空白溶液(pH=6)校零后,测得360和300 nm处的光密度分别为D2和D1[12]。△ε按照下式计算:
△ε=D/(C·L)
(2)
式中:C为木质素溶液浓度(g·L-1);D为吸光度;L为比色皿厚度(cm)。
按下面的公式计算出酚羟基(-OH)的百分含量:
[OH]=0.425△ε1+0.182△ε2
(3)
1.2.5.3 羧基含量的测定
称取40~60 mg木质素于25 mL容量瓶中,加入20 mL 0.4N乙酸钙溶液,盖好瓶塞,在85℃恒温水浴中反应30 min,取出冷却15 min,加蒸馏水定容到刻度,然后将溶液过滤,取滤液20 mL,用0.05N NaOH标准溶液电位滴定,并做空白实验[13]。
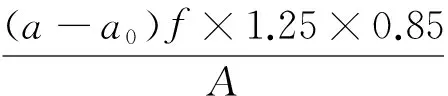
(4)
式中:a为样品消耗浓度为0.05N NaOH的体积(mL);a0为空白样品消耗浓度为0.05N NaOH的体积(mL);f为校正因子;1.25为换算系数;0.85为相当1 mL 0.05 mol·L-1NaOH木质素中酸性基的量;A为绝干木质素质量(mg)。
1.2.5.4 羰基含量的测定
称取80 mg木质素于磨口试管中,加二甲亚矾2 mL使之溶解。加入5 mL肟化试剂,先用氮气排除试管中空气,然后封住试管口。置于80℃恒温水浴反应120 min。取出加入20 mL蒸馏水,用0.1N HCI标准溶液电位滴定,并做空白实验[12]。

(5)
式中:a0为空白样品消耗浓度为0.1N HCl标准溶液体积(mL);a为样品消耗浓度为0.1N HCl标准溶液体积(mL);2.801为对应1 mL 0.1N HCl标准溶液的羰基量(mg);A为绝干木质素质量(mg);f为0.1N HCl标准溶液校正因子。
2 结果与讨论
2.1 木质素元素分析
木质素结构中常见的几种元素有碳(C)、氢(H)、氧(O)、氮(N)等元素组成。通过木质素的元素分析,可以了解木质素分子中元素组成及其比例。乙醇法木质素和碱法木质素的元素分析结果见表1,可以看出乙醇法木质素的碳含量和氢含量要高于碱法木质素,而氧含量低于碱法木质素。此外,随原料带入的部分含氮化合物和碱法脱木质素过程中使用试剂Na2S,造成的残留,所以碱法木质素元素分析结果中含有少量硫和氮元素存在。

表1 木质素的元素分析
通过仪器测得的木质素分子的元素组成情况,可计算并写出乙醇法木质素(C5.19H6.04O1.98)和碱法木质素(C2.76H4.14O3.63)经验式。可知,经过不同溶剂处理后,得到的木质素各元素的相对百分含量变化较为明显。
2.2 木质素分子量分布分析
采用凝胶色谱(GPC)法来测定木质素样品的分子量,乙醇法木质素和碱法木质素重均分子量(Mw)以及分散度(Mw/Mn)见表2。从表2中可以看出,木质素的分子量变化与制备方法有着很大关系,不同的制备方法木质素分子量分布差异很大。乙醇法木质素分散度为2.50,碱法木质素分散度要大于乙醇法木质素(分散度为2.82);乙醇法木质素的重均分子量(Mw)大于碱法木质素。

表2 木质素分子量
正是由于乙醇法制备木质素反应条件比较温和,得到的乙醇法木质素性质更接近天然木质素,所以乙醇法木质素分子量较碱法木质素分子量大。碱法木质素在制备过程中,由于有大量的浓度较高的碱存在,反应条件较为剧烈,造成木质素剧烈降解和不均匀断裂,所以碱法木质素分散度大于乙醇法木质素。乙醇法木质素分子量高于常规碱法木质素分子量,也说明乙醇法木质素更接近天然木质素。
2.3 木质素红外光谱分析
不同分离方法得到木质素的红外光谱都有所不同。根据红外光谱所使用的目的,可将红外光谱分析分为结构分析和定性分析。定性分析通常是根据红外谱图上特征谱带吸收,来确定官能团种类。结构分析则需要和其他分析检测手段相结合,相互佐证共同确定化合物的结构,即根据红外谱图的吸收峰的位置、吸收峰强度来判断试样化合物中是否存在特定官能团,再结合其他检测手段推断化学结构。
红外光谱是进行木质素定性分析的常用的有效的分析手段,在乙醇法木质素和碱法木质素的红外光谱图上(图1),3 429 cm-1处-OH伸展振动吸收峰有较明显变化,乙醇法木质素在此处峰值要大于碱法木质素,这说明乙醇法木质素酚羟基官能团含量高于碱法木质素,亚甲基、甲基的C-H伸展振动吸收峰分析位于红外谱图2 850、2 937 cm-1处,芳香环骨架振动吸收峰则分别位于1 600、1 514和1 458 cm-1处。1 714 cm-1处羰基(C=O)吸收峰是由于非共轭羰基和羧基振动产生,这种变化说明在有机酸存在条件下,制备乙醇法木质素的结构发生了显著改变。
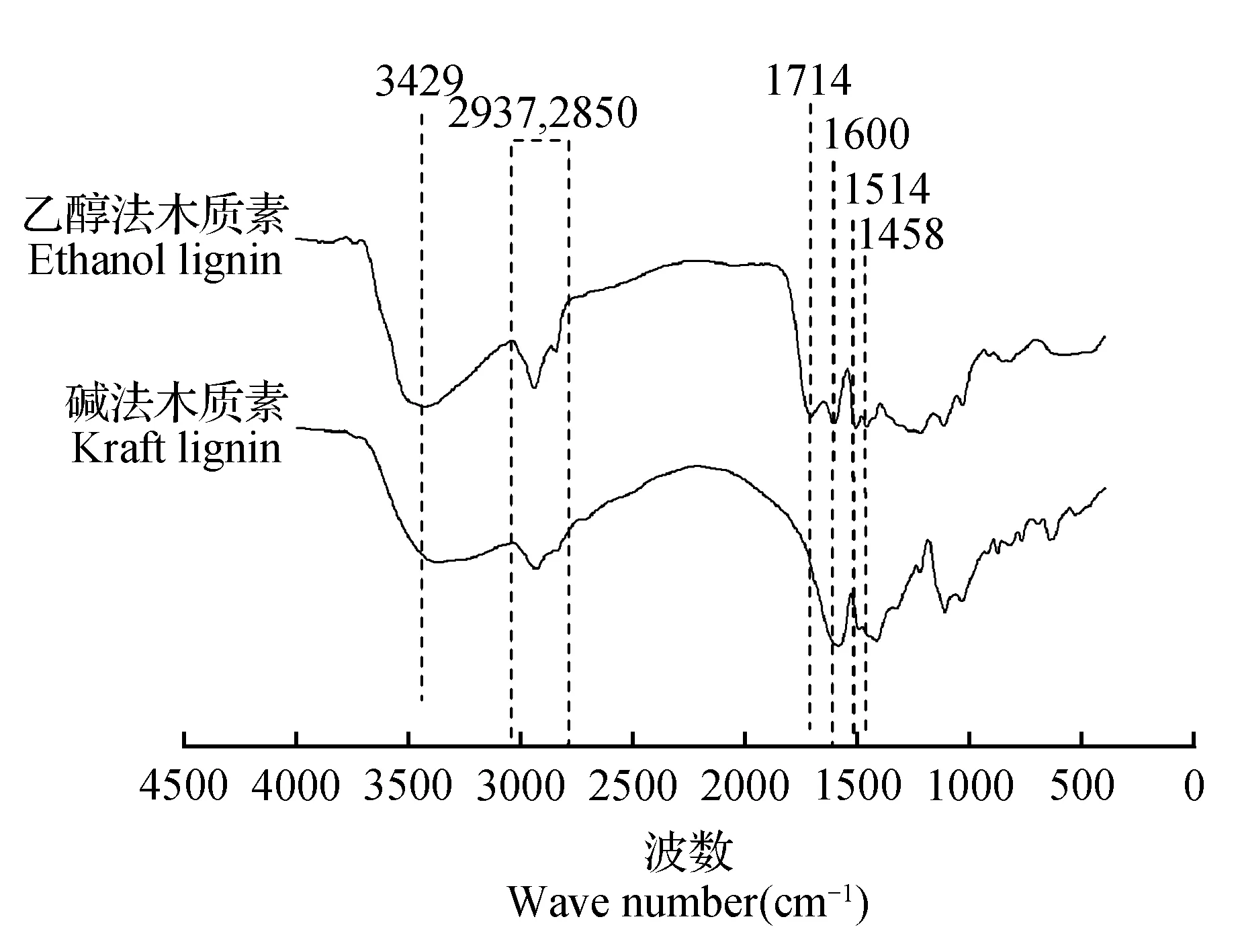
图1 乙醇法木质素和碱法木质素红外光谱图Fig.1 FTIR of ethanol lignin and kraft lignin
2.4 木质素热重与差热分析
2.4.1 热重分析
木质素热解分成三个阶段(图2),第一个阶段是脱除水分阶段,第二个阶段是半纤维素降解阶段(温度在200~300℃)[14~15],第三个阶段是木质素降解过程(温度在300~450℃)。
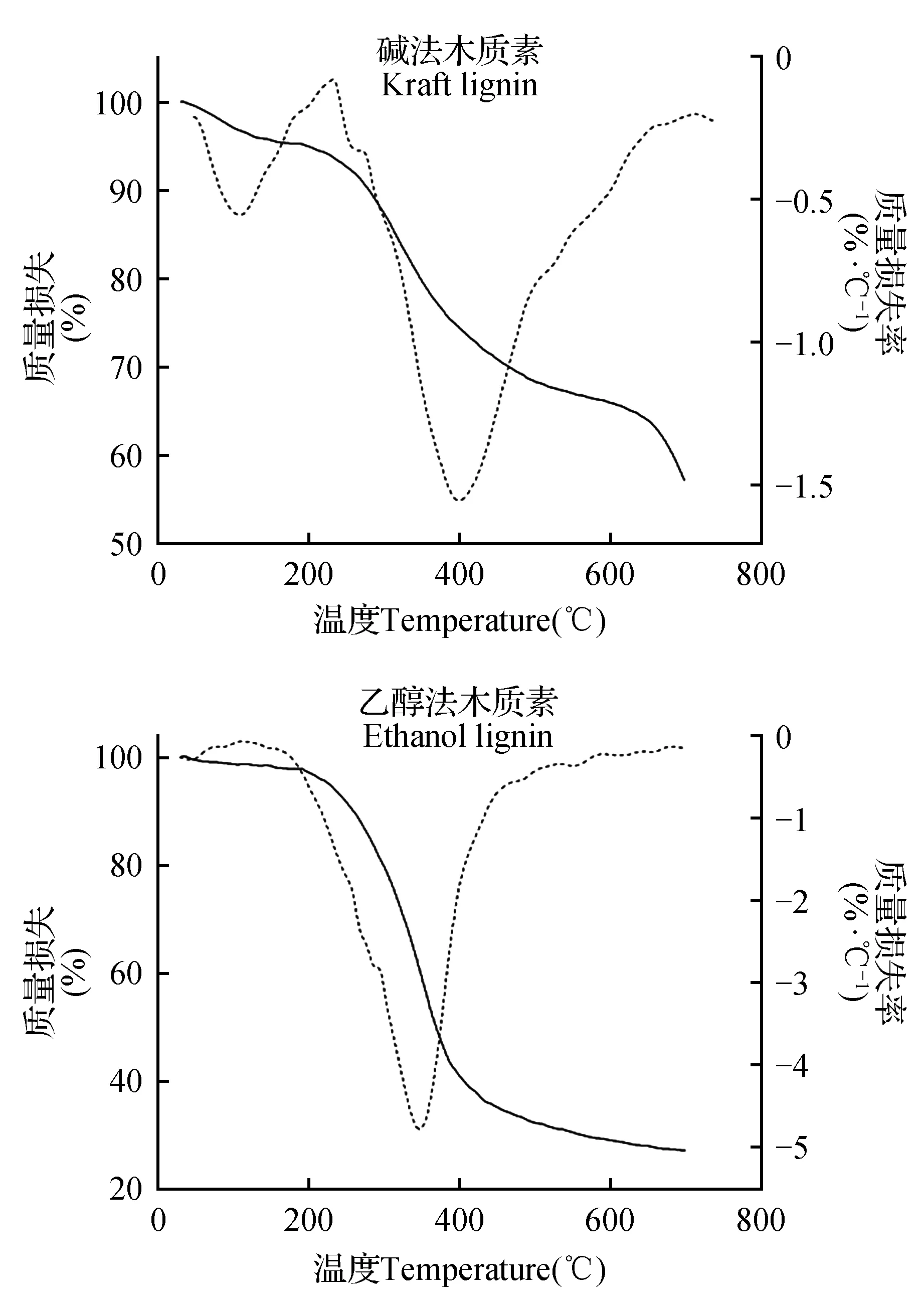
图2 乙醇法木质素和碱法木质素TG-DSCFig.2 TG(straight line) and DTG(dotted line) thermograms for alcohol and kraft lignin
木质素热解过程发生在第三个阶段,这个阶段木质素热重损失率很大程度上取决于木质素的结构和木质素制备方法。较高的热解残留率也表明试样具有较高的热稳定性,通过TG热重分析,发现当乙醇法木质素热解残留率为20%~30%时,碱法木质素热解残留率却为50%~60%,碱法木质素之所以有这么高的热解残留率是因为在脱木质素过程中使用无机物氢氧化钠,其残留造成的。
2.4.2 差热分析
DSC是用来研究木质素热解行为非常有效的工具,也常用来确定相转化如玻璃化温度和熔解温度等[16~18]。通过乙醇法木质素与碱法木质素的DSC数据分析,碱法木质素玻璃化温度最高(Tg=175℃),这说明碱法木质素热稳定性更好。乙醇法木质素和碱法木质素Tg值分别为106和175℃,数据表明乙醇法木质素玻璃化温度较低。
2.5 木质素化学结构分析
测定乙醇法木质素和碱法木质素官能团含量[19],结果见表3,可以看出乙醇法木质素的总羟基和酚羟基含量高于碱法木质素。

表3 木质素官能团
3 结论
通过对碱法木质素和乙醇法木质素进行元素分析,可以看出乙醇法木质素的碳含量和氢含量要高于碱法木质素,而氧含量低于碱法木质素。此外,碱法木质素元素分析结果中含有少量硫和氮元素存在,这是由于含氮化合物和碱法脱木质素过程中试剂Na2S残留造成的。
正是由于乙醇法制备木质素反应条件比较温和,得到的乙醇法木质素性质更接近天然木质素,所以乙醇法木质素的重均分子量(Mw)大于碱法木质素。另外,碱法木质素在制备过程中反应条件较为剧烈,造成木质素剧烈降解和不均匀断裂,碱法木质素分散度(2.82)大于乙醇法木质素(2.50)。
红外光谱图上,乙醇法木质素在3 429 cm-1处-OH伸展振动吸收峰要大于碱法木质素,这说明乙醇法木质素酚羟基官能团含量高于碱法木质素。1 714 cm-1处羰基(C=O)吸收峰是由于非共轭羰基和羧基振动产生,这种变化说明乙醇法木质素的结构发生了显著改变;TG热重分析表明碱法木质素有较高的热解残留率,这主要是碱法脱木质素过程中无机氢氧化钠残留造成的。
通过对木质素官能团含量检测,可知乙醇法木质素的总羟基和酚羟基含量均高于碱法木质素,说明乙醇法木质素在树脂合成方面性质优于碱法木质素。
1.邱卫华,陈洪章.木质素的结构、功能及高值化利用[J].纤维素科学与技术,2006,32(1):52-59.
2.林耀瑞,钟香驹.木素及其应用[J].中国造纸,1990,2(2):45-52.
3.张美云.非木材纤维自催化乙醇法制浆工艺与机理的研究[D].天津:天津科技大学,2003:2-7.
4.魏兰.以木质素为原料合成环氧树脂的研究[D].天津:天津科技大学,2004:3-5.
5.曲中原,金哲雄,高文昊,等.刺五加总苷提取工艺研究[J].哈尔滨商业大学学报:自然科学版,2005,21(1):14-16.
6.陶用珍,管映亭.木质素的化学结构及其应用[J].纤维素科学与技术,2003,11(1):42-55.
7.储富强,洪建国.木质素在高分子领域中的应用[J].林产化学与工业,2003,23(3):88-92.
8.李赢,石刚,石贵阳,等.不同提取方法对所得稻壳基木质素的影响研究[J].化学研究与应用,2015,27(6):903-909.
9.Chikako A,Yoshito S.Waste reduction system for production of useful materials from un-utilized bamboo using steam explosion followed by various conversion methods[J].Bioehemical EngineeringJournal,2004,25(3):151-157.
10.廖俊和,罗学刚.乙酸乙酯法竹材木质素分离技术研究[J].林产化工通讯,2004,38(4):19-21.
11.Mansouri N E,Salvadó J.Structural characterization of technical lignins for the production of adhesives:Application to lignosulfonate,kraft,soda-anthraquinone,organosolv and ethanol process lignins[J].Industrial Crops and Products,2006(24):8-16.
12.Mansouri N E E,Salvadó J.Analytical methods for determining functional groups in various technical lignins[J].Industrial Crops and Products,2007,26(2):116-124.
13.Gosselink R J A,Guran B,Abächerli A.Coordination network for lignin-standardization,production and applications adapted to market requirements [J].Ind Crops Prod,2004(20):121-129.
14.Domínguez J C,Oliet M,Alonso M V,et al.Thermal stability and pyrolysis kinetics of organ solve lignins obtained fromEucalyptusglobulus[J].Ind Crops Prod,2008,27(2):150-156.
15.Haiping Y,Rong Y,Hanping C,et al.Characteristics of hemicellulose,cellulose and lignin pyrolysis[J].Fuel,2007,869(12):1781-1788.
16.Rohella R S,Sahoo N,Paul S C,et al.Thermal studies on isolated and purified lignin[J].Thermochimica Acta,1996,287(1):131-138.
17.Anvar U,Buranov K A,Mazza G.Isolation and characterization of lignins extracted from flax shives using pressurized aqueous ethanol[J].Bioresource Technology,2010,101(19):7445-7446.
18.国婷,陈克利,杨淑蕙,等.从制浆黑液中分离木素及木素—苯酚—甲醛(LPF)树脂制备的研究[J].林产工业,1999,26(1):25-28.
19.周景辉,隋鑫金,平清伟.杨木乙醇法制浆中木素结构变化的研究[J].中国造纸学报,2008,23(3):16-20.
CharacterizationofKraftLigninandEthanolLignin
XU Lei1,2MENG Yong-Bin1,2ZHANG Zhi-Dong1,2LU Qi1,2LIU Ying1,2MENG Qing-Huan1,2NIE Si-Ming1,2ZU Yuan-Gang1,2*
(1.National Local Joint Engineering Laboratory for Ecological utilization of biological resources,Harbin 150040;2.Key Laboratory of Forest Plant Ecology,Northeast Forestry University,Ministry of Education,Harbin 150040)
We extracted the lignin by kraft and ethanol method, with the residues of Acanthopanax root and stem as raw materials. We obtained two kinds of lignin, and measured the contents of active groups and composition including phenolic hydroxyl, carboxyl, hydroxyl and carbonyl. Our study will provide the theoretical and experimental basis for high-value resources applications of organic lignin.
lignin;kraft lignin;ethanol;groups
林业公益性行业科研专项(201304601);中央高校基本科研业务费专项资金项目(2572014EA01-03)
徐蕾(1992—),女,硕士研究生,主要从事高分子材料研究。
2015-09-03
Q583
A
10.7525/j.issn.1673-5102.2016.02.023

