万古霉素壳聚糖缓释微球的制备及其体外释药特性和抑菌作用研究
刘 炜,刘 菊,黄义新(首都医科大学附属北京世纪坛医院药剂科,北京 100038)
万古霉素壳聚糖缓释微球的制备及其体外释药特性和抑菌作用研究
刘 炜*,刘 菊,黄义新(首都医科大学附属北京世纪坛医院药剂科,北京 100038)
目的:制备万古霉素壳聚糖缓释微球,考察其体外释药特性和抑菌作用。方法:采用乳化交联法制备万古霉素壳聚糖缓释微球,观察微球的粒径分布及形态;应用紫外分光光度法测定微球药物含量,计算载药量及包封率;通过体外释放试验,比较其与盐酸万古霉素24 h内的体外释药情况,考察其7 d内的累积释放度(Q);通过体外抑菌试验观察其作用20 d对金黄色葡萄球菌抑菌圈直径的影响。结果:所制万古霉素壳聚糖缓释微球呈圆球形,表面圆整,无明显凹凸和孔隙,平均粒径为(165.6±19.7)μm,平均载药量为(32.6±3.2)%,平均包封率为(53.8±6.3)%,Q7d为82.7%;其与盐酸万古霉素的Q2h分别为18.6%、91.3%;其作用1 d时的抑菌圈直径>3 cm,随其作用时间的延长,抑菌圈直径逐渐缩小。结论:成功制得万古霉素壳聚糖缓释微球,其体外缓释效果明显,且具有良好的体外抑菌作用。
万古霉素;壳聚糖;微球;体外释药;体外抑菌
临床修复骨损伤的过程中,常发生细菌感染难以控制的难题,常规静脉滴注抗生素治疗难以在局部产生高浓度的抗生素,无法达到理想的治疗效果。因此,近年来抗生素局部缓释系统在骨感染中的应用逐渐发展,该系统可以控制药物在局部释放,又能发挥良好抗菌活性[1-2]。微球作为缓控释药物载体应用广泛,其制备方法简便,适用于不同部位的给药,可用于注射、黏膜吸附或口服等不同给药方式,因此被广泛应用于载药缓释系统[3-4]。万古霉素是骨科应用较广的抗生素,细胞毒性较低,主要针对革兰氏阳性菌,对耐药金黄色葡萄球菌和表皮葡萄球菌抑制效果显著[5]。本研究应用壳聚糖微球良好的缓控释载体性能,制备万古霉素壳聚糖缓释微球,并探讨其载药性能、体外释放性能和体外抑菌性能,旨在为骨修复过程中的局部载药缓释系统的应用提供依据。
1 材料
1.1 仪器
JEM-200CX透射电子显微镜(日本日立公司);Lambda 650紫外-可见分光光度计(美国铂金埃尔默);Zetasizer-3000激光粒度分布测量仪(英国Malvern公司)。
1.2 药品与试剂
注射用盐酸万古霉素(浙江海正药业股份有限公司,批号:150607,规格:每支500 mg);壳聚糖(上海锐谷生物科技有限公司,分析纯);25%戊二醛、三氯甲烷、乙醇、NaOH等均为分析纯。
1.3 细菌
金黄色葡萄球菌(ATCC 25923),购自上海复祥生物科技有限公司。
2 方法与结果
2.1 万古霉素壳聚糖缓释微球的制备
采用水/油乳化交联法制备万古霉素壳聚糖缓释微球。将壳聚糖分散于稀乙酸水溶液中,溶胀12 h后制成0.2%的壳聚糖溶液,取适量盐酸万古霉素溶入壳聚糖溶液,边搅拌边将0.4%戊二醛稀溶液5 ml缓慢加入壳聚糖溶液中,继续搅拌10 min;加入液体石蜡和乳化剂油酸山梨坦,搅拌1 h后缓慢加入交联剂25%戊二醛溶液4 ml,40℃搅拌;加适量的NaOH溶液调节pH至微碱性,过滤后依次用三氯甲烷、乙醇溶液洗涤脱水,真空干燥器中干燥,制得万古霉素壳聚糖缓释微球。
2.2 微球的粒径分布与形态观察
将万古霉素壳聚糖缓释微球粉末均匀分散地黏附于导电胶上,观测前喷金,在透射电子显微镜下观察微球的形态结构。取2 ml万古霉素壳聚糖缓释微球混悬液,置于激光粒度分布测量仪中分析微球的粒径分布。结果显示,万古霉素壳聚糖缓释微球形貌较好,大致呈圆球形,表面光滑圆整,无凹凸和孔隙,粒径分布均匀,粒径分布在200 nm左右,平均粒径为(165.6±19.7)nm(n=3)。万古霉素壳聚糖缓释微球电镜扫描图见图1。
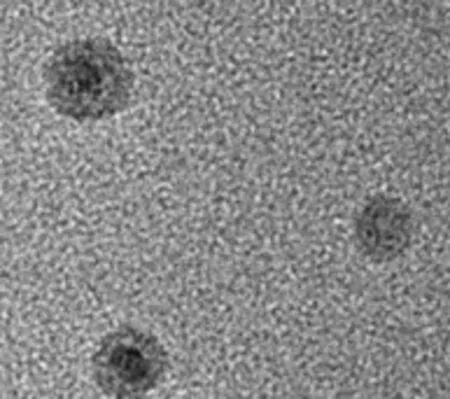
图1 万古霉素壳聚糖缓释微球的电镜扫描图(×200)Fig 1 TEM of vancomycin-loaded chitosan sustained-release microspheres(×200)
2.3 检测波长的选择
称取盐酸万古霉素和空白壳聚糖缓释微球在200~800 nm全波段行紫外扫描。结果显示,万古霉素在280 nm波长处有最大吸收峰,且空白壳聚糖缓释微球在此波长下不干扰测定,故选用280 nm作为万古霉素的检测波长,光谱图见图2。
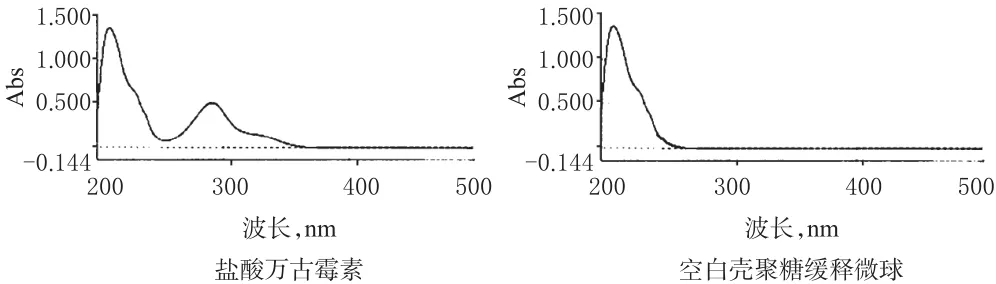
图2 紫外吸收光谱图Fig 2 UV spectrums
2.4 微球中万古霉素的含量测定
精密称取盐酸万古霉素100 mg溶解于HCl溶液中,置于100 ml量瓶中定容,制成1 mg/ml的对照品溶液;然后将对照品溶液稀释制成系列梯度浓度的万古霉素溶液,于280 nm波长处测定各浓度溶液的吸光度(A)。以A值对质量浓度(c)进行线性回归分析,得回归方程为A=2.967 2c+0.003 2(r2=0.999 6)。万古霉素检测质量浓度的线性范围为10~500 μg/ml。
2.5 微球载药量和包封率的测定
将万古霉素壳聚糖缓释微球溶解于HCl溶液中,于280 nm波长处测定万古霉素的吸光度,根据回归方程计算万古霉素的含量。按公式计算包封率与载药量,包封率(%)=微球中药物质量/药物的投药量×100%;载药量(%)=微球中药物质量/微球的质量×100%。结果显示,万古霉素壳聚糖缓释微球的载药量为(32.6±3.2)%,包封率为(53.8±6.3)%(n=3)。
2.6 体外释放试验
称取定量的万古霉素壳聚糖缓释微球和盐酸万古霉素对照品,置于截留分子质量为8 000~10 000 Da的透析袋内,以释放介质为pH 7.4的磷酸盐缓冲液、转速为100 r/min,于37℃恒温水浴中振摇。分别于1、2、4、6、8、12、16、24 h取样1 ml,并立即补加等量的释放介质1 ml,在280 nm波长处测定取样液的吸光度。根据回归方程计算万古霉素的浓度,再计算累积释放度(Q),绘制释放曲线,结果见图3。
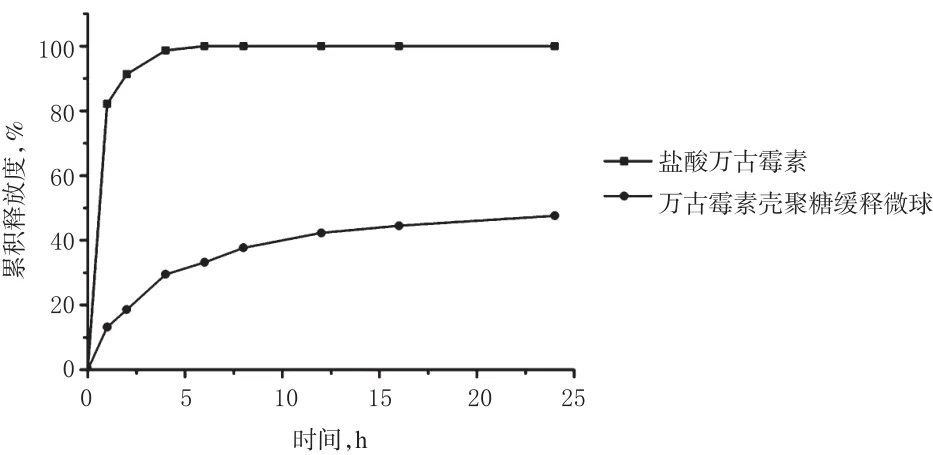
图3 万古霉素壳聚糖缓释微球和盐酸万古霉素24 h内的累积释药曲线Fig 3 Accumulative release curves of vancomycin-loaded chitosan sustained-release microspheres and vancomycin hydrochloride within 24 h
由图3显示,万古霉素壳聚糖缓释微球的Q1h为13.2%,Q2h为18.6%,Q4h为29.5%,Q12h为42.3%,Q24h为47.6%;盐酸万古霉素的Q1h为82.1%,Q2h为91.3%,Q4h为98.7%。通过对二者的体外累积释放度的比较,发现万古霉素壳聚糖缓释微球能减缓万古霉素的体外释放。同法测定万古霉素壳聚糖缓释微球7 d内的体外释放情况,结果显示,其Q7d为82.7%,表明万古霉素壳聚糖缓释微球具有较好的缓释作用。万古霉素壳聚糖缓释微球7 d内的累积释药曲线见图4。
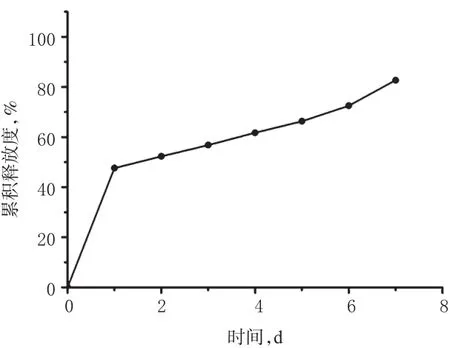
图4 万古霉素壳聚糖缓释微球7 d内的累积释药曲线Fig 4 Accumulative release curve of vancomycin-loaded chitosan sustained-release microspheres within 7 d
2.7 体外抑菌试验
将平行3组万古霉素壳聚糖缓释微球材料滴入含金黄色葡萄球菌的琼脂固体培养基中,37℃恒温培养24 h,测量抑菌圈直径。将微球材料置于新的金黄色葡萄球菌培养基中培养,每隔24 h重复此操作,共测量抑菌圈20 d,绘制抑菌圈直径-时间曲线。结果显示,万古霉素壳聚糖缓释微球对金黄色葡萄球菌具有持续抑菌作用,随着时间的延长,抑菌圈逐渐缩小。万古霉素壳聚糖缓释微球对金黄色葡萄球菌的体外抑菌圈直径-时间曲线见图5。
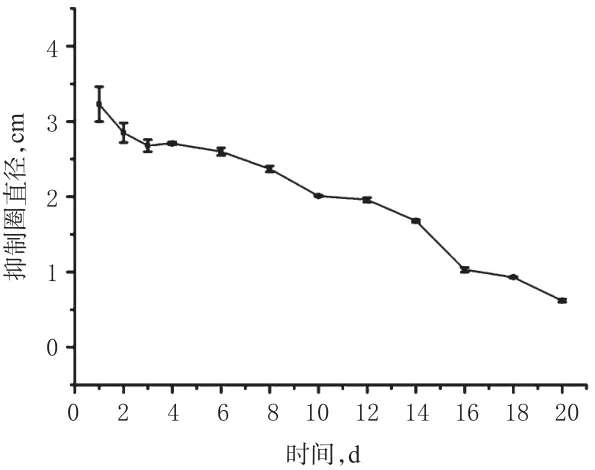
图5 万古霉素壳聚糖缓释微球对金黄色葡萄球菌的体外抑菌圈直径-时间曲线Fig 5 The diameter of inhibition zone-time curve in vitro of vancomycin-loaded chitosan sustained-release microspher-es to S.aureus
3 讨论
开放性骨折或感染性骨缺损,常因为存在感染因素,加大了治疗难度[6]。常规口服或静脉给予抗生素治疗,由于药物剂量大,易引发不良反应,且局部治疗效果较差。而采用药物缓控释技术可以降低药物的毒副作用,减少用药次数,避免耐药性的产生。
理想的抗生素缓释载体材料,应具有一定的载药量,释药速度平稳;不但能够有效释放抗生素以控制感染,且能实现局部给药增强药物的疗效,有效避免全身给药产生的不利影响[7-10]。壳聚糖是一种天然高分子生物材料,以其良好的生物相容性和可降解特性,被广泛应用于基因、药物载体载体[9-10]。
本实验以壳聚糖作为缓释载体、戊二醛为交联剂,采用乳化交联法制备万古霉素壳聚糖缓释微球,经测量载药量为(32.6±3.2)%,包封率为(53.8±6.3)%。推测万古霉素在微球中的载药机制为:万古霉素与壳聚糖分子中均含有氨基,戊二醛作为交联剂可以和氨基发生反应。在微球制备初期壳聚糖形成少量交联网络结构,将万古霉素分子包裹其中。当水相和油相混合之后能有效减少万古霉素的分散,从而提高微球交联度和万古霉素的交联密度,增加复合微球的载药性能[11-12]。
万古霉素壳聚糖缓释微球在释放介质中开始时释放较快,Q4h为29.5%,之后释放平稳。其机制在于盐酸万古霉素分子中含有亲水性羟基,呈水溶性,可以与水分子以氧键结合,能很快地扩散在溶液中[13]。由缓释微球和单药万古霉素的释放对比曲线可以看出,载药微球能显著抑制万古霉素的突释,避免瞬间局部产生高药物浓度。综上所述,万古霉素壳聚糖缓释微球在体外显示了良好的缓释作用和抑菌活性,可为其在骨感染治疗中的应用提供依据。
[1] Varma S,Sadasivan C.A long acting biodegradable controlled delivery of chitosan microspheres loaded with tetanus toxoide as model antigen[J].Biomedicine&Pharmacotherapy,2014,68(2):225.
[2] Li X,Ouyang J,Yang H,et al.Chitosan modified halloysite nanotubes as emerging porous microspheres for drug carrier[J].Applied Clay Science,2016,doi:10.1016/j. clay.2016.03.035.
[3] Zhang J,Tang Q,Xu X,et al.Development and evaluation of a novel phytosome-loaded chitosan microsphere system for curcumin delivery[J].International Journal of Pharmaceutics,2013,448(1):168.
[4] 冯淑莹,李国明,侯琼,等.金雀异黄素/壳聚糖微球的制备及其释药性能[J].华南师范大学学报:自然科学版,2013,45(5):64.
[5] Doty HA,Leedy MR,Courtney HS,et al.Composite chitosan and calcium sulfate scaffold for dual delivery of vancomycin and recombinant human bone morphogenetic protein-2[J].Journal of Materials Science:Materials in Medicine,2014,25(6):1 449.
[6] Meng D,Dong L,Wen Y,et al.Effects of adding resorbable chitosan microspheres to calcium phosphate cements for bone regeneration[J].Materials Science and Engineering:C,2015,doi:10.1016/j.msec.2014.11.049.
[7] Bitencourt CS,da Silva LB,Pereira PAT,et al.Microspheres prepared with different co-polymers of poly(lactic-glycolic acid)(PLGA)or with chitosan cause distinct effects on macrophages[J].Colloids and Surfaces B:Biointerfaces,2015,doi:10.1016/j.colsurfb.2015.10.011.
[8] Xie M,Zeng L,Zhang Q,et al.Synthesis and adsorption behavior of magnetic microspheres based on chitosan/organic rectorite for low-concentration heavy metal removal [J].Journal of Alloys and Compounds,2015,doi:10.1016/ j.jallcom.2015.06.065.
[9] 王明波,冯庆玲,等.乳酸-乙醇酸共聚物/壳聚糖复式微球缓释蛋白[J].复合材料学报,2011,28(5):156.
[10] 汪小乐,简晓顺,庞廷媛,等.叶酸偶联壳聚糖载多西他赛纳米粒的制备[J].中国药房,2014,25(29):2 740.
[11] Baimark Y,Srisuwan Y.Hollow chitosan microspheres prepared by an oil 1-in-water-in-oil 2 double emulsion method[J].Powder Technology,2013,249(11):436.
[12] Gaspar MC,Sousa JJ S,Pais AA CC,et al.Optimization of levofloxacin-loaded crosslinked chitosan microspheres for inhaled aerosol therapy[J].European Journal of Pharmaceutics and Biopharmaceutics,2015,doi:10.1016/j. ejpb.2015.07.010.
[13] Estevinho BM,Rocha FA,Santos LM,et al.Using water-soluble chitosan for flavour microencapsulation in food industry[J].Journal of Microencapsulation,2013,30(6):571.
(编辑:邹丽娟)
Preparation of Vancomycin-loaded Chitosan Sustained-release Microspheres and Its Drug Release in vitro and Antibacterial Effect
LIU Wei,LIU Ju,HUANG Yixin(Dept.of Pharmacy,Beijing Shijitan Hospital,Capital Medical University,Beijing 100038,China)
OBJECTIVE:To prepare vancomycin-loaded chitosan sustained-release microspheres and to study its drug release and antibacterial effects in vitro.METHODS:The emulsion cross-linking was used to prepare vancomycin-loaded chitosan sustainedrelease microspheres,and the particle size and morphology of microspheres were observed.The contents of vancomycin in microspheres was determined by UV spectrophotometry,and drug-loading amount of entrapment efficiency were calculated.Drug release of prepared microspheres and vancomycin hydrochloride within 24 h were compared by release trial in vitro,and then its accumulative release rate(Q)within 7 d was investigated.The effects of prepared microspheres on the diameter of inhibition zone to Staphylococcus aureus after treated for 20 d were observed through in vitro antibacterial test.RESULTS:The microspheres were spherical and complete round without obvious bump and pore.The average particle size of the microspheres was(165.6±19.7) μm;average drug-loading amount was(32.6±3.2)%;average encapsulation efficiency was(53.8±6.3)%;Q7dwas 82.7%.Q2hof prepared microspheres and vancomycin hydrochloride were 18.6%and 91.3%.The diameter of inhibition zone was higher than 3 cm after treated for 1 d,and then decreased gradually as time.CONCLUSIONS:Vancomycin-loaded chitosan sustained-release microspheres can be prepared successfully,and show obvious in vitro sustained-release effect and antibacterial effects.
Vancomycin;Chitosan;Microsphere;Release in vitro;Antibacterial effect in vitro
R943
A
1001-0408(2016)31-4443-03
2016-03-21
2016-06-20)
*副主任药师,硕士。研究方向:药物制剂、临床药学。电话:010-63926411。E-mail:liuwei8090@126.com
DOI 10.6039/j.issn.1001-0408.2016.31.36

