微波辅助与传统加热法合成植物油淀粉酯
王政洋,郑丽娜,么婷婷,郑洛昀,辛嘉英,2
(1.哈尔滨商业大学食品科学与工程重点实验室,黑龙江哈尔滨 150076;2.中国科学院兰州化学物理研究所羰基合成与选择氧化国家重点实验室,甘肃兰州 730000)
微波辅助与传统加热法合成植物油淀粉酯
王政洋1,郑丽娜1,么婷婷1,郑洛昀1,*辛嘉英1,2
(1.哈尔滨商业大学食品科学与工程重点实验室,黑龙江哈尔滨 150076;2.中国科学院兰州化学物理研究所羰基合成与选择氧化国家重点实验室,甘肃兰州 730000)
以植物油和预处理玉米淀粉为反应底物,利用脂肪酶分别在微波辅助和传统加热的方式下催化合成植物油淀粉酯。通过筛选不同反应底物,探究影响合成植物油淀粉酯反应的因素,并考察反应时间、反应温度、植物油添加量、反应转速及微波功率对酯化反应的影响。结果表明,在单因素试验的基础上,传统加热的最佳反应条件为反应温度65℃,反应时间20 h,植物油添加量20 g,反应转速200 r/min,取代度可达0.033 4;微波辅助的最佳反应条件为反应温度60℃,反应时间3 h,植物油添加量20 g,微波功率240 W,取代度可达0.036 2。
传统加热;微波辅助;脂肪酶;植物油淀粉酯
0 引言
脂肪酶催化合成植物油淀粉酯是近年兴起的一种淀粉改性手段。植物油淀粉酯不仅具有良好的去污、乳化、洗涤、润滑、起泡等性能[1-2],还具有无毒无臭、无污染、无刺激等优良特性,在食品、医药、纺织、化妆品等行业有着广泛的应用[3-4]。脂肪酶在催化酯化反应中具有优良的特性,使其变为了淀粉酯化改性的热门酶类[5]。相对于化学法来说,脂肪酶催化可以在底物含量较低、较温和的条件下进行,而且无需加入化学试剂,避免了有毒、有机溶剂的使用,副反应较少,符合当今“绿色化学”的要求。无溶剂体系中脂肪酶直接作用于底物,提高了底物和产物浓度及反应选择性,纯化过程简便、步骤少[6-7]。植物油淀粉酯既能为食品提供优良的质构,同时还能延长食品货架期[8-10];植物油淀粉酯在化妆品护肤膜和护肤沫中是一种重要的有效成分,可以提高化妆品的亲水性;在纺织工业中,低取代度的植物油淀粉酯能增加对合成纤维的黏结力,形成的浆膜耐弯曲、透明度好、稳定性强[11-12]。
试验以脂肪酶Novozym 435作为催化剂,探究微波辅助与传统加热对植物油淀粉酯合成反应的影响。在单因素试验的基础上,应用正交试验法对微波辅助和传统加热反应进行优化研究。
1 材料与方法
1.1 试验材料及仪器
固定化南极假丝酵母脂肪酶Novozym435(L4777)10 000 U/g、玉米淀粉(AR),苏州畅通化学有限公司提供;大豆油,九三粮油工业集团有限公司提供;棕榈油,天津市聚龙粮油有限公司提供;椰子油,Family Farm提供;油酸淀粉酯(DS=0.05,GR)、月桂酸淀粉酯(DS=0.05,GR),国药集团化学试剂有限公司提供;3A分子筛(AR),大连催化剂厂提供;二甲基亚砜(CP),天津嘉兴化工有限公司提供。
YY-1型数量超级恒温油浴锅,天津市欧诺仪器仪表有限公司产品;MCR-3型常压微波化学反应器,西安安泰仪器科技有限公司产品;GC7890F型气相色谱仪,上海天美科学仪器有限公司产品。
1.2 试验方法
1.2.1 植物油的前处理
分别取市售大豆油、棕榈油、椰子油500 mL,向其加入20 g分子筛,阴凉处放置24~48 h,备用。
1.2.2 淀粉的预处理
将质量比为2∶1的氢氧化钠和尿素加入到100 mL的去离子水中,配置成质量分数为9%的混合液,置于冰箱中放置24 h。
将配好的混合液快速搅拌10 min后缓慢加入5 g干基玉米淀粉,滴加9%HCl至中性;滴加无水乙醇使淀粉析出,用95%乙醇洗3次,再用无水乙醇洗涤,以脱去水分;置于110℃干燥箱中干燥 24 h,研磨后放入70℃烘箱,备用。
1.2.3 油浴无溶剂体系酶促植物油淀粉酯的合成
将处理好的植物油与预处理淀粉按照质量比20∶1的比例加入到50 mL的三角瓶中,待底物完全混合后,向其加入预处理淀粉质量10%的Novozym 435脂肪酶,2 g分子筛,放入65℃恒温油浴锅中进行反应;待反应一段时间后,用65℃无水乙醇反复洗涤,除去未反应的植物油;于70℃条件下烘干至恒质量,然后用80目筛子将固定化脂肪酶筛除,密封保存。
1.2.4 微波辅助无溶剂体系酶促植物油淀粉酯的合成
将处理好的植物油与预处理淀粉按照质量比20∶1的比例加入到50 mL的微波反应瓶中,待底物完全混合后,向其加入预处理淀粉质量10%的Novozym 435脂肪酶,2 g分子筛,放入微波反应器中进行反应;待反应结束后加入10 mL 95%乙醇使得植物油淀粉酯析出,然后用65℃无水乙醇反复洗涤,除去未反应的植物油;于70℃条件下烘干至恒质量,然后用80目筛子将固定化脂肪酶筛除,密封保存。
1.2.5 植物油淀粉酯取代度的测定
试验采用气象色谱法进行产物取代度的测定,首先进行产物的甲酯化,通过气相色谱扫描,利用内标法进行相关计算。
(1)植物油淀粉酯甲酯化。取0.8 g甲醇钠,加入到200 mL甲醇溶液中配置成0.4 g/mL甲醇钠溶液,备用。取植物油淀粉酯样品0.03 g,加入1 mL的二甲基亚砜进行溶解,待充分溶解后,加入1 mL 0.4 g/mL的甲醇钠溶液进行混合。将混合物在65℃下搅拌回流60 min,冷却后加入1 mL去离子水和1 mL正庚烷,置于磁力搅拌器上,强力搅拌1 min,静置分层,上层有机相即为植物油甲酯。
(2)气相色谱分析。取植物油甲酯0.5 mL,向其加入50 μL内标溶液后进行气相色谱扫描。气相色谱条件:DM-FFAP型石英毛细管色谱柱,30 mm×0.32 mm×0.25 μm;柱温220℃,进样口温度250℃,检测器温度260℃;载气:高纯氮;柱流速2.0 mL/min;尾吹流速40 mL/min;氢气流速35 mL/min;空气流速350 mL/min;分流比50∶1;进样量1 μL。
取代度计算公式:

式中:n——脂肪酸淀粉酯中脂肪酸物质的量,mol;
M0——样品的质量,g;
M1——葡萄糖残基相对分子质量,162;
M2——植物油中脂肪酸的摩尔质量,236。
2 结果与讨论
2.1 传统加热条件下不同植物油淀粉酯的结构
油浴加热式酶促反应红外光谱见图1。

图1 油浴加热式酶促反应红外光谱
由图1可知,NaOH-尿素法预处理淀粉及其与不同植物油分别在油浴加热和微波辅助下酶催化反应合成的植物油淀粉酯红外分析图谱。红外图谱的特征峰归属:在特征光谱的区间内,3 146~3 631 cm-1区域内的较大宽峰带由-OH的伸缩振动产生,在2 932 cm-1附近的峰带由C-H的伸缩振动产生;在1 364,1 167,1 050,857 cm-1处的吸收峰由葡萄糖残基的伸缩振动产生;在植物油淀粉酯红外光谱图的1 725~1 750 cm-1处出现一个新的特征峰,这是羰基的特征吸收峰,从而证明了酯键的形成,也从侧面证明了油浴加热条件下脂肪酶催化反应可以合成植物油淀粉酯。
2.2 传统加热不同植物油对淀粉酯合成的影响
植物油是由不饱和脂肪酸和甘油化合而成的化合物,广泛存在于自然界中,是从植物的果实、种子等中得到的油脂,如花生油、大豆油、棕榈油、椰子油等。植物油的主要成分是直链高级脂肪酸和甘油生成的酯,脂肪酸除软脂酸、硬脂酸和油酸外,还含有多种不饱和酸,如月桂酸、棕榈酸等。试验使用市售大豆油、棕榈油、椰子油。
2.2.1 反应时间对取代度的影响
油浴加热式酶促植物油淀粉酯的合成见图2。

图2 油浴加热式酶促植物油淀粉酯的合成
由图2可知,随着反应时间的延长,产物的取代度缓慢下降。这是因为在反应过程中,由于长时间搅拌,会使脂肪酶从载体上脱落,磨损也会引起粒度的减小而影响脂肪酶的稳定性,导致脂肪酶催化效率的降低,甚至失活。随着反应时间的延长,已生成的产物又部分水解,致使取代度缓慢降低。在油浴加热式酶促植物油淀粉酯的合成反应中,3种植物油与NaOH-尿素法预处理淀粉在最佳反应条件下反应24 h处反应的取代度分别达到最高,其中棕榈油与NaOH-尿素法预处理淀粉在该反应条件下取代度为最高的0.028 6。因此,油浴加热式酶促植物油淀粉酯合成选择棕榈油,反应时间应为24 h。
2.2.2 反应温度对取代度的影响
反应温度分别为55,60,65,70,75℃,脂肪酶添加量为10%,反应时间为24 h,已平衡水活度的预处理玉米淀粉与大豆油质量比为1∶20,反应时加入3A分子筛2 g。
反应温度对淀粉酯取代度的影响见图3。
由图3可知,反应温度65℃时取代度最大,为0.026 8,超过此反应温度取代度反而下降。试验所用的固定化脂肪酶Novozym 435在55~75℃内具有较高的反应活性,这可能是温度过高导致酶的部分失活。所以,选用的反应温度为65℃。

图3 反应温度对淀粉酯取代度的影响
2.2.3 棕榈油添加量对取代度的影响
加入已平衡水活度的预处理玉米淀粉与大豆油质量比为1∶10,1∶15,1∶20,1∶25,1∶30,脂肪酶添加量为10%,反应温度为65℃,反应时间为24 h,反应时加入3A分子筛2 g。
棕榈油添加量对淀粉酯取代度的影响见图4。

图4 棕榈油添加量对淀粉酯取代度的影响
由图4可知,棕榈油添加量20 g时取代度最大,为0.025 2,棕榈油添加量从5 g开始逐渐增加时,取代度也随之增加。这是因为棕榈油添加量过低时,参加反应的脂肪酸可以提供过量的脂肪酰基供体,是反应平衡向有利于产物生成的方向发展,从而取代度增加。当棕榈油添加量为20 g时,取代度达到最大值0.025 2;当继续增大棕榈油添加量时,取代度开始下降,直至平缓。这是因为过量的棕榈油将脂肪酶分子完全包围,致使其活性位点无法发生催化反应,导致取代度下降。因此,试验中棕榈油添加量定为20 g。
2.2.4 油浴反应转速对取代度的影响
加入已平衡水活度的预处理玉米淀粉与大豆油质量比为1∶20,脂肪酶添加量为10%,反应温度为65℃,反应时间为24 h,反应时加入3A分子筛2 g,油浴反应转速分别为100,150,200,250,300 r/min。
油浴反应转速对淀粉酯取代度的影响见图5。
由图5可知,随着油浴反应转速的增加,棕榈油淀粉酯的取代度上升,但是在转速超过200 r/min时,棕榈油淀粉酯取代度的上升趋势趋于平缓。这是因为在转速上升后,棕榈油与脂肪酶的接触更充分,脂肪酶的效率逐步升高,所以棕榈油淀粉酯的取代度上升;但是当油浴反应转速过高时,反应体系中的分子筛对体系的搅拌不均匀,反应底物与脂肪酶之间传质不充分,棕榈油淀粉酯的取代都下降。因此,试验中油浴反应转速选择为200 r/min,棕榈油淀粉酯的取代度较为理想。

图5 油浴反应转速对淀粉酯取代度的影响
2.3 传统加热棕榈油淀粉酯的条件优化
在单因素试验的基础上,对油浴加热式酶促反应的反应时间、反应温度、棕榈油添加量和反应转速安排L9(34)正交试验,以植物油淀粉酯的取代度作为指标。
正交试验结果见表1。

表1 正交试验结果
通过对正交试验的结果分析可以得出,各个因素对棕榈油淀粉酯取代度的主次顺序为反应温度、反应时间、反应转速、棕榈油添加量。同时,可以得出传统加热式酶促棕榈油淀粉酯合成的最佳反应条件为反应温度65℃,反应时间20 h,棕榈油添加量20 g,反应转速200 r/min,在该反应条件下的取代度为0.033 4。
因素与指标关系趋势见图6。
将处理好的棕榈油与预处理淀粉按照质量比20∶1的比例加入到50 mL的三角瓶中,待底物完全混合后,向其加入预处理淀粉质量10%的Novozym 435脂肪酶,2 g分子筛,放入65℃油浴锅内反应20 h,反应转速为200 r/min,在此条件下制备获得的棕榈油淀粉酯取代度为0.031 6。

图6 因素与指标关系趋势
3 微波辅助酶促棕榈油淀粉酯的合成及优化
3.1 微波辅助条件下不同植物油淀粉酯的结构
微波辅助酶促反应红外光谱见图7。
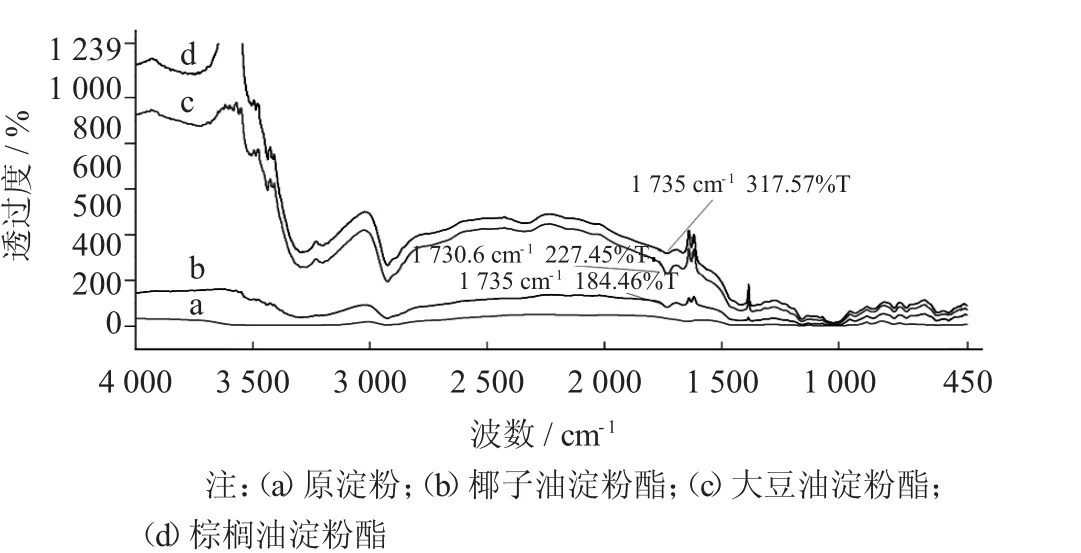
图7 微波辅助酶促反应红外光谱
由图7可知,原淀粉在1 160,1 025,930 cm-1处出现的峰是非对称C-O-C伸缩振动峰和骨架振动峰,在1 650 cm-1处有1个烯醇式C-O键的伸缩振动峰,在3 000~3 700 cm-1处出现长而宽的-OH伸缩振动峰;而大豆油淀粉酯、棕榈油淀粉酯、椰子油淀粉酯在1 725~1 750 cm-1处有典型的酯键特征吸收峰,从侧面说明微波辅助酶促植物油淀粉酯是可以合出产物的。
3.2 微波辅助酶促不同植物油对淀粉酯合成的影响以及反应时间对取代度的影响
微波辅助酶促植物油淀粉酯的合成见图8。

图8 微波辅助酶促植物油淀粉酯的合成
由图8可知,用微波辅助法进行的酶促植物油淀粉酯合成的反应中,同样是棕榈油在反应进行3 h处取代度达到最高的0.032 4,这说明用微波辅助法可以有效地提高植物油淀粉酯合成的取代度。因此,试验中使用棕榈油与NaOH-尿素法预处理淀粉在微波辅助条件下进行酶促植物油淀粉酯的合成反应。
3.3 反应温度对取代度的影响
反应温度分别为55,60,65,70,75℃,脂肪酶添加量为10%,反应时间为3 h,已平衡水活度的预处理玉米淀粉与棕榈油质量比为1∶20,反应时加入3A分子筛2 g。
微波辅助法反应温度对淀粉酯取代度的影响见图9。

图9 微波辅助法反应温度对淀粉酯取代度的影响
由图9可知,反应温度为65℃时,取代度最大0.034 2,超过此反应温度取代度反而下降。试验所用的固定化脂肪酶Novozym 435在60~65℃内具有较高的反应活性,当反应温度过高时可能导致酶的部分失活。同时,过高温度会使反应平衡逆向移动,已经生成的淀粉酯再次水解,导致反应平衡向逆向发展,从而使得取代度下降。所以,选用的反应温度为65℃。
3.4 微波功率对取代度的影响
采用MCR-3型常压微波化学反应器,微波功率可调至为80,160,240,320,400,480,560,640 W,棕榈油与NaOH-尿素法预处理淀粉在微波辅助条件下进行酶促棕榈油淀粉酯的取代度。
微波功率对棕榈油淀粉酯取代度的影响见图10。

图10 微波功率对棕榈油淀粉酯取代度的影响
由图10可知,当微波功率小于240 W时,棕榈油淀粉酯的取代度随微波功率升高而增大;但是当微波功率大于240 W以后,再升高微波功率时反而使得棕榈油淀粉酯的取代度下降。这主要是因为,当微波功率较低时脂肪酶的催化活性较低,微波功率缓慢增大时有利于底物的分散与分子碰撞;当微波功率过高时会导致脂肪酶的结构发生改变,致使脂肪酶失活,从而使得产物的取代度降低。
3.5 棕榈油添加量对取代度的影响
加入已平衡水活度的预处理玉米淀粉与棕榈油质量比为1∶10,1∶15,1∶20,1∶25,1∶30,脂肪酶添加量为10%,反应温度为65℃,反应时间为24 h,反应时加入3A分子筛2 g。
棕榈油添加量对淀粉酯取代度的影响见图11。

图11 棕榈油添加量对淀粉酯取代度的影响
由图11可知,因为试验中采用Novozym 435脂肪酶是固定化脂肪酶,其在非水相中的催化反应为非均相反应,比在水相中的分子扩散限制大,所以棕榈油添加量会影响脂肪酶的催化反应。在微波功率为240 W,反应时间为3 h这2个因素不变的条件下,棕榈油添加量从5 g开始逐渐增加时,取代度也随之增加,这是因为棕榈油添加量过低时,参与反应的脂肪酸可以提供过量的脂肪酰基供体,使反应平衡向有利于产物生成的方向发展,从而取代度增加。当棕榈油添加量为20 g时,取代度达到最大值0.031 8;当继续增大棕榈油添加量时,取代度开始下降,直至平缓,这可能是因为过量的棕榈油将脂肪酶分子完全包围,致使其活性位点无法发生催化反应,导致取代度下降。因此,试验中棕榈油添加量定为20 g。
3.6 微波辅助酶促棕榈油淀粉酯合成正交试验结果与分析
在单因素试验的基础上,对微波辅助酶促反应的反应时间、反应温度、棕榈油添加量、微波功率安排L9(34)正交试验,以植物油淀粉酯的取代度作为指标。
正交试验结果见表2。
由表2可知,微波辅助酶促棕榈油淀粉酯合成中各个因素对棕榈油淀粉酯取代度的主次顺序为反应温度、棕榈油添加量、微波功率、反应时间。同时,可以得出微波辅助酶促棕榈油淀粉酯合成的最佳反应条件为反应温度60℃,反应时间3 h,棕榈油添加量20 g,微波功率240 W,在该反应条件下的取代度为0.034 6。
因素与指标关系趋势见图12。
3.7 验证试验
将处理好的棕榈油与预处理淀粉按照质量比20∶1的比例加入到50 mL的三颈烧瓶中,待底物完全混合后,向其加入预处理淀粉质量10%的Novozym 435脂肪酶,2 g分子筛,将微波反应器的温度设定为60℃,微波功率为240 W,将三颈烧瓶放入微波反应器反应3 h,在此条件下制备获得的棕榈油淀粉酯取代度为0.036 2。

表2 正交试验结果
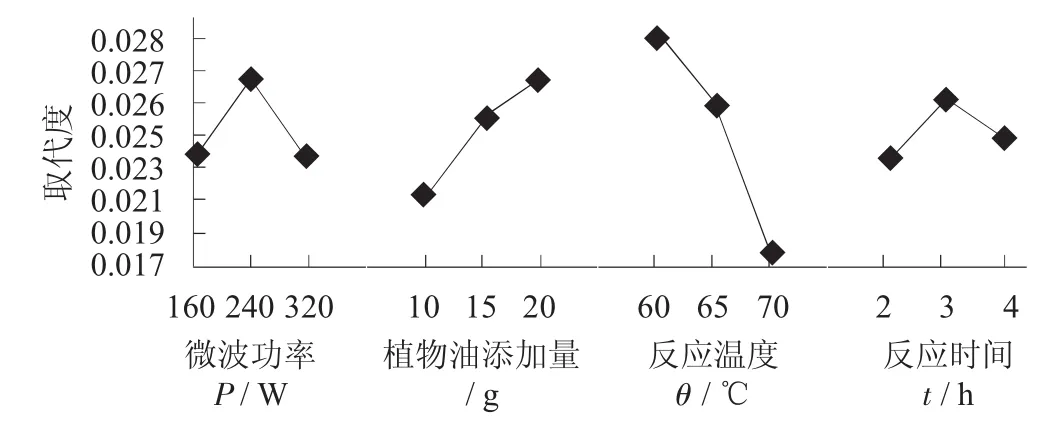
图12 因素与指标关系趋势
4 结论
试验中,首先选定一种植物油(棕榈油),以棕榈油和预处理淀粉为底物,利用脂肪酶Novozym 435为催化剂,分别以传统加热和微波辅助的方式进行植物油淀粉酯的酶促合成反应。由FT-IR图谱分析可知,该反应确实可以合成棕榈油淀粉酯,与传统加热相比,微波辅助不仅可以少量的提高棕榈油淀粉酯取代度,而且缩短了反应时间;在单因素试验的基础上,通过正交试验获得微波辅助酶促棕榈油淀粉酯合成的最佳反应条件。
[1]Brain W P.The first hundred years corn reifining in the United Staes[J].Starch,2001,53:257-260.
[2]Zhang Yanping.Modified starch manufacturing and application[M].Beijing:Chemical Industry Press,2001:2.
[3]Dejan B,Duan M,Slavica M.The effect of substrate polarity on the lipase-catalyzed synthesis of aroma esters in solvent-free systems[J].Journal of Molecular Catalysis B:Enzymatic,2007,45(4):97-101.
[4]具本植,尹荃,张淑芬,等.疏水淀粉衍生物研究进展 [J].化学通报,2007(10):727-733.
[5]Takashi K,Shuj A,Ryuichi M.Lipase-catalyzed condensation of p-methoxy-phenethyl alcohol and carboxylic acids with different steric and electrical properties in acetonitrile[J].Biotechnology Letters,2003,25(1):3-7.
[6]Marcin L,Stanislaw K.Low power microwave-assisted enzymatic esterification of starch[J].Starch Stärke,2012,64:188-197.
[7]Young Seon J,Ichon city,Arvind V,et al.Studies of starch esterification:Reactions with alkenyl succinates in aqueous slurry systems[J].Starch,1999,51:928-933.
[8]徐中岳,罗志刚.硬脂酸木薯淀粉酯的理化性质研究 [J].食品科技,2010,35(3):242-245.
[9]田颖,袁绍军.食用变性淀粉的特性及应用研究 [J].食品研究与开发,2002,23(6):69-71.
[10]Mullen J W.Starch derivatives[J].Industrial and Engineering Chemistyr,1942,34:807-812.
[11]陈丽华.变性淀粉在纺织工业中的应用 [J].天津纺织工学院院报,1998,18(1):25-27.
[12]葛杰,张功超,白立丰,等.变性淀粉在我国的应用及发展趋势 [J].黑龙江八一农垦大学学报,2005,17(1):69-73.
Conventional Heating and Microwave-assited Synthesis of Vegetable Oil Starch Ester
WANG Zhengyang1,ZHENG Li'na1,YAO Tingting1,ZHENG Luoyun1,*XIN Jiaying1,2(1.Key Laboratory for Food Science&Engineering,Harbin University of Commerce,Harbin,Heilongjiang 150076,China;2.State Key Laboratory for Oxo Syntinesis&Selective Oridation,Lanzhou Insititute of Chemical Physics Chinese Academy of Sciences,Lanzhou,Gansu 730000,China)
With vegetable oil and pretreatment of corn starch as substrate,synthesis of plant oil starch ester by lipase are investigated under microwave irradiation and conventional heating mode.On the different substrates are screened,and the influence factors in the synthesis of vegetable oil starch ester reaction is discussed,the reaction time,the reaction temperature,adding the amount of vegetable oil,reaction speed and effect of microwave power on the esterification reaction.On the basis of single factor,the optimum reaction conditions of traditional heating 65℃ of reaction temperature,20 h of reaction time,20 g of vegetable oil content,the reaction speed of 200 r/min.Substitution degree can be up to 0.033 4.The best microwave assisted reaction conditions are as follows 60℃ of reaction temperature,3 h of reaction time,20 g of vegetable oil content,microwave power 240 W.Substitution degree can be up to 0.036 2.
conventional heating;microwave assisted;lipase;vegetable oil starch ester
TS236.9
A
10.16693/j.cnki.1671-9646(X).2016.11.032
1671-9646(2016)11b-0013-06
2016-09-23
王政洋(1990—),男,在读硕士,研究方向为农产品加工及贮藏。
*通讯作者:辛嘉英(1966—),男,博士,教授,博士生导师,研究方向为农产品加工及贮藏。

