水飞蓟素肠溶聚乳酸-羟基乙酸共聚物纳米粒的制备及体外释药研究Δ
何 静,邱妍川,杨延音,刘松青,林凤云,江尚飞,朱照静(1.重庆医药高等专科学校继续教育学院,重庆 4011;.重庆医药高等专科学校药学院,重庆 4011;.第三军医大学第一附属医院药剂科,重庆 40008)
水飞蓟素肠溶聚乳酸-羟基乙酸共聚物纳米粒的制备及体外释药研究Δ
何 静1*,邱妍川2,杨延音2,刘松青3,林凤云2,江尚飞2,朱照静2(#1.重庆医药高等专科学校继续教育学院,重庆 401331;2.重庆医药高等专科学校药学院,重庆 401331;3.第三军医大学第一附属医院药剂科,重庆 400038)
目的:制备水飞蓟素肠溶聚乳酸-羟基乙酸共聚物(PLGA)纳米粒,并研究其体外释药行为。方法:以羟丙基甲基纤维素邻苯二甲酸酯(HPMCP)为肠溶材料,采用纳米沉淀法制备水飞蓟素肠溶PLGA纳米粒和水飞蓟素PLGA纳米粒,观察其形态,检测其粒径、Zeta电位、包封率、载药量、稳定性、体外释放度(Q)。以粒径、包封率、载药量为指标筛选水飞蓟素肠溶PLGA纳米粒中PLGA-HPMCP质量比。结果:PLGA-HPMCP的最佳质量比为1∶0.25。所制水飞蓟素肠溶PLGA纳米粒和水飞蓟素PLGA纳米粒的粒径分别为224、193 nm,Zeta电位分别为-37.8、-40.7 mV;包封率分别为(74.7±2.2)%、(71.7±2.5)%,载药量分别为(5.39± 0.24)%、(5.21±0.22)%;4℃下储存3个月后的渗漏率分别为0.2%、0.5%;人工胃液中Q48h分别为38.6%、70.5%,人工肠液中Q48h分别为80.2%、73.5%。结论:成功制得水飞蓟素肠溶PLGA纳米粒,其稳定性较好,能有效抑制水飞蓟素在人工胃液中的释放。
水飞蓟素;聚乳酸-羟基乙酸共聚物;羟丙基甲基纤维素邻苯二甲酸酯;纳米粒;体外释放度
水飞蓟素(Silymarin)是从菊科植物水飞蓟中提取精制而成的一类黄酮类化合物的总称,主要包含水飞蓟宾、水飞蓟宁和水飞蓟亭等,其中水飞蓟宾及其异构体异水飞蓟宾含量最高,约占该化合物的60%~70%,且具有最强的药理活性[1]。水飞蓟素在临床上是治疗肝脏疾病最为常用的一种植物药,体外研究证明其可通过抑制核因子κB(NF-κB)细胞发挥抗炎和免疫调节作用[2];还可以通过影响丙型肝炎核心蛋白和NS5A病毒的表达,发挥治疗慢性丙型肝炎病毒感染的作用[3]。此外,临床研究显示,水飞蓟素可有效用于非酒精性脂肪性肝病的治疗[4],并可减轻抗肺结核药物引起的肝损伤[5],减少化疗过程中顺铂造成的肾毒性等[6]。
尽管水飞蓟素在体外表现出了较好的药理活性,但由于其溶解度很低、体内吸收较差、生物利用度低,严重影响了其在临床的使用。目前临床上使用的水飞蓟素片剂或胶囊剂,患者需要每日给药3次,即每天需使用1.2~1.5 g才能维持有效的血药浓度。尽管水飞蓟素临床应用安全性较好,但高剂量长期使用仍会造成恶心、呕吐、腹泻等消化道不良反应。为提高水飞蓟素的生物利用度,国内外研究主要集中于制备其固体分散体、纳米脂质体、纳米混悬剂等[7-8],能一定程度上改善其体内吸收和靶向特征,但目前均未应用于临床。近年来,肠溶纳米粒的研究逐渐成为热点,已有研究显示其与普通纳米粒相比,可使药物以分子形态分布于肠溶载体,进一步提高药物的物理化学稳定性,减少对胃肠道的刺激;此外,以小肠定位给药可有效减少或避免用药的个体差异[9-10]。因此,本试验通过制备水飞蓟素肠溶聚乳酸-羟基乙酸共聚物(PLGA)纳米粒,以改善其溶解状况,降低其在人工胃液中的突释现象,进一步提高其口服给药的生物利用度和疗效,减少临床使用的不良反应。
1 材料
1.1 仪器
LC-2010C HT高效液相色谱仪(日本岛津公司);Tecnai G2 20200kV透射电子显微镜(厦门亿辰科技有限公司);纳米激光粒度仪(德国新柏泰克公司);超速离心机(美国贝克曼库尔特有限公司)。
1.2 药品与试剂
水飞蓟素对照品(西安瑞林生物科技有限公司,批号:130802,纯度:>98%);PLGA[中国科学院成都有机化学研究所,批号:141245-359,乙交酯(GA)-丙交酯(LA)(75∶25)];羟丙基甲基纤维素邻苯二甲酸酯(HPMCP,HP55,日本信越化学工业株式会社,批号:130906);聚乙烯醇(PVA,美国Sigma-Aldrich公司);甘露醇(重庆博方医药有限责任公司);丙酮(重庆川江化学试剂厂,化学纯);甲醇为色谱纯,水为去离子水。
2 方法与结果
2.1 水飞蓟素的含量测定
2.1.1 色谱条件 色谱柱为Dikma-C18(150 mm×4.6 mm,5 μm);流动相为甲醇-0.05 mol/L磷酸盐缓冲液(pH 2.77)(48∶52,V/V,经0.2 μm微孔滤膜滤过后使用),流速为1 ml/min;检测波长为288 nm;柱温为30℃;进样量为10 μl。该色谱条件下,水飞蓟宾和异水飞蓟宾的出峰时间分别为16.7、18.9 min,以两者峰面积之和计算水飞蓟素含量;其他辅料不影响水飞蓟素的含量测定。
2.1.2 方法学考察 按方法学考察相关方法进行试验。水飞蓟素峰面积(y)与质量浓度(x)的回归方程为y=16 548.6x+ 344.1(r=0.999 8,n=6),线性范围为5.03~150.9 μg/ml;日内(n=5)、日间(n=3)精密度试验的RSD均小于4.29%;10.06、50.30、100.60 μg/ml水飞蓟素溶液的方法回收率分别为(97.68±3.22)%、(98.32±3.51)%、(99.65±1.24)%(n=5)。
2.2 PLGA纳米粒的制备
采用纳米沉淀法制备PLGA纳米粒。称取水飞蓟素、PLGA各约0.7 g与一定量的HPMCP溶于10 ml丙酮,在磁力搅拌条件下,缓慢滴加到5%PVA水溶液中,调节pH至4~8,继续搅拌2 h。12 000 r/min(离心半径15 cm)离心10 min去除非目标粒径颗粒,加入甘露醇6 g,冷冻干燥,得水飞蓟素肠溶PLGA纳米粒。另精密称取水飞蓟素和PLGA各约0.7 g溶于丙酮中,之后照上述方法制备得到水飞蓟素PLGA纳米粒。
2.3 包封率和载药量测定
称取葡聚糖凝胶,加纯化水溶胀、煮沸、放冷、装柱。取制备好的水飞蓟素肠溶PLGA纳米粒或水飞蓟素PLGA纳米粒,采用蒸馏水重新分散为纳米粒混悬液后,精密吸取5.0 ml上样。脱气后超纯水洗脱,流速1.0 ml/min,收集洗脱液,弃去前20 ml洗脱液,取后55 ml,旋转蒸发浓缩至干,甲醇清洗旋蒸瓶并定容。用高效液相色谱法测定水飞蓟素含量,计算包封率和载药量。包封率(%)=Ws/Wa×100%,载药量=Ws/Wnp×100%,式中Wa为水飞蓟素投药量,Ws为包裹在纳米粒中的药物量,Wnp为载药纳米粒的量。
2.4 肠溶材料对水飞蓟素肠溶PLGA纳米粒的影响
固定水飞蓟素和PLGA处方量,以粒径、包封率和载药量为指标,考察不同比例PLGA-HPMCP(1∶0、1∶0.1、1∶0.25、1∶0.5、1∶0.75、1∶1)对水飞蓟素肠溶PLGA纳米粒的影响。结果显示,PLGA-HPMCP比例在1∶0.25之后,随HPMCP比例增大,纳米粒粒径增大,但包封率和载药量趋于稳定。因此,本试验选择PLGA-HPMCP比例为1∶0.25。不同比例PLGAHPMCP对水飞蓟素肠溶PLGA纳米粒的影响见表1。

表1 不同比例PLGA-HPMCP对水飞蓟素肠溶PLGA纳米粒的影响Tab 1 Effects of different ratios of PLGA-HPMCP on enteric-coated silymarin-PLGAnanoparticles
2.5 PLGA纳米粒质量评价
2.5.1 形态观察 按“2.3”项下方法制备水飞蓟素肠溶PLGA纳米粒和水飞蓟素PLGA纳米粒的混悬液,采用透射电子显微镜观察纳米粒的形态。结果显示,二者均呈圆形。透射电子显微镜图见图1。
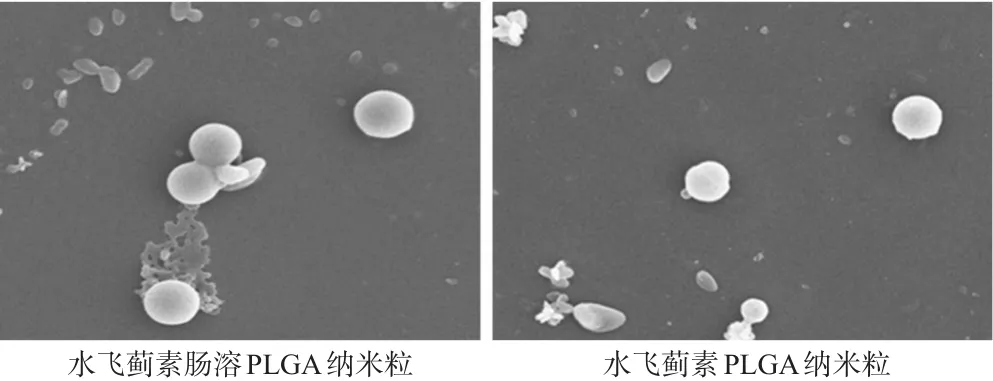
图1 两种纳米粒的透射电子显微镜图(×2 300)Fig 1 TEM of 2 kinds of nanoparticles(×2 300)
2.5.2 粒径和Zeta电位 按“2.3”项下方法制备水飞蓟素肠溶PLGA纳米粒和水飞蓟素PLGA纳米粒混悬液,加水稀释10倍,用纳米激光粒度仪测定其粒径和Zeta电位。结果显示,二者的平均粒径分别为224、193 nm,粒径分布为正态分布;Zeta电位分别为-37.8、-40.7 mV,表明两种纳米粒均较为稳定。两种纳米粒的粒径分布见图2。
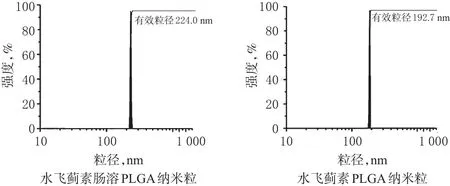
图2 两种纳米粒的粒径分布Fig 2 Particle size distribution of 2 kinds of nanoparticles
2.5.3 含量测定 取水飞蓟素肠溶PLGA纳米粒和水飞蓟素PLGA纳米粒,加入甲醇溶解并稀释混匀,进样测定水飞蓟素含量。结果,二者水飞蓟素的含量分别为(53.96±1.06)、(54.68±1.21)mg/g(n=6)。
2.5.4 稳定性考察 将水飞蓟素肠溶PLGA纳米粒和水飞蓟素PLGA纳米粒分别置于25 ml的敞口试管中,4℃下保存,分别于1、2、3个月时取出样品测定平均粒径与渗漏率(LR),LR(%)=(1-EEt/EE0)×100%,式中,EEt和EE0分别为在t时刻的包封率和初始包封率。结果显示,二者在4℃下储存3个月后粒径基本无变化,LR分别为0.2%、0.5%,具体结果见表2。
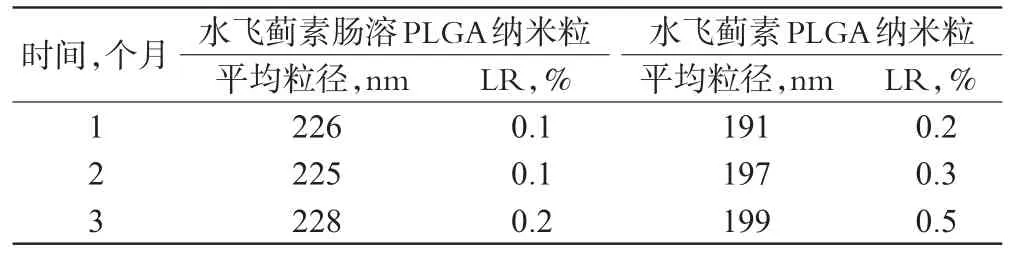
表2 两种纳米粒的稳定性试验结果Tab 2 Results of stability test of 2 kinds of nanoparticles
2.6 体外释放度考察
分别取水飞蓟素肠溶PLGA纳米粒和水飞蓟素PLGA纳米粒45 mg,放入棕色瓶中,分别加入150 ml人工胃液和人工肠液,37℃气浴恒温振荡,转速100 r/min。分别于试验前和开始振荡后0.5、1、2、4、8、12、24、48 h取样4 ml,并补充等体积的释放介质。接收液用0.22µm的微孔滤膜过滤,以甲醇稀释后于288 nm波长处测定吸光度,计算累积释放度,绘制体外释放曲线,结果见图3。
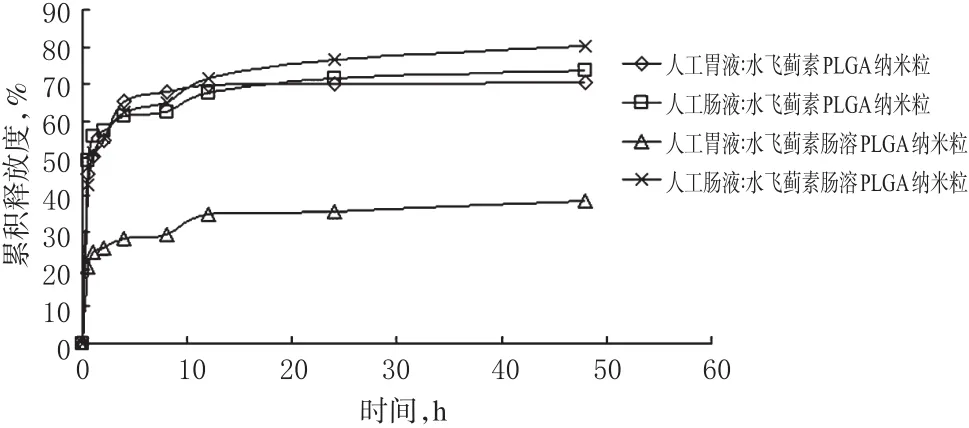
图3 两种纳米粒的体外释放曲线Fig 3 Release curves of 2 kinds of nanoparticles in vitro
由图3可见,水飞蓟素肠溶PLGA纳米粒在人工胃液中的释放速度和累积释放度明显低于水飞蓟素PLGA纳米粒;而在人工肠液中,水飞蓟素肠溶PLGA纳米粒的释放速度和累积释放度略高于水飞蓟素PLGA纳米粒。这是因为水飞蓟素溶解度较差,当人工肠液中肠溶材料溶解后,PLGA骨架对药物的阻滞作用占优势;而水飞蓟素肠溶PLGA纳米粒粒径较大,PLGA骨架对药物溶出的阻滞作用也相对较差,所以水飞蓟素溶出更快、溶出量更大。
3 讨论
PLGA是目前开发最为成功的一种生物可降解聚合物,可在机体内降解为乳酸和乙醇酸,进一步分解为二氧化碳和水排出体外,具有较好的生物相容性。其也是目前美国FDA和欧盟药品监管局(EMA)均批准的一种血管外给药的药物传递系统,可用于多种药物制剂的处方,包括亲水性、疏水性药物,也包括各种大分子或小分子药物,可有效用于延缓药物在体内的释放,降低药物在体内的代谢速度以及实现药物的靶向给药[11]。
由于PLGA纳米粒在胃液中有较强的突释现象,因此,本试验在制备水飞蓟素PLGA纳米粒的基础上,开发其肠溶剂型,以降低其在胃液中的突释,提高其在肠道的吸收,从而提高其口服给药的生物利用度;同时,还能有效避免其对胃肠道的刺激,减少不良反应的发生。从研究结果看,水飞蓟素肠溶PLGA纳米粒能有效抑制水飞蓟素在人工胃液中的释放。此外,笔者还需进一步试验评价其口服给药后体内的靶向作用,为其制剂的开发和临床应用提供依据。
[1] Cacciapuoti F,Scognamiglio A,Palumbo R,et al.Silymarin in non alcoholic fatty liver disease[J].World J Hepatol,2013,5(3):109.
[2]Morishima C,Shuhart MC,Wang CC,et al.Silymarin inhibits in vitro T-cell proliferation and cytokine production in hepatitis C virus infection[J].Gastroenterology,2010,138(2):671.
[3] Bonifaz V,Shan Y,Lambrecht RW,et al.Effects of silymarin on hepatitis C virus and haem oxygenase-1 gene expression in human hepatoma cells[J].Liver Int,2009,29(3):366.
[4] Aller R,Izaola O,Gómez S,et al.Effect of silymarin plus vitamin E in patients with non-alcoholic fatty liver disease.A randomized clinical pilot study[J].Eur Rev Med Pharmacol Sci,2015,19(16):3 118.
[5] Luangchosiri C,Thakkinstian A,Chitphuk S,et al.A double-blinded randomized controlled trial of silymarin for the prevention of antituberculosis drug-induced liver injury[J].BMC Complement Altern Med,2015,15(1):334.
[6] Momeni A,Hajigholami A,Geshnizjani S,et al.Effect of silymarin in the prevention of cisplatin nephrotoxicity,a clinical trial study[J].JCDR,2015,29(7):1 046.
[7] 陈晴宇,周建平,霍美蓉.水飞蓟素新型纳米制剂的研究进展[J].中国药科大学学报,2015,46(3):376.
[8] 李庆国,关世侠,郭慧珍.水飞蓟素缓释片的制备及体外释药机制研究[J].中国药房,2013,24(19):1 770.
[9] 王陆军,邱瑞桂,李建宇,等.葛根素肠溶纳米粒的制备及体外释放度研究[J].解放军药学学报,2009,25(6):514.
[10] 黄雅洁,李雅彬,袁海龙,等.南五味子总木脂素肠溶纳米粒的制备和药代动力学初步研究[J].药学学报,2009,44(9):1 046.
[11] Danhier F,Ansorena E,Silva JM,et al.PLGA-based nanoparticles:an overview of biomedical applications[J]. J Control Release,2012,161(2):505.
Preparation and in vitro Drug Release of Enteric-coated Silymarin-PLGA Nanoparticles
HE Jing1,QIU Yanchuan2,YANG Yanyin2,LIU Songqing3,LIN Fengyun2,JIANG Shangfei2,ZHU Zhaojing2(1.College of Extended Education,Chongqing Medical and Pharmaceutical College,Chongqing 401331,China;2.College of Pharmacy,Chongqing Medical and Pharmaceutical College,Chongqing 401331,China;3.Dept.of Pharmacy,the First Affiliated Hospital to Third Military Medical University,Chongqing 400038,China)
OBJECTIVE:To prepare enteric-coated silymarin-PLGA nanoparticles,and to study its in vitro release behavior. METHODS:Using HPMCP as enteric-coated material,nanoprecipitation method was used to prepare enteric-coated silymarin-PLGA nanoparticles and silymarin-PLGA nanoparticles.The morphology of nanoparticles were observed,and the particle size,Zeta-potential,encapsulation efficiency,drug-loading amount,stability and in vitro release rate(Q)were detected.The ratio of PLGA-HPMCP in enteric-coated silymarin-PLGA nanoparticles was screened by using particle size,encapsulation ratio and drug-loading capacity as indexes.RESULTS:The best PLGA-HPMCP ratio was 1∶0.25.The particle size of enteric-coated silymarin-PLGA nanoparticles and silymarin-PLGA nanoparticles were 224 nm and 193 nm,Zeta potential were-37.8 mV and-40.7 mV;encapsulation ratio were(74.7±2.2)%and(71.7±2.5)%,and drug-loading amount were(5.39±0.24)%and(5.21± 0.22)%;the percolation rates of them were 0.2%and 0.5%at 4℃ 3 months later;Q48hof them in simulated gastric fluid were 38.6%and 70.5%,and Q48hof them in simulated intestinal fluid were 80.2%and 73.5%,respectively.CONCLUSIONS:The enteric-coated silymarin-PLGA nanoparticles are prepared successfully with good stability,and can effectively inhibit the release of silymarin in simulated gastric fluid.
Silymarin;PLGA;HPMCP;Nanoparticle;Release rate in vitro
R943;R927
A
1001-0408(2016)34-4842-03
2016-02-05
2016-04-22)
(编辑:邹丽娟)
重庆市科技攻关计划项目(No.cstc2012gg-yyjs 10008);重庆市卫生局医学科研计划项目(No.2012-2-256)
*副教授,硕士。研究方向:缓控释制剂。E-mail:hejingt@126. com
#通信作者:教授,博士。研究方向:药剂学。E-mail:zhaojing6271@126.com
DOI 10.6039/j.issn.1001-0408.2016.34.28

